516例药物性肝损伤的临床研究
2019-10-31徐庆玲何兰兰柴一红郑丽青姚履枫
徐庆玲,何兰兰,李 纯,柴一红,郑丽青,姚履枫
随着人们生活水平的提高,体检的全面普及,无明显临床症状的药物性肝炎得以及早发现,及早治疗。目前认为药物性肝损伤(DILI)已成为最常见和最严重的药物不良反应之一,严重者甚至可以出现肝衰竭、死亡,同时也是世界范围内药物开发面临的挑战[1]。然而,迄今为止由于药物引起的肝脏损伤仍缺乏简便、客观、特异性的诊断和特效治疗手段,故而回顾性分析其临床特点尤为重要。
1 资料与方法
1.1一般资料 使用本院病案管理系统及大数据系统统计筛选出我院连续两年住院的DILI患者共计516例,均符合DILI诊断标准。其中,2016年1~12月288例,2017年1~12月228例患者。
1.2诊断方法 根据患者提供的用药史,既往史,表现出的临床症状,查体所见的体征;实验室检查包括肝功能、肝炎病原学检查、彩超等;对每一份病历资料汇总,归结出导致DILI的因果关系,同时得出明确的诊断。
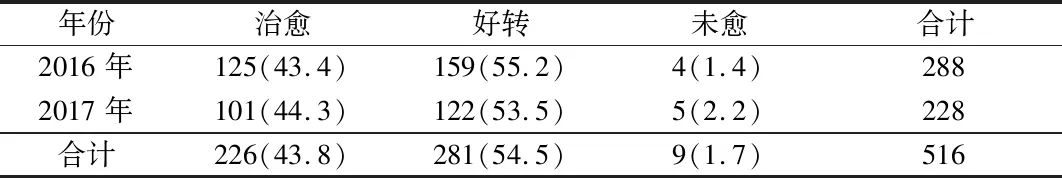
使用目前较为公认的RUCAM量表评分[2],内容包括:服药至发病的时间、停药后肝功能恢复情况、危险因子、合并用药,排除其他因素(抗-HAV-IgM、HBV、HCV、HEV感染、酒精中毒、近期有急性低血压病史、合并脓毒症、转移性恶性肿瘤、自身免疫性肝炎、原发性胆汁性胆管炎或原发性硬化性胆管炎、遗传性肝病等),所用药物既往肝损伤等。最后判断:>8分,非常可能;6~8分,很可能;3~5分,可能;1~2分,不像;0分,无关;此次统计中3分以下排除;另外针对每份病历进行R值计算:R值=[ALT/ALT正常范围上限]/[ALP/ALP正常范围上限],R值决定损伤类型:肝细胞型(R≥5.0),胆汁淤积型(R≤2.0)或混合型(2.0 根据量化评分进行DILI严重程度分级,即0级:患者对暴露药物呈现可耐受,无肝毒性反应;1级:患者血清中ALT和(或)ALP呈可恢复性升高,TBil<2.5 mg/dl,且国际标准化比值(INR)<1.5,多数患者可适应,可有或者无临床症状;2级:患者血清中ALT和(或)ALP升高,TBil≥2.5 mg/dl,或虽无TBil升高但INR≥1.5,临床症状可有或加重;3级:血清ALT和(或)ALP升高,TBil≥5.0 mg/dl,伴或不伴INR≥1.5,患者症状进一步加重,并需住院治疗(住院时间延长);4级:血清ALT和(或)ALP水平升高,TBil≥10.0 mg/dl或每日上升≥17.1 μmol/L,INR≥2.0或凝血酶原活动度(PTA)<0.4,可同时出现腹水或肝性脑病,或与DILI相关的其他器官功能衰竭;5级:因DILI死亡,或需接受肝移植才能存活。 1.3病情转归 患者停用药物并卧床休息。同时,给予还原型谷胱甘肽、复方甘草酸苷注射液或复方甘草酸苷片等治疗,如肝衰竭病情较重患者接受人工肝系统支持(如血浆置换)治疗。 2.1年龄及性别结构 2016~2017年DILI共516例。2016年288例,男102例(平均年龄45.55岁),女186例(平均年龄48.48岁);2017年228例,男97例(平均年龄44.33岁);女131例(平均年龄45.41岁)。 2.2DILI病因分类 2016年诊断为DILI病历288例,其中前六位药物为中草药及中成药占32.3%,抗结核药物占18.1%,抗肿瘤药物占29.2%,降脂药物占3.1%,保健品占4.9%,感冒药物占3.5%。而2017诊断为DILI病历228例,其中前六位药物为中草药及中成药占32.0%,抗结核药物占19.7%,抗肿瘤药物占15.8%,降脂药物占6.1%,感冒药物占5.7%,保健品占5.3%。两年中均以中草药及中成药所占比例最大。见表1。 2.3DILI严重程度分级及分型情况 DILI严重程度分级情况,见表2。严重程度共分为6级,0~2级患者较多,2016年0~2级共有235例(81.6%),2017年0~2级共有188例(82.5%),两年间分级比较,无明显差异(P>0.05)。 参照DILI国际临床分型标准,以入院时的实验室指标为依据对患者进行分型,见表3。两年临床分型中,肝细胞损伤型最多,共306例(59.3%),胆汁淤积型次之,共127例(24.6%),混合型最少,共83例(16.1%)。 根据因果关系评价表(RUCAM)进行DILI评分,结果见表4。其中6~8分的患者居多,两年间RUCAM评分比较,有明显差异(Z=2.86,P<0.01)。 2.4临床表现 临床表现以入院时患者所存在症状统计:2016及2017年,有临床症状404例(78.29%),无临床症状仅体检发现者为112例,症状包括乏力384例(74.42%)、食欲减退378例(73.26%)、食量减少297例(57.56%)、恶心290例(56.20%)、腹胀224例(43.41%)、尿黄307例(59.50%)、皮疹23(4.26%)、皮肤瘙痒35例(6.78%)、鼻衄3例(0.58%)、肝区疼痛48例(9.30%)、发热12例(2.33%)。 2.5转归 近两年DILI患者的临床转归情况,见表5。多数患者肝脏损伤程度较轻,经及时停药及保肝甚至人工肝血浆置换治疗后,可以恢复,预后较好;较少患者出现慢性化,甚至进展为肝硬化。2016年度及2017年度DILI好转率分别为98.6%、97.8%,两年治疗有效率比较,无明显差异(χ2=0.13,P>0.05)。其中,2016年出现肝衰竭病历为12例(早期肝衰竭6例,中期肝衰竭4例,晚期肝衰竭2例);慢性DILI有9例,2例因长期不规则服用中草药及中成药后出现肝硬化。2017年出现肝衰竭病历为8例(早期2例,中期4例,晚期2例);慢性DILI有7例,2例亦因长期服用中草药、保健品后进展为肝硬化。故而患者往往存在长期不规则服用中草药或保健品,因临床表现隐匿,被忽略,导致慢性化甚至肝硬化。 目前全球已知有1100多种上市药物存在或者潜在性存在肝毒性,据来自欧美的数据显示,乙酰氨基酚(APAP)已知在治疗剂量下是安全的。它的过度使用在许多国家引起急性肝损伤甚至肝功能衰竭,APAP诱导的肝损伤是目前最常用的DILI模型,N-乙酰对苯醌亚胺(NAPQI)是APAP的活性和毒性代谢产物,其积累是APAP过量致肝损伤的主要原因,在DILI的发生发展过程中,肝代谢的许多方面都存在异常,影响DILI的进展和预后[3]。 现阶段因中药肝毒性研究的局限性,缺少临床对照试验和毒理学研究的支持,导致缺乏药物的有效性和安全性。从本研究结果可见,中草药引起的肝损伤日趋严重。该结论不排除存在地区性影响可能,福建地区山区较多,人们对中草药的使用较为普遍,甚至成为餐桌中的常见物;该类药物引起DILI的缘由呈多样化,其中以药物中的萜类[4]以及吡咯双烷类生物碱[5]等代谢产物可引起的肝细胞脂质的过氧化反应,以及肝细胞的免疫性损伤,从而导致肝细胞过度凋亡、细胞色素代谢酶系的异常等,进而致肝细胞坏死[6]。 由于抗痨药物的使用,结核类疾病得到较好的控制[7,8],然而抗痨药物引起的DILI依然成为诱发该类疾病的重要因素之一,且病死率可达到5%。通常认为DILI原因可分为靶向药物的直接肝毒性或特异性肝毒性作用,导致肝脏细胞损伤通路和保护通路失衡,从而导致肝细胞毒性;另外,药物的直接肝细胞损伤,往往为剂量依赖性,通常可预测[9,10]。近几年来众多对特异质性肝毒性的研究提示,更倾向于适应性免疫攻击为DILI的共同机制,我们知道药物代谢酶系、跨膜转运蛋白及溶质转运蛋白的基因多态性可导致药物代谢酶系或转运蛋白功能异常[11];通过以上机制导致持久的、过强的内质网应激反应打破非折叠蛋白反应对氧化应激的缓解效应,从而促进药物性肝细胞损伤,同时启动死亡信号途径,促进肝细胞凋亡、坏死的发生[12]。药物在启动肝损伤的同时也将激发恢复性组织修复,肝损伤后,如肝组织修复作用下降,则肝损伤迅速进展,甚至出现肝细胞大量坏死,进入重型肝炎阶段,故而肝细胞损伤修复在DILI中起到决定性作用[13]。 表1 2016~2017年导致DILI的药物类别比较 [例(%)] 表2 DILI严重程度分级情况 [例(%)] 表3 DILI国际临床分型 [例(%)] 表4 DILI的RUCAM评分结果比较 [例(%)] 表5 2016~2017年DILI临床转归情况比较 [例(%)] 目前,DILI仍缺乏简便、客观、特异性的诊断方法和标准,希望回顾性分析DILI的临床特点,引起大家对该病的重视及预防,并对诊治有所帮助。
2 结 果
3 讨 论