南四湖底泥耐铅菌株的分离鉴定及吸附特性
2019-10-25董欣袁坤徐佳
董欣 袁坤 徐佳

摘要:重金属污染土壤中的微生物对重金属有较强的耐受能力并能起到富集作用,是进行土壤净化的重要力量。分离鉴定南四湖底泥中的抗铅菌株,并且对其吸附特性进行研究。从南四湖底泥中采集土样,经过分离、培养,最终筛选出2株抗铅菌株。对所得菌株进行16S rDNA测序和序列相似性分析,鉴定其种属后对其Pb2+质量吸附特性进行研究。结果:菌株1D、8A最大耐Pb2+浓度分别为700 mg/L和600 mg/L。16S rDNA序列相似性分析表明,菌株1D、8A分别与蜡样芽孢杆菌(Bacillus cereus)、彭氏变形杆菌(Proteus penneri)亲缘关系最近。经过吸附性能测试,菌株1D在 35 ℃、pH值=5、Pb2+质量浓度为100 mg/L、菌体投放量为30 g/L、转速为180 r/min、吸附时间为15 min时吸附效率最高;菌株8A在20 ℃、pH值=7、Pb2+质量浓度为300 mg/L、菌体投放量为20 g/L、转速为180 r/min、吸附时间为 5 min 时吸附效率最高。此外,2株菌株对Zn2+、Cu2+、Co2+和Fe2+等重金属也有一定的耐受性。筛选到的菌株抗铅性能高、吸附性好,丰富了微生物修复的生物资源库,同时对于吸附特性的研究又可以为抗重金属菌株筛选提供参考。
关键词:铅;吸附;蜡样芽孢杆菌;彭氏变形杆菌
中图分类号:S182 文献标志码: A 文章编号:1002-1302(2019)13-0314-06
南四湖属于典型的内陆浅水型淡水湖泊,由南阳湖、独山湖、昭阳湖和微山湖串联在一起组成,是山东省的“生态宝库”,是南水北调东线工程的重要枢纽和调蓄湖泊,水质安全至关重要。
长期以来,重金属污染是影响南四湖水质的重要因素。2003年和2005年对南四湖表层沉积物重金属元素的污染分析显示,南阳湖和独山湖的Pb污染较重[1-2]。2010年对南四湖表层沉积物重金属的赋存形态的研究发现,南阳湖区沉积物间隙水及界面上覆水中Pb的浓度均高于独山湖区,并与沉积物中重金属元素的有效结合态含量变化一致[3]。2013年对南四湖表层沉积物重金属的空间分布、来源及污染评价发现,南四湖表层沉积物中As、Hg、Pb、Cd等均超过环境背景值,在空间上表现出上级湖高、下级湖低的分布特征,各湖区沉积物污染程度由高至低依次为:南陽湖>独山湖>微山湖>昭阳湖[4]。2015年对南四湖的南阳湖区河口与湖心沉积物重金属潜在生态危害指数研究发现,南阳湖受Hg及Cd的污染较重,Pb、Cu及Cr为轻微污染[5-6]。2017年对南四湖入湖河流重金属的风险熵评价结果显示,铬、砷和铅含量的风险较小,南四湖入湖河流水质较好[7]。可见,随着南水北调东线工程的开通和湿地保护和治理力度的加强,南四湖的水质改善显著,水体和底泥重金属的含量逐步降低,但是,潜在的重金属污染问题仍然需要我们长期关注。
生物防护是预防和解决湖水污染的重要方法。湖底淤泥是重金属蓄积的主要场所。淤泥中的微生物长期处于重金属的选择压力下,对重金属有较强的富集作用。从湖底淤泥中分离出的抗性微生物在重金属修复领域具有很大的应用潜力,是进行湖水净化的重要力量。本研究拟从南四湖底泥中筛选出Pb2+抗性菌株,应用16S rDNA基因测序,结合形态和生理生化特性确定种类,对这些菌株的适宜生长条件和对Pb2+及其他重金属离子的抗性进行测试,为南四湖水体重金属污染的预防和治理提供数据支撑[8]。
1 材料与方法
1.1 试验材料及培养基
筛选菌株的土壤样品采自南四湖南阳湖区表层底泥。
基础LB液体培养基:酵母提取物(酵母浸粉)5 g,胰蛋白胨10 g,氯化钠10 g,蒸馏水1 000 mL;调节pH 值至7.0~7.2;1×105 Pa灭菌20 min。
基础牛肉膏蛋白胨固体培养基:琼脂10 g,牛肉膏3 g,蛋白胨10 g,氯化钠5 g,蒸馏水1 000 mL;调节pH值7.0~7.2;1×105 Pa灭菌20 min。
选择培养基:将不同重金属的离子试剂Pb(NO3)2、CoCl2、HgCl2、ZnSO4、CuSO4、Fe2(SO4)3分别加入基础培养基中,调节其至相应浓度。
1.2 菌株的分离与筛选
用LB液体培养基、牛肉膏蛋白胨培养基分别作液体基础培养基和固体基础培养基。取各个地点的待测土样,分别加入到已经装有无菌水的三角瓶中,在磁力搅拌器上搅拌后,使细菌与土样分离,充分洗脱,静置后取上清液加入到液体培养基中。在摇床上培养10~12h。取培养液涂布到的固体平板上。稀释培养液分别至10-1~10-6,共6种不同梯度,每个样品分别在6个平板培养3~4 d。待菌落长出后,从中选取菌落形态不同的菌种,菌种编号按照1A、1B、1C、1D等,代表1号样品中出现的不同菌种。将初筛得到的细菌分别接种到含Pb(NO3)2的平板上进行培养,设定质量浓度梯度,按50、100、150 mg/L……逐渐递增,经过不断提高铅离子浓度,确定微生物对Pb2+的喜好质量浓度和耐受限度,选择抗性最好的菌株进行培养[9]。
1.3 菌株鉴定
1.3.1 形态学特征观察 通过划线法将筛选得到的菌株接种到基础牛肉膏蛋白胨固体培养基,在恒温培养箱中30 ℃培养40~60 h,对菌落形态及显微镜下菌体细胞的形状进行观察。
1.3.2 16S rDNA基因测序和系统发育学分析 提取抗性菌株基因组DNA,使用通用引物27F/1492R扩增16S rDNA基因序列(27F:5′-AGAGTTTGATCCTGGCTCAG-3′;1492R:5′-GGTTACCTTGTTACGACTT-3′),送生工生物工程(上海)股份有限公司进行全长测序。将获得的序列与NCBI和RDP数据库中的现有数据进行比对,在数据库中选择同源性高的序列,使用MEGA 7.0软件包构建系统发育树以来判断抗性菌种的物种归属[10]。
1.4 菌株对其他重金属离子的耐受性研究
培养菌株,挑单菌落培养于基础LB液体培养基中,在 30 ℃ 、转速为120 r/min条件下培养8~10 h后得培养液。将ZnSO4加入10份牛肉膏蛋白胨固体基础培养基中,使其对应的Zn2+的质量浓度依次为10、20、30、…、90、100 mg/L(每间隔10 mg/L为1个梯度,共10个梯度),同理加入CuSO4、CoCl2、HgCl2、Fe2(SO4)3溶液至牛肉膏蛋白胨固体基础培养基中。在5种重金属不同离子浓度的固体培养基上分别涂布0.2 mL菌株培养液,在30 ℃的下培养3~5 d时间,观察菌落的生长情况[11]。
1.5 菌株吸附Pb2+的条件分析
挑取抗性菌的单菌落,120 r/min、30 ℃,于LB液体培养基中培养至对数期;于3 500 r/min离心10 min后,弃去上清,称量菌体的鲜质量;將离心后的菌体制成一定浓度的定量菌悬液。然后在不同质量浓度的Pb2+的培养基中分别加入 2 mL 菌悬液,在预先设置好的不同条件下吸附后,在 10 000 r/min 条件下离心5 min,上清液用原子吸收分光光度法测定Pb2+浓度(每组做3个重复),设置每组中不加入菌体的组为对照组[12]。按如下公式分别计算菌株对Pb2+的吸附容量q(mg/g)和吸附率Q:
q=(Ci-Cf)/Cb;
(1)
Q=(Ci-Cf)/Ci×100%。
(2)
式中:Ci代表在菌体吸附前的Pb2+的质量浓度,mg/L;Cf代表在菌体吸附后的Pb2+的质量浓度,mg/L;Cb代表吸附剂(菌体)的投加量,g/L,其中,各个数值均按鲜质量计算。
1.5.1 Pb2+质量浓度对吸附效率的影响 设置恒定条件:转速160 r/min、pH值6.0、菌量10 g/L,分别控制Pb2+的质量浓度为100~700 mg/L(每间隔100 mg/L为1个梯度,共7个梯度),在温度30 ℃条件下,振荡30 min,随后取上清液,经过稀释后,测定不同条件下上清液中Pb2+质量浓度。
1.5.2 吸附时间对吸附效率的影响 设置恒定条件:转速 160 r/min、pH值6.0、菌量10 g/L时,Pb2+质量浓度100 mg/L,在温度30 ℃条件下,分别控制振荡时间为5~35 min(每间隔 5 min 为1个梯度,共7个梯度),在吸附后取上清液,经过稀释后,测定不同条件下上清液中Pb2+质量浓度。
1.5.3 pH值对吸附效率的影响 设置恒定条件:转速 160 r/min、菌量10 g/L、Pb2+质量浓度100 mg/L,分别控制pH值至3.0~8.0(每间隔1.0为1个梯度,共6个梯度),在温度30 ℃条件下,振荡30 min,取上清液稀释后测定不同条件下的Pb2+质量浓度。
1.5.4 温度对吸附的影响 设置恒定条件:转速160 r/min、pH值6.0、菌量10 g/L、Pb2+质量浓度为100 mg/L,分别控制温度条件为20~40 ℃(每间隔5 ℃为1个梯度,共5个梯度),振荡30 min,取上清液稀释后测定不同条件下的Pb2+质量浓度。
1.5.5 菌体投加量对吸附的影响 设置恒定条件:pH值 6.0、转速160 r/min、Pb2+质量浓度100 mg/L,控制投加菌量分别为5~35 g/L(每间隔5 g/L为1个梯度,共7个梯度),在温度30 ℃条件下,振荡30 min,取上清液稀释后测定不同条件下的Pb2+质量浓度。
1.5.6 转速对吸附的影响 设置恒定条件:菌量10 g/L、pH值6.0、Pb2+浓度100 mg/L、控制转速分别为100~200 r/min(每间隔20 r/min为1个梯度,共6个梯度),在温度30 ℃条件下,振荡30 min,取上清液稀释后测定不同条件下的Pb2+质量浓度[9]。
2 结果与分析
2.1 耐铅菌株筛选与鉴定
在不断升高培养基的Pb2+质量浓度后,最终经过分离与筛选,得到了能在Pb2+质量浓度最高为700 mg/L培养基中生长的菌株1D,能够在Pb2+质量浓度最高为600 mg/L培养基中生长的菌株8A。
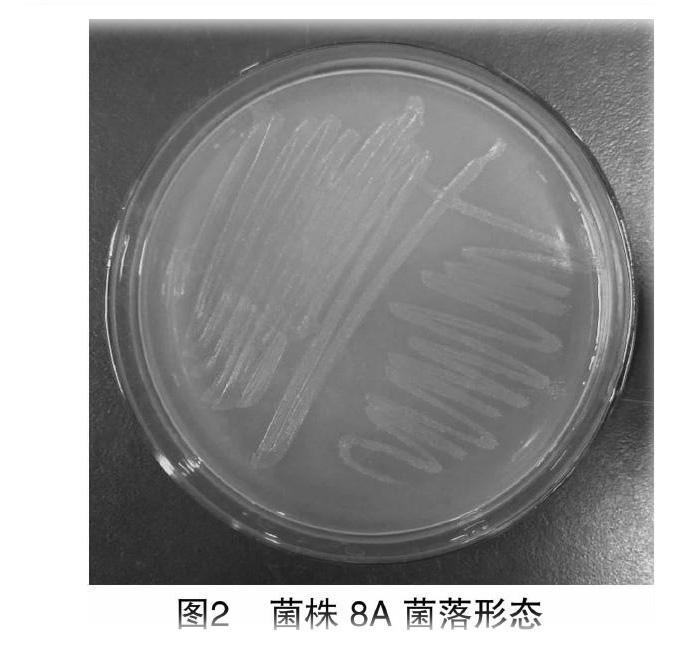
2.1.1 菌落形态特征 菌株1D、8A的菌落形态如图1、图2所示,表1为其菌落特征的描述。
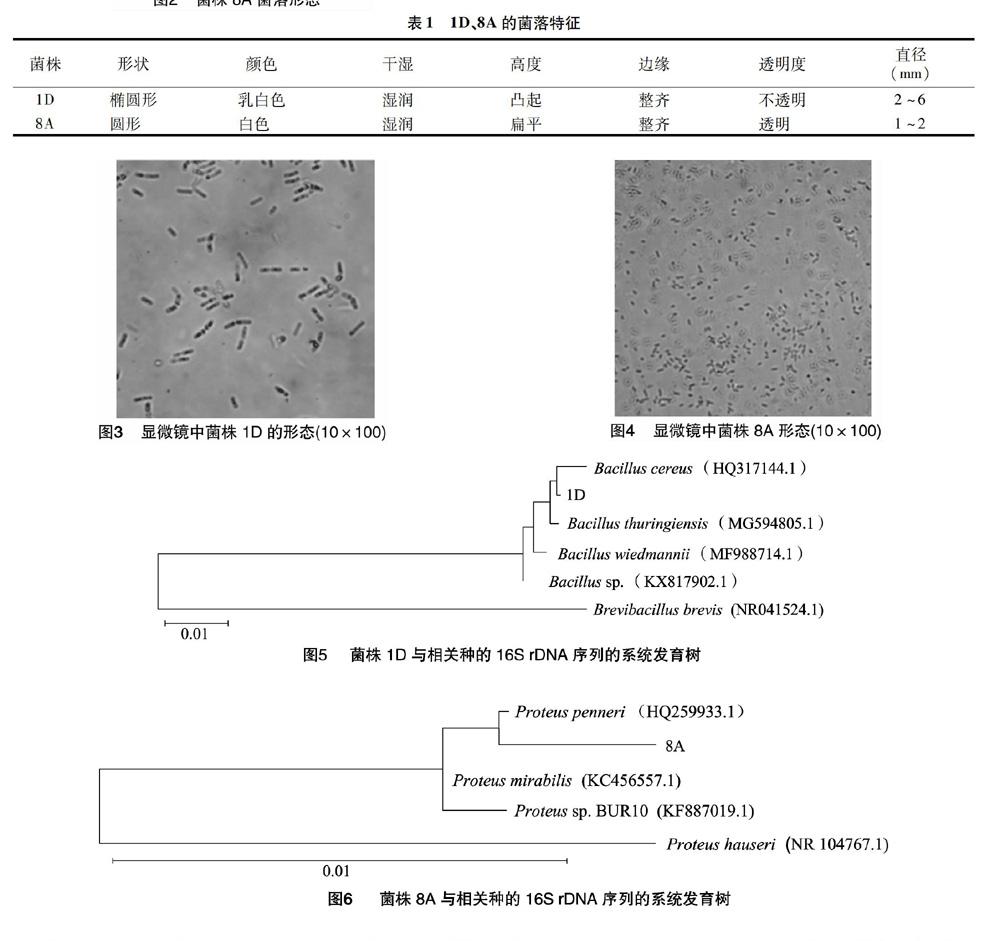
2.1.2 菌体形态、大小、运动性 显微镜下观察发现,菌株1D的菌体细胞呈直杆状,菌体粗壮,周生鞭毛或无鞭毛(图3、图4),其大小为(1.2~1.6) μm×(3.5~4.6) μm,常单生或呈短链状;菌株8A的菌体细胞呈椭圆形短棒状,其大小为(0.5~1.5) μm×(1.2~3.0) μm,具圆端,无芽孢,周生鞭毛,运动活泼。
2.1.3 基于16S rDNA基因序列的菌株分类地位确定 菌株1D、8A的16S rDNA基因序列已提交NCBI的GenBank数据库,登录号分别为MK583952、MK583953。通过将测序所得16S rDNA基因序列与NCBI数据库进行Blast比对,发现菌株1D与Bacillus cereus(GenBank登录号HQ317144.1)具有99.86%的同源性,8A菌与Proteus penneri(GenBank登录号HQ259933.1)具有99.72%的同源性。通过从NCBI下载相关种的16S rDNA序列,应用MEGA 7.0软件包构建了系统发育树[13],建树结果如图5、图6所示。
根据形态学观察结果和16S rDNA序列同源性对比分析以及系统发育树可以判断,菌株1D与蜡样芽孢杆菌(Bacillus cereus)亲缘关系最近,菌株8A与彭氏变形杆菌(Proteus penneri)亲缘关系最近。
2.2 抗性菌株的重金属耐受性分析
2.2.1 对Pb2+的耐受性分析 当固体培养基中Pb2+质量浓度范围在0~400 mg/L时,1D菌的菌落生长情况较好;随着Pb2+质量浓度不断升高,当其质量浓度值超过400 mg/L时,菌株的生长量明显下降,1D的生长受到抑制;当Pb2+质量浓度继续升高,直到升高到700 mg/L时,此时1D的生长几乎完全受到抑制。当固体培养基中Pb2+质量浓度范围在0~300 mg/L 时,8A菌的菌落生长情况较好;随着Pb2+质量浓度不断升高,当其质量浓度值超过400 mg/L时,菌株的生长量明显下降,8A的生长受到抑制;当Pb2+质量浓度继续升高,直到升高到700 mg/L时,此时8A的生长几乎完全受到抑制。
2.2.2 对其他重金属的耐受性分析 采用固体培养基进行菌株对其他重金属耐受性进行分析,菌株1D、8A对Zn2+、Cu2+、Co2+、Fe2+都具有一定程度的耐受浓度,另外2株菌对于Hg2+均无抗性,菌株1D、8A的生長情况见表2、表3。
2.3 吸附条件分析
2.3.1 Pb2+质量浓度对菌株吸附的影响 由图7可以看出,2种菌株都呈现出了随着初始的Pb2+质量浓度升高而吸附率下降的趋势。当Pb2+质量浓度低于一定值时,菌株1D、8A的吸附率变化不明显,吸附容量仍保持在一定水平;当Pb2+质量浓度不断增加超出此浓度值时,吸附率则明显下降,当菌株1D在Pb2+质量浓度升高至700 mg/L时,吸附率仅为36.86%,吸附容量仅为 25.8 mg/g;当菌株8A在Pb2+质量浓度升高至600 mg/L时,菌株8A的吸附率低至10.13%,此时的吸附容量下降至 51.01 mg/g。分析其原因,在较低的初始Pb2+质量浓度条件下,抗性菌株其菌体表面的吸附位点与培养液中的Pb2+之间的相互作用充分,吸附位点的作用效率高,所以有较好的吸附效果;但是伴随着Pb2+质量浓度的不断升高,吸附位点与Pb2+之间的作用不断达到饱和,菌体的Pb2+结合率随之下降[14-15];此外,也有研究表明,重金属的质量浓度过高往往会破坏细胞膜,改变膜的通透性[16],从而影响菌体的吸附作用,最终菌体吸附Pb2+的吸附效果下降。根据本试验所得,菌株1D、8A分别在初始的环境中的Pb2+质量浓度为600、300 mg/L时吸附Pb2+的效率最高。
2.3.2 吸附时间对菌株吸附的影响 由图8可见,菌株1D,菌株8A在吸附时间为5 min时,其菌株的吸附率已高达91.43%和96.43%,从而可见,菌株的吸附是一个快速的过程。同时,也有有相关试验表明,菌体在其吸附的最初阶段往往速度很快,并且几乎不消耗能量[17]。另外,随着吸附时间的延长,对于菌株1D吸附Pb2+几乎没有影响,但相对菌株1D,菌株8A受吸附时间影响较大,菌株8A在吸附时间为 5 min 时,吸附率达到最大值96.43%。菌株8A在25 min后,随着时间的增加,吸附率和吸附容量都有一定程度下降,表明菌株8A在吸附过程中还存在着与吸附位点解吸的现象[18]。又因为在25~35 min期间,菌株8A的吸附率下降了38.70%,猜测菌株8A的吸附多为菌体的表面吸附[12,19-20]。
2.3.3 pH值对菌株吸附的影响 在研究pH值对吸附的影响时,考虑到当金属离子在pH值过高条件下,离子沉淀严重,故试验中设计值pH值<8。pH值对菌体的胞外聚合物(EPS)吸附溶液中的重金属离子具有极其重要的影响[21]。由图9可知,pH值对2种菌株吸附Pb2+的影响较为一致,在pH值=3~5时,均呈现随着pH值的增加吸附率逐渐升高的趋势。当pH值>5时,菌株1D吸附率随pH值的增加稍有下降而后又趋于稳定;当pH值=7时,菌株8A吸附率达到最大值随后下降。当溶液pH值较低时,菌体的吸附率伴随着pH值的增大也随之增大。因为此时H+的浓度高,大量的H+会与重金属Pb2+竞争菌体表面的吸附结合位点,从而影响了菌株的吸附性[14]。另外,溶液中的pH值过高同样不利于细菌的吸附作用,当pH值过高时,Pb2+容易形成其氢氧化物沉淀Pb(OH)2,从而影响吸附效果,使吸附率降低[22]。因此,综合考虑pH值对Pb2+吸附的影响,菌株1D在试验中的最适pH值为5,菌株8A的最适pH值为7。
2.3.4 温度对菌株吸附的影响 图10中,温度在对2种菌株吸附Pb2+的影响中呈现出了相反的趋势,随着温度增加,菌株1D的吸附率呈现不断增加的趋势,在35 ℃时达到最大的吸附率97.76%,到40 ℃时,菌株1D吸附率有所降低,吸附容量有所减少。而菌株8A,随着温度增加其对Pb2+的吸附能力逐渐下降,在温度为20 ℃的条件下,菌株8A的吸附率为最大值,此时的菌株8A最大吸附率为95.98%。所以,菌株1D的吸附温度在35 ℃较为适宜,菌株8A的吸附温度在20 ℃较为适宜。分析温度对菌株吸附影响的原因,温度不仅会影响细菌的代谢,还会对其与金属离子的结合产生影响,当温度处于最适温度时,细菌的代谢为其主动吸附Pb2+的这一过程提供了能量,故有益于吸附效果;在温度条件不合适时,一方面影响细菌的正常代谢,导致相应的生理功能无法充分发挥,从而影响了菌体的吸附能力;另外还会对菌体和已经与菌体结合的金属离子两者之间结合的稳定性造成不利的影响[14]。
2.3.5 菌体投加量对菌株吸附的影响 从图11可见,菌体投加量的增加对于菌株8A对Pb2+的吸附率几乎没有影响;对于菌株1D,随着菌体投加量的不断增加,对Pb2+的吸附率也是不断升高,在菌体投加量为30 g/L时,吸附率达到最大值为95.82%,综合考虑吸附率的变化,菌株1D最佳的菌体加入量为25~30 g/L。对于菌株1D来说,可能在某种限定的金属离子浓度中,随着菌体投加量的增大,之前没有充分吸附完毕的菌体,此时由于个体的增加导致更多的菌体去和金属离子吸附结合,因而吸附率上升[23]。而菌株8A随着菌体投加量的增大,吸附率几乎保持不变。可能是由于在较低的金属离子浓度下,8A菌体已经与金属离子充分结合,此时即使再加入更多的菌体,也没有多余的金属离子与随后的菌体结合,所以吸附率不变[24];而后来的菌体则会与先前的菌体产生竞争,彼此阻碍从而导致整体吸附能力下降,这可能是导致菌体8A的吸附率曲线在20 g/L后稍有下降走势的原因。
2.3.6 转速对菌株吸附的影响 从图12中可以看出,菌株1D的吸附率随着转速增加呈现出不断升高的趋势,当转速升高至180 r/min时,其吸附效率达到最高,此时的吸附率是96.77%。菌株8A最初随着转速升高吸附率不断增加,当转速范围为120~180 r/min时,菌体8A吸附Pb2+的效果最佳,此时2种菌吸附率高达95.89%~96.87%。另外,2种菌在所设定的转速升高至180 r/min以上时,菌体的吸附率分别会有不同程度的下降,其中在200 r/min时,菌株1D的吸附率下降更为明显。这可能与Pb2+吸附传质速度等原因有关,Pb2+吸附传质速度因转速的增大而加快,在一定的转速范围内吸附率增加;但当吸附液的转速过大时,Pb2+传质速度过快,此时却难以对Pb2+再进行有效的吸附[25]。菌体吸附不仅有化学吸附还包括物理吸附,包括高转速造成的静电吸附,以及金属离子在高速旋转下在菌体的表面沉积等[14]。
3 结论与讨论
在南四湖底泥采集的土壤中,最终分离筛选出了2株耐铅菌株,其中菌株1D与蜡样芽孢杆菌(Bacillus cereus)亲缘关系最近,菌株8A与彭氏变形杆菌(Proteus penneri)亲缘关系最近。经过对它们耐受性与吸附能力的分析,得到菌株1D最大铅耐受质量浓度为700 mg/L,菌株8A最大铅耐受质量浓度为600 mg/L。
经过吸附性能测试,菌株1D在35 ℃、pH值=5、Pb2+质量浓度为100 mg/L、菌体投放量为30 g/L、转速为180 r/min、吸附时间为15 min时吸附效率最高,吸附Pb2+的效果最好;菌株8A在20 ℃、pH值=7、Pb2+质量浓度为300 mg/L、菌体投放量为 20 g/L、转速为180 r/min、吸附时间为5 min时吸附效率最高,吸附Pb2+的效果最好。
另外在菌株对其他重金属的耐受性分析中,菌株1D对Zn2+、Cu2+、Co2+、Fe2+的耐受质量浓度分别为40、80、40、90 mg/L,菌株8A对Zn2+、Cu2+、Co2+、Fe2+的耐受质量浓度分别为30、80、40、90 mg/L,且2株菌对于Hg2+均无抗性。
土壤或湖泊底泥中的细菌,往往具有种类丰富、繁殖周期短、在短时间内可以获得大量丰富菌体的特点[26-27],应该重视细菌等微生物对重金属离子的吸附作用[28],从而利用筛选到的对特定重金属存在抗性的菌种来有效防治受重金属污染的土壤。本试验中,最终筛选到的菌株抗铅性能高、对铅离子的吸附性好,丰富了重金属污染土壤微生物修复的生物资源库,同时对于吸附特性的研究又可以为抗重金属菌株特别是抗铅菌株的筛选提供参考及理论依据[29]。
参考文献:
[1]杨丽原,沈 吉,张祖陆,等. 南四湖表层底泥重金属和营养元素的多元分析[J]. 中国环境科学,2003(2):95-98.
[2]王晓军,潘恒健,杨丽原,等. 南四湖表层沉积物重金属元素的污染分析[J]. 海洋湖沼通報,2005(2):22-28.
[3]刘恩峰,沈 吉,王建军,等. 南四湖表层沉积物重金属的赋存形态及底部界面扩散通量的估算[J]. 环境化学,2010,29(5):870-874.
[4]刘 良,张祖陆. 南四湖表层沉积物重金属的空间分布、来源及污染评价[J]. 水生态学杂志,2013,34(6):7-15.
[5]张智慧,李 宝,梁仁君. 南四湖南阳湖区河口与湖心沉积物重金属形态对比研究[J]. 环境科学学报,2015,35(5):1408-1416.
[6]王云倩,曹霏霏,顾聪敏,等. 南四湖的水环境问题研究[J]. 江苏师范大学学报(自然科学版),2014,32(2):7-11.
[7]刘 莹,董文平,刘 鹏,等. 南四湖主要入湖河流水环境质量状况及风险评估[J]. 科技导报,2017,35(9):56-61.
[8]蒋万祥,田忠景,陈 静,等. 微山湖水域重金属分布特征及水质评价[J]. 淡水渔业,2012,42(4):66-70.
[9]金 羽,曲娟娟,李 影,等. 一株耐铅细菌的分离鉴定及其吸附特性研究[J]. 环境科学学报,2013,33(8):2248-2255.
[10]Tamura K,Dudley J,Nei M,et al. MEGA 4:molecular evolutionary genetics analysis (MEGA) software version 4.0[J]. Molecular Biology Evolution,2007,24(8):1596-1599.
[11]蔡佳亮,黄 艺,礼 晓. 生物吸附剂对污染物吸附的细胞学机理[J]. 生态学杂志,2008(6):1005-1011.
[12]任广明,曲娟娟. 铅抗性细菌的分离及吸附性能研究[J]. 东北农业大学学报,2010,41(2):55-60.
[13]龙建友,罗定贵,陈永亨. 一株Tl+抗性菌株的鉴定及吸附特性[J]. 应用与环境生物学报,2014,20(3):426-430.
[14]张 敏,郜春花,李建华,等. 一株耐铅土著微生物的吸附特性及机制研究[J]. 山西农业科学,2018,46(8):1321-1328.
[15]徐雪芹,李小明,杨 麒,等. 丝瓜瓤固定简青霉吸附废水中Pb2+和Cu2+的机理[J]. 环境科学学报,2008(1):95-100.
[16]郭金英,史明科,赵艳丽,等. 发状念珠蓝细菌细胞对Cu2+、Cr2+和Pb2+胁迫的响应[J]. 微生物学报,2013,53(6):553-560.
[17]Volesky B. Detoxification of metal- bearing effluents:biosorption for the next century[J]. Hydrometallurgy,2001,59(2/3):203-216.
[18]李 冉,歐 杰,代启虎,等. 植物乳杆菌对重金属Pb2+、Cr6+和Cu2+的耐受性与吸附作用相关性比较[J]. 微生物学杂志,2019,39(1):52-58.
[19]许旭萍,沈雪贤,陈宏靖. 球衣菌吸附重金属Hg2+的理化条件及其机理研究[J]. 环境科学学报,2006(3):453-458.
[20]陈永华,向 捷,吴晓芙,等. 三株耐铅锌菌的分离、鉴定及其吸附能力[J]. 生态学杂志,2015,34(9):2665-2672.
[21]曾远 . 铅锌矿区土壤中特异性微生物吸附转化铅机理研究[D]. 北京:中国地质大学(北京),2017.
[22]刘瑞霞,潘建华,汤鸿霄,等. Cu(Ⅱ)离子在Micrococcus luteus细菌上的吸附机理[J]. 环境化学,2002(1):50-55.
[23]Zumriye A. Biosorption of reactive dyes by dried activated sludge:equilibrium and kinetic modeling[J]. Biochemical Engineering Journal,2001,7(1):79-84.
[24]张晓青,杜 瑾,曹军瑞,等. 一株耐铅菌株NY-3的分离鉴定及其吸附特性研究[J]. 生物技术通讯,2018,29(6):783-788.
[25]Yalcin S,Sezer S,Apak R.. Characterization and lead (Ⅱ),cadmium(Ⅱ),nickel(Ⅱ) biosorption of dried marine brown macroalgae Cystoseira barbata[J]. Environmental Science and Pollution Research,2012,19(8):3118-3125.
[26]赵 帆,赵密珍,王 钰,等. 草莓不同连作年限土壤养分及微生物区系分析[J]. 江苏农业科学,2017,45(16):110-113.
[27]钱 玮,朱艳霞,邱业先. 太湖底泥中聚磷菌多样性的垂直分布[J]. 江苏农业科学,2017,45(3):221-224.
[28]Mohamedy M,Ghazy M A,Sayeda,et al. Isolation and characterization of a heavy metal-resistant,thermophilic esteraserom a Red Sea brine pool[J]. Scientific Reports,2013,28(3):3350-3358.
[29]Kaplan H,Raterings,Hanauer T,et al. Impact of trace metal contamination and in situ remediation on microbial diversity and respiratory activity of heavily polluted kastanozems[J]. Biology and Fertility of Soils,2014,50(5):735-744.
