将化学史引入课堂教学的探索
2019-10-22黄谦
黄谦


摘要:原电池原理的发现和利用是近代化学的一个重要事件。作者在高中化学课堂教学中以这一探索发现过程为线索,适当引入化学史的教学,对新课程改革中提升学生化学学科核心素养做出尝试。
关键词:原电池;探索;学科核心素养;化学史教学
文章编号:1008-0546(2019)09-0031-03
中图分类号:G632.41
文献标识码:B
doi: 10.3969/j .issn.1008-0546.2019.09.009
高中化学学科核心素养是高中学生发展核心素养的重要组成部分,是学生综合素质的具体体现,反映了社会主义核心价值观下化学学科育人的基本要求,全面展现了化学课程学习对学生未来发展的重要价值。化学学科核心素养包括“宏观辨识与微观探析”“变化观念与平衡思想”“证据推理与模型认知”“科学探究与创新意识”“科学态度与社会责任”5个方面。我们的课堂教学,偏重于教材知识的传授和基本技能的训练,学生更多地掌握了一些能够应付考试的知识,通过大量、反复的练习提高了自己的应试能力。但是对化学这门学科的来龙去脉却没有一个较为全面的认识。做为教师,我们有责任在课堂上向学生介绍一些化学发展的历史。在教学中渗透化学史的探索故事、探索精神、探索思路,对于培养学生的化学学科核心素养大有裨益。
一、问题提出
当前化学史教育在课堂教学中的应用主要如下:①开阔学生视野,活跃课堂气氛;②以化学家献身科学、探索过程的曲折和艰辛进行情感态度价值观的教育。这些做法存在的问题是:教师讲少了,学生接触到的化学史内容是零碎的,很难系统化。讲简单了,就难以体现化学发现的艰辛和逻辑思维的力量。比如,讲到苯的结构式发现历史的时候,大多数老师都是说凯库勒做了一个梦然后恍然大悟,得到了苯的分子结构。然后强调“以事实为依据,以严肃的科学态度进行多方面的分析和探讨,这一切都为他取得成功奠定了基础”。但是这样又过于笼统,学生很难有深刻的认识。其三,化学史讲得太过详细,课时又不够,同时也冲淡了每节课的教学目标和教学重点。
二、问题思考
以化学史的发现为主线,在探索中组织课堂教学。让学生在问题的层层推进中不断思考探索,体会前人的探索历程。
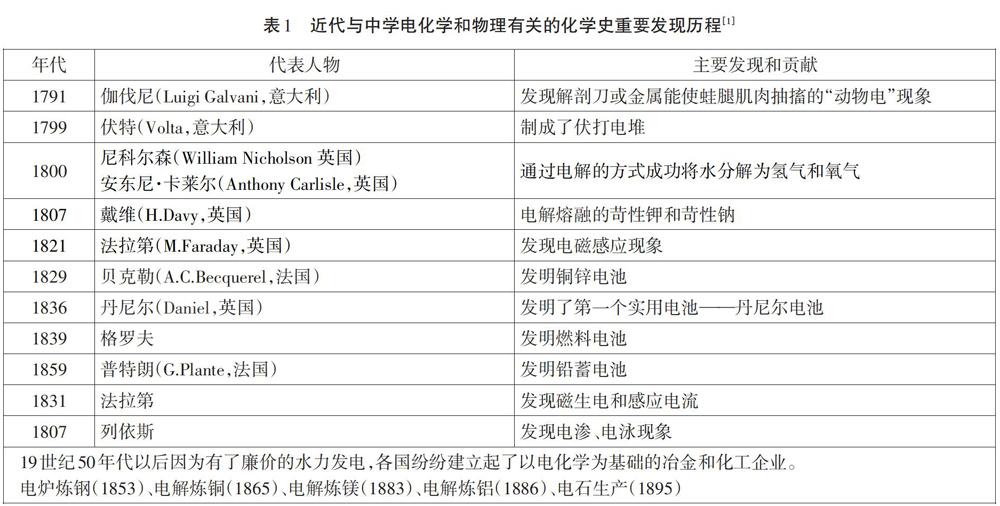
本文以“原电池”的教学设计来做探讨。提炼电化学发展历程中与中学化学教学有关的重要事件和节点(表1),设计各环节的教学思路和方法,以人类对于电化学认识的历程为主线,层层推进,达成过程与方法、知识与能力、情感态度价值观的统一。
三、课堂探究
1.原电池实验的引入
这是一个学生非常熟悉的实验。教师准备好导线、灵敏电流计、番茄、铜片、锌片。组装成如图1所示的番茄电池。
实验中最显著的现象就是灵敏电流计指针发生了偏转。显示本实验中有电流产生并且通过。课堂讨论由此开始。
是不是番茄内部带有电呢?
事实上,1780年,意大利解剖学教授伽伐尼在一次解剖青蛙中,获得了一个偶然的发现。当时,他将剥去皮的青蛙放在实验桌上的金属板上,金属板在起电机的旁边。他的妻子在取一把解剖刀时偶然触及了青蛙的腿神经。这时起电机刚好打出一个火花,同时,青蛙的腿猛烈地抽搐了一下。
是不是蛙腿带电呢?
他立即抓住这一现象重复这个实验,不但又观察到了同样的结果,而且还发现了用金属接触青蛙神经才有电火花。之后他又以严谨的科学态度,选择各种不同的条件,在不同的天气重复这类实验,青蛙的腿都能发生痉挛。以后他又用各种不同的物体做实验,但是当用玻璃、橡胶、松香、石头和干木头等代替金属导体时,就不发生上述现象。针对这些现象,伽伐尼猜想,在动物体内存在着某种电,如果使神经和肌肉同两种不同的金属相接触,再使这两种金属相连接,这种电就会被激发出来,所以这很可能是从神经传到肌肉的特殊的“电流质”引起的“动物电”。
2.原电池原理及构成
【探究实验一】将Zn片、Cu片分别插入H2S04溶液中,有什么现象?为什么?
【探究实验二】用导线把实验一中的锌片和铜片用导线连接起来有什么现象?为什么? 学生通过观察发现:实验一中锌与稀硫酸发生置换反应,锌片表面产生气泡,同时试管发热。学生已经有了氧化还原反应本质的认识,明确该反应中有电子的得失。实验二中学生很快发现铜片表面产生气泡这一最明显的现象。如果此时用灵敏电流计接在铜锌之间的导线上,会发现指针偏转,显示有电流通过。显然,这样的装置与番茄或是蛙腿没有任何关系,无论是“动物电”还是“番茄电”都是不存在的。伽伐尼的解释在历史上曾经引发了长达10年之久的学术争论,并直接促成了伏打电池的发明。
意大利物理学家伏特在自己的實验室无数次地重复伽伐尼的实验。但是,他的注意力主要集中在那一对金属片上而不是蛙腿上。实验证明,只要两种金属片中间隔有用盐水、或者碱液浸泡过的纸张、布匹,并用导线将两种金属连接起来,不管有没有蛙腿,都有电流产生。伏特在自己的发现的基础上终于发明了具有实用价值的伏打电堆。为此当时还受到了拿破仑的特别嘉奖。
在实验二潜在的电子转移过程中,建立了有序的电子转移路径从而改变了能量的转换形式。原先实验一中化学能到热能的转换在实验二中绝大多数变成了化学能到电能的转换。从而说明有电子转移的氧化还原反应确实构成了一种将化学能转化为电能的装置,这就是原电池。
归纳总结原电池的构成条件:活泼性不同的两个电极、有电解质溶液、构成闭合回路、有自发的氧化还原反应。
3.电池的发展
学生在实验二中实际上是会有困惑的。根据原电池原理,做为正极的铜片表面产生气泡,做为负极的锌片应该仅有逐渐溶解这一很不明显的实验现象。但是实际情况是不仅铜片表面有大量气泡,锌片表面也有大量气泡。事实上,由于锌片表面产生气泡,使得早期的伏打电堆的效率很低。
对实验二进行微观分析。在原电池反应发生过程中,锌片表面的H+并不会立刻消失,而是围绕在锌片周围,这就导致了锌与H+的置换反应必然要发生。也正是由于该置换反应在锌片表面直接发生,导致了原先往铜片有序转移的电流效率的降低。
如何才能让原电池反应依旧发生,同时采取措施赶开锌片表面的H+,提高电池的电流效率?学生对此继续展开探讨。在教师的引导下,学生将铜锌稀硫酸原电池的各部分逐一拆开,再重新组装研究。经历了下图的四个研究步骤。
从①到②是为了赶开锌片表面的H+。从②到③发现缺少了闭合回路这一条件,于是教师引导加了盐桥。从③到④是升级版,自由电子从锌片表面经过导线到了铜片表面上,在③装置中H+在铜片表面得到电子放出氢气。放出氢气会导致电池体积庞大且安全系数降低,故不易推广。但是正极上必须发生还原反应构成原电池的另一个半反应。照此思路,装置④用Cu2+代替H+继续实验,得到很好的效果。
1836年英国科学家丹尼尔为了提高伏打电堆的电流效率研发了一种新的实用性电池。后人为纪念他的成就,将这种电池命名为丹尼尔电池。今天同学们所经历的探讨、想象、实验在不经意间重温了丹尼尔当年所走过的路。从丹尼尔电池研发问题的提出,到研发过程中解决问题的思路,同学们在教师的引领下,领略了化学史发展道路上的别样风景[2]。
人们研究化学的历史过程在宏观上反映了科学认识发展的逻辑规律。循着人类前行的足迹,我们踽踽而行。每一次的交汇仿佛是与前人发生了思维的碰撞。我们以化学史的发现为主线,在探索中组织课堂教学,让学生在问题的层层推进中不断思考探索,体会前人的探索历程。他们走过的弯路、他们考虑问题的方式、他们的成功或者失败带给我们的启发无不照亮了新时代的我们学习化学、探究化学的前行道路。“教育所给予人们的无非是当一切已学过的东西都忘记后所剩下来的东西”。化学核心素养就是化学学科所赋予学生最有价值的宝贵财富。
参考文献
[l] 白建娥,刘聪明.化学史点亮新课程[M].北京:清华大学出版社,2012:160-161
[2]江敏,发现人类思维的脉络——“原电池”教学实践与思考[J].中学化学教学参考,2014(12):1,5-9