CT 引导下蝶腭神经节低温等离子射频消融治疗蝶腭神经痛的临床研究
2019-10-22郭玉娜杨光辉刘京杰唐元章杨立强
郭玉娜 窦 智 杨光辉 刘京杰 王 琦 唐元章 杨立强▲
1.首都医科大学宣武医院疼痛科,北京 100053;2.中国人民解放军66011 部队门诊,北京 102600
蝶腭神经痛(sphenopalatine neuralgia,SPN)是临床上比较罕见的头面部疼痛,发病率仅0.4‰~0.8‰[1],1908 年由Sluder[2]首次提出,因而又被称为Sluder 综合征。原发性SPN 临床表现多为一侧眶周、眼球后方、颞部、鼻腔、上颌等部位的剧烈疼痛,以胀痛、电击样痛为主,可放射至同侧枕部、耳部及乳突,位置深在且弥散。部分患者疼痛发作有一定的季节或时间规律性,发作时常伴有同侧鼻塞、结膜充血、流泪等副交感症状,影像学检查少有异常发现[3-4]。临床常用的治疗手段包括口服药物、蝶腭神经节(sphenopalatine ganglion,SPG)阻滞、化学毁损、射频热凝以及SPG 切断术等,其中,SPG 射频热凝术因其微创、效果确切,目前临床应用最为广泛,但也存在毁损范围小、易复发、以及面部麻木等不足[5]。首都医科大学宣武医院(以下简称“我院”)疼痛科在CT 引导下SPG 射频热凝术的基础上,采用低温等离子射频消融替代射频热凝,实现蝶腭神经节的低温毁损,以期达到更加理想的毁损效果,同时减少面部麻木的发生率及严重程度。
1 资料与方法
1.1 一般资料
选择2015 年1 月~2016 年8 月在我院疼痛科接受低温等离子射频消融治疗的61 例原发性SPN 患者为研究对象。其中男28 例,女33 例;年龄18~72 岁,平均(47.2±12.4)岁;病程3 个月~32 年,平均(13.6±11.5)年;每次发作持续(33.6±31.9)min;疼痛视觉模拟评分(VAS)(7.9±1.5)分。本研究经我院医学伦理委员会审核通过,所有患者均知情同意并签署知情同意书。
1.2 纳入及排除标准
1.2.1 纳入标准 患者诊断均符合国际疼痛协会(IHS)公布的SPN 诊断标准[6];经口服药物等保守治疗3 个月,症状无明显改善。
1.2.2 排除标准 头颅及鼻旁窦MRI、眼眶CT 检查明显异常者;凝血功能障碍或正在接受抗凝药物治疗者;穿刺部位有感染者;颅脑损伤及肿瘤、鼻窦、副鼻窦炎及鼻中隔偏曲者;哺乳及妊娠期妇女;存在社会-精神-心理因素的患者及不能配合者。
1.3 方法
1.3.1 术前准备 完善常规检查,60 岁以上患者术前30 min 给予抗生素预防感染。监护心电图、血压、心率和血氧饱和度。静脉给予氟哌利多(上海旭东海普药业有限公司,批号:31807051,2.5 mg 静推)、舒芬太尼(宜昌人福药业有限公司,批号:1180428,10 μg 静推)以及阿托品(天津金耀氨基酸有限公司,批号:180305-1,0.5 mg 静推)等术前药。
1.3.2 手术方法 患者取仰卧位,颈下垫一薄枕。采用颧弓中点入路,以1.0 mm 层厚进行CT 扫描,寻找蝶骨翼突外侧板及其前缘的翼腭窝周围结构,显示翼腭窝[5]。消毒铺巾,利多卡因浸润后,使用22 G、10 cm 穿刺射频套管针刺破皮肤,沿扫描定位的穿刺路线及角度进针,确定穿刺针进入翼腭窝后,拔出针芯,置入等离子刀头,连接低温等离子射频消融仪。在1 档热凝(Coagulation)模式下,轻踩刺激,测试患者对刺激的反应,并进一步微调刀头位置,以复制出患者的疼痛,确保刀头位于蝶腭神经节附近(图1)。测试成功后,充分给氧去氮,根据患者的体重及体质给予丙泊酚静脉麻醉。在3 档低温消融(Coblation)模式下消融,每个周期10 s,共4~6 个周期。术后拔出等离子刀头及穿刺针,粘贴无菌敷料。所有操作均由具备低温等离子射频消融术资质的高年资主任医师进行,以尽可能避免因技术问题造成临床数据结果的偏差。
所有手术均使用西安高通低温等离子体多功能手术系统,设备型号为SM-D380C,配套等离子刀头型号DXR-G0900-A105。
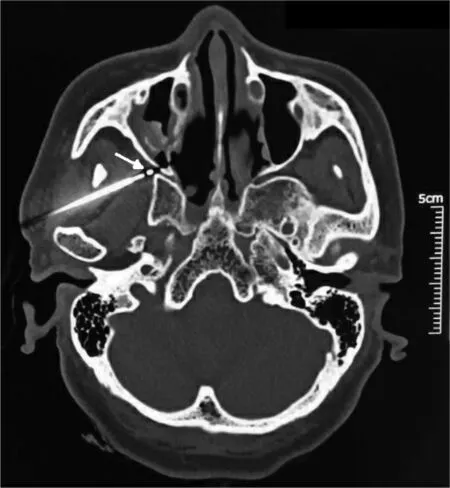
图1 蝶腭神经节低温等离子射频消融术中CT 扫描图像
1.4 疗效评价标准
记录患者术前一般情况:性别、年龄、病变位于左/右、病程、每年发作次数、每次持续时间、术前发作时VAS、缓解期VAS 评分;是否有夜间痛,与季节变化有无关系;是否伴有结膜充血、流泪、流涕等副交感症状等。
分别记录患者术前及术后1 d、3 d、1 周、1 个月、3 个月、半年、1 年、2 年的VAS 评分;术后1 周、1 年的面部麻木程度。疼痛VAS 评分范围0~10 分,0 分表示无痛,10 分表示有难以忍受的疼痛。VAS 评分降低>3 分认为治疗有效[7]。麻木评分范围0~10 分,0 分为基本无麻木,10 为无法忍受的麻木,其中1~3 分为轻度麻木,4~6 分为中度麻木,7~10 分为重度麻木。分别于术后1 周和术后1 年采用改良的MacNab 评分量表(优、良、中、差)评价患者的主观满意度,MacNab评定标准,优:疼痛完全缓解,工作生活恢复正常;良:疼痛明显改善,工作生活基本恢复正常,有时仍出现疼痛,不用口服止痛药物;中:疼痛部分缓解,常需用止痛药,难以正常工作,发作期间自理受限;差:疼痛基本无缓解,需服用强效镇痛药及抗癫痫药,发作期间生活不能自理。记录患者手术并发症,如出血、面部肿胀、颅内感染等。
1.5 统计学方法
采用SPSS 19.0 统计学软件进行数据分析,计量资料用均数±标准差(±s)表示,两组间比较采用t 检验;计数资料用率表示,组间比较采用χ2检验,等级资料采用Mann-Whitney 检验。以P <0.05 为差异有统计学意义。
2 结果
2.1 术后随访情况
61 例患者中,共有10 例患者失访,3 例在半年后疼痛复发,口服加巴喷丁效果不佳,再次行蝶腭神经节低温等离子射频消融术后疼痛消失。随访期间失访及疼痛复发的患者均按照最后一次随访时VAS 评分计入随访结果。
2.2 手术前后患者VAS 评分比较
61 例患者中,59 例术后疼痛均有明显缓解,有效率达96.7%。患者术后1 d、3 d、1 周、1 个月、3 个月、6 个月、1 年、2 年的VAS 评分均明显低于术前(P <0.05),术后各随访时点之间VAS 评分差异无统计学意义(P >0.05)。见表1。
表1 手术前后患者VAS 评分比较(分,±s)
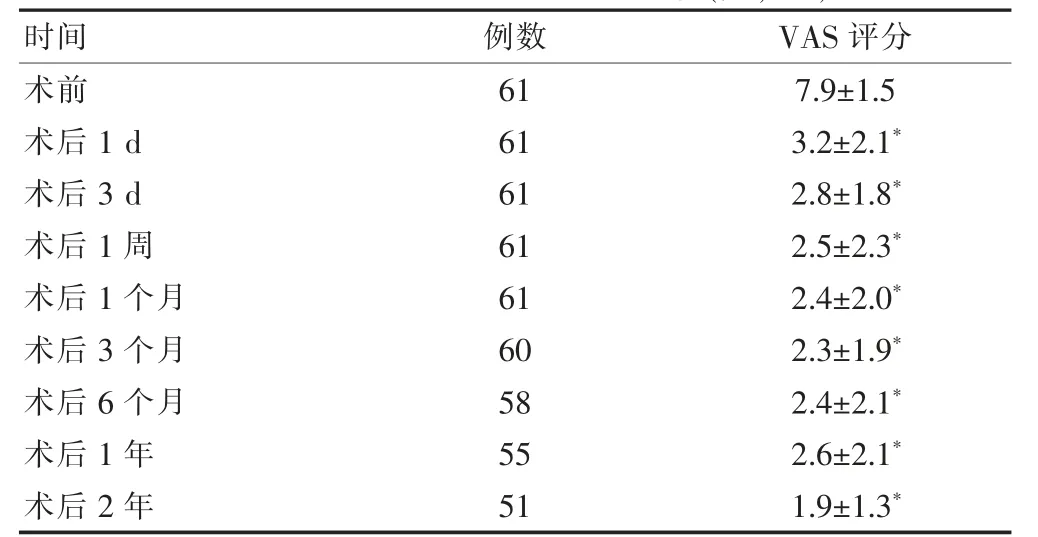
表1 手术前后患者VAS 评分比较(分,±s)
注:与术前比较,*P <0.05。VAS:视觉模拟评分
2.3 患者术后面部麻木程度及满意度
61 例患者中,术后1 周出现轻度麻木者19 例(31.1%),麻木评分为(2.2±1.5)分,术后1 年麻木发生率为0。患者术后1 年的MacNab 评分与术后1 周比较,差异无统计学意义(P >0.05),见表2。术后1 周随访的61 例患者中MacNab 评分为优或良者56 例(优良率为91.8%),术后1 年随访的55 例患者中Mac-Nab 评分为优或良者46 例(优良率为83.6%)。术后2 例患者出现穿刺部位肿胀,冰敷后缓解消失。所有患者术中及术后均无颅内感染及其他严重手术并发症发生。
3 讨论
原发性SPN,是指在没有器质性病变,经过头颅CT、MRI 等系统检查,仍查不出确切病因的SPN。SPG有3 个神经根,感觉根来自三叉神经的上颌支,副交感根来自面神经分出的岩大神经,交感根来自颈动脉丛及岩深神经纤维。该神经节发出许多小分支,分布于眼眶、泪腺、鼻腔蝶窦、上颌窦及口腔内硬腭、软腭、上齿龈、咽部等处的黏膜,支配一般感觉、腺体分泌、小血管运动和泪腺分泌[8]。疼痛发作存在季节周期性是SPN 的典型特征[9]。
SPG 作为头颈部最大的副交感神经节,位于中鼻甲水平鼻腔外侧壁的翼腭窝内。翼腭窝呈一狭长的漏斗形间隙,其前方是上颌窦,后方是翼突内侧板,内侧是颚骨垂直板,下方是蝶骨,部位深在、空间狭小、难于到达[10]。因此,通过影像定位准确地穿刺是提高介入治疗效果和降低副作用的关键[11],螺旋CT+三维重建,能够清晰地显示翼腭窝及其通道的形态结构,骨结构及周围组织的毗邻关系。本研究在CT 引导下完成SPG 的穿刺,穿刺针成功率达到100%[12-13]。胡玉婷等[14]、李培等[15]研究发现翼腭管内壁骨质多数较薄,甚至有程度不一的骨质缺损,因此进针不能过于粗暴,以免穿透骨壁,严重者可引起颅内感染,这也是该手术最严重的并发症[9]。同时翼腭窝内有上颌神经、上颌动脉经过,选择最佳的穿刺路径可以避免对其造成损而导致上颚感觉减退、麻木及颅内出血[16]。本研究中无一例患者出现出血、感染、鼻黏膜损伤等并发症。
本研究发现,低温等离子射频消融治疗起效快,术后疼痛迅速缓解,有49 例(80.3%)患者术后1 周可停服各种镇痛药。有8 例(13.1%)患者术后疼痛程度减轻,发作次数减少,术前口服药物减量服用可控制疼痛。3 例患者半年后疼痛复发,二次手术后疼痛消失。本研究发现61 例患者中,有19 例术后1 周出现轻度麻木,发生率为31.1%,可能与等离子射频消融后,紧邻蝶腭神经节上方的上颌神经炎症水肿有关[17]。这些患者的面部麻木均在术后1 年内消失。有3 例患者疼痛仅轻度缓解,考虑可能与SPG 跟其他周围神经存在交联有关。SPG 还发出许多细小的神经分支与枕小神经、颈神经皮支相互交联,诱发头部、颈部等部位的疼痛[18]。
微创介入手术是保守治疗无效的原发性SPN 患者首选的治疗方式,既往主要以射频热凝的方式进行毁损。但是SPG 临近部位神经丰富,热凝容易造成周围其他神经的热损伤,而且SPG 与上颌神经之间存在交通支,热凝后面部麻木的发生率极高[5]。低温等离子消融术广泛应用于耳鼻喉科,其工作原理是通过一个直径1 mm 的双极射频等离子刀头,将射频能量作用在导电介质上,在等离子刀头周围形成由高度电离的粒子组成的低温离子薄层(钠离子),粒子可获得足够动能打断蝶腭神经节组织细胞间的分子键,实现消融蝶腭神经节的效果[19]。与射频热凝术75℃以上的热凝毁损温度相比,整个低温等离子消融过程中刀头温度维持在70℃,刀头1 mm 之外的区域,温度即降为40℃,所以是一种低温(40~70℃)消融技术,可有效减少周围组织损伤[20]。鉴于SPN 发病率极低,因此本研究尚存在样本量偏低、观察期偏短的不足,应当在未来研究中进一步完善。
综上所述,CT 引导下蝶腭神经节低温等离子射频消融术治疗原发性SPN,患者可获得较为满意的临床疗效,且除自限性的面部麻木外其他不良反应轻微,值得在临床推广。
