Varian 23EX加速器固定剂量率旋转调强技术的Portal Dosimetry验证
2019-10-22王杰邵凯南陈鹏曾嵘姜琦郑士明闵旭红
王杰,邵凯南,陈鹏,曾嵘,姜琦,郑士明,闵旭红
1.安徽省胸科医院肿瘤放疗科,安徽合肥230022;2.浙江省肿瘤医院放射物理室,浙江杭州310022
前言
调强放射治疗目前已经成为我国大部分医院针对恶性肿瘤的主要治疗方式之一。旋转调强或容积调强技术(Volumetric Modulated Arc Therapy,VMAT)因能够获得更好的剂量分布和更高的执行效率,逐渐成为目前的主流趋势。VMAT技术可分为固定剂量率旋转调强(Constant Dose Rate VMAT,CDRVMAT)和可变剂量率旋转调强(Variable Dose Rate VMAT, VDR-VMAT)[1]。CDR-VMAT 相较于VDRVMAT 可调制参数少,计划质量和执行效率略差,但在靶区适形度、剂量均匀性和执行效率上仍然优于IMRT 技术[2]。相对于VDR-VMAT,CDR-VMAT 对加速器硬件要求低,成为一些发布较早的机器开展旋转治疗更为经济有效的选择,如笔者所在单位使用的Varian 23EX。Varian 23EX 是Varian 公司2002年发布的一款较为成熟稳定的放疗直线加速器,目前在国内市场保有量较大,可支持ss-IMRT、dIMRT和CDR-VMAT。开展CDR-VMAT 的同时必须保证治疗计划的绝对剂量验证工作[3-4]。目前对于VMAT技术的剂量验证,三维半导体阵列Delta4 和ArcCheck等已成为主要的第三方验证工具。近年来随着非晶硅电子射野影像系统(Amorphous Silicon Electronic Portal Imaging Device,a-Si EPID)的发展,其具有成像分辨率高、采集数据快、图像便于处理、摆位方便等优点,因此现在被越来越多地应用在剂量验证上[5]。尤其以Varian Portal Dosimetry 系统的发布,使得采用EPID进行剂量验证更加简便易行[6]。
由于目前尚未见有使用EPID和Portal Dosimetry进行CDR-VMAT 剂量验证的相关报道,本研究基于Varian 23EX 加速器实现CDR-VMAT 计划,采用Varian公司的Portal Dosimetry系统和a-Si EPID对30例CDR-VMAT 计划(包括头、胸、腹部肿瘤各10 例)进行绝对剂量验证,并与Delta4的验证结果进行对比分析,讨论其在临床计划设计及验证中的意义,有效提高Varian 23EX 加速器在实际使用中的计划执行效率。
1 资料与方法
1.1 仪器设备
采用笔者所在单位的Varian 23EX作为执行加速器,能量为6 MV X 线。23EX 支持剂量率为100、200、300、400、500、600 MU/min 的CDR-VMAT,实际使用数值由计划系统优化给出。该加速器选配了aS1000 型EPID,可配合Varian Portal Dosimetry 11.0实现绝对剂量验证和Gamma通过率分析工作。加速器剂量校准工具采用PTW 的0.6cc 指形电离室。ScandiDos公司的Delta4三维半导体阵列和配套软件作为对比工具进行计划验证。
1.2 临床病例选择
随机选取2017年1月~2018年8月期间接受治疗的10例头颈部肿瘤患者、10例胸部肿瘤患者和10例腹部肿瘤患者。每个患者的放疗靶区和处方剂量均经审核通过。
1.3 计划设计与验证
采用RayStation4.5 计划系统对每个患者设计CDR-VMAT 计划,选取23EX 作为执行机器,X 射线能量为6 MV。剂量率和机架转速恒定,并由计划系统优化给出。采用卷积叠加算法,每2°一个控制点,单次优化迭代60次。对于头颈部肿瘤设计181°~179°对偶双弧计划。胸部肿瘤根据靶区位置合理选择对偶双弧、4弧或6弧,保证靶区受量的同时尽量降低肺的受照体积。腹部肿瘤均设计230°~130°的对偶双弧计划。经过RayStation 设计好的计划采用Delta4 三维半导体阵列作为模体生成验证计划并导出至加速器执行。同时计划传输至已经配置了PDIP 算法的Eclipse11.0 系统,生成适用于aS1000 EPID 的Portal Dosimetry验证计划。
在进行计划验证之前采用PTW 0.6cc 指形电离室和水箱对加速器进行剂量校准,确保其输出的稳定性。此外对Delta4 三维半导体阵列应进行绝对剂量校准工作。对于EPID,需要进行暗野、泛野、坏点、机械等相关校准和修正。
1.4 评估方法
对所有的验证结果采用3 mm DTA、3%Dose 标准进行绝对剂量Gamma 通过率分析。Gamma 通过率大于95%可认为验证通过。鉴于目前采用的Portal Dosimetry11.0系统无法完成多野合成分析,本研究对每个射野进行Gamma 通过率分析,包括头颈部20个射野、胸部42个射野和腹部20个射野。
1.5 统计学方法
采用SPSS 22.0 软件对两种验证方式的Gamma通过率进行统计学分析,数据用均数±标准差表示,进行配对样本t检验,P<0.05 表示差异有统计学意义。
2 结果
两种验证方法所有射野的Gamma 通过率如图1~3 所示,可见所有射野的Gamma 通过率均大于95%。Portal Dosimetry 和Delta4 典型的验证结果如图4所示。头颈部、胸部和腹部计划的验证数据和配对t检验结果如表1所示。从验证结果可看出,头颈部、胸部和腹部CDR-VMAT计划的Gamma通过率均满足要求(>95%)。对于头颈部计划,Portal Dosimetry 的Gamma 通过率明显小于Delta4,且具有统计学差异,但也达到了95%以上,20个射野中最小Gamma 通过率为95.6%。对于胸部和腹部计划,两种验证方法的Gamma通过率无统计学差异。

图1 头颈部肿瘤CDR-VMAT计划Gamma通过率Fig.1 Comparison of Gamma passing rates of CDR-VMAT plans for head and neck cancer
3 讨论
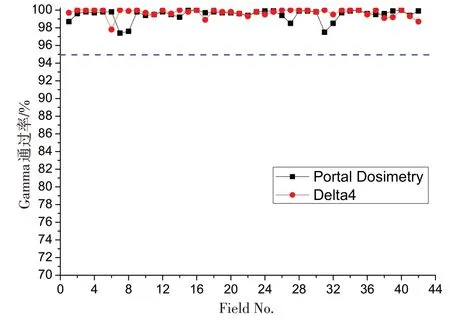
图2 胸部肿瘤CDR-VMAT计划Gamma通过率Fig.2 Comparison of Gamma passing rates of CDR-VMAT plans for chest cancer

图3 腹部肿瘤CDR-VMAT计划Gamma通过率Fig.3 Comparison of Gamma passing rates of CDR-VMAT plans for abdominal cancer
VMAT 作为一种先进的治疗方式,在靶区适形度、执行效率等方面优于固定野调强技术(IMRT)已经得到共识[7]。同时为保证VMAT计划的执行质量,第三方验证工具(以三维半导体阵列为主)已经成为开展VMAT 技术的必备条件[3]。由于开展VDRVMAT技术所要求的加速器条件更高,目前国内可用机器较少,且第三方三维剂量验证工具价格偏高,对于多数国内基层医院来说开展VDR-VMAT 技术代价较高。CDR-VMAT 相对于VDR-VMAT 初始成本更低,是一个更为经济而有用的选择[8]。Didona等[9]通过对15例头颈部CDR-VMAT和IMRT计划的研究分析,CDR-VMAT在靶区适形性、均匀性和执行时间上均优于IMRT。Zhang 等[10]对18 例胸段食管癌Varian 23EX上的CDR-VMAT计划分析得出,其计划质量与IMRT 相同或者更优,治疗时间则明显缩短。Yang 等[11]对9 例腹部肿瘤患者研究分析了VDRVMAT、CDR-VMAT 和9F-IMRT 计划,结果表明CDR-VMAT和VDR-VMAT的剂量分布十分相似,计划质量高于IMRT,并且验证通过率均在95%以上。相关研究结果均表明CDR-VMAT能够有效提高加速器治疗效率,开展CDR-VMAT具有重要现实意义。
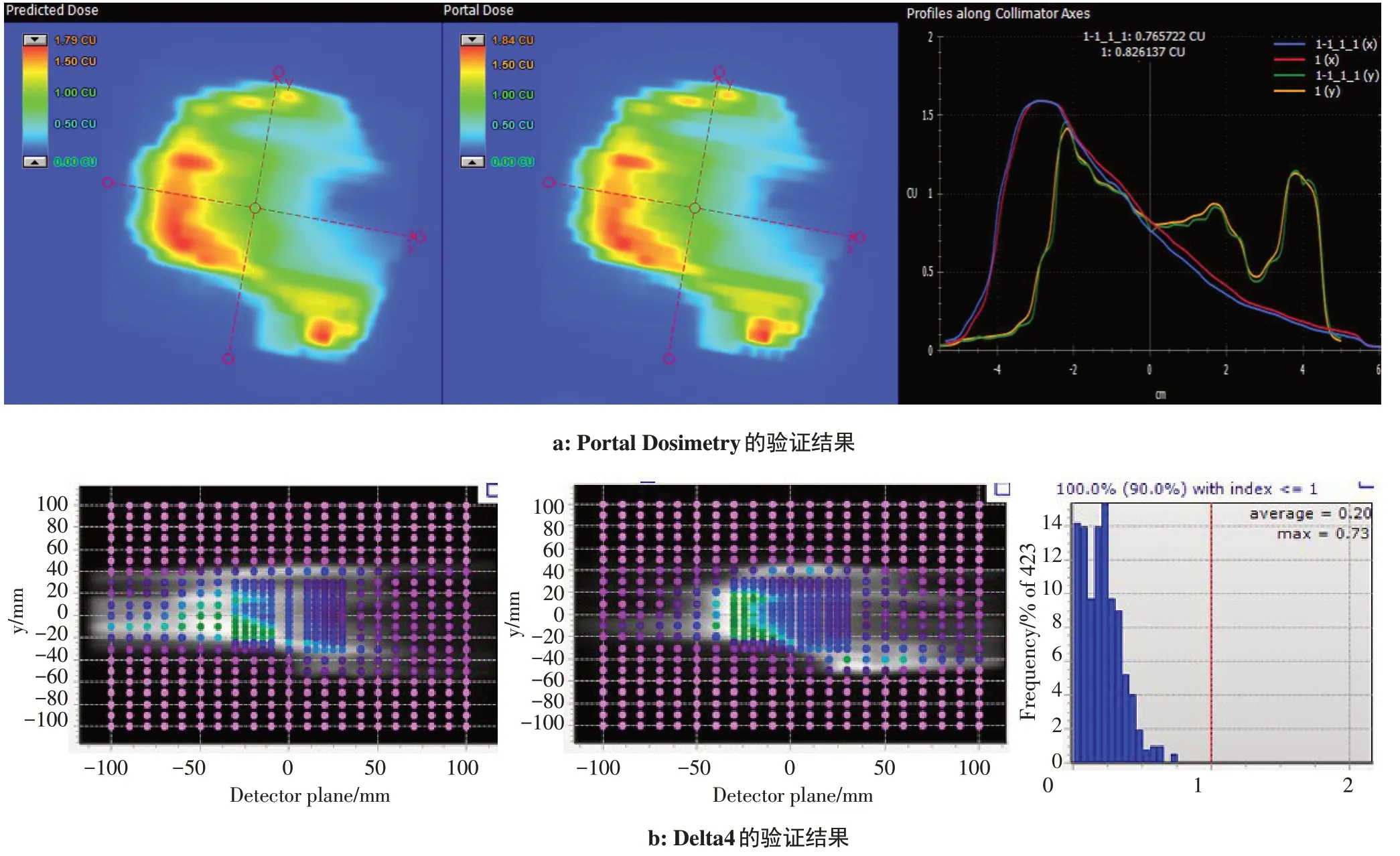
图4 两种方法绝对剂量验证示例Fig.4 Typical examples of dose verification with two methods
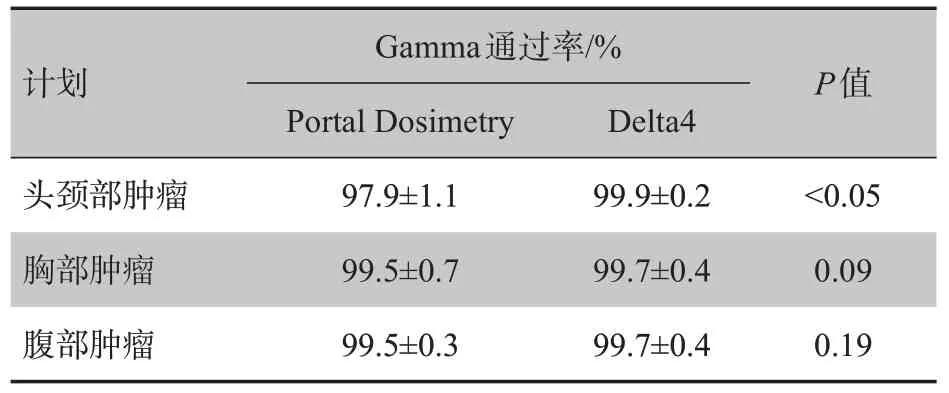
表1 两种验证方法Gamma通过率和t检验结果Tab.1 Comparison of Gamma passing rates between two verification methods and t test results
在剂量验证方面,Varian Portal Dosimetry 配合EPID 验证VMAT 能够进一步降低开展CDR-VMAT技术的代价。Bakhtiari等[12]证实EPID在旋转调强计划QA上应用的可行性。Mohamed等[13]采用EPID完成了24 例VMAT 计划的剂量验证工作,3 mm/3%Gamma 通过率均在97%以上。Maroote 等[14]开展了Portal Dosimetry 联 合EPID 与Delta4 在RapidArc 剂量验证上的对比分析,结果表明两种验证方式可以相互佐证。Van Uytven等[15]研究了基于EPID图像实现患者体内的三维剂量重建,不仅能完成治疗前的绝对剂量验证,并且能够实现治疗中的三维剂量验证。Kavuma 等[16]对EPID 的响应参数进行了研究分析,提出实际用于剂量验证中需要修正的参数。本研究中对所使用的EPID亦进行了必要的修正。
从本文研究结果来看,Varian Portal Dosimetry联合a-Si EPID 能够有效完成对CDR-VMAT 计划的绝对剂量验证,所有的验证Gamma 通过率均满足临床要求,大于95%。Portal Dosimetry 的通过率要低于Delta4,以头颈部最为突出,这主要是因为本研究采用的aS1000 EPID 有效探测面积为40 cm×30 cm,有效分辨率为0.39 mm,远高于Delta4 5 mm 的分辨率。同时头颈部靶区一般包括颈部淋巴结及引流区,范围较大,靶区内要求的剂量梯度也比较大,易产生不通过的检测点,因此Portal Dosimetry 的验证结果相对更为可靠。对于胸部和腹部计划来说,两种验证方法完全可以做到相互替代。目前绝大多数加速器均配备了EPID,可方便地开展验证工作,并且EPID 的有效探测面积大、分辨率高能够有效确保验证的准确性。此外采用Portal Dosimetry 和EPID 进行CDR-VMAT剂量验证免去了第三方验证模体的摆位时间,并在一定程度上避免了不同验证人员摆位的差异。
在实际工作中,使用Portal Dosimetry 和EPID 验证CDR-VMAT计划也存在一定缺点。首先笔者目前使用的Portal Dosimetry 和EPID 尚不能实现多野合成计算,仅可进行单野剂量验证;其次EPID在伸缩和随机架的转动过程中不可避免地出现位置偏移,需要经常进行机械修正;最后目前版本的Portal Dosimetry 需要在Eclipse 计划系统内配置,对于其他TPS 的计划需要传输至Eclipse 后方可生成验证计划。后续应开展相关工作克服这些问题,进一步完善采用Portal Dosimetry 和EPID 实现绝对剂量验证工作。
总之,本研究结果说明在Varian 23EX 直线加速器上开展CDR-VMAT 技术,并采用Portal Dosimetry系统完成对CDR-VMAT计划的绝对剂量验证工作是可行的,能够有效降低开展VMAT计划的代价,提高Varian 23EX在实际使用中的计划执行效率。
