ZnO催化作用下甲醇与碘甲烷反应的机理
2019-10-19陈微微周思侬周晓龙李承烈
陈微微,宗 睿,周思侬,周晓龙,李承烈
(华东理工大学 化工学院 绿色能源化工国际联合研究中心,上海 200237)
以煤或天然气为原料,与甲醇反应制备烃类化合物,作为一种非石油制烃工艺,成为近年来的研究热点。甲醇制烯烃(MTO)、甲醇制汽油(MTG)、甲醇制芳烃(MTA)统称为甲醇制烃(MTH)。采用不同的催化剂、不同的工艺条件,MTH反应所得到的产物分布也不相同。硅铝磷型分子筛SAPO-34是MTO的常用催化剂;而其它甲醇制烃工艺多采用ZSM-5分子筛催化剂[1-2]。目前也有金属卤化物催化剂用于甲醇制烃的报道[3],尤其是碘化锌和碘化铟,对催化生成2,2,3-三甲基丁烷(Triptane)有较高的选择性,可达30%。而Triptane的马达法辛烷值为101,研究法辛烷值为112,沸点为80.9 ℃,是一种优质的汽油调和组分,尤其适用于调和高辛烷值绿色无铅航空汽油[4]。
在酸性催化剂上进行的甲醇制烃的反应机理较为复杂,普遍认为甲醇转化进程分为:二甲醚的形成、C—C键的形成和深度反应,而深度反应包括烷基化、氢转移、聚合、环化、异构化等反应过程。生成低碳烯烃的反应按照烃池反应机理进行,而低碳烯烃继续生成汽油组分、芳烃、长链烷烃等的反应则遵循碳正离子反应机理[5-7]。以甲醇制备Triptane的反应除了遵循上述反应机理外,其在无择形功能催化剂作用下生成Triptane的高选择性受到部分研究者的关注。Bercaw等[8-9]对碘化锌、碘化铟催化甲醇反应生成Triptane的工艺条件进行了系统的研究;Plaisance等[10-11]通过计算各步反应的反应活化能,对催化剂催化生成Triptane的选择性进行了解释;Walspurger等[12]以锌为催化剂催化甲醇与碘甲烷的混合物生成Triptane,并提出初始C—C形成的机理。
笔者以甲醇与碘甲烷为反应物,在ZnO的催化作用下制备得到Triptane,考察了甲醇与碘甲烷摩尔比对反应的影响,通过考察采用不同种类的醇和碘代烃作为替代反应物对反应产物分布的影响,探讨反应中间物、产物的形成机理,并采用能谱仪(EDS)和热重(TG)表征手段分析反应前后催化剂组成的变化,探讨甲醇和碘甲烷在ZnO作用下的催化反应机理。
1 实验部分
1.1 主要试剂
无水甲醇、无水乙醇、异丙醇,AR,国药集团化学试剂有限公司产品;碘甲烷、碘乙烷、氧化锌,AR,阿拉丁化学试剂有限公司产品;高纯氮,纯度99.99%,上海加杰气体有限公司产品。
1.2 实验装置与流程
反应装置为100 mL高压釜式反应器,反应器内部采用石英管内衬以避免腐蚀,反应器采用热油浴进行加热。按比例称取甲醇、碘甲烷及氧化锌装入反应器内,用高纯氮气吹扫整个反应体系后,将反应器放入油浴内加热到200 ℃进行反应,反应压力为体系自发产生的压力,随反应时间先升高后降低,最高可至1.5 MPa左右。反应3 h后将反应釜从油浴中取出,用冰水浴冷却至釜内压力恒定后,将釜内产物按气相、油相及水相产物分别收集。固体催化剂采用减压蒸馏方法,在氮气氛围下回收。
1.3 产物及催化剂评价
采用上海灵华色谱公司的GC-9890A型色谱,色谱柱为SE-30毛细管柱(100 m×0.25 μm×20 μm),FID检测器。产物的定性分析采用美国HP公司的HP-5973气相色谱-质谱联用仪器,色谱柱为HP-5MS(0.25 mm×30 m),质谱的扫描范围为(m/z)20~800。
采用美国TA公司的SDTQ600热分析仪对反应前后的催化剂进行热失重分析,测试条件:氮气氛围,气速为10 mL/min,从室温升至800 ℃,升温速率为10 ℃/min。
采用美国EDAX公司的Phoenix电子能谱仪(EDS)对反应前后的催化剂进行元素分析,能谱仪能量分辨率为133 eV,元素检测范围为4Be~94Pu。
烃类产物总质量产率(yo)的计算公式如下:
(1)
Triptane的收率(yt)以碳原子摩尔量为基础进行计算[8-9,11,13],计算公式如下:
(2)
甲醇和碘甲烷的转化率x1、x2计算公式分别如下:
(3)
(4)
式(1)~(4)中,mo为烃类产物的总质量,g;m1为甲醇的质量,g;m2为碘甲烷的质量,g;n1、n2、nt分别为甲醇、碘甲烷和triptane的物质的量;ma1为未反应的甲醇的质量,g;mg2和mo2分别为气相及油相物料中未反应完的碘甲烷的质量。
2 结果与讨论
2.1 CH3OH与CH3I摩尔比对反应产物分布的影响
将原料与催化剂按照n(CH3OH)∶n(CH3I)∶n(ZnO)=2∶2∶1的比例,在200 ℃下反应3 h,反应前后物料组成情况如表1所示,反应产物可分为油相产物,气相产物及水。气相产物及油相产物的色谱图如图1所示。由图1(a)可知,气相产物中异丁烷的质量分数最高,约30%左右;由图1(b)可知,油相产物的分布很广,组分多达两百多种,其中Triptane的质量分数最高,为35%左右。油相产物的分布特点与CH3OH在ZnI2的催化作用下反应的产物分布相似[8-9,13]。从产物分布的特点来看,在CH3OH与CH3I反应中,采用ZnO和ZnI2催化作用下生成各烃类物质的过程是类似的[11]。

表1 反应前后物料组成Table 1 Feed composition before and after reaction
Reaction conditions:n(CH3OH)∶n(CH3I)∶n(ZnO)=2∶2∶1;T=200 ℃;t=3 h
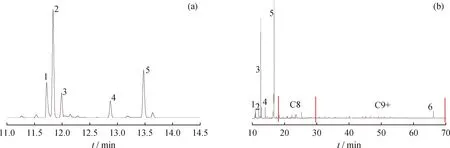
图1 CH3OH与CH3I反应产物的气相色谱图Fig.1 Gas chromatogram of products(a)Gas products:1—Dimethyl ether (DME);2—Isobutane;3—Isobutene;4—Isopentane;5—Methyliodide(b)Oil products:1—Isobutane;2—Isopentane;3—Methyl iodide;4—2,3—Dimethylbutane;5—Triptane;6—Hexamethylbenzene (HMB)
n(CH3OH)/n(CH3I)对原料转化率及产物分布的影响分别如图2和图3所示,由于产物分布较广,所以将产物按照所生成烃的碳数进行分类。由图2可知,当n(CH3OH)/n(CH3I)≥1时,CH3I的转化率达到最高。CH3OH的转化率随CH3OH/CH3I摩尔比增大而降低。说明CH3OH比例过低将不利于CH3I的转化,过高将不利于CH3OH的转化。由图3可知,在气相产物中,C4烃类的质量分数最高,其次是二甲醚。随甲醇比例的增加,产物中二甲醚的质量分数增加,C4组分的质量分数减少;油相产物中,C7烃类的质量分数是最高的,n(CH3OH)/n(CH3I)对油相产物分布的影响不大。
n(CH3OH)/n(CH3I)的变化对总产物和Triptane收率的影响如图4所示。由图4可知:当n(CH3OH)/n(CH3I)=1时,总产物收率和Triptane收率均为最高,总产物收率为8.36%,其中Triptane碳摩尔收率为9.50%;当n(CH3OH)/n(CH3I)<1时,CH3OH量不足导致CH3I的转化率下降;当n(CH3OH)/n(CH3I)>1时,CH3I量不足导致CH3OH的转化率下降;因此,n(CH3OH)/n(CH3I)大于1或小于1时,原料均不能得到充分的转化,产物收率都会降低。可见,CH3OH与CH3I在转化中相互制约。实验发现,在缺少CH3OH的实验中,CH3I无法进一步转化,同样在缺少CH3I的实验中,CH3OH也无法转化,因此笔者将继续对CH3OH及CH3I二者的反应机理进行探讨。
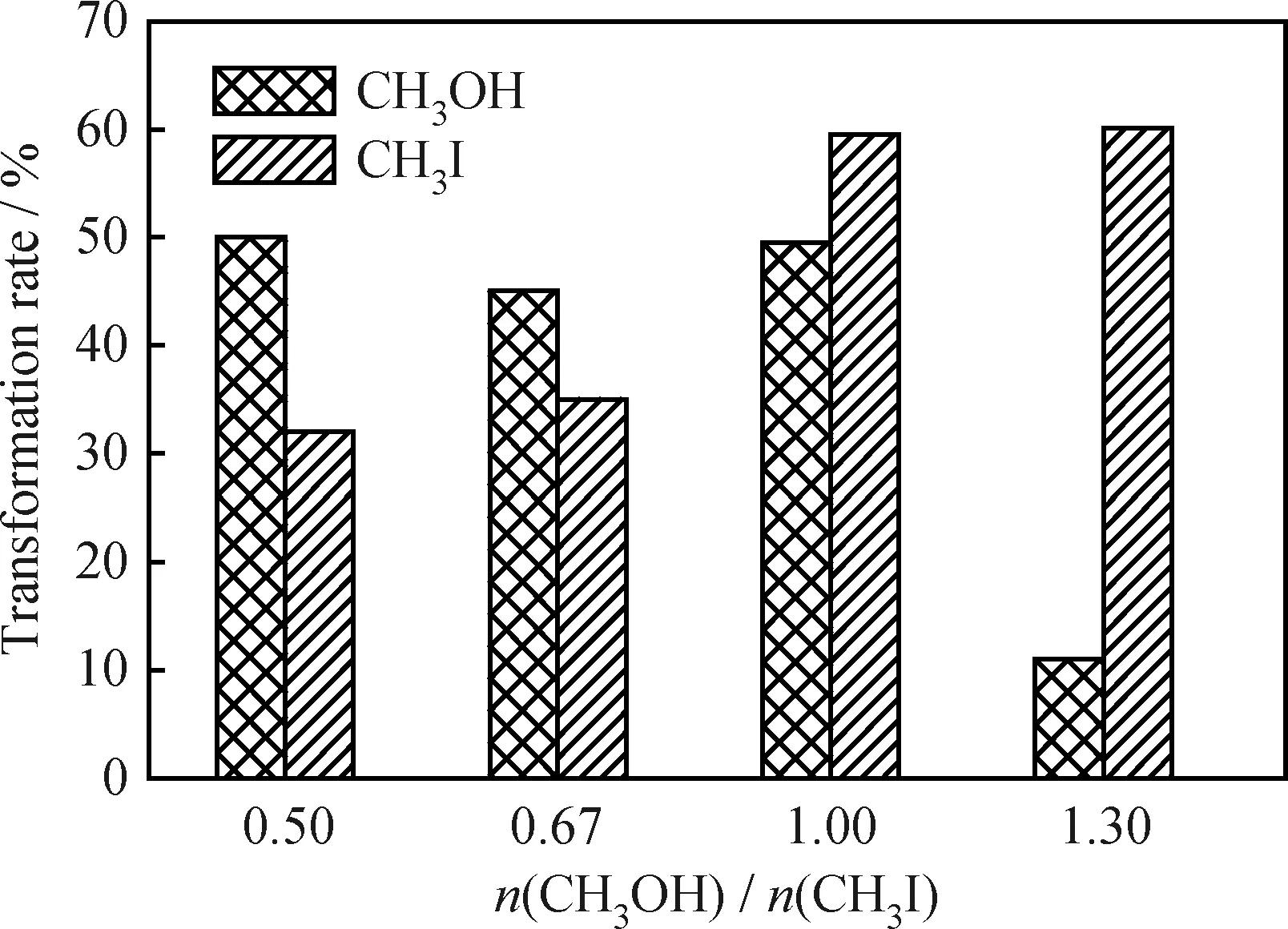
图2 n(CH3OH)/n(CH3I)对原料转化率的影响Fig.2 Effect of n(CH3OH)/n(CH3I)on transformation rateReaction conditions:n(CH3I)/n(ZnO)=2;T=200 ℃;t=3 h
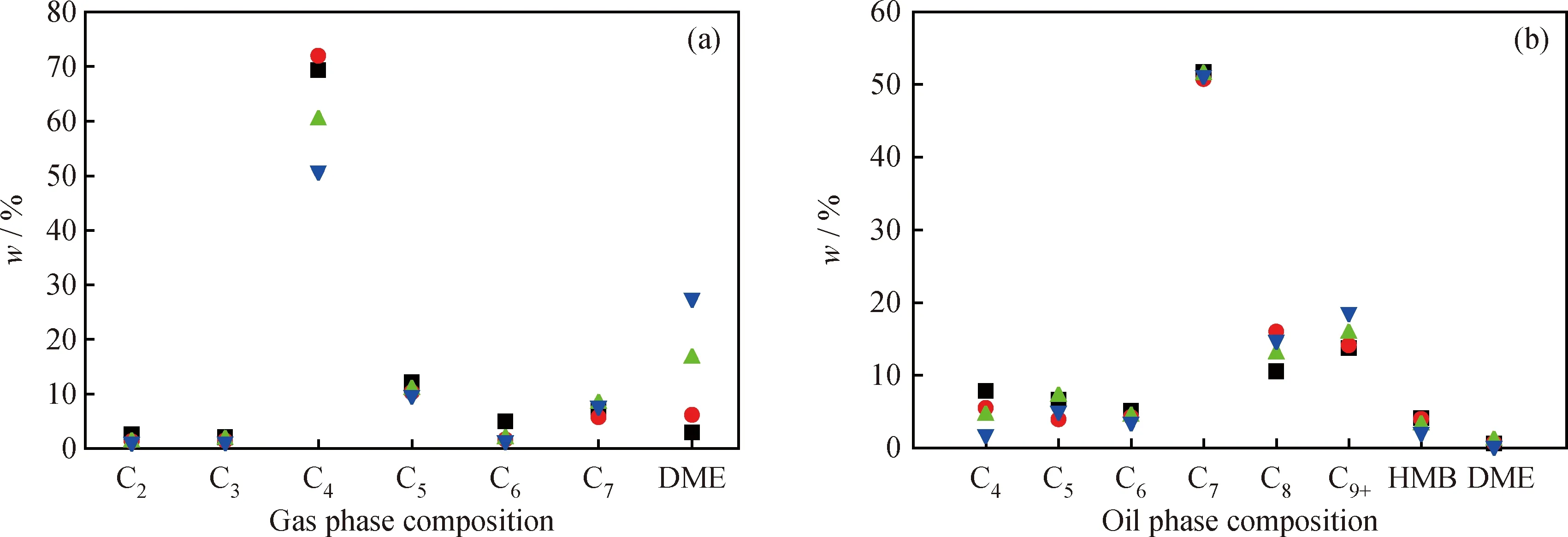
图3 n(CH3OH)/n(CH3I)对气相和油相产物分布的影响Fig.3 Effect of n(CH3OH)/n(CH3I)on gas and oil products distribution(a)Gas phase products;(b)Oil phase productsReaction conditions:n(CH3I)/n(ZnO)=2;T=200 ℃;t=3 h;HMB—Hexamethylbenzene;DME—Dimethyl ether n(CH3OH)/n(CH3I)=0.5; n(CH3OH)/n(CH3I)=0.67; n(CH3OH)/n(CH3I)=1; n(CH3OH)/n(CH3I)=1.3
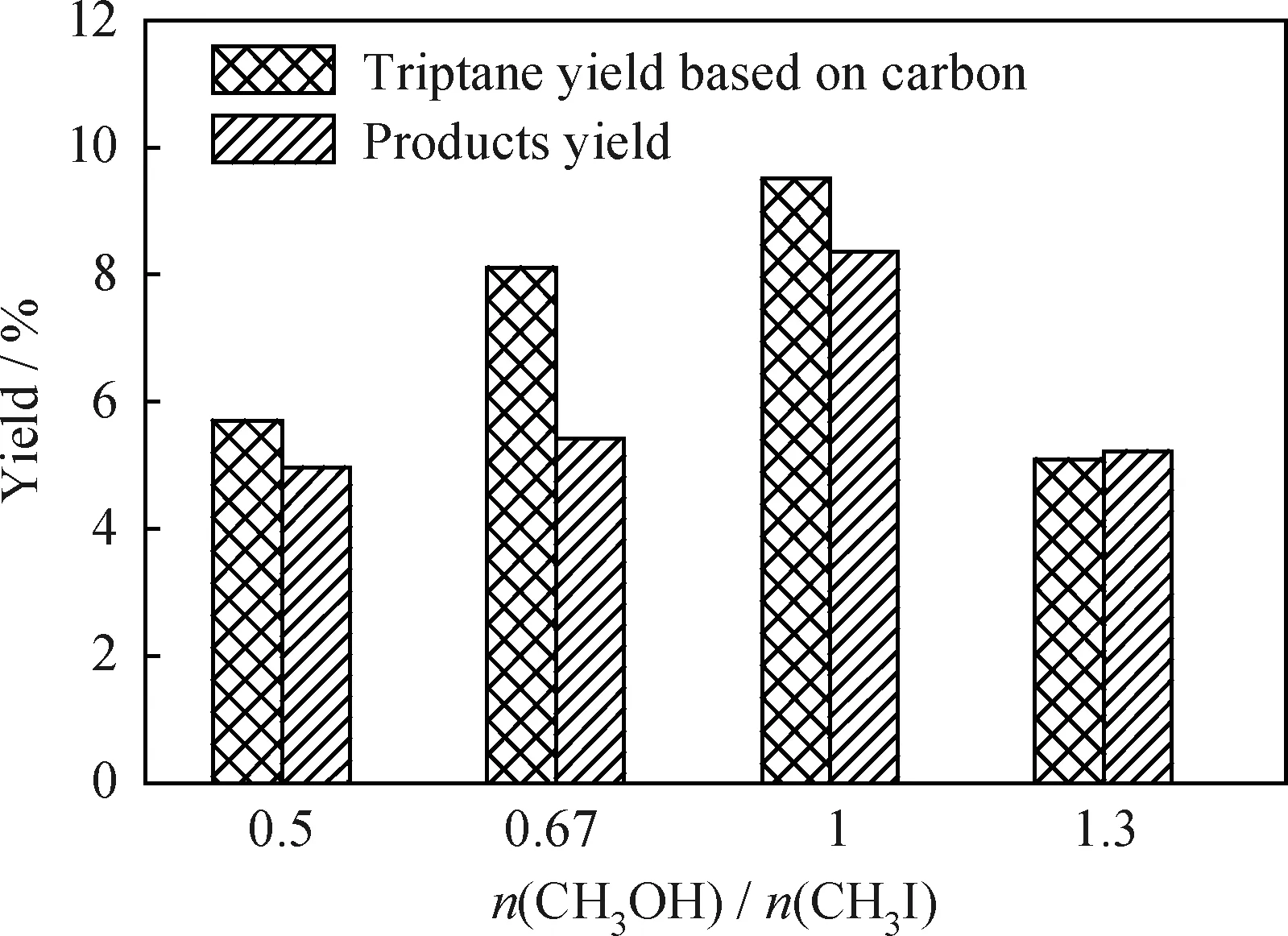
图4 n(CH3OH)/n(CH3I)对Triptane及总产物收率的影响Fig.4 Effect of n(CH3OH)/n(CH3I)on total products and triptane yieldReaction conditions:n(CH3I)/n(ZnO)=2;T=200 ℃;t=3 h
2.2 甲醇和碘甲烷的反应机理
为了探索甲醇与碘甲烷反应的反应机理,分别将CH3I替换为其他碘代烃,将CH3OH替换成水或其他羟基醇,考察反应物变化对产品分布的影响,探讨反应中间体和产物的形成机理。
图5为n(CH3OH)∶n(CH3CH2I)∶n(ZnO)=2∶2∶1时反应所得产物分布。由图5可见,采用碘乙烷替换碘甲烷后:气相产物中C2的质量分数从2%增加至55%,此外,气相产物中还检测到了新产物乙醇;而油相产物中C7的质量分数从52%降至26%,C6、C9+的质量分数也有少许增加,且有新产物乙醇和甲乙醚生成。可以推测,碘乙烷中的乙基会直接转化为乙烷和乙烯,也会与体系中羟基结合转化为乙醇。该反应体系中C7产物的选择性大大降低,表明碘甲烷作为原料比碘乙烷更有利于C7产物的生成。
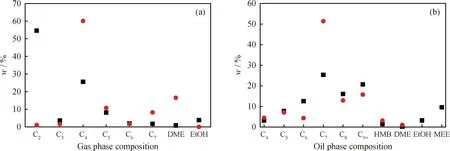
图5 碘代烃种类对反应产物分布的影响Fig.5 Effect of alkyl iodide type on products distributionReaction conditions:n(CH3OH)∶n(R-I)∶n(ZnO)=2∶2∶1;T=200 ℃;t=3 h;EtOH—Ethanol;MEE—Methyl ethyl ether(a)Gas phase products;(b)Oil phase products Reactant:CH3I CH3CH2I
分别以水、乙醇、异丙醇替换甲醇,n(R—OH)∶n(CH3I)∶n(ZnO)=2∶2∶1,其他反应条件不变,反应产物混合物的分布情况如图6所示。由图6可知:将甲醇替换为水后,其气相及油相产物分布变化不大,但碘甲烷的转化率及产物总收率均显著下降(见图7),表明水的反应活性低于甲醇;将甲醇替换为乙醇后,气相产物中C2的质量分数大大提升,且有乙醇和甲乙醚生成,而气相及油相产物中C7的质量分数均有所降低;将甲醇替换为异丙醇后,气相产物中有C3的含量大大增加,液相产物中C7的质量分数降低,C8的质量分数增加。这说明乙醇和异丙醇中烷基可被释放生成相应的烃类物质。
从图6中可以看出,甲醇被替换后,气相产物中仍有二甲醚生成,而二甲醚分子中的甲基必定是碘甲烷分子,说明在水或醇(统称R—OH)存在的情况下,碘甲烷能最终转化为甲醇,并进一步生成了二甲醚。此外,实验发现在缺失羟基物种的反应中,CH3I却无法转化成为二甲醚或烃类物质,说明羟基物种在烃类物质的生成中必不可少,同样,在缺少CH3I的反应中,甲醇也无法进一步转化为二甲醚或烃类物质。虽然关于MTH反应中初始C—C键的形成尚存争议,但在具有代表性的MTH反应氧鎓离子机理和正碳离子机理中,均涉及表面活性甲氧基和二甲醚的生成[1-2,5]。Plaisance等[10]也认为MTH过程中碳链增长的中间物种为活性烷氧基,烷氧基释放出烷基最终生成对应的烷烃或烯烃。因此可推测在该反应中,羟基物种在中间物种活性烷氧基的形成过程中至关重要。
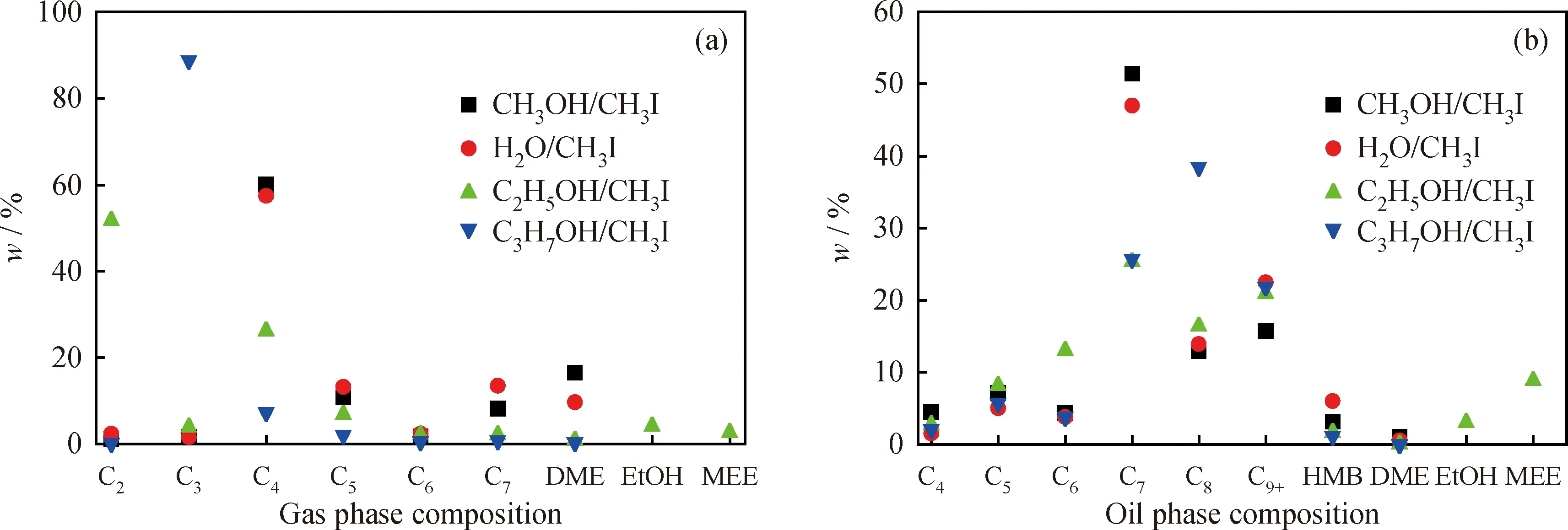
图6 R—OH种类对反应产物分布情况Fig.6 Effect of R—OH type on products distribution(a)Gas phase products;(b)Oil phase productsReaction conditions:n(R—OH)∶n(CH3I)∶n(ZnO)=2∶2∶1;T=200 ℃;t=3 h
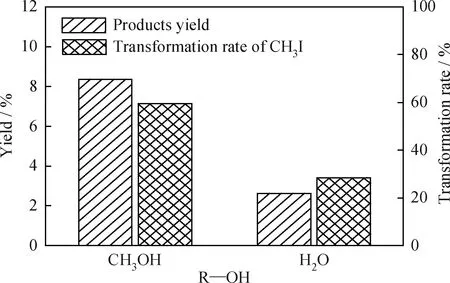
图7 羟基物种的种类对产物收率及CH3I转化率的影响Fig.7 Effect of R—OH type on products yield and CH3I transformation rateReaction conditions:n(R—OH)∶n(CH3I)∶n(ZnO)=2∶2∶1;T=200 ℃;t=3 h
2.3 氧化锌的催化机理
经称量,反应后回收得到的催化剂质量是反应前的2.75倍,说明催化剂在反应过程中发生了变化。采用EDS对反应前后催化剂进行元素分析,分析结果如图8及表2所示。由图8可知,新鲜的ZnO只检测到锌和氧两种元素,n(Zn)/n(O)≈1∶1,与ZnO分子组成相符;而反应后回收的催化剂中检测到碘元素,回收催化剂的分子式经计算为ZnO0.15I1.41,相对分子质量为246.4,是ZnO的3.04倍。
反应前后催化剂的热重分析结果如图9所示。由图9可知,新鲜的氧化锌在持续升温至800 ℃的过程中没有发生质量损失,而回收的催化剂在升温至350 ℃左右开始热质量损失,质量损失率达95%以上。回收催化剂与新鲜ZnI2(350 ℃,热质量损失100%)的质量损失规律相似。
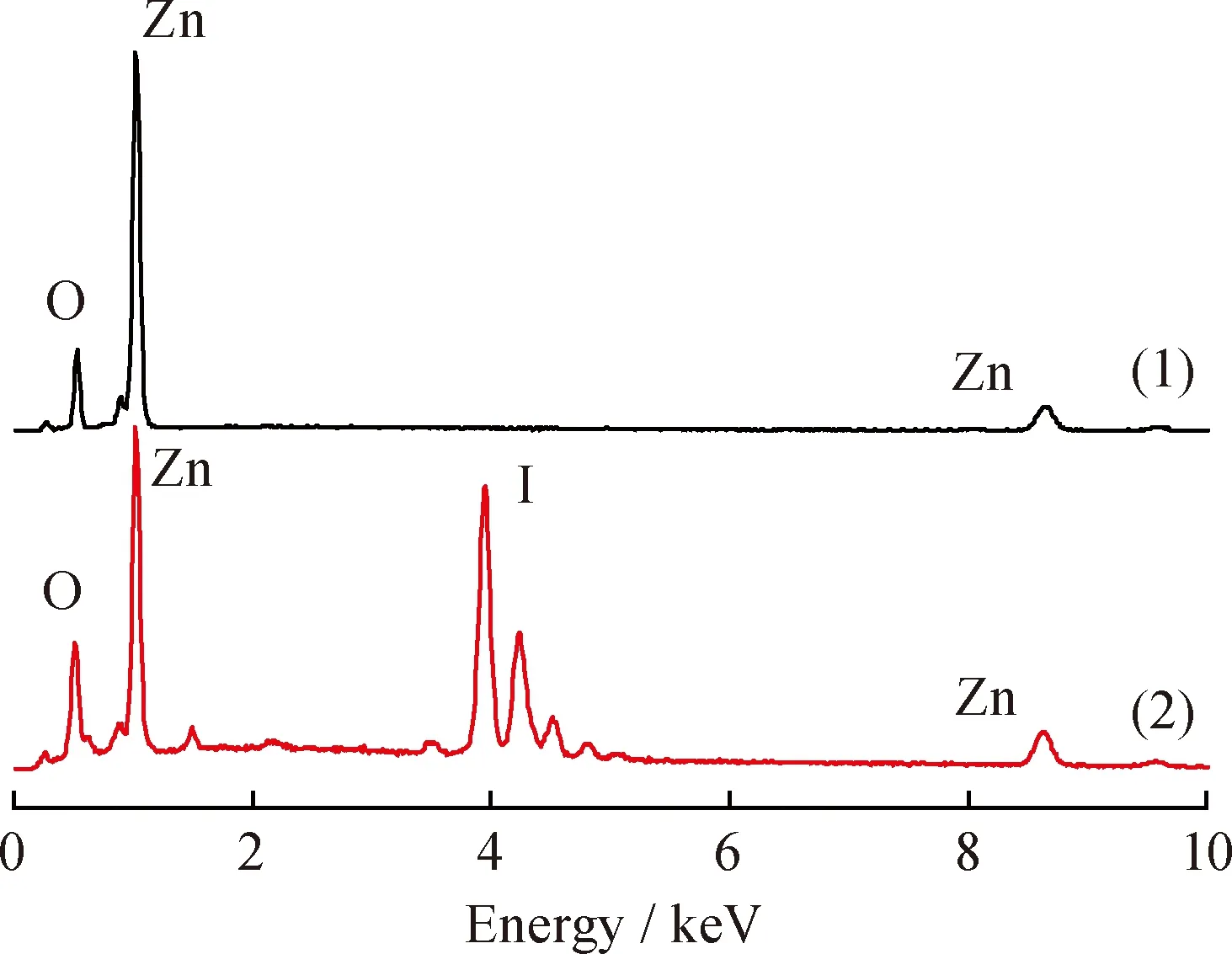
图8 反应前后催化剂EDS扫描能谱图Fig.8 EDS spectra of fresh catalyst and catalyst after reaction(1)Before reaction;(2)After reaction

表2 反应前后催化剂元素分析结果Table 2 Elemental analysis of fresh catalyst and catalyst after reaction w/%
通过EDS和TG表征可知,回收催化剂中含有大量碘化锌,因此可以推测,部分氧化锌在催化反应的过程中转化成了ZnI2。
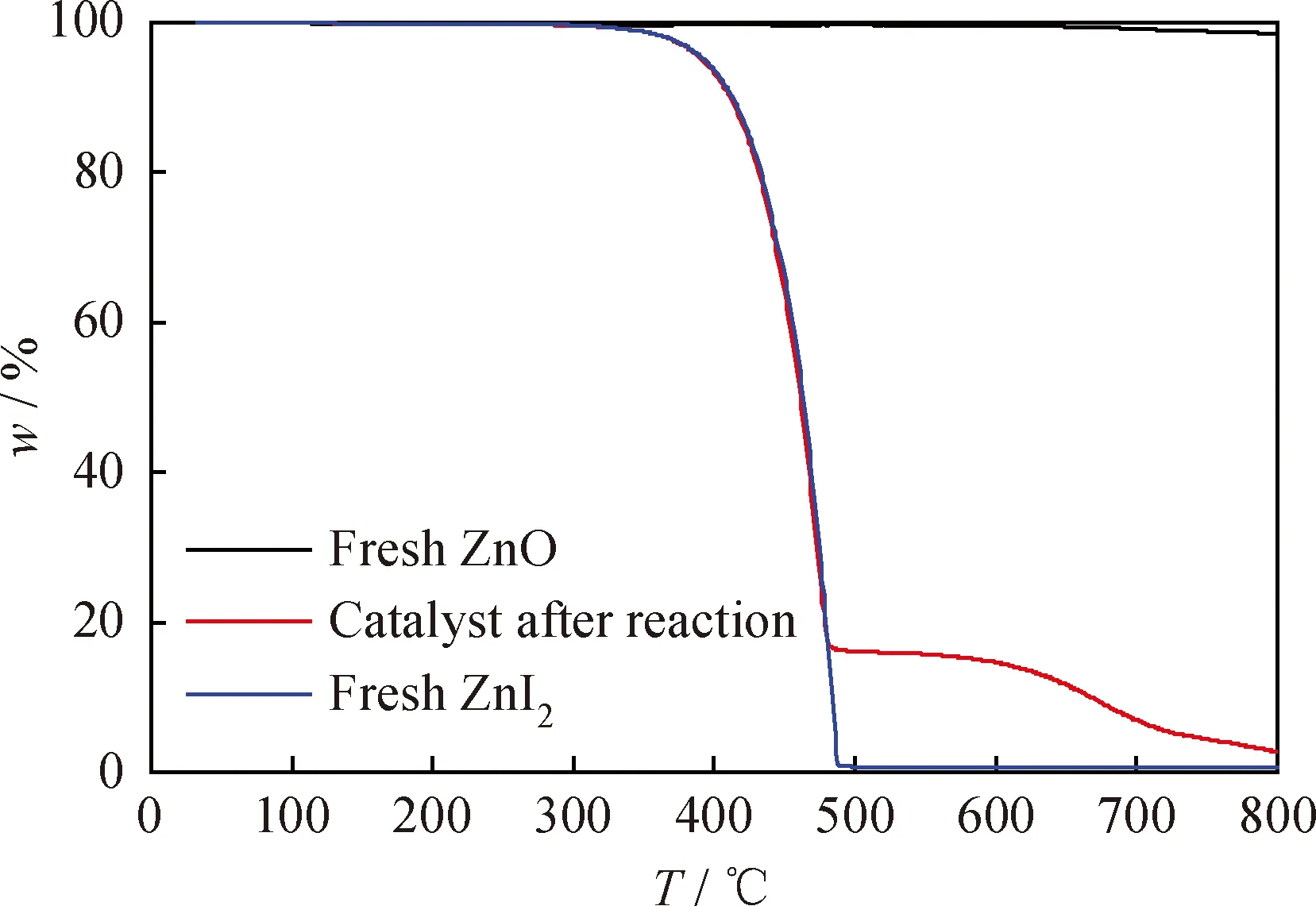
图9 反应前后催化剂热重(TG)曲线Fig.9 TG curve of fresh catalyst and catalyst after reaction
结合不同原料对反应产物分布情况的影响与反应前后催化剂的表征结果,我们对ZnO催化机理做如下探讨:ZnO单独与CH3OH或CH3I均不能发生反应,却能在有羟基物种存在的情况下与CH3I发生反应转化成为ZnI2,并生成烃类物质,说明真正起催化作用的物质是ZnI2而不是ZnO。这与ZnI2能催化MTH反应并生成类似反应产物的结论一致。ZnI2的生成路径如图10所示。以CH3I与羟基物种(R′—OH)的反应为例,由图10可知:ZnO分子中的Zn原子夺取CH3I分子中的I原子;同时,来自R′—OH的烷氧基-Lewis碱被Zn原子-Lewis酸吸引生成活性烷氧基[OR′]基团。当R′—OH为H2O时,活性基团为羟基。ZnO中的O原子则与 R′—OH 中的H原子形成新羟基[OH]。新[OH]与CH3I分子中失去I原子的[CH3]结合成为甲醇。活性中间体(I—Zn—O—R′)中的Zn原子继续与一分子CH3I作用,形成ZnI2;而与Zn原子相连的活性烷氧基[OR′]则与CH3I分子中的[CH3]作用形成醚。R′—OH脱H后的烷氧基[OR′]继续与一分子CH3I作用,最终生成ZnI2和醚。具有催化活性的ZnI2则继续催化CH3I及R′—OH转化为烃类物质。CH3I及R′—OH中的烷基最终均作为烷基化物种为烃类物质的形成实现碳链的增长。
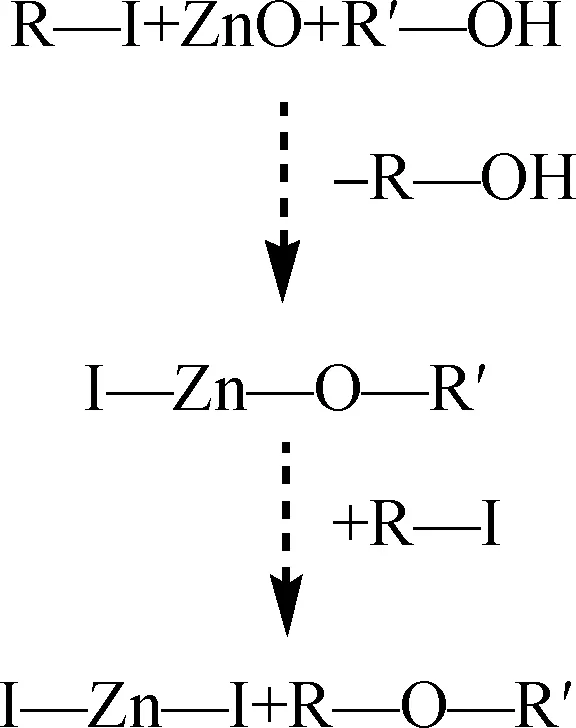
图10 碘化锌生成示意图Fig.10 Generation path of ZnI2R=CH3 or C2H5,R′=CH3;or R=CH3,R′=H,CH3,C2H5 or C3H7
3 结 论
(1)CH3OH甲醇与CH3I碘甲烷在ZnO作用下生成了合成烃。反应物的摩尔比对烃类产物分布影响不大,Triptane在总产物中含量最高,其碳摩尔收率为9.5%。当n(CH3OH)/n(CH3I)=1时,原料的转化率和总烃产物的质量收率均为最高,总烃质量收率为8.36%。
(2)ZnO自身没有催化作用。在反应过程中,ZnO夺取CH3I中的I原子生成的ZnI2具有催化活性,而羟基物种为反应提供活性烷氧基,因此,只有在碘代烃和羟基物种同时存在时,才会发生制烃反应。
