硫酸羟氯喹联合抗凝药物治疗抗磷脂综合征的临床研究
2019-10-16连若纯余姝毅王晓晖陈现许健李玉叶刘冬思曾勇
连若纯,余姝毅,王晓晖,陈现,许健,李玉叶,刘冬思,曾勇
(深圳中山泌尿外科医院生殖医学中心,深圳市围着床期生殖免疫重点实验室,深圳中山生殖与遗传研究所,深圳 518045)
抗磷脂综合征(antiphospholipid antibody syndrome,APS)是一组与抗磷脂抗体(antiphospholipid antibody,APA)有关的自身免疫性疾病,主要临床表现为动脉、静脉血栓形成和病理妊娠(如妊娠早期流产、中晚期死胎等)以及血小板减少等[1]。主要的抗磷脂抗体包括抗β2糖蛋白1抗体(抗β2-GP1抗体)、抗心磷脂抗体(anticaridiolipin antibody,aCL)、狼疮抗凝物(lupus anticoagulant,LA)。目前针对APS的治疗主要是运用常规抗凝药物如低剂量阿司匹林、普通肝素及低分子肝素等,然而仍有20%~30%的APS患者治疗失败[2]。如何改善这些患者的妊娠结局,成为目前亟需解决难题之一。
硫酸羟氯喹(hydroxychloroquine,HCQ)是4-氨基喹啉类抗疟药,20世纪50年代随着抗疟药在系统性红斑狼疮(systemic lupus erythematosus,SLE)和类风湿性关节炎治疗中的应用,HCQ用于风湿性疾病治疗的疗效得到肯定,并且应用越来越广泛。进一步研究揭示HCQ具有免疫调节、调节代谢、抗肿瘤等作用,同时具有抗血栓形成的重要作用[3]。第13届APS国际研讨会中提出APS患者合并血栓病史或SLE,建议给予HCQ辅助治疗[4]。那么经过常规抗凝治疗后再次妊娠失败的APS患者,联合HCQ治疗效果如何呢?目前鲜有关于HCQ联合抗凝药物治疗难治性APS患者的报道,因此本研究拟探讨HCQ联合抗凝治疗对APS患者妊娠结局的影响及相关机制。
资料与方法
一、研究对象
收集在2011年1月至2016年12月于深圳中山泌尿外科医院生殖免疫诊疗中心就诊查尿HCG阳性且诊断符合悉尼标准[1]的APS患者109例。纳入标准:(1)年龄≤38岁;(2)符合以下任意一项临床标准:≥1次孕10周及以上不能解释的形态学正常的死胎;≥1次孕34周以内形态正常的早产儿;3次以上孕10周以内不能解释的自发性流产;(3)符合以下任意一项实验室标准:抗β2-GP1抗体IgM和/或IgG连续2次间隔12周以上检测阳性;aCL-IgM和/或IgG连续2次间隔12周以上检测阳性;LA连续2次间隔12周以上检测阳性;(4)常规抗凝治疗:低剂量阿司匹林联合低分子肝素治疗后再次出现自然流产患者;(5)无炎症系统性损伤,如出现全身脏器损伤的SLE、自身免疫性肝病、肾间质性病变等。排除标准:(1)治疗后因宫颈机能不全、胎儿畸形或染色体异常等导致的流产;(2)过敏体质;(3)眼底病变;(4)伴有心、脑、肾等重要器官病变。
根据不同治疗方案,分为HCQ组(48例)和对照组(61例)。HCQ组予HCQ联合抗凝药物治疗,对照组只接受抗凝药物治疗。
二、研究方法
1.APA检测方法:运用酶联免疫吸附法(ELISA法),采用德国欧蒙试剂盒定量检测血清中aCL-IgG、aCL-IgM、抗β2-GP1抗体IgG、抗β2-GP1抗体IgM、抗Annexin V抗体的表达。阳性判断标准:aCL-IgG>20 GPL,aCL-IgM>20 MPL,抗β2-GP1抗体IgG>20 U/ml,抗β2-GP1抗体IgM>20 U/ml,Annexin V>25 U/ml。
2.APA检测时机:(1)孕前2次检测间隔6周;(2)验孕日。
3.治疗方法:对照组孕前1个月开始给予阿司匹林肠溶片50 mg,每日1次,排卵后或胚胎移植前一周低分子肝素钠或低分子肝素钙4 000~6 000 IU,每日2次。HCQ组在对照组治疗方案基础上,孕前1个月服用HCQ(赛能,赛诺菲,法国) 200 mg,每日2次。停药时机:(1)连续复查2次以上APA均阴性,可逐渐停抗凝药物及HCQ;(2)出现副反应时停药。
4.冻融胚胎移植内膜准备方案:激素替代周期,月经第3天开始服用戊酸雌二醇(补佳乐,拜耳,德国)4 mg/d,每5天递增2 mg至第18天,第19天添加黄体酮注射液(浙江仙琚制药)60 mg/d,第22天移植卵裂期胚胎或第24天移植囊胚。
三、观察指标
两组孕前第2次检测与验孕日aCL-IgM/IgG、抗β2-GP1抗体IgM/IgG及抗Annexin V抗体滴度水平;早期流产率、妊娠满3个月继续妊娠率、胚胎种植率、活婴出生率;不良反应发生情况。
早期流产率=妊娠<12周自然流产周期数/临床妊娠周期数×100%;妊娠满3个月继续妊娠率=妊娠≥12周周期数/临床妊娠周期数×100%;胚胎种植率=超声下可见孕囊数/移植胚胎数×100%;活婴出生率=活婴出生数/移植周期数×100%。
四、统计学方法
结果
一、HCQ组与对照组患者基本情况
两组患者平均年龄、基础FSH水平、既往流产次数、移植胚胎数、移植优质胚胎数及囊胚占比均无显著差异(P>0.05)。HCQ组33例,对照组37例进行冻融胚胎移植后妊娠,其余患者自然妊娠(表1)。
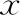
表1 HCQ组与对照组患者基本情况及相关指标的比较[(-±s),%]
二、HCQ联合抗凝药物治疗前后APA滴度变化情况
分别记录孕前第二次检测与验孕日复查APA滴度的情况,HCQ患者两次检测期间均使用HCQ治疗。与治疗前比较,HCQ组治疗后抗β2-GP1抗体IgG、aCL-IgM、aCL-IgG滴度均有显著降低(P<0.05),抗Annexin V抗体及抗β2-GP1抗体IgM滴度虽然下降,但无统计学差异(P>0.05)(图1)。
三、HCQ组与对照组治疗后验孕日APA抗体滴度水平比较情况
与对照组比较,验孕日HCQ组抗β2-GP1抗体IgG、aCL-IgG及抗Annexin V抗体平均滴度较对照组低,而aCL-IgM及抗β2-GP1抗体IgM滴度较对照组高,但均无统计学差异(P>0.05)(图2)。
四、HCQ联合抗凝药物治疗后妊娠结局情况比较
对所有研究对象的妊娠结局进行随访,HCQ组48例、对照组59例获得临床妊娠,对照组2例生化妊娠。临床妊娠中,HCQ组有2例双胎妊娠,对照组有7例双胎妊娠。HCQ组妊娠满3个月继续妊娠率高于对照组(85.4% vs.72.9%),但无统计学差异(P>0.05)。HCQ组早期流产率显著低于对照组(P<0.05)。HCQ组的活婴出生率高于对照组,但无统计学差异(P>0.05)(表2)。
五、HCQ联合抗凝药物治疗后副作用情况分析
HCQ组48例患者平均服用HCQ时间为(7.47±3.45)月,其中3例患者出现眼睛干涩不适症状,发生率为6.3%(3/48)。43例出生婴儿随访1年,结果显示均未发现任何先天性缺陷。
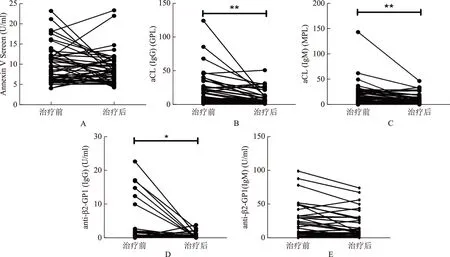
A:抗Annexin V抗体;B:aCL-IgG;C:aCL-IgM;D:抗β2-GP1抗体IgG;E:抗β2-GP1抗体IgM;前后比较,*P<0.05,**P<0.01
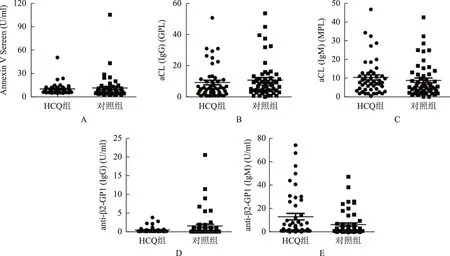
A:抗Annexin V抗体;B:aCL-IgG;C:aCL-IgM;D:抗β2-GP1抗体IgG;E:抗β2-GP1抗体IgM

表2 HCQ组与对照组患者治疗后妊娠结局情况比较(%)
讨论
APS是指APA阳性合并有动静脉血栓形成和/或病理妊娠的一组临床征象的总称,其中血栓形成是APS的主要病理基础,也是造成病理妊娠的重要因素,其致病性抗体为APA。妇产科APS主要发病机制可能为:(1)APA可诱导胎盘血栓形成、破坏膜联蛋白A5在胎盘局部形成的保护膜;(2)APA可与蜕膜细胞结合而诱导胎盘局部产生炎症;(3)APA可与滋养细胞结合抑制滋养层细胞增殖和分化,从而诱导滋养细胞凋亡[5-7]。针对APS导致的不良妊娠结局,临床上主要通过运用抗凝药物如低分子肝素、小剂量阿司匹林进行预防和治疗,数据提示约70%患者保胎成功,然而仍有部分APS患者再次出现妊娠失败[8-9]。
研究表明,HCQ可有效改善SLE和类风湿性关节炎等风湿免疫疾病病情,安全有效且耐受性良好,可用于妊娠妇女,与其他抗风湿药物联合应用可进一步提高疗效[10-11]。在国内外临床研究中HCQ也逐步被运用在APS治疗中并取得较好疗效,为这部分难治性APS患者带来了福音。报道显示HCQ在APS治疗中的主要作用机制是:抑制β2-GP1与磷脂层结合而抑制其复合物形成,抑制GPⅡb/Ⅲa通路阻断血小板聚集和黏附,破坏磷脂层表面Annexin V保护膜等,从而抑制血栓形成[12-14]。本研究发现HCQ联合抗凝治疗后aCL抗体IgM/IgG及抗β2-GP1抗体IgG滴度均较治疗前显著降低(P<0.05),而抗Annexin V抗体及抗β2-GP1抗体IgM滴度无显著变化,提示HCQ可通过降低aCL-IgG、抗β2-GP1抗体IgG滴度来有效缓解APS。同时数据进一步显示,与单纯服用常规抗凝药物相比,HCQ联合常规抗凝药物治疗后,aCL抗体IgG、抗β2-GP1抗体IgG滴度及抗Annexin V抗体滴度均呈降低趋势。研究结果提示HCQ联合抗凝治疗比常规抗凝药物治疗可以更有效降低APA的滴度。
2015年欧洲一项多中心回顾性研究结果显示HCQ联合低分子肝素、小剂量阿司匹林等抗凝治疗后,可显著降低早期流产率,提高活婴出生率(P均<0.05)[15]。Sciascia等[16]的一项回顾性研究同样发现,HCQ辅助治疗组较单纯低分子肝素联合阿司匹林抗凝治疗组的活婴出生率显著提高,并能显著降低病理妊娠的发生(P均<0.05)。我们的研究数据表明与单纯使用阿司匹林和低分子肝素相比,HCQ联合阿司匹林和低分子肝素的患者临床妊娠率及3个月继续妊娠率有升高趋势,而早期流产率显著降低,与国外研究结果一致。提示HCQ联合抗凝药物治疗对降低难治性APS患者早期流产率有一定的疗效。Rand等[14]研究显示,HCQ可显著降低抗β2-GP1抗体IgG、aCL抗体IgG,抑制APA与β2-GP1复合物形成,从而发挥抗血栓形成作用。另外,HCQ还可能抑制GPⅡb/Ⅲa通路阻断血小板聚集和黏附,从而改善局部血液循环,降低早期流产风险。本研究结果显示,HCQ治疗后aCL抗体IgG、抗β2-GP1抗体IgG滴度及抗Annexin V抗体滴度亦有降低趋势,但无显著差异(P>0.05)。因此,HCQ是否通过降低APA滴度改善难治性APS患者妊娠结局,仍须扩大样本量进一步研究。
另外,HCQ在妊娠期使用的安全性亦是临床医生甚为关注的问题。HCQ主要的不良反应是眼底视网膜损害,此损害一般是不可逆的。但该不良反应出现与用药剂量及用药时间有关,且发生概率较低。故用药前需先排除眼底疾病,一旦发现眼睛不适,立即停药。HCQ在FDA评级属C类药物,可少量通过胎盘和乳汁,但欧洲风湿病防治联合会指出HCQ在妊娠期间及哺乳期均可安全使用,不影响胎儿及新生儿发育[17-18]。国内外多项研究表明,妊娠期间使用HCQ,胎儿出生后并未增加先天性畸形、视网膜病变等,妊娠期使用安全[11,18-19]。本研究中使用HCQ患者中有3例出现眼睛干涩不适症状,停药后症状缓解。43名活婴出生时均未发现先天性缺陷,随访1年亦未发现任何后遗症。
综上所述,HCQ联合常规抗凝治疗可改善难治性APS患者的妊娠结局,有效降低早期流产率,且HCQ毒副作用较小,耐受性较好,目前没有证据提示HCQ对胎儿存在不良影响。故对于常规抗凝治疗效果不佳的患者,可联合使用HCQ。其主要机制可能是通过降APA的滴度,抑制β2-GP1与磷脂双分子层结合从而使其不能发挥作用,或抑制GPⅡb/Ⅲa通路阻断血小板聚集和黏附,从而改善胎盘局部血液循环。但其对难治性APS妊娠结局的疗效评估、作用机制及安全性问题仍须进一步研究。
