GnRH-a降调节-HRT内膜准备方案在PCOS首次FET移植失败人群中的应用
2019-10-16孙晓晓李欢李东晗陈圆辉王雪张翠莲
孙晓晓,李欢,李东晗,陈圆辉,王雪,张翠莲
(河南省人民医院,河南省生殖医院,郑州大学人民医院,郑州 450003)
多囊卵巢综合征(PCOS)是一种以月经稀发、高雄激素血症、胰岛素抵抗、不孕为主要特征的育龄期女性最常见的内分泌疾病。据文献报道,PCOS患者在体外受精-胚胎移植(IVF-ET)治疗中卵巢过度刺激综合征(OHSS)的总发生率高达20%~30%[1]。随着玻璃化冷冻技术的发展,冻融胚胎移植(FET)作为IVF-ET的重要衍生技术在临床上得到了广泛应用,其有效降低了OHSS的发生风险[2]。而FET周期中的胚胎发育潜能、子宫内膜容受性及子宫内膜与胚胎发育的同步性是影响FET临床妊娠结局的主要因素,因此选择合理的内膜准备方案至关重要。降调节方案最早应用于临床,但逐渐被非降调节方案取代,近期文献提示应用长效GnRH-a降调节后人工周期内膜方案可能改善PCOS患者的FET结局[3]。结合降调节FET在本中心的应用情况,本文通过回顾性分析2016年1月至2019年5月河南省人民医院生殖中心行FET的PCOS患者的临床资料,探究降调节FET在有1次移植失败史的PCOS人群中的应用。
资料与方法
一、研究对象
2016年1月至2019年5月于河南省人民医院生殖中心行FET的PCOS患者。
纳入标准:按照2003年欧洲人类生殖和胚胎年会与美国生殖医学学会(ESHRE/ASRM)修订的鹿特丹标准诊断为PCOS的患者;因卵巢过度刺激或其他原因行全胚冷冻的患者;首次FET失败行第二周期FET的患者。
排除标准:患者双方任何一方有染色体异常;子宫畸形;有子宫内膜结核病史;宫腔粘连;子宫腺肌症或者子宫肌瘤压迫宫腔者;有输卵管积水或宫腔积液;子宫内膜息肉;植入前胚胎遗传学诊断(PGD)/植入前胚胎遗传学筛查(PGS)周期;转化日内膜<7 mm的患者。
共纳入符合标准的553个FET周期。根据在子宫内膜准备过程中是否应用长效GnRH-a降调节,将553个周期分成2组:降调节-激素替代治疗(HRT)组(A组,221个周期),HRT组(B组,332个周期);再根据胚胎情况分为不同亚组:降调节-HRT卵裂期组(A1组,101个周期),HRT卵裂期组(B1组,122个周期 ),降调节-HRT囊胚组(A2组,120个周期),HRT囊胚组(B2组,210个周期)。
二、诊疗回顾
1.胚胎来源:卵巢刺激方案主要包括早卵泡期长效长方案、黄体中期短效长方案及拮抗剂方案,IVF-ET均按本中心常规进行。取卵后第3天(卵裂期胚胎)或者第5~6天(囊胚)根据患者情况评估,将可利用胚胎进行移植,达到冷冻标准的胚胎进行冻存,择期行FET。
2.内膜准备:本中心对于因各种原因行全胚冷冻首次FET的PCOS患者,常规行单纯人工周期内膜准备方案,对有1次移植失败史的患者再次FET时部分患者行降调节后人工周期准备内膜方案。
降调节FET:于月经周期第2~4天皮下注射GnRH-a(达菲林,博福-益普生,法国),注射后第14天,当达到降调标准时给予补佳乐(拜耳,德国)3~4 mg/次,2次/d,口服,一周后行阴道B超检查监测卵泡发育及子宫内膜厚度与声像情况,根据子宫内膜厚度情况决定是否添加17β-雌二醇片(芬吗通红片,雅培制药,美国)。当子宫内膜厚度≥7 mm时给予地屈孕酮片(达芙通,苏威制药,荷兰,10 mg/片)10 mg口服,3次/d,联合8%黄体酮阴道缓释凝胶(雪诺同,默克雪兰诺,德国,90 mg/支)90 mg阴道给药,1次/d,或黄体酮软胶囊(安琪坦,法杏大药厂,法国,100 mg/粒)200 mg阴道给药,2次/d,转化内膜。转化后第4天移植卵裂期胚胎,第6天移植囊胚期胚胎。
单纯人工周期:月经第2~4天给予补佳乐,期间药物调整同降调节FET,当子宫内膜厚度≥7 mm时给予地屈孕酮片口服,10 mg,每日2次,联合8%黄体酮阴道缓释凝胶90 mg阴道给药,1次/d,或黄体酮软胶囊200 mg阴道给药,2次/d,转化内膜。转化后第4天移植卵裂期胚胎,第6天移植囊胚期胚胎。
3.黄体支持:转化日开始直到移植14 d查血HCG≥30 U,建议继续用药,直到移植后35 d开始逐渐减药。
4.胚胎复苏及移植:所有胚胎均采用玻璃化冷冻与快速复温法复苏。优质胚胎:第3天(D3)卵裂期胚胎,卵裂球数目为7~9个,胞质均匀,形态规则,碎片<10%或囊胚评分在3BB及以上。不符合优质胚胎标准的为非优质胚胎。
5.妊娠结局判断:移植后14 d抽血测血清β-HCG,移植后第4~5周在阴道超声下见妊娠囊、胎芽及胎心搏动者确定为临床妊娠。
6.观察指标:比较A组与B组、C组与D组患者的一般情况及临床结局相关指标,如:胚胎种植率、临床妊娠率、异位妊娠率、早期流产率。移植后28 d行B超检查,有孕囊者为临床妊娠;异位妊娠记为临床妊娠。早期流产定义为孕12周内自然流产。
三、统计学方法
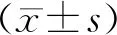
结果
一、A组与B组一般资料、实验室指标及妊娠结局比较
共纳入符合入组标准的553个周期,总妊娠率为64.92%。A组与B组的平均年龄、不孕年限、体重指数(BMI)、移植胚胎个数、内膜厚度等比较均无显著性差异(P>0.05);B组的囊胚移植比例显著高于A组,卵裂期胚胎移植比例显著低于A组(P<0.05)(表1)。两组的妊娠结局比较,种植率、临床妊娠率、早期流产率及宫外孕率均无显著性差异(P>0.05)(表2)。
二、A1组与B1组一般资料、实验室指标及妊娠结局比较
A1与B1组间比较,一般资料及实验室各指标均无显著性差异(P>0.05)(表3)。两组的妊娠结局比较,A1组的临床妊娠率、胚胎种植率有高于B1组的趋势,早期流产率有低于B1组的趋势,但均无显著性差异(P>0.05)(表4)。
三、A2组与B2组一般资料、实验室指标及妊娠结局比较
A2与B2组间比较,其一般资料及实验室指标均无显著性差异(P>0.05)(表5)。两组的临床妊娠率、胚胎种植率、早期流产率及宫外孕率相近,组间比较均无显著性差异(P>0.05)(表6)。
四、Logistic回归分析结果
以临床妊娠为因变量,对平均移植胚胎数、平均移植优胚数、子宫内膜厚度、是否应用降调节-HRT内膜准备方案等因素进行Logistic回归分析提示:总数据:平均移植胚胎数、平均移植优胚数、是否为囊胚移植是入组所有患者临床妊娠的主要影响因素;卵裂期胚胎移植组:平均移植胚胎数、是否行GnRH-a降调节是临床妊娠的主要影响因素;囊胚移植组:平均移植胚胎数、平均移植优胚数是临床妊娠的主要影响因素(表7)。
表1 A、B两组患者一般资料及实验室指标比较[(-±s),%]
注:与A组比较,*P<0.05

表2 A、B两组患者妊娠结局比较(%)
表3 A1、B1组患者一般资料及实验室指标比较(-±s)

表4 A1、B1组患者妊娠结局比较(%)
表5 A2、B2组患者一般资料及实验室指标比较(-±s)
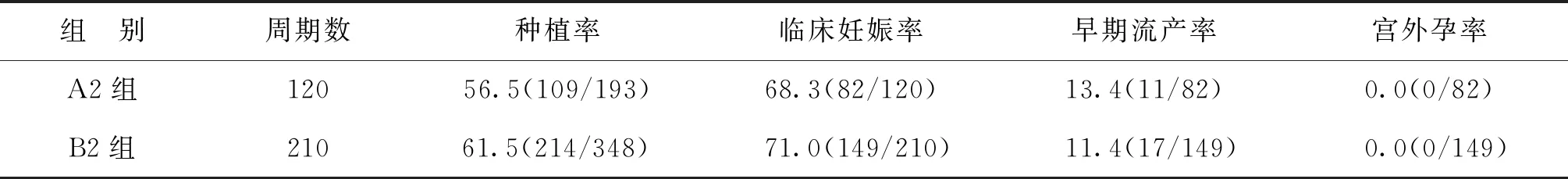
表6 A2、B2组患者妊娠结局比较(%)
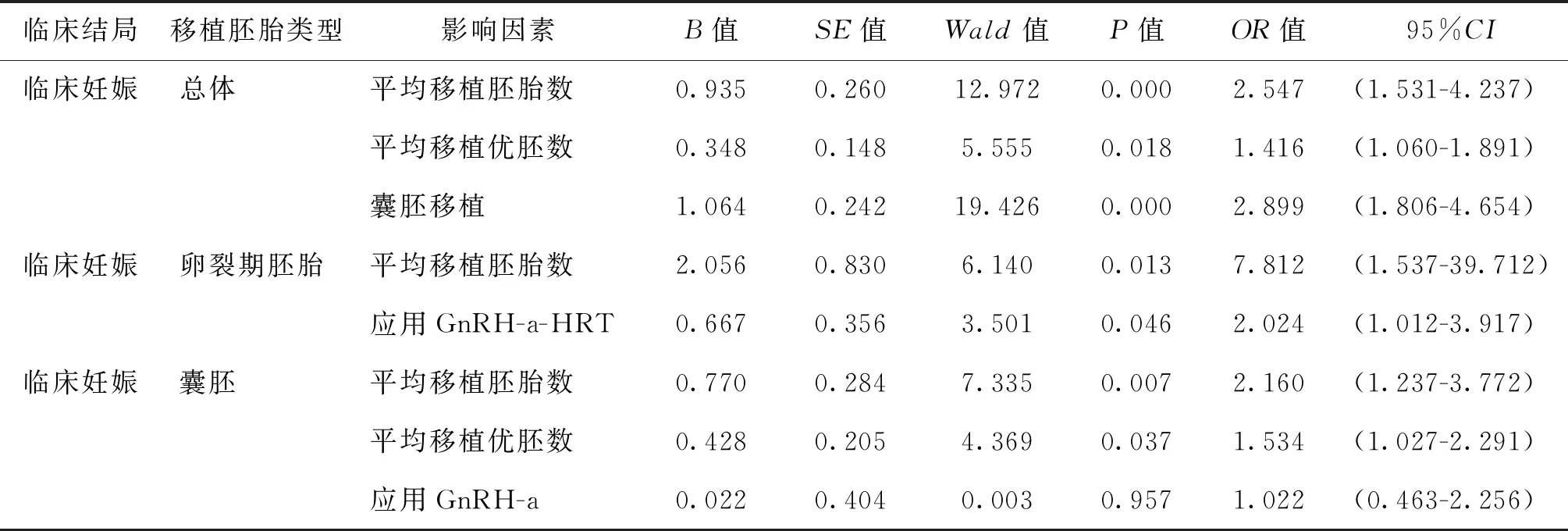
表7 临床妊娠结局相关影响因素Logistic回归分析
讨论
PCOS患者行IVF助孕时获卵及可利用胚胎数较多,同时PCOS患者因OHSS高危倾向而行全胚冷冻择期行FET的人群越来越多。Chen等[4]的一项多中心随机对照试验(RCT)研究表明,PCOS患者行FET较新鲜胚胎移植具有更高的活产率及更低的OHSS发生风险。国外的一项Meta分析也提示在高反应人群中,FET的活产率要高于新鲜移植活产率[2]。因此本研究比较降调节内膜准备方案在首次FET移植失败的PCOS患者中的应用。
一项纳入FET助孕失败、尚有冷冻胚胎的PCOS患者研究的结果提示,对于有移植失败史的PCOS患者,降调节-HRT方案准备子宫内膜其FET周期临床妊娠率及种植率均显著高于HRT组FET周期妊娠结局[5]。但此研究未排除反复移植失败对研究结局的影响,而本研究筛选行全胚冷冻的PCOS患者首次FET失败再次行FET的患者,排除了这一影响因素。张京顺等[3]认为对曾有过移植失败史的PCOS患者FET周期应用降调节-HRT方案准备子宫内膜,可以改善FET周期临床结局。但该研究未对卵裂期胚胎移植及囊胚移植进行分组分析,本研究在进行分组分析后发现降调节-HRT在首次FET失败后的PCOS患者行卵裂期胚胎移植时可以改善临床结局,但在囊胚组并未观察到此现象。之前有回顾性队列研究分析提示,对于有高雄激素血症的PCOS患者行FET时,GnRH-a降调节-HRT周期准备内膜相比于直接替代周期方案准备内膜能增加持续妊娠率,临床妊娠率无明显差别[6]。国外学者Hill等[7]认为,在囊胚移植中HRT内膜准备方案可以得到较好的妊娠率,而降调节可以使内膜与胚胎更同步,可以得到更高的活产率。本研究结果提示对于首次FET失败的患者再次行囊胚移植时,是否应用降调节-HRT内膜准备方案对临床结局无影响。
Logistic回归分析显示,是否应用GnRH-a、平均移植胚胎数为卵裂期胚胎移植临床结局的影响因素。提示排除混杂因素的影响后,降调节-HRT是首次FET移植失败的PCOS患者行卵裂期胚胎移植时临床结局的影响因素,可能因数据量偏小,独立样本t检验统计学无差异,后续研究需要继续扩大样本量进一步分析探讨。既往也有研究表明移植2个胚胎改善妊娠结局[7],本研究结果与之相似,认为移植胚胎个数是临床结局的影响因素,但临床工作中控制移植胚胎个数,降低双胎或多胎妊娠率,减少母婴并发症也是临床中的重点工作之一。本研究结果显示流产率及宫外孕率各组间比较无显著性差异,这和之前一些文献[3-8]研究结果一致。
关于其可能的影响机制探讨,之前国内一项RCT研究提示,超生理剂量的E2水平可能影响PCOS人群妊娠结局[9]。郭燕红等[10]发现长期应用大剂量雌激素会致小鼠子宫内膜着床窗口期缩短。GnRH-a降调节后可能通过抑制内源性雌激素水平,形成低雌内环境,提高子宫内膜容受性,改善胚胎和子宫内膜同步性,从而改善临床结局。PCOS患者的血清FSH/LH多呈倒置状态,体内过高LH水平会使子宫内膜过早转化,内膜发育与胚胎着床不同步,导致胚胎种植率下降[11-12]。国内一项回顾性研究提示,降调节方案可明显降低移植前后的LH水平,增加种植率和临床妊娠率[13]。但本研究未涉及降调节前后及各组间激素水平的比较,且尚未随访到活产率是本研究的不足之处,后期会进一步完善实验设计加以探讨。国外有学者研究表明,新鲜周期HCG注射日孕酮升高、子宫内膜过早转化影响卵裂期胚胎妊娠结局,而对囊胚移植却没有影响[14],在FET周期中GnRH-a降调节后可能通过降低移植前LH水平,抑制子宫内膜过早转化,从而改善卵裂期胚胎移植结局,对囊胚移植亦无影响。另有研究表明囊胚相对于卵裂期胚胎具有更好的发育潜能,着床过程更符合生理状态,与子宫内膜种植窗具有更好的同步性[15-16],降调节内膜准备方案在卵裂期胚胎移植组可以通过提高卵裂期胚胎和子宫内膜同步性,从而改善临床结局,却不影响囊胚移植的临床结局。
综上所述,GnRH-a降调节内膜准备方案在首次FET失败的PCOS患者行卵裂期胚胎移植时可能改善临床结局,但需要前瞻性或更大样本量的研究去深入探究。
