华蟾素注射液联合全身化疗治疗中晚期乳腺癌的临床效果
2019-09-25孙成刘艳翠赵微
孙成 刘艳翠 赵微
[摘要]目的 探讨中晚期乳腺癌患者应用华蟾素注射液联合全身化疗的效果。方法 选取2016年1月~2018年1月本院收治的112例中晚期女性乳腺癌患者作为研究对象,随机分为试验组(56例)和对照组(56例)。对照组采用化疗方案,试验组采用华蟾素注射液联合全身化疗方案。比较两组的临床疗效、生活质量变化情况以及不良反应发生率。结果 治疗后,试验组的总有效率为73.21%(41/56),明显高于对照组的53.57%(30/56),差异有统计学意义(χ2=4.655,P=0.031);试验组的生活质量明显优于对照组,差异有统计学意义(P<0.05)。治疗后,试验组的急性皮疹、胃肠道反应发生率明显低于对照组(χ2=11.720、6.619,P=0.001、0.010)。结论 对于中晚期乳腺癌患者,华蟾素注射液联合全身化疗的临床疗效显著,可明显改善其生活质量,且不良反应少。
[关键词]华蟾素注射液;全身化疗;中晚期乳腺癌;临床疗效
[中图分类号] R737.9 [文献标识码] A [文章编号] 1674-4721(2019)7(b)-0043-03
[Abstract] Objective To investigate the effect of Cinobufotalin Injection combined with systemic chemotherapy in patients with advanced breast cancer. Methods A total of 112 women with advanced breast cancer admitted to our hospital from January 2016 to January 2018 were selected and randomly divided into the experimental group (56 cases) and the control group (56 cases). The control group was treated with chemotherapy, while the experimental group was treated with Cinobufotalin Injection combined with systemic chemotherapy. The clinical efficacy, quality of life and the incidence of adverse reactions were compared between the two groups. Results After treatment, the total effective rate of the experimental group was 73.21% (41/56), which was significantly higher than 53.57% of the control group (30/56), with statistical significance (χ2=4.655, P=0.031). The quality of life of the experimental group was significantly better than that of the control group, and the difference was statistically significant (P<0.05). After treatment, the incidence of acute rash and gastrointestinal reaction in the experimental group was significantly lower than that in the control group (χ2=11.720, 6.619; P=0.001, 0.010). Conclusion For patients with advanced breast cancer, Cinobufotalin Injection combined with systemic chemotherapy has significant clinical efficacy, which can significantly improve their quality of life, and less adverse reactions.
[Key words] Cinobufotalin Injection; Systemic chemotherapy; Advanced breast cancer; Clinical efficacy
乳腺癌是發生在乳腺腺上皮组织的恶性肿瘤,近年来,其发病率呈逐渐上升的趋势。目前,乳腺癌对女性身心健康造成极大的影响,已成为当前社会的重大公共卫生问题[1]。原位乳腺癌并不致命,但由于乳腺癌细胞之间连接松散,容易脱落,使游离的癌细胞随血液或淋巴液播散全身,发生转移,导致病情恶化[2]。乳腺癌不易诊治,早期发现、早期诊断是提高疗效的关键。化疗虽然可有效杀死乳腺癌细胞,但亦存在胃肠道反应、骨髓抑制等毒副作用,使患者难以耐受。相关研究显示[3],华蟾素注射液具有解毒、消肿、镇痛的功效,可用于中、晚期肿瘤,明显提高患者的生活质量,且不良反应较小。本研究旨在探讨中晚期乳腺癌患者应用华蟾素注射液联合全身化疗的临床疗效,现报道如下。
1资料与方法
1.1一般资料
选取2016年1月~2018年1月本院收治的112例中晚期女性乳腺癌患者作为研究对象,年龄33~66岁,平均(42.67±3.12)岁。随机将112例患者分为试验组(56例)和对照组(56例)。试验组中,年龄33~66岁,平均(41.85±2.25)岁;对照组中,年龄35~66岁,平均(43.56±3.02)岁。两组患者的年龄等一般资料比较,差异无统计学意义(P>0.05),具有可比性。此外,本研究符合相关医学伦理学标准。
1.2纳入与排除标准
1.2.1纳入标准 ①对华蟾素不过敏者;②预期生存期>3个月;③近2个月内未使用其他抗肿瘤药者;④患者及家属均已签署知情同意书者;⑤依从性较好者。
1.2.2排除标准 ①KPS评分<60分者;②合并其他部位恶性肿瘤者;③心血管疾病者;④妊娠期妇女;⑤存在神志不清、沟通表达障碍者;⑥依从性较差者。
1.3实施方法
1.3.1对照组疗法 应用TEC化疗方案,具体为多西他赛(浙江海正药业股份有限公司,国药准字 H20093092,规格:0.5 ml︰20 mg)75 mg/m2+表柔比星(北京协和药厂,国药准字 H20143165,规格:0.1 g)80 mg/m2+环磷酰胺(通化茂祥制药有限公司,国药准字 H22026738,规格:50 mg)500 mg/m2静脉滴注,每个疗程为21 d,维持2个疗程;在治疗过程中,采用5-羟色胺拮抗剂酮舍林和严格的水化治疗,保持患者良好的胃肠道功能,防止其发生严重呕吐并减轻痛苦。
1.3.2试验组疗法 在对照组疗法的基础上采用华蟾素注射液(安徽华润金蟾药业股份有限公司,国药准字 Z34020273,规格:5 ml/支),并加入5%葡萄糖注射液500 ml稀释,静脉滴注,1次/d,15 ml/次。每个周期为7 d,休息2 d,每个疗程为4个周期,维持2个疗程。
1.4观察指标
比较两组的临床疗效、生活质量、不良反应发生率,其中临床疗效评价标准如下。完全缓解:治疗后肿瘤完全消失,未出现新病灶;部分缓解:治疗后肿瘤缩小>50%,未出现新病灶;无变化:治疗后肿瘤缩小包块缩小25%~50%或无显著好转,未出现新病灶;进展:治疗后肿瘤缩小<25%,出现新病灶[4]。总有效率=(完全缓解+部分缓解)例数/总例数×100%。生活质量评价采用卡氏评分(Karnofsky,KPS)[5],得分越高,健康状况越好,变化<10分为稳定,增加≥10分为提高,降低≥10分为下降。不良反应包括急性皮疹、胃肠道反应、肝肾功能异常、骨髓抑制、心脏毒性等。
1.5统计学方法
采用SPSS 22.0统计学软件对数据进行分析,计量资料以均数±标准差(x±s)表示,采用t检验,计数资料以率(%)表示,采用χ2检验,等级资料采用秩和检验,以P<0.05为差异有统计学意义。
2结果
2.1两组患者临床疗效的比较
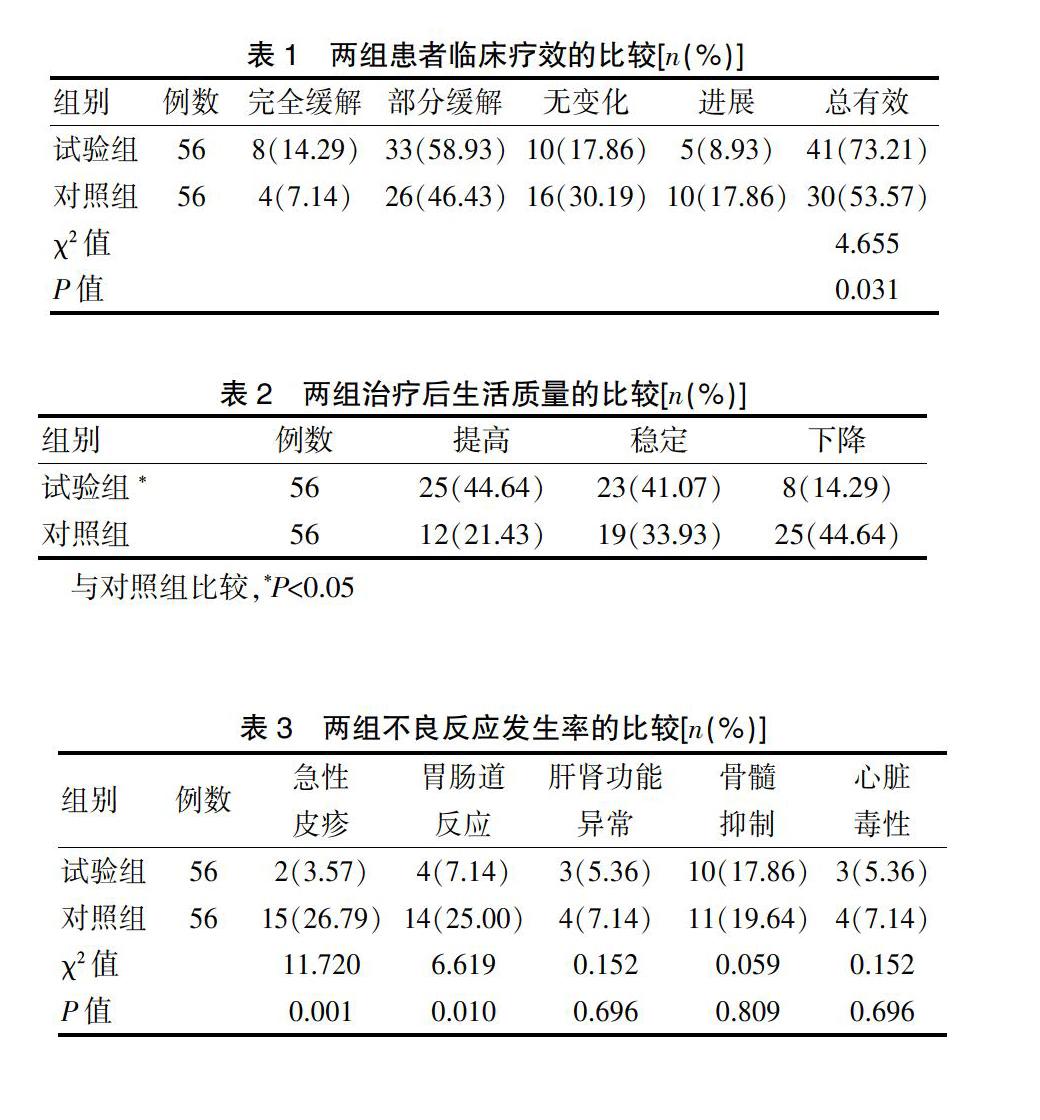
试验组治疗后的总有效率为73.21%(41/56),明显高于对照组的53.57%(30/56),差异有统计学意义(χ2=4.655,P=0.031)(表1)。
2.2两组治疗后生活质量的比较
试验组治疗后的生活质量显著优于对照组,差异有统计学意义(P<0.05)(表2)。
与对照组比较,*P<0.05
2.3兩组不良反应发生率的比较
试验组的急性皮疹、胃肠道反应发生率明显低于对照组(χ2=11.720、6.619,P=0.001、0.010);两组的肝肾功能异常、骨髓抑制、心脏毒性发生率比较,差异均无统计学意义(P>0.05)(表3)。急性皮疹、胃肠道反应、骨髓抑制为主要不良反应,肝肾功能异常和心脏毒性为偶发不良反应。
3讨论
相关研究显示,近年来乳腺癌的发病率呈不断上升趋势[6]。乳腺的癌细胞易通过血液或淋巴结循环而发生活跃的转移、扩散,严重威胁患者的身体健康和生命安全。乳腺癌早期无明显的症状,不易确诊,导致多数女性患者未及时接受治疗,直至发现时,病情已进展至中晚期,从而加大了该病的治疗难度。中晚期乳腺癌的治疗通常是化疗,目前,TEC化疗方案可在一定程度上控制恶性肿瘤细胞[7]。然而,化疗只能按照一定的比例杀死部分乳腺癌细胞,并且由于患者恶病质、免疫功能降低,使得残余的乳腺癌细胞有机可乘、发展迅速,并形成新的病灶,侵害机体[8]。化疗所需的化学药物种类多、给药剂量大,且产生毒副作用,导致患者正常组织功能丧失,严重影响患者的身心健康,进而限制化学药物的给予剂量,影响治疗效果[9]。
近年来,以增强疗效、减少不良反应为目的的辅助化疗方案受到重视[10]。华蟾素注射液是干蟾皮经提取制成的灭菌水溶液,内含蝶啶类、强心苷元以及吲哚类生物碱活性成分,具有解毒、消肿、镇痛之功效,可抑制肿瘤细胞、增强免疫功能,常被应用于中晚期肿瘤的治疗[11]。华蟾素可明显增强巨噬细胞的吞噬作用,有效吞噬肿瘤细胞,并通过调控细胞周期蛋白cyclin(A1,D1,E1)和p21等因子的表达,有效促进肿瘤细胞凋亡,并增强免疫功能,从而抑制乳腺癌细胞侵袭和增殖的作用[12]。相关研究显示[13],华蟾素联合化疗的疗效显著,可增强免疫功能,有效消灭残余的乳腺癌细胞,从而使病情得到有效控制。病理分析结果显示[14],华蟾素可在一定程度上使乳腺癌细胞数目减少、肿瘤体积缩小。
在化疗过程中,乳腺癌患者会出现胃肠道反应、毛发脱落、急性皮疹、肝肾功能异常、骨髓抑制、心脏毒性等不同程度的不良反应,严重影响其生活质量,部分患者由于无法耐受而被迫中止治疗。相关研究显示[15],中医药对于缓解化疗期间的不良反应具有独特的优势。华蟾素中的华蟾蜍精、蟾蜍苷元活性成分远多于阿霉素等抗生素,并且安全性较高,无毒副作用[16]。在进行单纯化疗方案时,患者的耐受性较差,大剂量给药易产生耐药性,无法取得令人满意的疗效,而华蟾素用于中晚期乳腺癌的辅助治疗可减少化疗次数和给药剂量,降低患者的耐药性,获得令人较满意的疗效。华蟾素注射液联合化疗方案可发挥协同作用,有效减少患者化疗产生的不良反应,提高其生活质量[17-18]。在研究中,试验组的总有效率明显高于对照组;试验组治疗后的生活质量显著优于对照组;治疗后,试验组的急性皮疹、胃肠道反应的发生率明显低于对照组(χ2=11.720、6.619,P=0.001、0.010),而两组的肝肾功能异常、骨髓抑制、心脏毒性发生率比较,差异均无统计学意义(P>0.05)。急性皮疹、胃肠道反应、骨髓抑制为主要不良反应,肝肾功能异常和心脏毒性为偶发不良反应,这是因为华蟾素注射液的毒副作用小,其使试验组的生活质量提高,症状和体征减轻,且有效降低化疗引起的胃肠道反应,增进食欲,明显改善患者的精神状态。
综上所述,对于中晚期乳腺癌患者,华蟾素注射液联合全身化疗的临床疗效显著,可明显改善其生活质量,且安全性高,不良反应少,具有重要的临床推广价值。
[参考文献]
[1]高波,魏晓露,韩玲玉,等.华蟾素注射液中酯蟾毒配基的分离及体内外抗肿瘤活性筛选[J].中国实验方剂学杂志,2017,23(16):86-92.
[2]杜娟,赵秀莉,张文周,等.我院108例化疗致Ⅳ度骨髓抑制的晚期乳腺癌患者用药合理性分析[J].中国药房,2016, 27(20):2756-2758.
[3]Shi J,Gao P,Song Y,et al.Efficacy and safety of taxane-based systemic chemotherapy of advanced gastric cancer:a systematic review and meta-analysis[J].Sci Rep,2017,7(1):5319.
[4]Fracchia AA,Farrow JH,Adam YG,et al.Systemic chemotherapy for advanced breast cancer[J].Cancer,2015,26(3):642-649.
[5]温坚.紫杉醇酯质体或多西他赛联合表柔比星在局部晚期乳腺癌新辅助化疗中的疗效及预后的比较[J].中国临床医生杂志,2018,46(2):190-193.
[6]于童,陈喆.华蟾素注射液治疗中晚期肝癌临床研究进展[J].中西医结合肝病杂志,2017,27(5):319-320.
[7]田金徽,葛龙,娄丽丽,等.中药注射剂联合CF化疗方案治疗乳腺癌有效性及安全性的网状Meta分析和试验序贯分析[J].中国全科医学,2016,19(27):3326-3335.
[8]Wang J,Shi H,Yang G,et al.Combined intra-arterial and intravenous chemotherapy for unresectable,advanced gastric cancer has an improved curative effect compared with intravenous chemotherapy only[J].Oncol Lett,2018,15(4):5662-5670.
[9]Dong HM,Wang Q,Wang WL,et al.A clinical analysis of systemic chemotherapy combined with radiotherapy for advanced gastric cancer[J].Medicine,2018,97(23):e10786.
[10]Hall BR,Cannon A,Atri P,et al.Advanced pancreatic cancer:a meta-analysis of clinical trials over thirty years[J].Oncotarget,2018,9(27):19 396-19 405.
[11]柯紅,崔洁,金锦莲,等.华蟾素胶囊联合CAF方案治疗中晚期乳腺癌的临床效果分析[J].世界中医药,2017,12(10):2358-2361.
[12]马梅梅,朱青山,温文斌,等.恶性肿瘤患者焦虑、抑郁状况调查及影响因素分析[J].长治医学院学报,2016,30(5):354-357.
[13]金京哲.华蟾素注射液治疗晚期恶性肿瘤临床疗效观察[J].世界最新医学信息文摘,2016,16(58):178.
[14]Chan K,Clarke AE,Ramseygoldman R,et al.Breast cancer in systemic lupus erythematosus (SLE):receptor status and treatment[J].Lupus,2018,27(1):120-123.
[15]Sato J,Horinouchi H,Goto Y,et al.Long-term survival without surgery in NSCLC patients with synchronous brain oligometastasis:systemic chemotherapy revisited[J].J Thorac Dis,2018,10(3):1696-1702.
[16]邬晓宇,田芳,朱学军,等.华蟾素抗肿瘤研究进展[J].现代中药研究与实践,2018,32(5):82-86.
[17]周俊,刘明华.华蟾素治疗实体肿瘤的临床研究进展[J].世界最新医学信息文摘,2018,18(14):33-34.
[18]胡慧.中药注射液调节肿瘤化疗患者免疫功能的临床研究进展[J].陕西中医,2018,39(4):543-545.
(收稿日期:2019-01-31 本文编辑:祁海文)
