盐酸合成工艺的物料衡算
2019-09-24单译
单译

摘 要:盐酸在我国的使用范围随着社会工业化的发展越来越广,盐酸的生产工艺不断提高,得到改进。为提高盐酸产量对其合成设备的研究和工艺的改进是极其必要的,文章以年合成6000吨盐酸为例进行物料衡算。
关键词:氯化氢;盐酸;物料衡算
中图分类号:TQ111.3 文献标志码:A 文章编号:2095-2945(2019)25-0118-02
Abstract: The scope of use of hydrochloric acid in China is more and more extensive with the development of social industrialization, and the production process of hydrochloric acid has been improved and improved. In order to increase the output of hydrochloric acid and improve the synthesis equipment and process, this paper takes the annual synthesis of 6000 tons of hydrochloric acid as an exemplar.
Keywords: hydrogen chloride; hydrochloric acid; material balance
1 基础数据及条件
生产规模按6000吨/年计算;生产时间按300天/年(24小时/天)计算;产品要求为31%以上的浓盐酸;储存及包装损失按照0.1%计算;腐蚀等其他损失按0.05%计算。
2 合成炉的物料衡算
根据生产规模和生产时间等条件,计算单位时间合成HCl的产量为:
根据化学反应方程式 Cl2+H2→2HCl可知,为确定反应过程中氯气完全反应,实际生产中控制H2过量,控制进合成炉Cl2与H2的物质的量比为1:(1.05-1.10),取Cl2:H2=1:1.06。根据原料组成和化学反应方程式可以分别计算出反应物和生成物的量。
2.1 进入合成炉各物质的量
(1)原料H2带入H2O(g)的量
(2)原料Cl2带入H2O(g)的量
基本条件:H2O(g)含量按与所在地大气压平衡水蒸气分压计算,H2进合成炉的压力为250mmHg,合成炉进口温度为30℃,查水和水蒸气表得P=4247.0Pa
2.2 合成炉中的物料计算
合成炉内主要发生H2+Cl2→2HCl和2H2+O2→2H2O两个反应,其他副反应因量很小,在工程计算上忽略不计。
(1)主反应
通过分析可知,HCl的生成量为7.0958kmol/h,参与反应的Cl2和H2的量均为3.5479kmol/h,所以参与主反应的H2的量为:
4.1549-3.5479=0.6070(kmol/h)
(2)副反应
假定通过H2与O2反应生成水,O2全部参加反应,剩余部分H2(因H2加入过量),则副反应生成的H2O量为:
0.0423×2=0.0847(kmol/h)
由此可知参与副反应的H2的量也为0.0847kmol/h,系统最后剩余H2的量为:
0.6070-0.0847=0.5223(kmol/h)
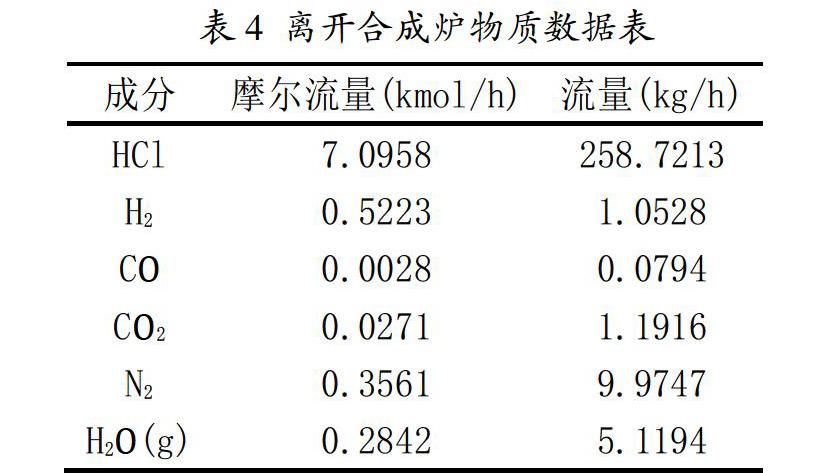
2.3 离开合成炉各物质的量
3 降膜吸收塔与尾部填料吸收塔的物料衡算
3.1 一段降膜吸收塔
离开合成炉的气体组分经过空气的自然冷却进入一段降膜吸收塔顶部,一段降膜吸收塔吸收率为50%。则进入的HCl量为258.7213 kg/h(7.0958kmol/h),离开的HCl量为129.3606kg/h(3.5479kmol/h),H2O(g)则全部被吸收,产生成品盐酸830.0419kg/h。
3.2 二段降膜吸收塔
二段降膜吸收塔吸收率为45%,则进入的HCl量为129.3606kg/h(3.5479kmol/h),离开的HCl量为12.9361kg/h(0.3548kmol/h),产生稀盐酸700.6812kg/h。
3.3 尾部填料塔
尾部填料吸收塔吸收率为5%,则进入的HCl量为12.9361kg/h(0.3548kmol/h),离开的HCl量为0,产生稀盐酸584.2566kg/h。
4 吸收剂的用量
吸收剂清水从尾部填料塔顶部加入,吸收HCl需用水的量为:
5 产品质量核算验证
从一段塔流入储罐盐酸浓度为31.17%大于设计要求的31%,故设计合理。
參考文献:
[1]张述伟.化工单元操作及工艺过程实践[M].大连:大连理工大学出版社,2015,6.
[2]于志家,赵宗昌.化工过程物料衡算与能量衡算[M].大连:大连理工大学出版社,2008,5.
[3]张晓春.盐酸生产中的物料和能量衡算[J].氯碱工业,2010,46(10):27-31.
[4]吴志泉,涂晋林,徐汛.化工工艺计算[M].上海:华东化工学院出版社,1992,10.
[5]刘光启,马连湘,刘杰.化学化工物性数据手册(无机卷)[M].北京:化学工业出版社,2002,3.
[6]北京石油化工工程公司.氯碱工业理化常数手册[M].北京:化学工业出版社,1988,11.
