碳酸盐对煤焦的催化气化作用及动力学研究*
2019-09-23李令权李寒旭毛立睿窦媛媛郑久强
李令权 李寒旭 毛立睿 窦媛媛 胡 侠 郑久强
0 引 言
煤气化是煤化工产业的关键技术,也是煤清洁利用的核心技术,是生产清洁燃料和煤基化学品等工业的基础[1]。大力发展煤气化技术,减少煤炭直接燃烧带来的环境污染,提高资源利用率,对我国的经济发展和环境保护都有重要意义。
传统的煤气化技术存在操作温度高、能耗高、原料煤反应不充分导致粗渣中残碳含量高等问题,而催化剂的应用可显著降低煤气化反应温度,提高反应速率,因此煤催化气化技术受到了越来越多的研究者关注[2-4]。张志远等[5]研究了四种钠盐对准东煤与CO2反应性影响,结果表明,催化剂的活性由强到弱依次为Na2CO3,NaHCO3,Na2SO4,NaCl。闫小霞等[6]研究了含有不同阴离子的钾、钠、铁催化剂对府谷煤与CO2反应性的影响,结果表明,对于钾、钠催化剂,催化剂的活性由强到弱依次为K2CO3和Na2CO3,K2SO4和Na2SO4,KCl和NaCl。对于铁盐催化剂,催化剂的活性由强到弱依次为FeSO4,FeCl2。张云等[7]研究了五种催化剂对不同煤阶煤焦的催化气化作用,结果表明,催化剂的负载均降低了煤焦气化的初始温度,最多的降低了200 ℃,催化剂活性由强到弱依次为K2CO3,Na2CO3,KCl,Fe(NO3)3,CaO。DING et al[8]研究了Na2CO3负载量在5%~15%时,对两种不同煤阶煤的催化作用,结果表明,遵义煤的反应活性与Na2CO3负载量成正比,而随着Na2CO3负载量的增加,神府煤的反应活性先提高后降低。WANG et al[9]研究了一种Ca(OH)2和K2CO3混合型的催化剂,结果表明,负载该催化剂后,煤焦的气化速率明显高于原煤焦。王少龙等[10]以贵州无烟煤为研究对象,探究了不同的制焦方式及CaCO3添加量对煤焦气化活性的影响,结果表明,先制焦再添加CaCO3的气化活性比先添加CaCO3再制焦的气化活性高,气化活性随CaCO3负载量增加先增大后趋于稳定。
结合目前煤催化气化的研究现状,可知煤催化气化所用的催化剂大多是碱金属(如K+,Na+)[11-12]、碱土金属(如Ca2+和Mg2+)[13-14]和过渡金属(如Fe2+/Fe3+和Ni2+)[15-16],其中碱金属是最活跃的。研究表明,煤催化气化过程受到很多因素影响,如煤阶、催化剂种类、催化剂负载方式、催化剂负载量和气化条件等[17-18]。目前,对催化剂的作用机理尚不清楚,因此,有必要对其进行深入研究。为进一步利用催化技术解决粗渣中残碳含量高的问题,本实验选用了钠、钾、钙三种碳酸盐为催化剂,考察其对不同煤阶煤焦催化气化的影响,从而为清洁高效地利用煤炭资源提供参考。
1 实验部分
1.1 原料煤
实验选用三种不同等阶的煤样,分别为印尼褐煤(YN)、大同烟煤(DT)、卧龙湖无烟煤(WLH)。原煤经破碎后筛分粒径<74 μm的粉煤,煤样的工业分析和元素分析数据见表1,煤灰化学组成分析见表2。由表1和表2可知,YN的灰分最低,为5.65%,WLH的挥发分最低,为6.89%;YN的Na含量比DT和WLH高,为4.12%,属于高钠煤。

表1 煤样的工业分析和元素分析Table 1 Proximate and ultimate analysis of coal samples
* By difference.

表2 煤样的灰化学组成分析(%*)Table 2 Ash composition analysis of coal samples(%*)
* Mass fraction.
1.2 焦样制备
煤焦的制备在通氮气的管式炉中进行,其结构如图1所示。将原煤放入Al2O3坩埚中,置于刚玉管中心,通入300 mL/min的N2(99.9%),由室温以30 ℃/min的升温速率,升温至900 ℃,并在此温度下保温1 h,反应结束后冷却至室温,得到煤焦样品。
1.3 催化剂负载
催化剂选取K2CO3,CaCO3和Na2CO3,催化剂的负载量为煤焦质量的10%,负载方式为机械搅拌。将催化剂和煤焦按上述配比称取后,充分混合均匀,密封备用。YN煤焦负载10%的K2CO3催化剂,记为YN-K2CO3,依此类推。
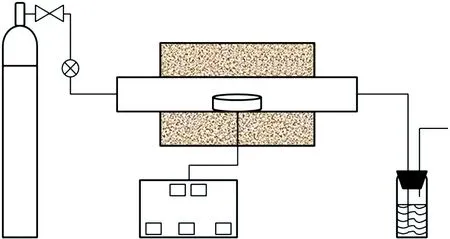
图1 煤焦制备系统Fig.1 Schematic diagram of coal char preparation system
1.4 气化实验
采用程序升温法进行气化实验,煤焦的二氧化碳气化实验在耐驰公司生产的STA 449 F3热重分析仪中进行。实验条件为:以15 ℃/min的升温速率由30 ℃升温至1 400 ℃,每次样品质量控制为(10±0.5) mg,N2(99.999%)作保护气,流量为20 mL/min,炉膛通CO2(99.999%)和N2(99.999%),流量均为50 mL/min。
碳转化率定义为wc,其表达式为:
(1)
式中:wc为碳转化率,%;m0为煤焦的初始质量,mg;mt为反应时间为t时的煤焦质量,mg;mend为反应结束后煤焦质量,mg。
2 结果与讨论
2.1 气化起始温度及终止温度
图2所示为煤焦与CO2气化反应的TG-DTG曲线。由图2可知,气化反应初始温度t0及终止温度tend的定义为过DTG峰值垂直于横坐标的直线与TG曲线相交于A点,过A点作TG曲线的切线分别与TG曲线的平行线相交于B点和C点,分别为气化反应初始温度和终止温度。
2.2 碳酸盐的催化气化作用特性
负载催化剂后煤焦的碳转化率及气化反应速率如图3所示。由图3可知,负载催化剂后,三种煤焦的气化活性均有不同程度的提高,且K2CO3和Na2CO3的催化效果优于CaCO3。
原煤煤焦及负载催化剂后煤焦的气化反应特征参数见表3。由表3可以看出,对于YN,DT和WLH煤焦,负载10%的K2CO3后,气化初始温度t0分别提前了77 ℃,182 ℃和178 ℃,气化终止温度tend分别提前了96 ℃,223 ℃和207 ℃。负载10% Na2CO3后,t0分别提前了90 ℃,176 ℃和174 ℃,tend分别提前了109 ℃,200 ℃和154 ℃;负载10% CaCO3后,t0分别提前了10 ℃,19 ℃和28 ℃,tend分别提前了7 ℃,40 ℃和7 ℃。最大气化反应速率也均有不同程度的提高。
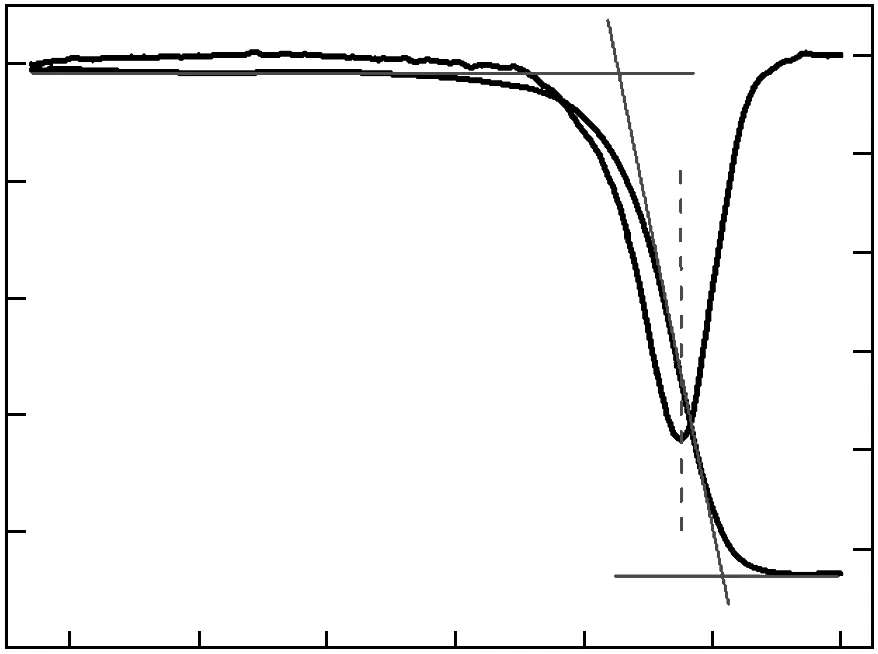
图2 气化初始温度和终止温度Fig.2 Gasification initial temperature and termination temperature definition

图3 煤焦碳转化率和气化反应速率随温度的变化曲线Fig.3 Change curves of conversion rate and gasification reaction rate of coal char with temperature
由图3和表3还可知,与原煤焦相比,负载催化剂后碳转化率曲线及气化反应速率曲线均向低温区偏移,催化剂的加入降低了气化初始温度和终止温度,提高了煤焦的气化反应速率,在相同的反应时间内,使样品气化更充分,可有效减少粗渣中的残碳含量。负载碱金属钾、钠催化剂效果显著,这是由于碱金属抑制煤焦碳晶结构形成,降低煤焦的石墨化程度,从而提高了气化反应速率[19]。文献[20]表明,催化剂的催化效果和催化剂的流动性有关,流动性越好,就能很好地分散在C基质的表面,接触面就越大,因此,催化效果就越明显。由于CaCO3的流动性较差,导致其催化效果较差。
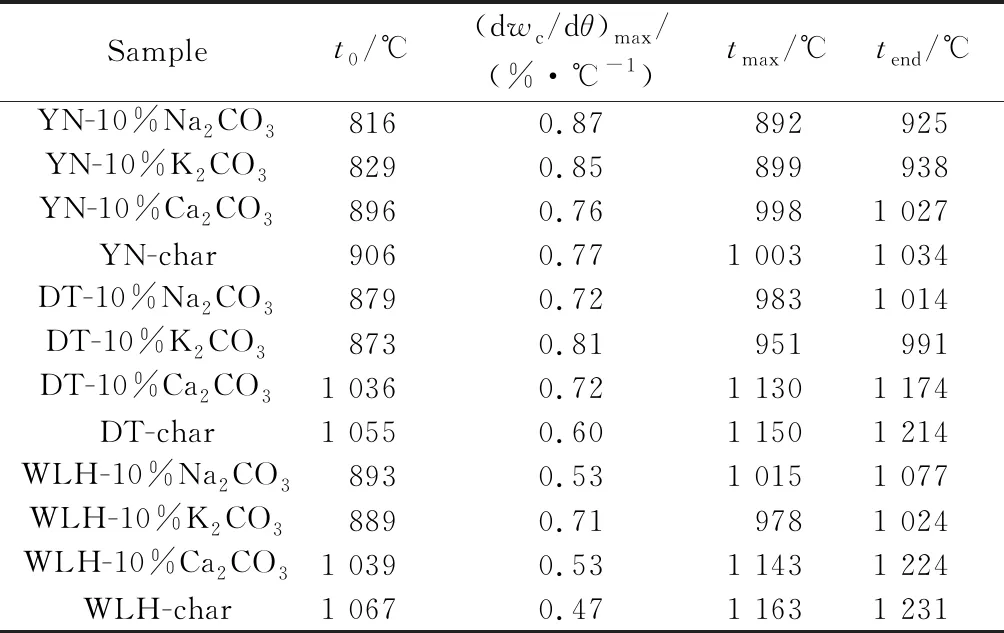
表3 煤焦负载催化剂前后的气化反应特征参数Table 3 Characteristic parameters of coal chars gasification reaction before and after loaded catalyst
Note:tmaxmeans the temperature when (dwc/dθ) reaches the maximum.
煤焦的气化活性以反应活性指数以R0.5[21]表示,计算方法见公式(2):
(2)
式中:R0.5为反应性指数,min-1;τ0.5为碳转化率达到50%时的气化时间,min。
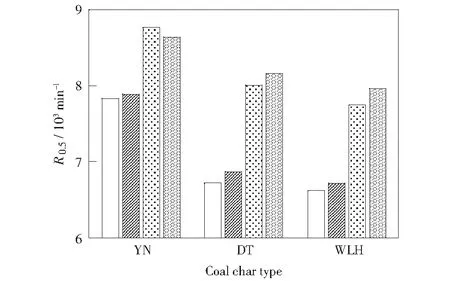
图4 煤焦反应性指数Fig.4 Gasification index of coal char
2.3 动力学分析
本实验采用缩核模型(SCM)[22]处理实验数据,进行动力学分析,缩核模型假设气-固两相反应只在固体颗粒的外表面进行,随着时间的推移,反应的作用面逐渐由外向内迁移,未反应核逐渐减小。反应见公式(3):
(3)
式中:E为表观活化能,kJ/mol;R为通用气体常数,R=8.314 J/(mol·K);T为热力学温度,K;β为升温速率,K/min。
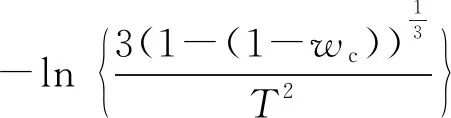
图5为煤焦及负载催化剂后动力学拟合结果。并由图5计算得到动力学参数。表4为缩核模型对煤焦及负载催化剂后计算得到的动力学参数。由表4可知,所有样品的相关系数R2数均在0.958以上,说明用该模型来描述煤焦的气化反应是可行的。负载K2CO3,CaCO3,Na2CO3三种催化剂后,三种煤焦反应活化能都有所降低;但负载CaCO3后煤焦活化能降低并不明显,其催化效果弱于K2CO3和Na2CO3。YN煤焦、DT煤焦和WLH煤焦负载10%K2CO3后,活化能分别降低14.64 kJ/mol,19.63 kJ/mol,21 kJ/mol;负载10% Na2CO3后,活化能分别降低4.88 kJ/mol,12.30 kJ/mol,19.84 kJ/mol,负载CaCO3后,活化能分别降低1.49 kJ/mol,9.67 kJ/mol,11.98 kJ/mol。
2.4 催化气化作用机理分析
催化剂可以侵蚀固体表面,起到开槽的作用,使反应表面的活性位数量增多,比表面积变大,从而提高气化反应速率[23-24]。一般催化气化反应速率随碳转化率的变化大致可分为四个阶段(见图6)。由图6可知:1) 反应速率增长阶段(反应开始至x1),这一阶段主要是催化剂对固体表面的侵蚀开槽,提高活性位数量,使反应速率迅速增加;2) 反应速率缓慢增长升或停止增长阶段(x1~x2),当转化率达到特征转化率x1时,固体反应物不断被消耗,活性部位不断扩展,使某些可能成为活性位的微孔被相邻的活性空间吞没,导致实际活性位数量减少,因此,反应速率增长缓慢甚至停止增长;3) 反应速率再次迅速成长阶段(x2~x3),当转化率达到临界转化率x2后,随着固体反应物的不断消耗,催化剂相对含量增加,使孔隙率增大,这些因素对反应速率的影响超过了由于微孔的吞并而使活性位减少的不利影响,使反应速率再次增长;4) 反应速率迅速下降阶段(x3至反应结束),当转化率达到临界转化率x3后,反应物剩余极少,煤焦孔隙空间较大,导致反应气分子游离的空间增大,与煤焦表面的固有活性位碰撞几率减小,使得本阶段反应速率迅速下降。

图5 SCM对煤焦载催化剂前后的拟合曲线Fig.5 Fitting curve of SCM on coal chars before and after loading catalyst

SampleR2E/(kJ·mol-1)YN-10%Na2CO30.980174.97YN-10%K2CO30.985165.21YN-10%CaCO30.996178.36YN-char0.996179.85DT-10%Na2CO30.996146.30DT-10%K2CO30.989138.97DT-10%CaCO30.969148.93DT-char0.975158.60WLH-10%Na2CO30.989113.16WLH-10%K2CO30.975112.95WLH-10%CaCO30.958121.97WLH-char0.977133.95

图6 反应速率与碳转化率关系Fig.6 Relationship between reaction rate and carbon conversion
负载碳酸盐催化剂,煤焦气化反应速率与碳转化率的关系如图7所示。
由图7可以看出,负载碳酸盐催化剂后,煤焦气化反应速率与碳转化率关系与上述描述的进程基本相符。气化反应速率随转化率的提高,呈现先增大后减小的趋势。但图7中第二阶段(x1~x2)并不明显,这是由于本实验中催化剂的添加量相对较高,活性位的扩展快而且多,使某些可能成为活性位的微孔被相邻的活性空间吞没的时间更短。钾、钠在整个气化过程中提高了反应速率,而钙在前两阶段作用不明显,后两阶段作用明显,是由于钙相对钾钠流动性差,前期对煤焦的开槽作用较弱,而后期固体反应物的不断消耗,钙相对含量增加,使孔隙率增大,超过了微孔的吞并使活性位减少的不利影响,因此反应速率比原煤高。
目前,对于催化剂的作用机理主要有氧传递理论和电子转移理论。氧传递理论认为,催化剂可以形成活性中间体,承载氧原子不断在气相和固相之间循环,从而达到催化作用,而电子转移理论则认为,催化剂能使碳原子上的电子发生转移,引起石墨结构上π电子重新分布,边缘C—C键变弱以及C—O键合力增强[25]。
3 结 论
1) 负载催化剂后,煤焦的反应性均有所提高,对于YN褐煤,催化剂活性强弱依次为Na2CO3,K2CO3,CaCO3;对于DT烟煤焦和WLH无烟煤,催化剂活性强弱依次为K2CO3,Na2CO3,CaCO3;CaCO3的流动性较差,导致其催化效果较弱。
2) 缩核模型可以较好地反映煤焦及负载催化剂后的CO2气化过程,相关系数均在0.958以上;负载催化剂后,煤焦的气化反应活化能均有所降低。
