西那卡塞联合骨化三醇对MHD尿毒症继发甲状旁腺功能亢进患者矿物质及骨代谢的影响*
2019-09-20鹿冬梅杨沿浪王金宝童昌军高潮清周健美
鹿冬梅, 杨沿浪, 王金宝, 童昌军, 高潮清, 周健美
(皖南医学院弋矶山医院 血液净化中心, 安徽 芜湖 241001)
尿毒症继发性甲状旁腺功能亢进(SHPT)是终末期肾病(ESRD)患者在维持性血液透析(MHD)期间常见、且严重的并发症之一,SHPT以钙磷等矿物质代谢紊乱、血清全段甲状旁腺激素(iPTH)升高为主要表现,可增加患者血管钙化及死亡的风险[1-2]。SHPT多表现为高转运型骨病,患者骨代谢明显增强,患者易发生骨质疏松及骨折[3]。药物仍是目前治疗SHPT的主要疗法,采用以骨化三醇为代表的活性维生素D受体激动剂(VDRAs)进行冲击治疗能够有效降低患者iPTH的分泌,起到一定的治疗效果,但也容易诱发高钙、高磷血症,会导致患者血管钙化及骨病发生风险升高,同时,该疗法对部分重度SHPT患者无明显疗效,需行甲状旁腺手术切除(PTX)进行治疗[4]。有研究发现,西那卡塞等钙敏感受体(CaSR)激动剂对重度SHPT患者具有一定的疗效,使患者避免了PTX[5]。目前,西那卡塞联合骨化三醇对SHPT患者影响的研究多集中于矿物质代谢的改变,而对血iPTH水平、骨代谢指标及骨密度(BMD)变化的研究较少。本研究采用西那卡塞联合骨化三醇对MHD继发SHPT患者进行治疗,观察治疗前后患者矿物质及骨代谢指标的变化,报告如下。
1 对象与方法
1.1 研究对象
选取2015年1月-2018年1月行MHD治疗继发SHPT患者92例,纳入标准:(1)年龄18~75岁,性别不限;(2)MHD>6个月,透析方案为3次/周,4 h/次,透析充分性(KT/V)≥1.2;(3)符合SHPT诊断标准[6],血iPTH为300~1 000 ng/L,离子选择电极法测得血清钙磷乘积<4.52 mmol2/L2;(4)预计生存时间>6个月。排除标准:(1)原发性甲状旁腺功能亢进者;(2)具有明确手术指征者;(3)合并严重心、脑、肝及肾等重要器官功能障碍者;(4)合并严重呼吸系统、消化系统、免疫系统及神经系统疾病者;(5)合并严重感染、恶性肿瘤者;(6)具有认知功能障碍、癫痫病史或精神疾病史者;(7)对本研究用药过敏或不耐受者。本研究经医院伦理委员会审核批准,患者均自愿参与并签署知情同意书。患者按随机数字表法分为观察组与对照组,每组46例,两组患者的年龄、性别、透析时间、原发病等比较,差异无统计学意义(P>0.05)。见表1。

表1 两组MHD治疗继发SHPT患者一般资料比较(n,%)Tab.1 Comparison of general condition of patients in the two groups
1.2 治疗方法
1.2.1MHD方案 两组患者均采用碳酸氢盐透析液标准化血液透析治疗,钠浓度140 mmol/L、钙浓度1.5 mmol/L,透析液流量500 mL/min,血流量200~280 mL/min,透析时间为4 h/次,透析频率为3次/周。两组患者透析期间均予以低磷饮食。
1.2.2药物治疗 对照组参照文献[7-8]采用标准化骨化三醇进行冲击治疗。 血清iPTH在300~500 ng/L患者给予口服骨化三醇胶囊0.5~1.5 μg/次、1次/d。 血清iPTH在501~1 000 ng/L患者给予口服骨化三醇胶囊1.0~2.0 μg/次、2次/周,血清iPTH>1 000 ng/L患者给予口服骨化三醇胶囊2.5~5.0 μg/次、2次/周;根据血清iPTH水平每2~4周进行1次剂量调整,维持治疗12周, iPTH达标时逐步减停药。观察组在对照组基础上加用盐酸西那卡塞口服,初始剂量为25 mg/d,此后根据iPTH水平每2~4周进行1次剂量调整,最大剂量不超过75 mg/d,维持治疗12周,如血清钙≤1.8 mmol/L则停用西那卡塞,继续应用骨化三醇维持治疗。
1.3 观察指标
于治疗前,治疗4、12及24周时,采用日立7600型全自动生化分析仪以比色法检测血清钙及血清磷,采用放射免疫分析仪法检测血清iPTH;于治疗前及12周时,采用酶联免疫吸附法(ELISA)检测血清碱性磷酸酶(ALP)、骨保护素(OPG)及β-胶原蛋白(β-CTX)水平,于治疗前及24周时,采用DPX-L双能X线吸收仪测定患者的腰椎L2~4及股骨颈的BMD。
1.4 统计学分析
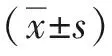
2 结果
2.1 血清钙水平
治疗前,两组血清钙水平比较,差异无统计学意义(P>0.05);治疗4、12及24周时,各iPTH水平的观察组血清钙比较,差异无统计学意义(P>0.05),治疗后对照组则有轻度升高趋势,但组内及组间比较差异均无统计学意义(P>0.05)。见表2。

表2 各组治疗前后血清钙水平比较Tab.2 Comparison of blood calcium levels before and after treatment in each group
2.2 血清磷水平
治疗前,两组患者血清磷比较,差异无统计学意义(P<0.05);与治疗前比较,治疗后各iPTH水平观察组患者血清磷水平显著下降,差异有统计学意义(P<0.05),对照组则有轻度升高,但差异无统计学意义(P>0.05),治疗后各iPTH水平同时点观察组低于对照组,差异有统计学意义(P<0.05)。见表3。

表3 两组患者治疗前后血清磷水平比较Tab.3 Comparison of blood phosphorus levels before and after treatment in each group
注:(1)与同iPTH水平同组治疗前比较,P<0.05;(2)与同iPTH水平对照组比较,P<0.05。
2.3 血清iPTH水平
治疗前,两组患者血清iPTH比较,差异无统计学意义(P<0.05);治疗4、12及24周时均显著降低,且同时点、同等基线iPTH的观察组血清iPTH水平显著低于对照组(P<0.05),iPTH水平达标率比较,差异无统计学意义(P>0.05)。见表4。

表4 两组患者治疗前后iPTH水平及达标率比较Tab.4 Comparison of iPTH levels before and after treatment in each group
注:(1)与同iPTH水平同组治疗前比较,P<0.05;(2)与同iPTH水平对照组比较,P<0.05。
2.3 血清ALP、OPG及β-CTX水平
治疗前,同iPTH水平2组患者血清ALP、OPG及β-CTX水平比较,差异无统计学意义(P>0.05);治疗后,同iPTH水平两组患者血清3项指标均显著下降,且观察组均显著低于对照组(P<0.05)。见表5。


组别基线iPTH(ng/L)例数ALP(U/L)治疗前治疗后OPG(ng/L)治疗前治疗后β-CTX(μg/L)治疗前治疗后观察组300~50015113.24±18.25 70.36±13.21(1)(2)75.32±9.14 66.31±8.21(1)(2)1.53±0.520.82±0.11(1)(2)501~1 00017188.14±22.9198.75±10.21(1)(2)84.16±12.1971.36±7.04(1)(2)2.01±0.641.44±0.32(1)(2)>1 00014714.21±97.25161.43±50.01(1)(2)99.32±15.2180.32±9.11(1)(2)3.95±1.132.03±0.56(1)(2)对照组300~50014111.09±16.4190.21±15.64(1)74.01±8.5370.17±8.82(1)1.49±0.511.26±0.40(1)501~1 00020190.47±21.85162.14±16.69(1)85.01±13.1780.32±9.17(1)2.03±0.671.71±0.43(1)>1 00012716.17±99.43603.31±85.74(1)97.27±13.3686.95±9.96(1)4.02±1.173.07±0.95(1)
注:(1)与同iPTH水平同组治疗前比较,P<0.05;(2)与同iPTH水平对照组比较,P<0.05。
2.4 BDM
治疗前及治疗24周时,两组相同iPTH水平患者腰椎、骨盆及股骨颈BDM比较,差异无统计学意义(P>0.05)。见表6。


组别基线iPTH(ng/L)nL1~4腰椎治疗前治疗后股骨颈治疗前治疗后观察组300~500151.04±0.341.06±0.361.00±0.161.03±0.17501~1 000170.92±0.300.93±0.310.85±0.150.88±0.17>1 000140.81±0.150.82±0.160.78±0.130.79±0.12对照组300~500141.05±0.361.06±0.371.02±0.171.01±0.18501~1 000200.95±0.310.92±0.330.88±0.130.89±0.15>1 000120.82±0.160.80±0.140.79±0.140.76±0.13
3 讨论
MHD继发SHPT的病理生理特征为PTH分泌过多及甲状旁腺肥大增生等,可损害神经、骨骼及血液等多系统,将增加骨质疏松、骨折等骨病发生风险,且可增加心血管疾病的发生风险[9-10]。现已证实,SHPT是影响MHD患者死亡率的独立危险因素[11]。维持血清钙达标并降低高磷血症是SHPT治疗的关键,VDRAs药物骨化三醇是当前临床治疗SHPT的一线药物,可有效抑制PTH的合成与分泌而降低iPTH水平,但长期使用可导致血清钙、血清磷水平升高,增加心血管钙化及骨病发生风险[12]。虽然磷结合剂辅助VDRAs治疗SHPT可在一定程度上降低血清磷,但对临床预后的影响并不明确[13]。此外,部分患者由于初期未及时诊断和治疗,当发展为严重的SHPT时,对VDRAs药物的敏感性较低甚至产生抵抗,往往需行PTX或介入治疗。拟钙剂西那卡塞作为一种CaSR激动剂,可模拟钙作用于机体,变构激活CaSR而降低其活化阈值,提高其对细胞外钙离子的敏感性,抑制PTH的合成与分泌。同时,活化CaSR有利于血清钙离子转移至骨内,从而降低血清Ca及血清P水平,减少破骨细胞的形成以及骨质吸收,抑制甲状旁腺细胞及腺体的增生[14]。周凌辉等[15]认为,西那卡塞与骨化三醇联用可在一定程度上减少骨化三醇用量,减少其所致血清Ca或血清P升高风险,在一定程度上具有相互弥补的作用。但两药联用在降低iPTH水平和减少高磷血症、高钙血症的有效性,降低骨病的发生风险等方面是否优于单用VADRAs治疗仍存在一定争议。Pronai等[16]则认为,SHPT应用西那卡塞治疗的效果受诸多因素的影响,尤其是基线iPTH水平越高者经西那卡塞治疗后的达标率越低,可能与病情严重程度有关。因此,探讨不同基线iPTH水平患者的联合用药治疗效果及对矿物质、骨代谢的影响非常必要。
本研究结果显示,观察组与对照组不同基线iPTH患者中,iPTH水平在治疗后的近期iPTH达标率存在一定差异。基线iPTH在300~500 ng/L 时,两组患者24周达标率均较高,在501~1 000 ng/L时有所降低,而>1 000 ng/L患者中两组的达标率均更低,这与Komaba等[17]研究结果相符。虽然两组的近期iPTH达标率比较差异无统计学意义,但观察组的iPTH水平始终显著低于对照组(P<0.05),表明联合用药方案可能能够更好地抑制iPTH的分泌。同时,随着疗程的延长,两组的iPTH水平均程序持续减低趋势,且基线iPTH<1 000 ng/L者多在治疗12周时iPTH降低率达50%,而>1 000 ng/L者则需要更长疗程,几乎到24周时降幅才达50%,而基线iPTH水平较高时可能需要延长疗程方可提高控制率。同时,观察组在治疗后血清Ca水平整体变化不明显,认为西那卡塞的应用不易造成低钙血症。本研究结果还显示,治疗后观察组血清P均呈下降趋势,而对照组略有升高,这与两药的作用机理相符。进一步证实西那卡塞的应用能够抑制VDRAs所致血清P升高,降低血清P水平[18]。
SHPT多表现为高转运型骨病,高水平PTH可激活成骨以及破骨细胞而导致骨合成及分解代谢均增强,促进骨重建[19]。既往对MHD伴SHPT患者骨代谢的研究多为现状研究,缺乏在治疗结果中的检测,或仅限于反应成骨细胞功能的ALP的观察,难以全面评价患者的骨代谢变化。OPG是一种肿瘤坏死因子受体,能够与核因子κB受体活化因子(RANK)竞争性结合其配体RANKL而抑制破骨细胞的分化、成熟,从而抑制骨吸收。β-CTX主要由成熟Ⅰ型胶原蛋白部分降解生成,反映破骨细胞活性及骨吸收状态,研究显示其在SHPT患者中明显升高,且iPTH>800 ng/L时其水平更高[20]。本研究中,患者治疗前的ALP、OPG及β-CTX均处于高表达状态,且随iPTH基线水平的增高呈上升趋势,以基线iPTH>1 000 ng/L者最高。提示SHPT患者具有明显的骨转运异常,且基线iPTH越高时患者的骨合成及分解代谢越强。治疗后,观察组与对照组患者的血清ALP、OPG及β-CTX水平均有不同程度的降低,且观察组显著低于对照组,且在基线iPTH越低患者中各指标水平越低(P<0.05)。说明西那卡塞与骨化三醇联用能够改善患者的骨代谢状态,可能对预防或延缓骨质疏松等骨病的发生具有积极意义。Moe等[21]研究显示,在>65岁老年MHD患者中辅助应用西那卡塞后骨折发生率为6%,低于未用西那卡塞组的8.6%;Behets等[22]多中心研究亦显示,西那卡塞用于SHPT治疗1年后,骨组织病理异常得以改善,且有20%左右的患者异常骨组织形态学得以恢复正常。上述研究结论与本研究相互佐证,提示西那卡塞对高转运骨病具有潜在防治作用。MHD患者由于异常矿物质及骨代谢,可引起骨强度异常,而BMD是评价骨强度的重要指标。本研究中,两组治疗后BMD虽有轻微改善,但并不明显,且组间比较差异无统计学意义(P>0.05)。考虑为SHPT患者钙磷代谢及骨代谢异常的改善在一定程度上有利于BMD的改善,但BMD的改善是一个长期的过程,而本研究样本较小且观察时间尚短,药物对其的影响仍不得而知。
综上,西那卡塞与骨化三醇联用治疗不同iPTH基线水平MHD继发SHPT患者均可维持血清钙在正常范围内,不易发生低钙血症,且可有效降低血清P及iPTH水平,长期应用对患者的骨代谢状态具有一定的改善作用,但对高iPTH患者而言短期内iPTH达标率较低,可能需要更长疗程的治疗,部分患者可能仍需考虑手术或介入治疗。由于本研究样本有限,随访时间较短,且在心血管及骨病终点事件的评估方面存在缺陷,还有待进一步研究完善。
