甲型流感病毒快速基因分型POCT方法的建立
2019-09-17王大刚王雅杰潘美晨焦炳欣郭晶晶吴吟妮
王大刚,王雅杰,潘美晨,焦炳欣,郭 杰,王 爽,郭晶晶,徐 飞,吴吟妮
WHO估计全球每年有10亿流行性感冒(流感)病例,其中重症病例约300万~500万,流感相关呼吸道疾病死亡病例约29万~65万。流感病毒是具有高度频繁变异特性的RNA病毒,容易对药物产生耐药并可跨种间传播。国家流感中心报告近年我国冬春季流行的主要是甲型H1N1、H3N2和乙型流感病毒,流感大流行威胁着全球公共卫生安全[1]。由于流感病毒各亚型之间存在交叉感染的风险,在流感暴发流行期间,早期快速分型检测便于及时隔离不同型别和亚型的流感患者,对防止流感传播意义重大。
目前流感病毒的检测方法主要有胶体金筛查流感抗原、免疫血清学检测抗体以及RT-PCR和实时荧光定量PCR检测核酸[2]。抗原初筛检测尽管快速,但其敏感性低且不能区分亚型;血清学方法只能检测IgM和IgG,且耗时较长;核酸检测方法敏感性高,特异性强,可以区分亚型,但需要专业的实验室和昂贵的仪器设备,操作复杂,专业性要求高,不能满足基层单位筛查防控的需求[3-4]。ParaDNA核酸POCT检测仪及其配套的HyBeacon荧光探针检测技术是当前POCT分子诊断的前沿代表,由于准确度和灵敏度高、设计灵活、兼容性好、无交叉污染及支持现场快速检测等特点已广泛应用于法医学鉴定、病原微生物检测、食品卫生安全以及药物基因组学等领域[5-6]。本研究旨在建立一种基于HyBeacon-ParaDNA技术平台对甲型流感病毒进行快速基因分型的方法,以实现无需核酸提取,无需专业实验室支持,直接对患者鼻咽拭子标本开展现场快速检测。
1 材料和方法
1.1 标本来源 2018年12月—2019年3月留取的门诊发热患者甲型流感病毒抗原胶体金法初筛阳性的鼻咽拭子标本50例。其中经过实时荧光定量PCR检测证实M基因和H1N1基因阳性的标本48例,M基因阳性而H1N1基因阴性的2例。全部标本于-80 ℃冰箱保存,检测前恢复至室温。
1.2 试剂与仪器 HyBeacon荧光探针、dNTP、Phire Hot Start II DNA聚合酶、 GoScript 反转录酶等试剂,生物标本采集器和ParaDNA核酸POCT检测仪均由北京英诺特生物技术有限公司提供。甲型/乙型流感病毒抗原检测试剂盒(胶体金法)购自杭州创新生物检控技术有限公司。
1.3 引物和HyBeacon荧光探针设计 从Genbank下 载A/Beijing/501/2009(H1HA pdm09)、A/Guangdong/09/2005(H3HA)、A/WSN/33(H1HA non-pdm09)3种流感病毒株的HA基因序列,用比对工具ClustalOmega识别序列同源性区域,确定保守区用于引物和探针设计。使用NCBI的BLAST工具进行序列比对验证引物的特异性。按照引物设计原则,用Primer Explorer V5软件进行引物设计。采用FAM、CFO560、CFR610和Q670荧光素分别标记HyBeacon探针,用于M基因、H3HA基因、H1HA non-pdm09/RNase P和H1HA pdm09的检测。
1.4 多重PCR反应体系的建立以及ParaDNA核酸POCT检测仪的应用 多重PCR反应体系的优化流程主要包括:①探针设计,选取最佳的核苷酸错配和染料标记间距,熔解温度(melting temperature, Tm)设计为58~62 ℃,避免二级结构,能够用FAM等多重染料标记。②引物设计,设计多个引物对确定最佳组合,Tm值60~65 ℃,靶序列长度60~200 bp,避免二级结构。③评估探针和引物的扩增效率以及二聚体的形成。④选择最佳引物对与探针,通过修改退火温度和维持时间优化热循环方案,优化检测试剂配方(引物、探针、MgCl2、dNTPs、聚合酶等的浓度),将设计并优化的引物与探针按不同浓度混合于35 μl的反应体系中,优化变性、退火、循环数等反应条件。⑤用已知的模板进行PCR反应,以验证优化后的反应体系。将优化好的反应体系制成密封试剂盒应用于ParaDNA核酸POCT检测仪。
1.5 检测下限和特异性分析 为评价反应体系的检测下限,采用合成的已知拷贝数的甲型流感病毒RNA 为模板,按 5000 copies/μl、500 copies/μl、50 copies/μl、5 copies/μl不同浓度稀释后进行扩增。用7种常见的呼吸道病原微生物(柯萨奇病毒、副流感病毒、腺病毒、呼吸道合胞病毒、肺炎衣原体、肺炎支原体、乙型流感病毒)和已知的流感病毒株A/Beijing/501/2009(H1HA pdm09)、A/Guangdong/09/2005(H3HA)、A/WSN/33(H1HA non-pdm09)检测试剂盒的特异性。
1.6 临床样本验证 用生物取样器直接刮取保存的临床鼻咽拭子样本,插入paraDNA多重反应试剂盒中并密封,启动paraDNA核酸POCT检测仪进行检测。并用50例甲型流感病毒抗原阳性标本的ParaDNA核酸POCT检测结果与实时荧光定量PCR核酸检测结果对比,初步评价试剂盒对甲型流感病毒抗原初筛阳性标本检测的灵敏度和特异度。
2 结 果
2.1 引物和HyBeacon荧光探针序列 针对检测甲型流感病毒的通用M基因和特异的HA基因序列进行引物和HyBeacon荧光探针设计,同时设计人RNase P基因的引物和探针用于内部对照。合成的引物和探针序列见表1。
2.2 ParaDNA核酸POCT检测仪多重反应体系的成分和反应条件 将各种引物和探针混合于单管反应液中,经过不断优化后建立单管多重PCR反应体系,加入凝胶后形成半固体状态并制作成密封试剂盒,用于ParaDNA核酸POCT检测仪。单管试剂总反应体积为35.000 μl。其主要成分如下:GoScript 缓 冲 液 7.000 μl,MgCl21.750 μl,LGC stock dNTP 混合物 1.120 μl,DFP 2.800 μl,Phire Hot Start II DNA 聚 合 酶 2.800 μl,GoScript酶 0.875 μl,RNasin Plus 0.875 μl,引物和探针混合物10.780 μl,琼脂糖凝胶7.000 μl。反应条件如下:50 ℃ 反转录5 min,95 ℃变性1 min,扩增阶段为94 ℃ 10 s,60 ℃ 15 s,72 ℃ 15 s,50 个循环。然后进行熔解曲线分析,98 ℃ 1 min,20℃ 5 s,之后温度每升高0.5 ℃采集1次荧光信号,直至90 ℃。检测完毕后仪器自动报告结果,并降温。ParaDNA核酸POCT检测仪各荧光通道检测基因及对应结果见表2。
2.3 反应体系的检测下限和特异性 不同浓度梯度的病毒RNA扩增结果证实其检测下限可达到50 copies/μl。该反应体系对7种常见的呼吸道病原微生物无交叉反应,且能对3种流感病毒株 A/Beijing/501/2009(H1HA pdm09)、A/Guangdong/09/2005(H3HA)、A/WSN/33(H1HA non-pdm09)实现特异性扩增,见图1。

表1 甲型流感病毒基因分型引物和HyBeacon荧光探针Table 1 Primers and HyBeacon fluorescent probes for influenza A virus genotyping
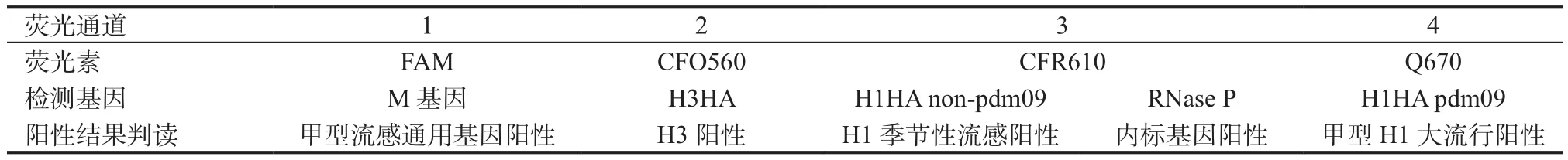
表2 ParaDNA检测仪各荧光通道检测基因阳性结果判读Table 2 Fluorescence channels and gene positive results interpretation of ParaDNA instrument

图1 3种甲型流感病毒的熔解曲线分析Figure 1 Analysis of 3 influenza A viruses by melting curve
2.4 临床样本检测结果 用生物取样器直接采集50例甲型流感病毒抗原胶体金法阳性患者的鼻咽拭子标本,启动ParaDNA核酸POCT检测仪进行检测。结果显示,检出48例为H1HA pdm09,2例 为 H3HA。48例 H1HA pdm09样本经实时荧光定量PCR验证均为H1N1阳性,2例H3HA样本经实时荧光定量PCR验证为H1N1阴性,因此,该快速分型检测方法的灵敏度和特异度均为100%,见表3。2例H1N1阴性标本ParaDNA报告结果为H3HA,显示出可以同时分型的优势。检测结果如图2所示。
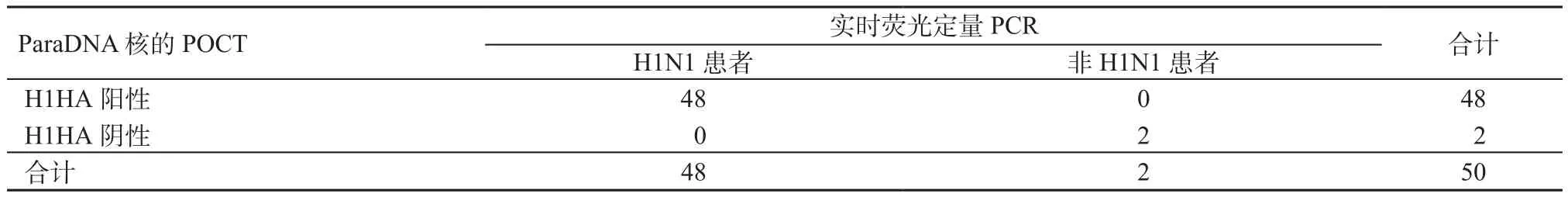
表3 2种方法甲型流感病毒H1N1检测结果(例)Table 3 The detection result of influenza A virus H1N1 by 2 methods(cases)

图2 ParaDNA仪器检测甲型流感病毒亚型的熔解曲线Figure 2 The melting curves of influenza A virus subtypes detected by ParaDNA instrument
3 讨 论
HyBeacon荧光探针是一种新型荧光探针,不需要淬灭剂,借助DNA碱基固有的荧光淬灭特性,HyBeacon探针上荧光染料的发光可被与荧光素相邻的核苷酸抑制。当HyBeacon探针与互补DNA靶序列杂交时,荧光强度显著升高。PCR反应扩增后,可通过熔解曲线分析鉴定目标基因。探针杂交的稳定性和Tm取决于HyBeacon与目标序列的同源性。将反应温度升高到HyBeacon的Tm以上,探针/靶基因双链解链,荧光发射强度降低。通过针对熔解峰Tm值的分析,可以检测并区分低至单个核苷酸序列的不同。诸多研究表明,HyBeacon探针不仅能基于熔解曲线分析的方法实现单条探针分析,检测多个序列变异位点,而且能够耐受针对唾液、血液等样品的直接PCR扩增检测(无需DNA提取)。ParaDNA核酸POCT检测仪是基于HyBeacon探针技术的可移动荧光PCR仪器平台,支持现场快速检测,目前ParaDNA-HyBeacon平台已有商品化试剂盒用于法医学、病原微生物检测和食品卫生安全和药物基因组等领域。
基于该系统简便、快速、准确以及便携式一体化的特点,特别是其可针对临床样本直接进行检测的优点,英诺特生物技术公司设计并开发了甲型流感病毒快速分型检测试剂盒,并在本实验室进行了验证。本实验室利用ParaDNA-HyBeacon平台对50例甲型流感病毒抗原胶体金法阳性的鼻咽拭子标本进行了分型检测,其中48例检测结果为H1HA pdm09型,2例检测结果为H3HA型。48例H1HA pdm09阳性标本经核酸提取后实时荧光定量PCR证实为甲型H1N1,与快速分型检测结果基本一致,说明其特异性较好。与实验室常用的实时荧光定量PCR相比,该方法的优势主要体现在:①单管多重反应体系,可同时对H3HA、H1HA non-pdm09和H1HA pdm09进行分型。②取样器与试剂盒为一次性、密闭性设计,无须配置试剂,不用担心核酸污染。③无须核酸提取,可直接对鼻咽拭子标本进行检测。④无需专业实验室和专业PCR操作人员,操作简单,可实现现场快速检测。⑤检测速度快,从标本采集到自动报告结果仅需1.5 h。然而,该检测方法仍须进一步改进,因本研究仅检测了甲型流感病毒抗原阳性的标本,未对甲型流感病毒抗原阴性而核酸检测阳性的标本进行分析,后续将进行大样本量的检测,以评价该方法检测临床样本的灵敏度和特异度,目前该多重PCR体系核酸检测的下限可达到50 copies/μl,还须进一步优化。
综上,基于ParaDNA-HyBeacon技术平台建立的甲型流感病毒快速基因分型的方法,可用于现场分型检测,对于流感的诊治和防控具有重要的应用价值。
