UPLC-MS测定杜仲的3种成分及其药代动力学研究
2019-09-10贲晶晶葛建彬秦清清
贲晶晶 葛建彬 秦清清
摘要 目的:通过超高效液相色谱联合质谱法测定杜仲的3种成分及其药代动力学研究。方法:本研究的质谱采用电喷雾电离源(ESI),通过多反应离子监测这一扫描方式对京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分及内标用于定量分析的监测离子。结果:1)杜仲中京尼平苷酸、绿原酸、松脂醇二葡萄糖苷等3个指标性成分的分离良好,无内源性物质干扰,具有较好的专属性。2)UPLC方法严谨性,其精密度、稳定性试验、重复性试验、加样回收率等均良好。3)京尼平苷酸和松脂醇二葡萄糖苷在大鼠体内的药代动力学具有非线性特征,仅绿原酸存在线性特征;而CLz、Vz参数指标的差异比较大,显示大鼠血浆中杜仲提取物中的3种成分在大鼠体内的药代动力学代谢过程不一致。结论:UPLC-MS/MS的操作简单,结果具有较好的精密度、稳定性和重复性,可作为杜仲有效成分及药代动力学研究的可靠方法。
关键词 超高效液相色谱法;质谱;杜仲;京尼平苷酸;绿原酸;松脂醇二葡萄糖苷;药代动力学;研究
Determination of 3 Components and Pharmacokinetics of Cortex Eucommiae by UPLC-MS
Ben Jingjing,Ge Jianbin,Qin Qingqing
(Pharmaceutical Department,Nantong Second People′s Hospital,Nantong 226002,China)
Abstract Objective:To determine the 3 components of Cortex Eucommiae by ultra-high performance liquid chromatography combined with mass spectrometry and their pharmacokinetics.Methods:Electrospray ionization source(ESI)was used to monitor the monitoring ions of geniposide chlorogenic acid and terpineol diglucoside,and internal standards for quantitative analysis of geniposide chlorogenic acid and terpineol diglucoside.Results:1)The 3 index components of Cortex Eucommiae such as geniposide,chlorogenic acid and terpineol diglucoside,were well separated and had no interference of endogenous substances,with good specificity.2)The UPLC method was rigorous,and its precision,stability test,repeatability test and sample recovery rate were all good.3)The pharmacokinetics of geniposide and turpentine diglucoside in rats was nonlinear,but only chlorogenic acid was linear.However,there were significant differences in the 2 parameters of CLz and Vz,indicating that the pharmacokinetic metabolism of the 3 components of Cortex Eucommiae extract in rat plasma was inconsistent.Conclusion:The operation of UPLC-MS/MS is simple,and the results have good precision,stability and reproducibility.It can be used as a reliable method for the study of effective components and pharmacokinetics of Cortex Eucommiae.
Key Words Ultra high performance liquid chromatography; Mass spectrometry; Cortex Eucommiae; Geniposide; Chlorogenic acid; Turpentine diglucoside; Pharmacokinetics; Study
中圖分类号:R284.1文献标识码:Adoi:10.3969/j.issn.1673-7202.2019.12.011
杜仲(Eucommia ulmoides Oliver)为我国名贵滋补药材,其取药部位是树皮,为杜仲科植物的干燥树皮,别名木棉,从《神农本草经》上可见杜仲被列为上品,其味甘,性温,主要治疗功能有补益肝肾、强筋壮骨、调理冲任、固经安胎等[1-3]。纵观杜仲2 000多年的药用历史,可知杜仲能够治疗肾阳虚引起的腰腿痛和(或)腰膝酸软无力[4],男性之阴囊湿痒[5],女性之肝气虚引起的胞胎不固[6-7]等症。由现代药理学研究可知[8],杜仲中具有的降血压[9-10]、抗肿瘤[11]、降血脂[12-13]、抗血栓[14]、抗氧化[15]等药理作用是由哪些具体的成分发挥的功效,同时这些药理成分的药代动力学是如何变化的,因此课题组将杜仲提取物注射入大鼠尾静脉后,研究杜仲的3个指标性成分(分别是京尼平苷酸、绿原酸、松脂醇二葡萄糖苷)在大鼠体内的具体经时过程和药代动力学参数特征,为临床上使用杜仲这味药物的前药动学研究提供实验依据。本课题研究主要采用UPLC-MS的技术手段,超高效液相色谱(Ultra Performance Liquid Chromatography,UPLC)是分离科学中的一个全新类别,UPLC是在高效液相色法(High Performance Liquid Chromatography,HPLC)的理论及原理的基础上发展而来的,这一技术方法不仅秉承了HPLC的快速检测手段,而且涵盖了小颗粒填料进一步提高也HPLC的精密度和灵敏度,同时以非常低系统体积增加分析通量和色谱峰容量[16]。通过以物质离子化为基础建立质谱分析系统,测量并分析离子谱峰的强度来联合分析杜仲3种成分,进一步阐释药代动力学的经时过程,首先杜仲提取物样品经过液相色谱纯化后的样品,再通过电场和磁场的综合作用将样品气化离子化,形成的离子按照质量数和电荷数的记录并分析,在液相色谱质谱中通常所用的离子源有电喷雾电离源(Electrospray Ionization,ESI)和大气压化学电离源(Atmospheric-Pressure Chemical Ionization,APCI),其中最常用的是ESI,根本原因是ESI比APCI软电离程度较小的电离方式,因此在实际检测应用中适用范围较APCI的大[17-18]。现将结果报道如下。
1 仪器与试药
1.1 仪器 ACQUITY UPLC超高效液相色谱-三重四级杆质谱联用仪(美国Waters公司生产,产品型号:H-class-Xevo TQ MS);冷冻高速离心机(美国Beckman Coulter公司生产,产品型号:Allegra64-R);氮吹仪(北京众信佳仪科技有限公司生产,产品型号:ZX-DC);涡旋混合器[莱普特科学仪器(北京)有限公司生产,产品型号:Vortex dancer Ⅳ];电子分析天平(上海精密仪器仪表公司生产,产品型号:FA1004N型);超声波清洗器(上海精密仪器仪表公司生产,产品型号:KQ-100DE);超纯水系统(法国MILIPORE公司生产,产品型号:Mili-RO Plus型)。
1.2 试剂 京尼平苷酸对照品(上海纯优生物科技有限公司生产,生产批号27741-01-1,药品纯度≥98%);和绿原酸对照品(上海纯优生物科技有限公司生产,生产批号327-97-9,药品纯度≥98%);松脂醇二葡萄糖苷对照品(上海顺勃生物工程有限公司生产,生产批号201206,药品纯度≥98%);葛根素对照品(中国药品生物制品鉴定所生产,生产批号111-090623,药品纯度≥98%)。色谱纯乙腈(美国Fisher公司生产,生产批号102489)和甲酸(美国Fisher公司生产,生产批号101437),AR级磷酸分析纯(上海拓国沪试实验室器材股份有限公司生产,生产批号20170412)。
1.3 分析样品 杜仲药材来源于湖北,经过南通市第一人民医院专业药物研究人员鉴定为优质杜仲科植物杜仲的干燥树皮,研究室以此为原材料自制杜仲提取物进行进一步研究。
1.4 实验动物 动物清洁级SD大鼠,体质量(260±20)g,由广东省医学实验动物中心提供(批号2006A010),实验室常规环境饲养。
2 方法与结果
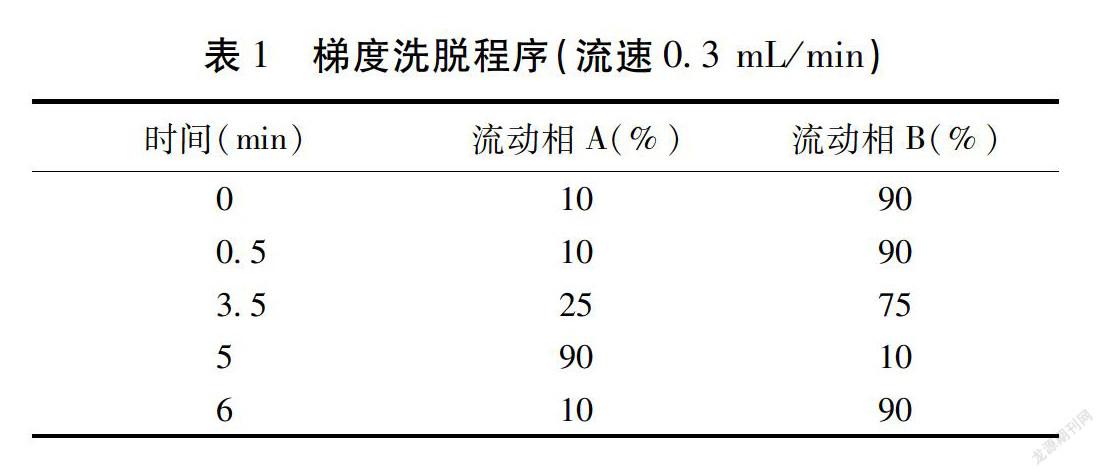
2.1 色谱条件 进样体积为2 μL;色谱柱采用Waters-BEHC18(产品规格:采用窄径柱2.1 mm,短柱100 mm,填料粒径1.7 μm),色谱柱的温度控制在45 ℃左右,进样器的温度设置控制在15 ℃,流动相则以流动相A的主要试剂配置由0.1%甲酸和乙腈组成,流动相B的主要试剂配置由0.1%甲酸和水组成,以进行梯度洗脱。具体的梯度洗脱程序见表1。
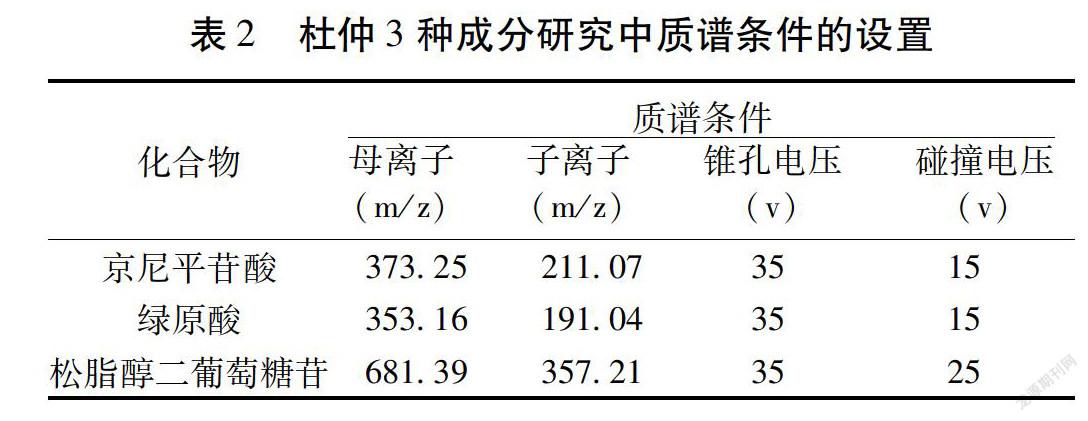
2.2 质谱条件 本研究的质谱采用ESI,首先设置毛细管电离电压,经过多个预实验最终确定该电压设置为3 kV,离子源温度设置为120 ℃,并将氮气作为本研究过程中涉及到的喷雾气与反吹气,并将反吹气流速设置为50 L/h,而将氩气作为本研究过程中涉及的碰撞气,并将其流速设置为0.16 mL/min;去溶剂气流速经过多个预实验最终确定该电压设置为650 L/h,去溶剂气温度最终确定为350 ℃左右;通过多反应离子监测(Multiple Reaction Monitoring,MRM)這一扫描方式对京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分及内标用于定量分析的监测离子。见表2。
2.3 对照品溶的配制 取4个装有适量甲醇的广口瓶用以配制浓度为1.35 mg/mL的京尼平苷酸、浓度为1.00 mg/mL的绿原酸、浓度为1.00 mg/mL的松脂醇二葡萄糖苷、浓度为1.00 mg/mL的葛根素的储备液。其中葛根素是作为本研究的内标液,用甲醇按梯度稀释成所需浓度,配制5 μg/mL的葛根素内标溶;同时分别精密量取京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种对照品储备液适量,用甲醇按梯度稀释成所需浓度,得混合对照品溶液。
2.4 供试品溶液的配制 将杜仲用药材剪剪成碎片,反复揉成絮状,精密称定2 g,采用索氏提取器中提取杜仲提取物,加入氯仿适量,加热回流6 h,待冷却后弃去氯仿液,药渣室温挥发去氯仿,再将药渣放置索氏提取器中进一步提取,加甲醇适量,加热回流6 h,待冷却后将提取液转移至100 mL量瓶,加甲醇至刻度线,充分混合均匀摇匀即得杜仲供试品溶液。
2.5 血浆样品处理方法 采用1.5 mL塑料离心管取大鼠血浆100 μL,加入已知浓度的葛根素内标溶液50 μL,再加入等量的1%甲酸溶液和300 μL甲醇,涡旋混合器上混合1 min,超声5 min,4 ℃低温离心机上15 000 r/min离心10 min,取上清液并在48 ℃下的氮气吹干,残留物加入300 μL甲醇充分溶解,4 ℃低温离心机上转速采用15 000 r/min,离心时间控制在10 min以内,最终只取上清液作为分析样品进样UPLC-MS/MS分析。
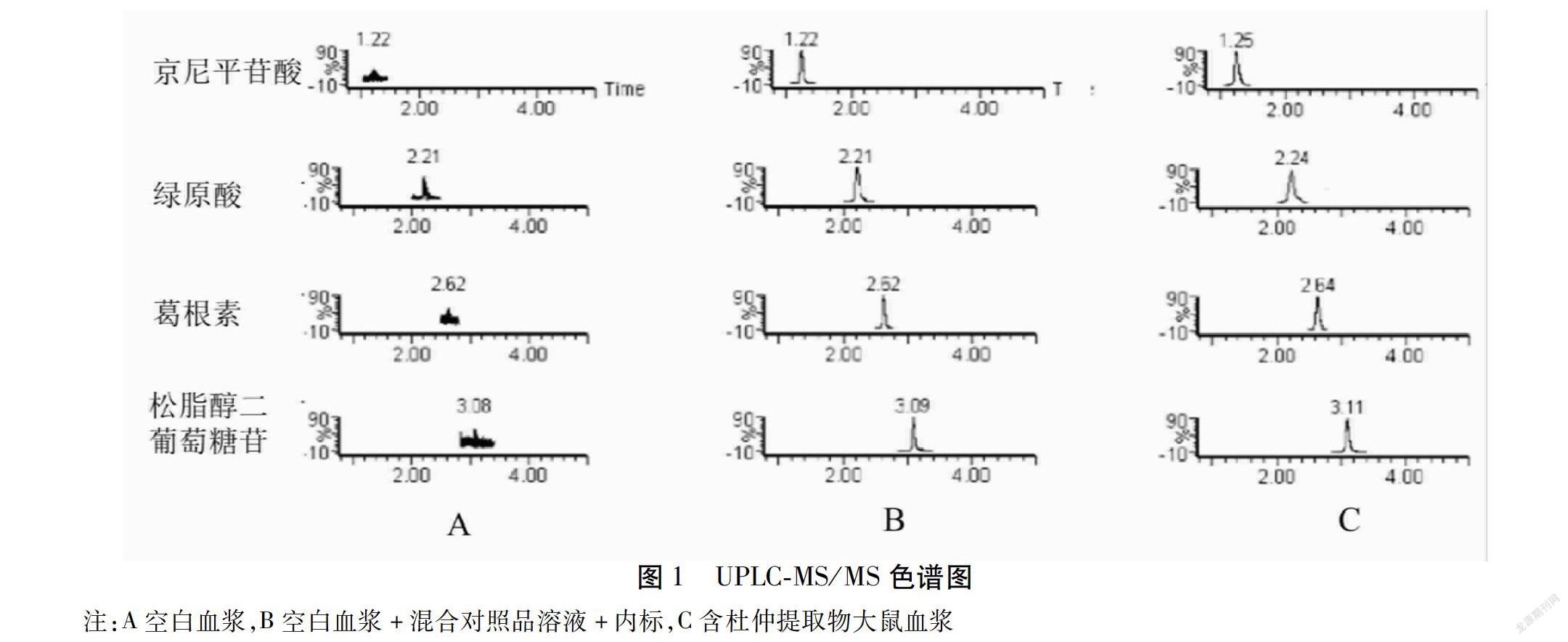
2.6 杜仲提取物的专属性试验 如图1所示,根据A空白血浆,B空白血浆+混合对照品溶液+内标,C含杜仲提取物大鼠血浆等3种情况对杜仲的3种成分及内标液进行专属性试验,A、B、C 3种情况中的大鼠空白血浆、含杜仲提取物大鼠血浆均取100 μL,根据“2.5”依次操作得相应UPLC-MS/MS色谱图A、B、C;本研究结果显示,杜仲提取物中可见分离程度良好的3种不同成分,且各个成分间不存在内源性干扰物质,具有较好的专属性。
2.7 线性关系考察 根据梯度稀释浓度配制混合对照品溶液100 μL的大鼠空白血浆作为标准参照曲线,纵坐标Y是将含有大鼠杜仲提取物的待测血浆的峰面积除以葛根素内标峰面积得到的比值比值,横坐标X是京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等各成分物质浓度,将权重系数设置为1/X进行计算直线回归方程,京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分最低检测限(LLOD)定义为S/N≥3,结果显示京尼平苷酸、绿原酸和松脂醇二葡萄糖苷均具有良好的线性关系,详见表3。
2.8 精密度试验 取统一批次含有杜仲提取物的大鼠血浆,按“2.5”项下分别配制京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分大鼠血浆低、中、高3个浓度的质量控制样品(Quality Control,QC),通过3 d不间断的连续测定,并根据每日测得的不同数据计算该日的标准曲线,计算求得3种成分当日的平均浓度值,京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分日内和日间精密度RSD(%)均小于10%,准确度范围为95.473%~112.086%。表明该UPLC-MS/MS方法准确度、日内和日间精密度良好,结果见表4。
2.9 稳定性试验 按“2.7”项下分别配制京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分,分别根据大鼠血浆低、中、高3个浓度的京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分QC,对3种成分在室温下放置6 h,4 ℃下冷藏8 h和冻融3次,通过在1 d内重复测量多次来考察样品的稳定性。本研究结果表明含有杜仲提取物的大鼠血浆样品中京尼平苷酸RSD=9.04%<15%、绿原酸RSD=10.12%<15%和松脂醇二葡萄糖苷RSD=8.83%<15%,提示本研究中含有杜仲提取物的大鼠血浆在UPLC的中具有较好的稳定性。
2.10 重复性试验 根据同一批次同一厂家的杜仲药材制备制备6份杜仲供试品溶液,处理后分别进样测定,根据葛根素内标法计算得京尼平苷酸、绿原酸和松脂醇二葡萄糖苷的RSD分别为1.842%、2.018%、2.856%,表明本研究采用的UPLC方法重复性良好。
2.11 回收率试验 精密量取大鼠空白血浆100 μL,按“2.7”项下分别配制京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分的大鼠血浆或葛根素内标液,且分别配置低、中、高3个浓度的3种京尼平苷酸、绿原酸和松脂醇二葡萄糖苷QC,经过反复测量5次,计算平均加样回收率。京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分回收率分别为:86.106%~96.461%,86.147%~99.828%,86.344%~96.679%,提示本研究中UPLC的加样回收率良好。
2.12 样品检测结果 药代动力学研究结果显示:健康SD大鼠分为低、中、高3个剂量组,尾静脉注射杜仲提取物溶液前所有大鼠均禁食12 h,期间可自由饮水,给药剂量分别为0.17、0.34、0.68 g/kg。采用涂有肝素的塑料离心管于给药前与给药后2、5、10、15、20、30、45、60、80 min经尾静脉取血约0.3 mL,于离心机上采用4 500 r/min的转速,离心时间控制在10 min。本研究采用UPLC-MS分析杜仲提取物的药代动力学,并以DAS 2.0数据处理软件数据拟合,本研究选取血药浓度(AUC0-80)、平均驻留时间(MRT0-80)、清除率(CLz)、分布容积(Vz)等参数选用统计矩方法计算。获得京尼平苷酸、绿原酸和松脂醇二葡萄糖苷3个成分C-t曲线图和相应的药动学参数,具体详细见图2和表5。
3 讨论
本次研究完成了京尼平苷酸、绿原酸和松脂醇二葡萄糖苷3种药物成分的UPLC-MS/MS分析及其药时曲线和药代动力学的分析。研究前期主要从方法学的准确度、稳定性和可重复性进行考察,紧接着对京尼平苷酸、绿原酸和松脂醇二葡萄糖苷等3种成分的专属性进行鉴定,并进一步对这3种成分进行线性方程回归和回收率的计算。而在药代动力学的研究中,主要从低、中、高3个不同剂量浓度的杜仲提取物入手,建立体内符合二室药动学模型,进而计算出大鼠血浆中杜中提取物内3种成分的药代动力学参数指标。AUC0-80、MRT0-80都随着浓度计量的升高而升高,从结果可得大鼠血浆中杜仲提取物中的3种成分中的京尼平苷酸和松脂醇二葡萄糖苷在大鼠体内的药代动力学具有非线性特征,仅绿原酸存在线性特征;而CLz、Vz参数指标的差异比较大,显示大鼠血浆中杜仲提取物中的3種成分在大鼠体内的药代动力学代谢过程不一致。本研究中前期在考察大鼠血浆样品的处理优化方法过程中,首先从溶剂入手,对甲醇、乙腈、乙酸乙酯,乙醚4种不同的有机溶剂对大鼠血浆中的蛋白进行沉淀,结果显示,对大鼠血浆中蛋白的沉淀效果最好的有机溶剂是甲醇,而在进一步的研究中更发现甲醇不仅无内源性物质干扰而且回收率最好,因此本研究最终选择甲醇沉淀处理大鼠血浆样品。在提取方法的选择上,以京尼平苷酸、绿原酸、松脂醇二葡萄糖苷3种成分作为考察指标,对提取溶剂进行考察:取样品2 g 3份,分别精密加入甲醇,80%甲醇,50%甲醇25 mL,超声6 h。结果表明:用80%甲醇提取的京尼平苷酸、绿原酸、松脂醇二葡萄糖苷3种成分均得到较高的含量,所以本研究最终选用80%甲醇作为杜仲提取物成分的提取溶剂。对提取方式及时间进行考察:取样品2 g 6份,精密加入80%甲醇25 mL,取其中3份回流,提取时间分别为2 h、4 h、6 h;取另外3份超声,提取时间分别为2 h、4 h、6 h。结果表明,回流和超声2种提取方式对含量结果影响不大,因超声操作较为简便,且6 h能将京尼平苷酸、绿原酸、松脂醇二葡萄糖苷等3种成分提取完全,故选择超声处理。
综上所述,采用超高效液相色谱法操作简便,结果准确,重复性好,加样回收率高,可用于研究杜仲的3个指标性成分在体内的药代动力学特征,考察3个指标成份在大鼠体内的经时过程,并记录3个指标成分的动力学参数,为研究杜仲临床前药动学研究提供实验依据。
参考文献
[1]刘荣华,唐芳瑞,陈兰英,等.不同产地杜仲叶中5种主要有效成分的含量比较[J].中国实验方剂学杂志,2015,56(18):31-34.
[2]陶益,盛辰,李伟东,等.杜仲不同炮制品化学成分研究[J].中国中药杂志,2014,71(22):4352-4355.
[3]杨林军,黄文平,吴永忠,等.杜仲板皮和枝皮中4种有效成分差异性比较[J].中草药,2015,16(4):584-587.
[4]朱换平,赵继荣,邓强.杜仲腰痛丸对腰椎间盘突出症患者血清TNF-α、IL-1β的影响[J].西部中医药,2015,20(4):103-106.
[5]杜津莉,樊炜骏,李建,等.独活寄生汤含药血清对膝关节OA大鼠滑膜细胞TNF-α、IL-6、IL-8、IL-10表达的影响及其机制[J].山东医药,2017,57(44):14-17.
[6]林娜,吕绍光.白术杜仲合剂安胎疗效的临床观察[J].光明中医,2015,11(5):975-977.
[7]王桂萍,玄明实.哈孝贤治疗不孕症经验[J].中医杂志,2014,34(3):195-197.
[8]张英.杜仲木脂素类成分及其测定方法的研究进展[J].北方药学,2014,29(3):53-54.
[9]雷燕妮,张小斌.杜仲叶总黄酮降血压作用的研究[J].陕西农业科学,2016,33(5):6-8.
[10]袁云香.杜仲降血压成分提取方法的研究进展[J].北方园艺,2011,59(24):236-238.
[11]袁带秀,舒丽霞,黄蓉.杜仲黄酮对H22小鼠的抑瘤作用及其机制[J].中国老年学杂志,2016,10(2):291-293.
[12]曾桥,韦承伯.杜仲叶药理作用及临床应用研究进展[J].药学研究,2018,21(8):482-486.
[13]雷燕妮,张小斌.杜仲叶总黄酮降血脂作用研究[J].西北大学学报:自然科学版,2015,34(5):777-780.
[14]陈云华,张硕峰,孙建宁,等.杜仲红景天胶囊抗血栓形成与溶栓作用研究[J].北京中医藥大学学报,2007,46(5):333-336.
[15]席晓志,王婉卿,崔晓伟,等.响应面优化杜仲提取物抗氧化活性及其工艺研究[J].中国现代中药,2018,18(3):310-315.
[16]李欣,袁培耘,何亚平,等.ASE-UPLC法同时测定杜仲制剂中3种成分[J].信阳师范学院学报:自然科学版,2016,22(3):431-434.
[17]曹旭,谢玉敏,朱迪,等.杜仲提取物中五个成分血浆蛋白结合率的测定[J].中国药理学通报,2015,8(1):131-135.
[18]夏鸿林,胡翔.UPLC-MS/MS法同时定量分析暖宫孕子胶囊中的10个成分[J].药物分析杂志,2018,15(7):1158-1164.
(2018-12-11收稿 责任编辑:杨阳)
