锰离子对厌氧发酵的影响及生物利用度研究
2019-09-09张佳佳石先阳
张佳佳,石先阳
(安徽大学 资源与环境工程学院,安徽 合肥 230601)
厌氧消化在处理有机废弃物的同时可回收能源[1],但其易受多种因素如pH、碱度、温度、微量金属元素等的影响[2]。添加适量微量金属元素可增强厌氧污泥的产甲烷活性以及酶活性,促进基质降解[3]。其中锰作为厌氧污泥的重要组成元素,是丙酮酸羧化酶、精氨酸酶和甲基转移酶的辅助因子[4]。
在以牛粪为原料的厌氧发酵中,添加6 g MnSO4可有效提高COD转化为挥发性脂肪酸(VFAs)的速率,使厌氧发酵系统的产气时间缩短了7 d,累积产气量提高41.2%[5];通过测定污泥胞外聚合物(EPS),发现当Mn2+浓度为0.05 mg/L时,污泥内EPS总量下降11.91%[6];在厌氧发酵过程中,添加0.3 mg/L的Mn2+使中间产物-丁酸的转化速度加快17%[7];以隔油池垃圾为原料的厌氧发酵中,22.9 mg/L 的Mn2+使最大甲烷产率提高了40%,产甲烷滞后时间则缩短了66.7%[8]。然而微量金属元素添加过量会增加厌氧反应器的运行成本及造成重金属的二次污染[9]。此外,现有研究对象多集中在微量金属元素种类方面,测定指标比较单一,且较少涉及微量金属元素形态与厌氧污泥生物利用度之间的关系。
本文通过间歇实验探究不同浓度Mn2+对厌氧消化的影响,分析厌氧消化过程中金属元素锰的形态与其生物利用度间的关系,为实现Mn2+的精准投加,提高厌氧消化系统的经济适用性提供理论依据。
1 实验部分
1.1 材料与仪器
C12H22O11、NH4Cl、KH2PO4和NaHCO3均为化学纯;微量元素溶液、MnCl2储备液(400 mg/L)、硝酸溶液(1+1)均为分析纯;所有溶液均用去离子水配制;厌氧颗粒污泥,取自一个实验室规模的上流式厌氧污泥床反应器(UASB);实验用水采用人工配水,营养母液成分为:C12H22O1117.82 g/L,NH4Cl 1.91 g/L,KH2PO40.44 g/L,NaHCO318.6 g/L。每L人工配水中加入0.26 mL微量元素溶液,微量元素溶液组成见表1。
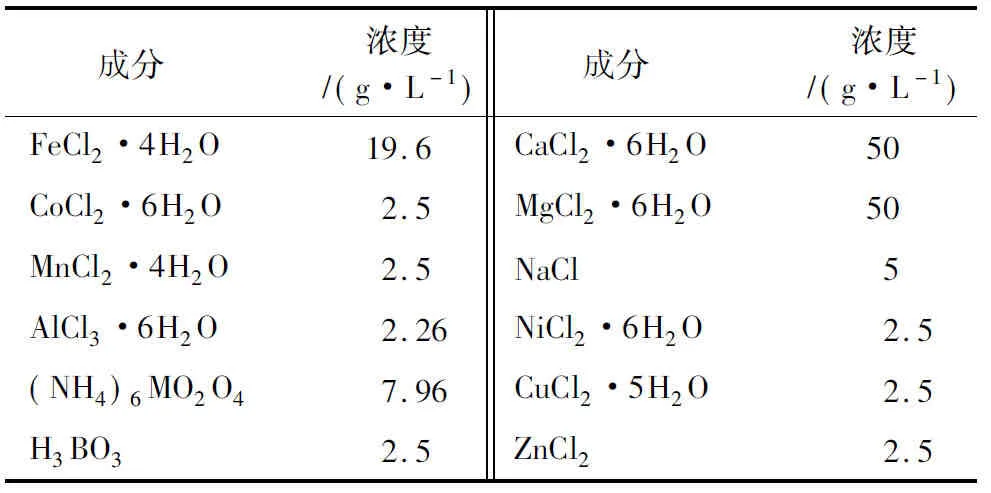
表1 微量元素溶液组成Table 1 Components of trace element solution
PHS-3G酸度计;BIO-DL移液器;IS-RDV1恒温振荡器;SP-6800A气相色谱仪;GC-7860A气相色谱仪;Philips XL30扫描电子显微镜(SEM);DK-S28数显恒温水浴锅;AAS-990AFG原子吸收分光光度计。
1.2 实验方法
实验所用玻璃器皿均经硝酸溶液(1+1)浸泡12 h,反复用去离子水冲洗干净后烘干备用。间歇实验在650 mL玻璃反应器中进行。取15 g经去离子水清洗3次后的厌氧颗粒污泥及40 mL实验用水置于上述反应器中,分别添加0,20,50,100,200 mL的MnCl2储备液,并加入去离子水使其总体积为400 mL,相应的Mn2+浓度为0,20,50,100,200 mg/L,依次编号为1#(对照组)、2#、3#、4#、5#。持续充氩气10 min后迅速用丁基胶塞以及铝帽密封。置于温度为(35±1)℃,转速为135 r/min的恒温振荡器中培养,每组实验设置两个平行。
1.3 分析方法
TSS、VSS、COD、Mn2+浓度采用标准方法测定[10];气体组分采用气相色谱仪测定;气体总体积用排水法测定[11];累积产甲烷动力学参数利用修正后的Gompertz模型分析[12];VFAs的浓度利用气相色谱仪测定;EPS的提取与测定参考文献[13];辅酶M(CoM)的测定参考文献[14];采用扫描电子显微镜观察厌氧污泥的形态;厌氧污泥的光电子能谱(XPS)测定参考文献[15];厌氧污泥中不同形态Mn2+的提取与测定参考Tessier五步提取法[16]。
2 结果与讨论
2.1 Mn2+对产甲烷量的影响
添加不同浓度Mn2+下的累积产甲烷量的变化曲线如图1所示,厌氧消化结束后,1#(对照)累计产甲烷量为75 mL,2#累计产甲烷量为84 mL,较1#提高了12%,3#~5#累计产甲烷量分别为57,61,45 mL,较1#分别降低了24%,18.4%,40%。以修正过的Gompertz模型(式1)对产甲烷过程进行动力学模拟,得到累计产甲烷动力学参数(表2)。
(1)
式中H——反应时间t(h)内的累计产甲烷量,mL;
P——潜在产甲烷量,mL;
Rm——最大甲烷产率,mL/h;
λ——产甲烷滞后时间,h;
e——常数(2.718 281 828)。
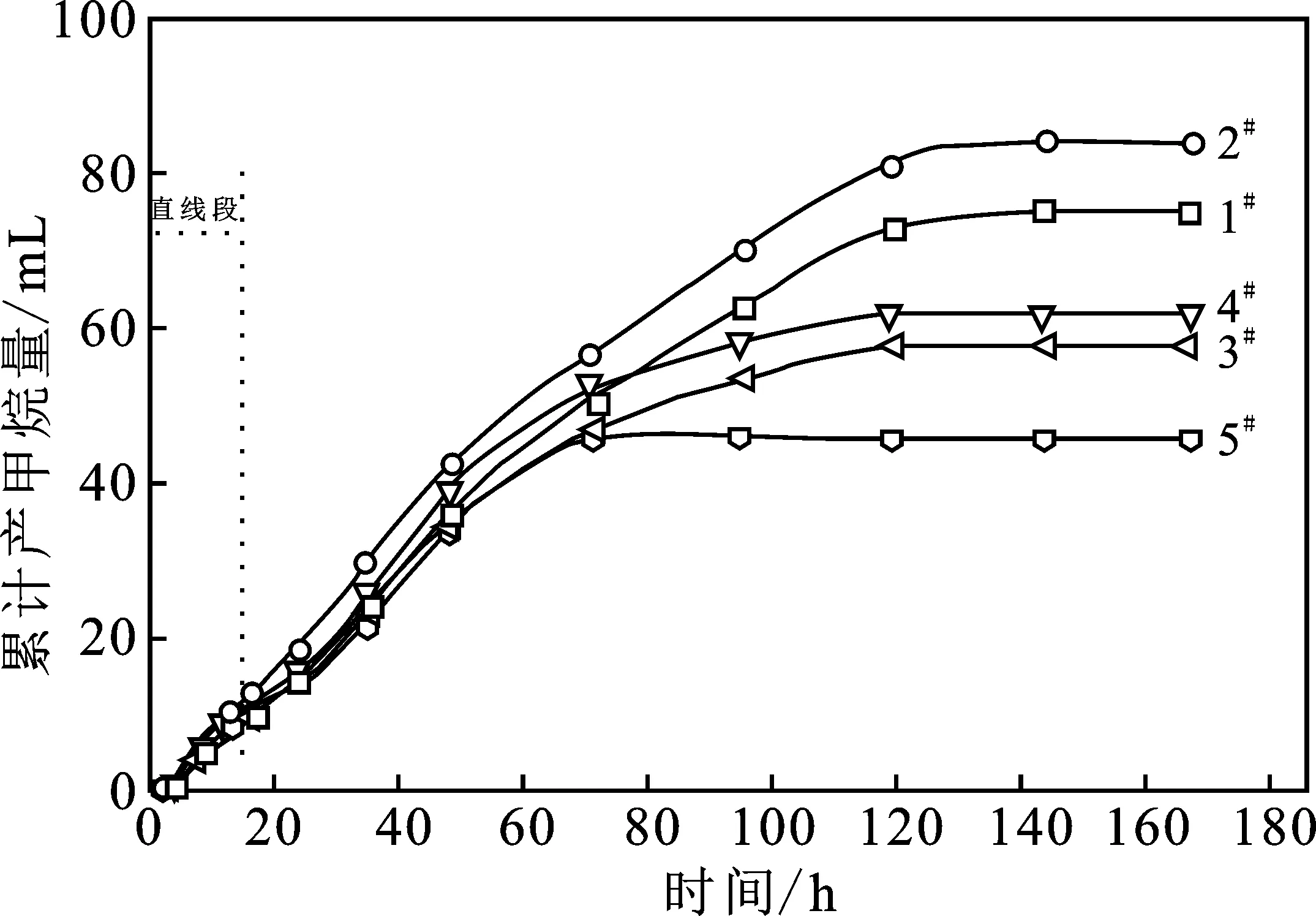
图1 Mn2+对累计产甲烷量的影响Fig.1 Effects of Mn2+ on the cumulative methane production
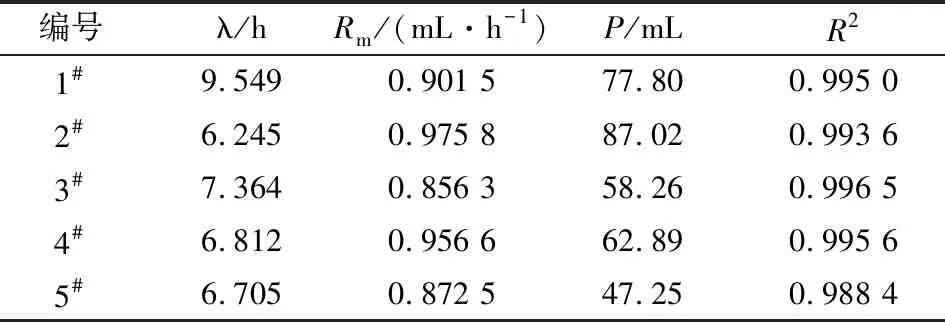
编号λ/hRm/(mL·h-1)P/mLR21#9.5490.901 577.800.995 02#6.2450.975 887.020.993 63#7.3640.856 358.260.996 54#6.8120.956 662.890.995 65#6.7050.872 547.250.988 4
由表2可知,修正过的Gompertz模型可以很好地模拟厌氧污泥产甲烷的动力学过程(R2>0.988)。20 mg/L的Mn2+使产甲烷滞后时间缩短至6.2 h,较对照组降低了34.6%,而潜在产甲烷量则提高至87.02 mL,较对照提高了11.9%。
以最大比产甲烷速率Umax·CH4[mL CH4/(g VSS·d)]和最大比COD去除速率Umax·COD[g COD/(g VSS·d)]作为衡量厌氧污泥活性指标[式(2),式(3)][17],计算结果见图2。
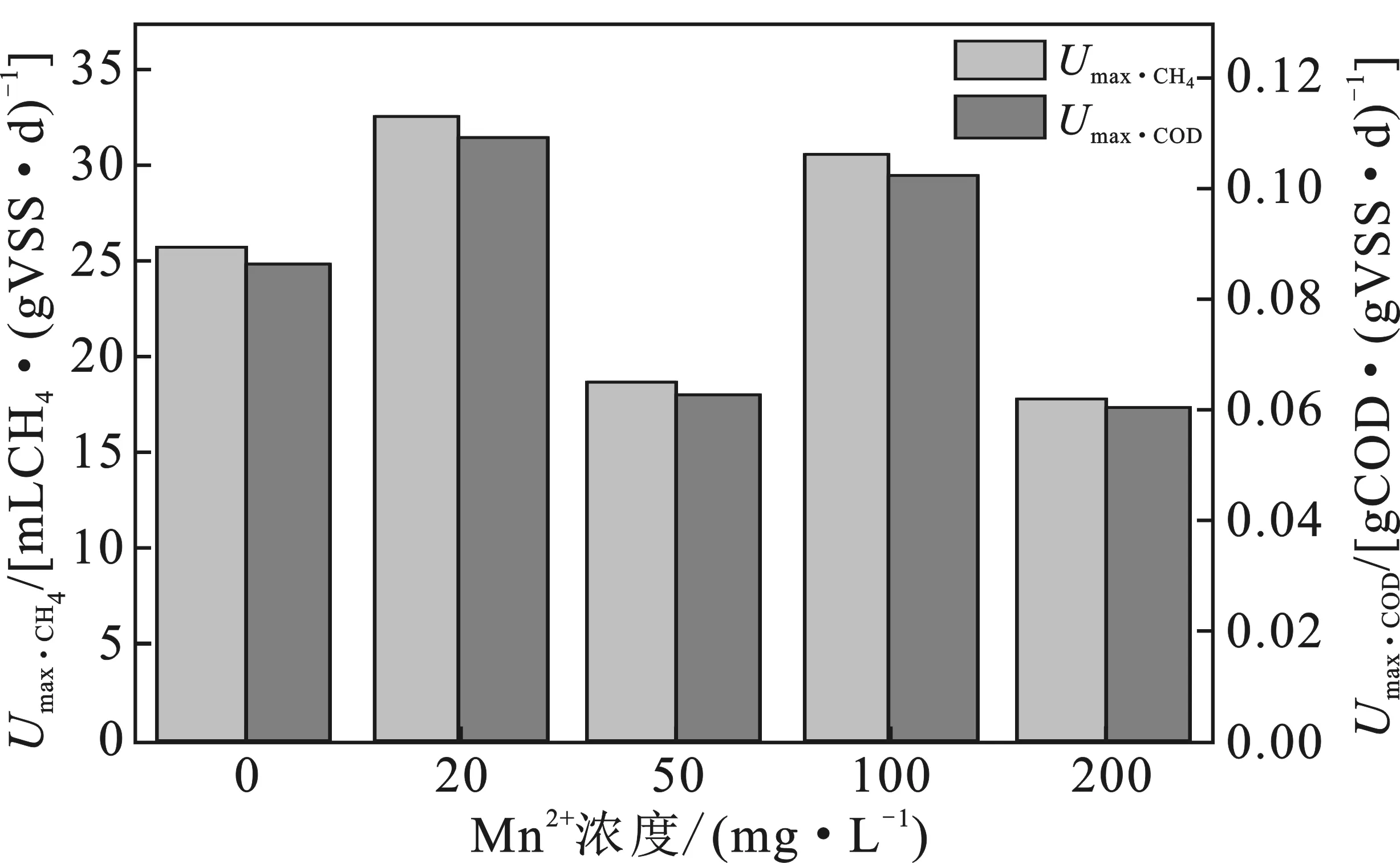
图2 Mn2+对最大比产甲烷速率和 最大比COD去除速率的影响Fig.2 Effects of Mn2+ on Umax·CH4 and Umax·COD
由图2可知,添加Mn2+浓度为20 mg/L时,反应体系的最大比产甲烷速率和最大比COD去除速率分别达到32.63 mL CH4/(g VSS·d)和0.109 1 g COD/(g VSS·d),表明20 mg/L Mn2+的添加促进了基质的降解,此浓度下厌氧污泥的产甲烷活性最高。
(2)
(3)
式中K——累计产甲烷量曲线直线段的斜率,
mL CH4/h;
X——微生物浓度,g VSS/L;
Vn——反应区容积,mL;
T0——反应体系温度,K;
T1——273 K。
CoM(2-巯基乙烷磺酸)作为产甲烷菌特有的一种辅酶,能以甲基维生素B12为甲基供体,经甲基转移酶的作用,形成甲基辅酶M。甲基辅酶M在甲基辅酶M还原酶(MCR)的催化下最终形成甲烷[18]。在一定程度上,产甲烷量和产甲烷速率与CoM的含量及浓度成正比[19]。在厌氧发酵结束后,2#CoM含量较对照提高了15.02%,而3#~5#CoM含量较对照则分别降低了10.06%,19.05%,21.66%(图3),这就从酶学角度解释了累计产甲烷量和产甲烷速率增加的原因。
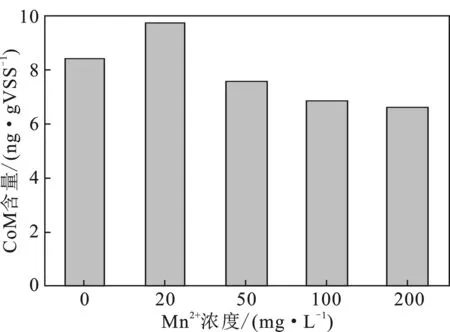
图3 Mn2+对CoM含量的影响Fig.3 Effects of Mn2+ on the CoM concentration
2.2 Mn2+对VFAs的影响
厌氧消化反应中VFAs含量随时间的变化曲线见图4,其主要组分为乙酸(图4b)和丙酸(图4c)。乙酸浓度在0~574.21 mg/L之间,丙酸浓度为0~977.02 mg/L。
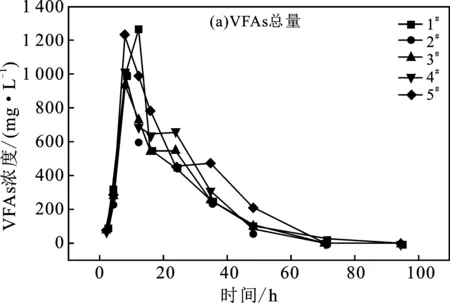

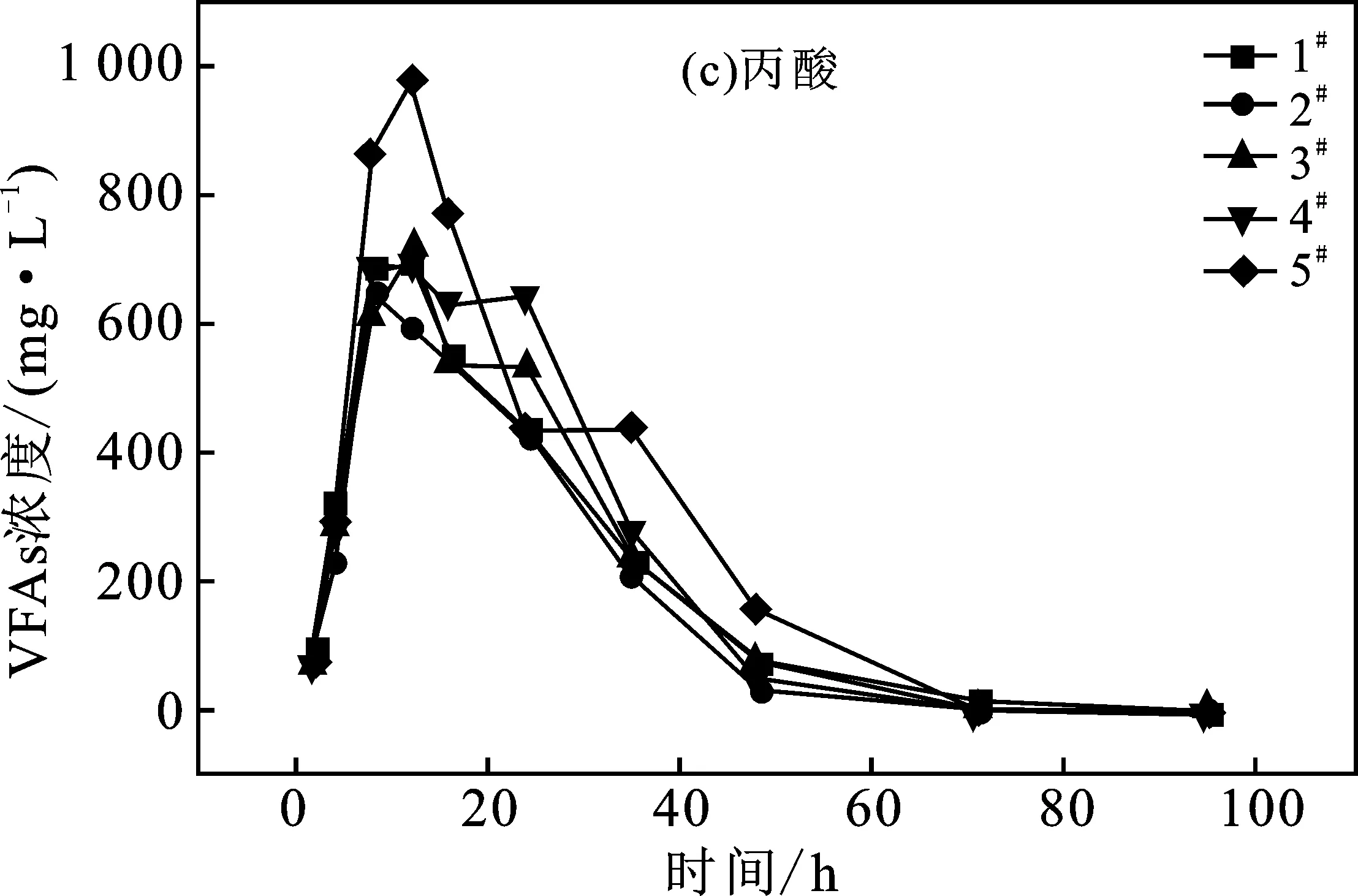
图4 Mn2+对VFAs总量、乙酸以及丙酸含量的影响Fig.4 Effects of Mn2+on the total VFAs, acetic acid and propionic acid
由图4可知,丙酸含量变化趋势和VFAs总量(图4a)变化趋势一致。在0~8 h,VFAs总量迅速增加,2#乙酸最高浓度达350.178 mg/L,而在8~12 h内迅速降低到2.950 mg/L,转化率为99.16%,乙酸浓度达到最高和趋于零的时间较1#均缩短了4 h。随Mn2+浓度的提高,发酵系统出现丙酸积累,导致酸化,从而对甲烷化作用产生了抑制[20]。添加20 mg/L Mn2+可使乙酸含量提前4 h达到峰值,且加速其转化,最大程度地促进VFAs降解为甲烷,提高产气量。
2.3 Mn2+对EPS的影响
颗粒污泥松散型胞外聚合物(LB-EPS)和紧实型胞外聚合物(TB-EPS)主要由蛋白质(PNs)和腐殖质(HSs)组成(图5),其中PNs占45.48%~56.49%,HSs占33.49%~46.20%,而多糖(PSs)所占比例相对较小,为3.55%~14.92%。因LB包裹在TB外部,Mn2+对LB的影响大于TB。Mn2+浓度从0 mg/L增至20 mg/L,LB-EPS从518.28 mg/L增至529.15 mg/L,增加了2.1%。当Mn2+浓度增至50,100,200 mg/L时,LB-EPS则分别降低了38.77%,51.41%和53.91%。LB-EPS的增加增强了颗粒污泥活性,从而促进甲烷化反应的进行[21]。但在高浓度Mn2+暴露下,颗粒污泥结构受到严重破坏,这和图6厌氧污泥的扫描电镜分析结果相一致。

图5 LB-EPS和TB-EPS的多糖、蛋白和腐殖质的浓度Fig.5 Concentrations of the PSs,PNs and HSs of the LB-EPS and TB-EPS
如图6所示,1#厌氧污泥呈现杆状和丝状(图6a),2#(图6b)和5#(图6c)厌氧污泥形态发生变化,出现大量球状菌。微量元素添加会导致厌氧系统甲烷菌形态发生变化,由甲烷丝菌和甲烷杆菌逐渐转化为甲烷球菌[22]。大的比表面积使得球菌拥有比杆菌和丝菌更强的比产甲烷能力。但当Mn2+浓度达到200 mg/L时,厌氧污泥表面排列变得松散,其结构被高浓度Mn2+所破坏,污泥产甲烷活性降低。

图6 扫描电镜下的厌氧污泥形貌Fig.6 SEM images for morphology of anaerobic sludge a.1#;b.2#;c.5#
2.4 Mn2+形态与生物利用度分析
厌氧消化前后,2#污泥的光电子能谱图见图7。

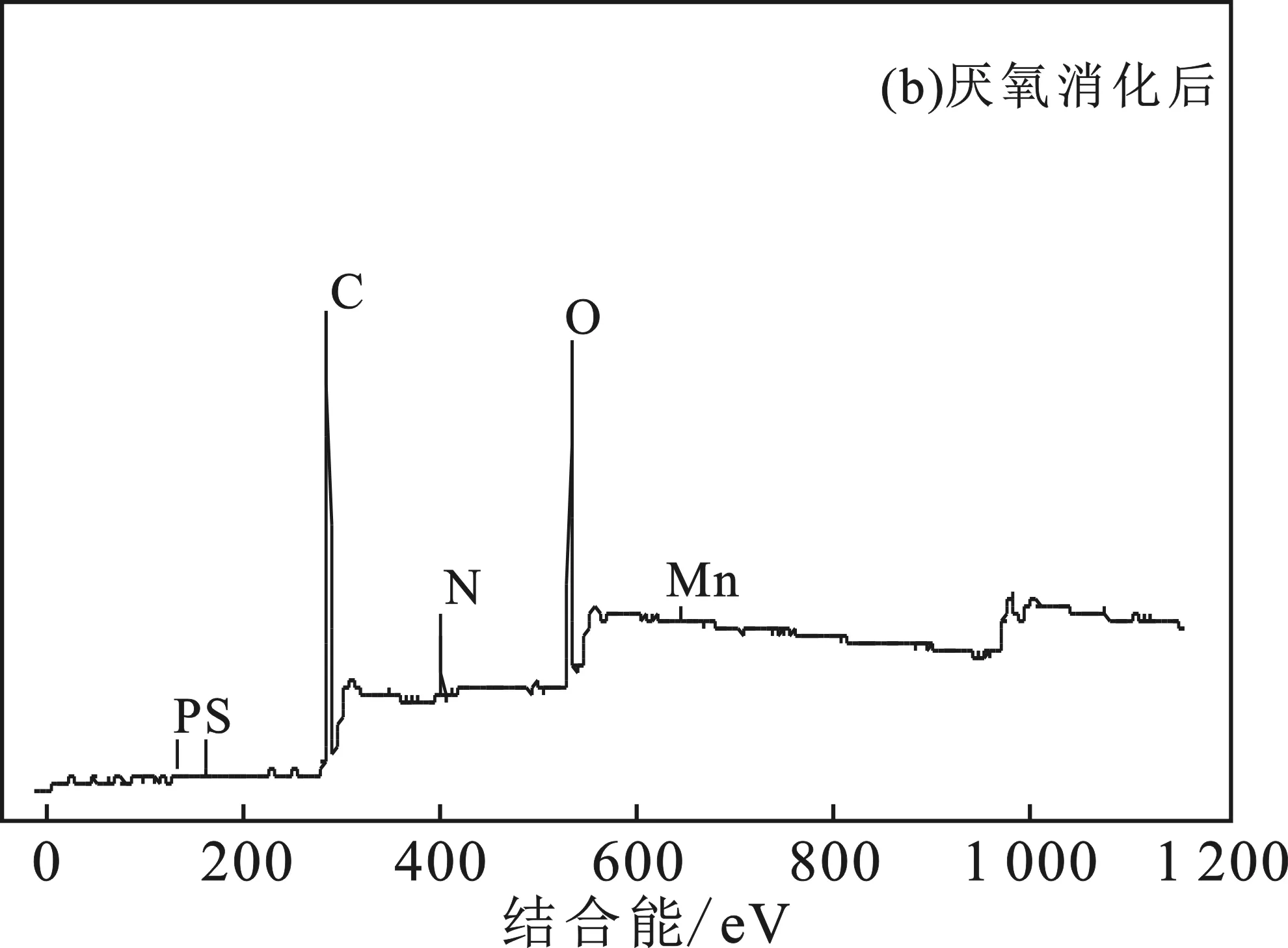
图7 污泥厌氧消化前后的X射线光电子能谱图Fig.7 X-ray photoelectron spectroscopy of sludge before and after anaerobic digestion

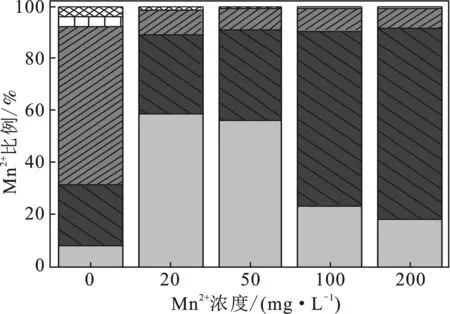
图8 连续提取法所测各形态Mn2+含量及占比(上图为含量,下图为占比)
由图7可知,在厌氧消化结束后观察到锰的特征谱线,说明厌氧消化过程中,厌氧污泥对Mn2+有吸附作用,进而对厌氧消化反应产生影响,1#污泥厌氧消化前后均未观察到锰离子的吸附(图中未显示)。离子可交换态和碳酸盐结合态离子(以下简称有效态离子)最容易被释放出来而被生物体吸收[23]。
由图8可知,向反应体系中加入Mn2+,有效态离子所占比例显著增加,而铁锰氧化物结合态、有机态以及残渣态在一定程度上与添加的Mn2+呈现负相关。其中2#~5#的有效态离子含量较1#分别提高了2.89,5.46,13.91,28.80 mg/L,所占比例较1#提高了57.51%,59.74%,59.20%,60.00%,此时2#~5#对有效态离子的生物利用度[24]分别为15.57%,11.37%,14.13%,14.51%,说明当Mn2+浓度高于20 mg/L,继续增大Mn2+浓度至200 mg/L时,有效态离子生物利用度并未得到提高。综合分析上述实验结果以及考虑到重金属的污染问题,认为20 mg/L的Mn2+能最大程度地增强反应体系性能。
3 结论
(1)Mn2+的添加可提高厌氧系统累计产甲烷量,其最佳浓度为20 mg/L,同时CoM含量较对照提高15.02%,VFAs转化速度加快;但高浓度Mn2+则会抑制乙酸和丙酸的降解,导致系统中VFAs积累。
(2)Mn2+添加后2#的厌氧污泥形态由1#的杆状和丝状转变为球状,同时其LB-EPS总量相对1#提高了2.1%,而3#~5#分别降低了38.77%,51.41%和53.91%。高浓度Mn2+破坏了污泥表面结构,颗粒污泥出现破损。
(3)Mn2+浓度为20 mg/L时,厌氧污泥所利用的有效态离子含量为3.11 mg/L,生物利用度为15.57%,继续提高Mn2+浓度,有效态离子生物利用度并未得到提高。
