三种不同品牌ELISA试剂盒检测ASCA的结果比较及性能评估
2019-09-06余悠悠曾俊祥潘秀军
余悠悠, 曾俊祥, 罗 婷, 邓 琳, 潘秀军
(上海交通大学医学院附属新华医院检验科,上海 200092)
炎症性肠病 (inflammatory bowel disease,IBD)是一种病因不明的慢性非特异性肠道炎症性疾病,主要包括克罗恩病(Crohn's disease,CD)和溃疡性结肠(ulcerative colitis,UC)。 近年来我国IBD的发病率呈明显上升趋势[1]。目前,IBD的病因和发病机制尚未完全明确,可能与遗传、环境、感染、免疫等因素相关[2-3]。抗酿酒酵母抗体(anti-Saccharomyces cerevisiae antibodies,ASCA)在国际上已被认可是IBD特异性的血清学抗体之一[4],其在CD鉴别诊断方面的价值目前也已得到了世界胃肠病学组织的肯定[5]。在国内ASCA也日益得到重视,但国内的研究结果存在很大争议,尚未达成共识[6-7],这给临床推广工作带来一定的障碍。目前,ASCA实验室检测技术主要包括间接免疫荧光法(indirect immunofluoescence,IIF)和酶联免疫吸附试验(enzyme-linked immunosorbent assay,ELISA)。本研究选取了市场上3个试剂厂家的ASCA-ELISA试剂盒进行临床样本的检测,分析检测结果之间的一致性,比较各试剂盒的检测性能,评估ASCA在IBD诊断和鉴别诊断中的价值,以期为该指标的临床应用提供有效参考。
资料与方法
一、资料
1.IBD患者组:140例IBD患者中,CD患者87例,UC患者53例,为2016年6月至2017年11月期间在上海交通大学医学院附属新华医院消化内科、肛肠外科住院的确诊患者,诊断均符合《炎症性肠病诊断与治疗的共识意见(2012年,广州)》[6]。
2.疾病对照组(disease control,DC):DC 组 40 例患者包括急性感染性肠炎、肠息肉、肠结核、肠易激综合征等,主诉为均腹痛、腹泻,后经内镜排除IBD。
本研究通过上海交通大学医学院附属新华医院医学伦理委员会审核批准(No.XHEC-D-2017076),所有研究对象均签署知情同意书。
二、方法
1.血标本的采集:经患者知情同意后,抽取空腹静脉血5 mL,置有分离胶的真空管,待室温凝固后,采用3 000 r/min,常温离心5 min,分离血清,均放置于-80℃储存、备用。
2.试剂和方法:ASCA-IgA和ASCA-IgG检测采用ELISA方法,试剂盒分别采用一家国产品牌试剂A[抗酿酒酵母IgA/IgG抗体定量检测试剂盒(酶联免疫吸附法)96人份,山西瑞豪生物科技有限公司生产,生产批号 IBDB16112901、IBDC16112901];二家进口品牌试剂B、C[试剂B为抗酿酒酵母IgA/IgG抗体检测试剂盒(酶联免疫法)96人份,美国INOVADiagnostics,Inc.生产, 生产批号 031113、029392;试剂C为抗酿酒酵母IgA/IgG测定试剂盒(酶联免疫吸附法)96人份,德国EUROIMMUN公司生产;生产批号CE160504AV、CE160504CG]。标准品和阴、阳性质控物均采用各试剂盒配套产品,操作步骤严格按照各试剂盒说明书进行检测,分别根据各试剂盒说明书提供的临界值判断结果。
3.使用仪器:洗板采用科华ST-36WT全自动洗板机,在Thermo酶标仪上读取及采集数据。
三、统计学处理
采用SPSS 19.0统计学软件进行统计分析,组间比较采用χ2检验或Fisher精确概率法;对3种试剂盒检测的结果一致性进行Kappa检验,根据Kappa值定义一致性强弱程度,当Kappa<0,一致性强度极差;0~0.2,微弱;0.21~0.40,弱;0.41~0.60,中度;0.61~0.80,高度;0.81~1.00,极强[8]。 以临床和(或)病理诊断为金标准,采用四格表分别计算ASCA-IgA、IgG和ASCA-IgA和 (或)IgG诊断IBD的灵敏度、特异度及约登指数,并采用MedCal Version 15.22进行3种试剂盒受试者工作特征(receiver operating characteristic,ROC)曲线分析,通过分析曲线下面积(area under curve,AUC)评判各试剂盒的诊断效能。 当 AUC 接近 0.5 时,表示无诊断价值,AUC<0.7表示诊断准确率较低,AUC 在 0.7~0.9表示诊断准确率中等,AUC>0.9时表示诊断有较高的准确率[9]。

表1 3种ELISA试剂盒检测ASCA的主要实验参数比较
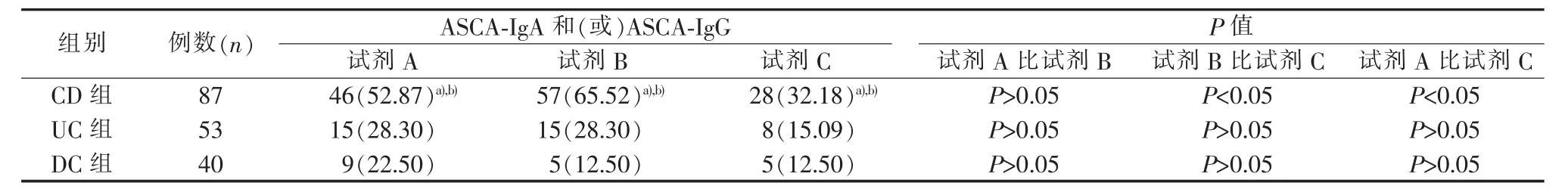
表2 3种试剂检测ASCA-IgA和(或)ASCA-IgG总阳性率比较[n(%)]
结 果
一、3种ELISA试剂盒检测ASCA的主要实验参数比较
列表比较3种ELISA试剂盒检测的几项主要实验参数,关于临界值的建立,因为尚无ASCA的国际参考血清,与国际通用单位之间的关系并未验证,所以暂无国际标准单位,各试剂盒按自身实验室结果设立(见表1)。
二、3种试剂检测ASCA-IgA和 (或)ASCA-IgG总阳性率结果比较
ASCA-IgA和ASCA-IgG两者有1项结果阳性或2项同时阳性即作为ASCA-IgA和 (或)ASCAIgG阳性。同一种试剂在CD组中的检出率均高于UC 组及 DC 组(P<0.05),而在 UC 组的阳性检出率与 DC 组比较,差异无统计学意义(P>0.05)。同一组别不同试剂的阳性检出率情况显示,3种ELISA试剂在UC组及DC组中阳性检出率无统计学意义(P>0.05);而在 CD 组中,试剂 A 与试剂 B 检测结果之间差异无统计学意义,而试剂C的阳性检出率低于试剂 A 及试剂 B(P<0.05)(见表 2)。
三、3种试剂盒对同一批样本的检测结果一致性评价
根据美国临床实验室标准化协会EP12-2A文件对3种试剂的总样本检测结果作一致性分析,ASCA-IgA两两比较的一致性为,试剂A与B、试剂B 与 C、试剂 A 与 C 的 Kappa值分别为 0.423、0.074和0.111,前一组为中等一致性,后2组为极低一致性;3种试剂ASCA-IgG两两比较的,试剂A与B、试剂B与C、试剂A与C的Kappa值分别为0.414、0.447 和 0.584,3 组结果均为中等一致性(见表 3)。
四、3种ELISA试剂检测ASCA的性能比较
分析评价3种试剂检测ASCA的结果对IBD的诊断能力,统计3种试剂盒在ASCA-IgA、ASCAIgG及ASCA-IgA和 (或)ASCA-IgG这3种情况下的灵敏度、特异度以及约登指数,并采用ROC曲线分析得出各组AUC,评判各试剂盒的诊断准确性。结果显示,3种试剂检测IgG和IgA抗体时的灵敏度都欠佳,但联合检测2种抗体的灵敏度都高于单项检测;ASCA-IgA的特异度相对较高,其中试剂C最高为97.5%;ASCA-IgA中试剂A的AUC面积最大为0.72,ASCA-IgG中试剂B的AUC面积最大为0.72,ASCA-IgA和(或)ASCA-IgG的结果AUC面积最大为试剂B的0.69。结合以上各项约登指数,比较3种试剂的检测性能,试剂盒B综合效能最佳,试剂盒A次之,试剂盒C较低(见表4、图1)。

表3 3种试剂盒ASCA-IgA和ASCA-IgG检测结果一致性比较

表4 3种试剂盒主要检测指标诊断效能

图1 ASCA-IgA、ASCA-IgG及ASCA-IgA和(或)ASCA-IgG检测结果ROC曲线
讨 论
IBD是一种病因不明的慢性非特异性肠道炎症性疾病,主要包括CD和溃疡性结肠UC,是北美和欧洲的常见病,但近十余年来本病就诊人数在我国呈逐步增加,趋势非常明显,已成为消化系统常见病[1]。IBD的诊断取决于临床表现、内镜、组织学、放射学等,而内镜检查为侵入性,耗时且有时不被患者接受[10]。特别是在患者的临床表现、内镜和病理特征不典型或有疑惑时,还可能会出现漏诊或误诊现象[9],这会给个人和社会的医疗经济支出带来沉重的负担,因此早期诊断并尽早干预是改善患者预后的关键[11],IBD相关血清生物学标志物的出现有望弥补、甚至部分解决这一问题[12]。
ASCA是国外报道最早的且最具特征性的应用于IBD诊断及鉴别诊断的血清学指标之一[10,13]。2010年最新亚太消化学会炎症性肠病学组推出的关于IBD诊断与治疗的共识意见[2]中也将ASCA列为一项鉴别CD与UC的指标。本研究结果显示,每种试剂在CD组中的阳性率都明显高于UC组及DC组,差异有统计学意义,这与国外Vermeire等[14]、Herszényi等[15]、国内张蜀澜等[16]的研究结果相符,表明ELISA检测ASCA的结果有利于 UC、CD的鉴别。但同时,该结果在国内仍存在争议,高翔等[17]的结果显示,ASCA检测阳性率在CD患者仅为11.8%,而UC患者为58.6%。此外,袁柏思等[18]的研究中,ASCA在CD患者中的阳性率也较低,且以上2项研究之间的结果也不尽一致,与本研究结果更是大相径庭。分析发现,他们皆采用的是间接免疫荧光法检测ASCA。检测方法的不同可能是造成这种差异的主要原因。
本文分析3种ELISA试剂盒在各组中检测的结果一致性,总体来说ASCA-IgG的一致性较好,ASCA-IgA的一致性不甚理想。分析导致这种差异的原因有以下几点。①不同生产单位ELISA板的原料、制作工艺不同。②不同厂家抗原的来源,用量及纯化方式的差异,或各厂家包被技术的差异。③抗原本身的复杂性和可能存在的交叉反应。④本文结果显示,试剂A与试剂B的一致性较高,而与试剂C的结果差异较大,试剂盒C酶结合物使用的是兔抗人抗体,其他2种是羊抗人抗体,考虑可能是酶标记抗体的种类不同导致了更大的结果差异。
有报道称,ASCA诊断CD的灵敏度和特异度分别为33%和83%,且灵敏度与特异度呈负相关[19],本研究则通过灵敏度、特异度、约登指数和AUC等指标来评估3种试剂盒对IBD的鉴别诊断效能,发现也存在这样的情况,3种试剂盒单独检测IgA和IgG的灵敏度均较低,特异度相对较高,约登指数也较低。因此,不推荐将单一抗体指标作为IBD的筛查方法,容易漏诊,若同时检测2种抗体,则检测灵敏度有所提高,有利于IBD的检出,以试剂B最优。就特异度而言,ASCA-IgA的特异度总体优于ASCA-IgG,试剂C的ASCA-IgA结果特异度最高,用于诊断时的误诊率可能较低。ROC曲线结果显示,试剂B的各项检测结果AUC都较高。因此,综合来说,试剂B的诊断效能相对较佳,而试剂A作为国产试剂,与进口试剂B相比,其主要诊断效能比较接近,填补了国内慢性IBD检测产品的空白,且其更具有价格优势,树立了国产试剂在自身免疫检测领域健康快速发展的信心与骄傲。
总之,3种试剂盒ASCA的ELISA检测结果对IBD的阳性诊断价值有限,不适合IBD的人群筛查,但在CD的鉴别诊断方面具有一定的临床应用价值;3种试剂盒各有特点,但检测结果尚存在一定的差异;国产试剂在此领域也具有一定的竞争力,在实际应用中,可根据具体情况合理选用。
