溶解性有机质对溶液中铁离子检测的影响及原因分析
2019-09-05吴东明李怡陈耀华邓晓武春媛
吴东明 李怡 陈耀华 邓晓 武春媛


摘 要 铁离子的定量检测是探索铁元素地球化学过程的重要手段。环境介质中广泛存在的溶解性有机质(DOM)与铁离子存在络合作用,这可能影响溶液中铁离子的测定。为此,本文研究了DOM对原子吸收光谱法和邻菲罗啉比色法测定溶液中铁离子的影响,并初步探讨其原因。结果表明:(1)原子吸收光谱法测定铁离子的精密度与比色法相当,小于5%,但准确度更高,回收率达86.4%~97.8%;检出限更低,可达0.012 mg/L。(2)DOM对比色法的影响显著,使显色时长增加11.5 h,相对标准偏差增加1.2%~22.2%,准确度下降28.3%~44.4%。随着DOM浓度的增加,比色法的准确度下降趋势符合指数函数模型,精密度下降趋势符合先增大后减小的一元二次函数模型。而且,铁离子浓度越低,受DOM影响越大。相反,DOM对原子吸收光谱法測定铁离子的影响不大。(3)红外光谱和荧光光谱结果表明:DOM对比色法的影响主要是通过氢键结合或π-π共轭作用与铁离子/邻菲罗啉发生络合作用,减少了铁离子与邻菲罗啉的络合而产生的。
关键词 铁离子;检测;溶解性有机质;准确度;精密度
中图分类号 S31 文献标识码 A
Abstract Quantitative detection is a crucial technique for investigating the geochemical processes of ferric ion (Fe). However, due to the ubiquity of dissolved organic matter (DOM) in environmental medium, the combination of Fe with DOM may affect the determination of Fe in solution. Therefore, the effect of DOM between atomic absorption spectrometry (AAS) and colorimetry for Fe determination was tested. Precision of AAS was as good as colorimetry, both of them were less than 5%. However, AAS was more accurate with a recovery rate of 86.4%97.8% and its detection limit was as low as 0.012 mg/L. DOM had a significant effect on colorimetry. The presence of DOM increased testing time and relative standard deviation of 11.5 h, 1.2%22.2%, respectively. Moreover, the accuracy was also decreased by 28.3%44.4%. As the concentration of DOM increasing, the accuracy was decreased in the tendency of exponential function, and the trend of the veracity fitted well with unary quadratic model. Moreover, the effect of DOM was greater with the decreasing concentration of iron. On the contrary, the presence of DOM had no significant influence on AAS. The results of EEMs and FTIR indicated that existed hydrogen bonding or π-π interaction occurred between DOM and Fe/phen that affected the interaction of Fe and colorimetry in a drive to influence the testing results.
Keywords ferric ion; determination; dissolved organic matter; veracity; accuracy
DOI 10.3969/j.issn.1000-2561.2019.07.028
铁是地球表面和地壳中较为丰富的金属元素之一[1]。特别是溶解态铁离子,生物/化学活性强,不仅参与铁循环、碳/氮循环、污染物迁移转化等地球化学过程,更参与动、植物的生命系统活动过程[2-6]。为了深入探索这些过程,准确定量溶液中的铁离子十分必要。常用的铁离子含量测定方法主要有两类。一是原子光谱法,包括原子吸收光谱法、电感耦合等离子体质谱法等,此方法准确度高、检出限低,但仪器昂贵[7-8];二是比色法,此方法仪器成本低、操作简单、应用广泛,其中又以邻菲罗啉比色法使用最为广泛[1, 9-10]。铁离子测定的准确性和精密度除了与所选方法有关,还与铁离子所在的介质组成密切相关。有研究表明,环境介质的温度、酸度、盐度、离子成分均能影响铁离子的测定[7, 9-10]。如Braunschweig等[9]发现:对于邻菲罗啉比色法测定铁离子,酸性介质下的准确度更高;20 ℃下的回收率是60 ℃的4~6倍;基质中的微量元素组分可使回收率下降5%~9%;维生素组分可使浓度被高估20%,并认为干扰物的自我吸收和络合作用、高温的非生物氧化是导致准确度降低的原因,低pH环境的抑制氧化作用是保证准确测量的重要因素。Paipa等[10]研究表明酸性矿床废水中的铜离子是导致邻菲罗林比色法准确度低、精密度高的原因。溶解性有机质(DOM)通常也与铁离子共存于同一环境介质中。理论上,DOM含有的羟基、羧基、酚羟基等多种活性基团能与铁离子发生络合结合[11-14]。然而关于DOM对铁离子测定的影响未见报道,更不清楚其作用过程。
因此,本文以邻菲罗啉比色法和原子吸收光谱测定溶液中的铁离子为研究对象,研究DOM对两种方法的影响,并以红外光谱法、荧光光谱法探讨DOM影响检测的原因,拟为含DOM介质下铁离子检测方法的开发提供基础数据。
1 材料与方法
1.1 材料
(1)铁离子标准溶液配制。称取0.4965 g FeSO4·7H2O溶于20 mL盐酸(1+1)溶液中待溶解后加蒸馏水定容至1 L,即为100 mg/L铁离子。
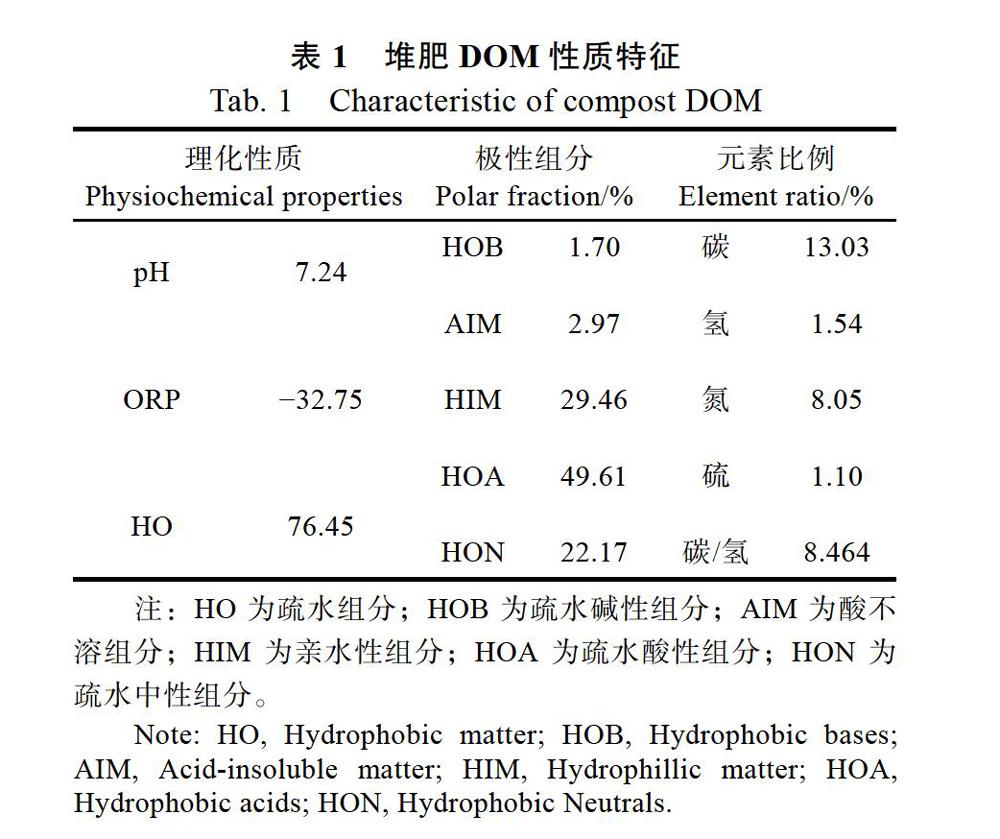
(2)DOM的制备。由木薯杆堆肥为原料提取而成,并以总有机碳/氮分析仪(multi N/C 3100,Analytikjena)测定含量,具体方法见文献[15]。理化性质、极性组分、元素比例等特征见表1.
(3)含DOM铁离子溶液配制。将一定量DOM与铁离子混合后,于25℃、200 r/min避光振荡24 h,即为含DOM的铁离子溶液。
1.2 方法
1.2.1 铁离子测定方法 (1)比色法。吸取3 mL水样溶液,加入10%乙酸钠1 mL,再加入10%盐酸羟胺0.2 mL,放置5min后加入0.1%邻菲罗啉(Phen)1 mL,去离子水定容至10 mL,显色15 h后,于分光光度计(UV-2600,Shimadzu)测定吸光值。波长设置为510 nm。
(2)原子吸收光谱法。将水样以纯水稀释5倍后直接于原子吸收光谱仪(PinAAcle 900T,Perkin Elmer)测定。分析线为248.35 nm;狭缝宽度为0.2 nm,空气-乙炔焰。
1.2.2 DOM对铁离子测定的影响 (1)对检测时长的影响。预实验表明DOM对原子吸收光谱检测时长的影响不大。此处主要考察DOM对比色法显色时间的影响,观察显色剂添加后,吸光度随时间的变化情况。DOM添加量为100 mg/L。
(2)对方法准确度和精密度的影响。为分别考察“不同浓度DOM对铁离子检测的影响”“DOM对不同浓度铁离子检测的影响”,共设置以下2组添加回收实验(表2),每个处理5次重复。含DOM铁离子溶液的配制参考1.1小节。
1.2.3 DOM影响铁离子测定原因分析 为分析DOM影响铁离子检测的原因,分别将5 mg/L铁离子、80 mg/L Phen与20 mg/L DOM混合,于25 ℃、200 r/min避光振荡24 h后,测定混合物的荧光光谱特征、红外光谱特征。
(1)荧光光谱表征。采用荧光光度计(LS-55,Perkin Elmer)对待测样品进行扫描。激光光源为150 W氙弧灯,PMT电压为700 V,激发波长(Ex)为200~650 nm,发射波长(Em)为250~750 nm,扫描速率为1500 nm/min,响应时间设为“自动”。
(2)红外光谱表征。将DOM样品真空冷冻干燥后,称取1~2 mg样品粉末与光谱纯KBr混合、磨细、压片,于傅里叶红外光谱仪(Frontier,Perkin Elmer)上进行扫描。扫描波数设置为400~ 4000 cm?1。
2 结果与分析
2.1 比色法和原子吸收光谱法的比较
2.1.1 标准曲线与检出限 由图1可知,铁离子浓度为1~5 mg/L时,铁离子浓度与吸光度均符合比尔定律,呈现出良好的线性关系。比色法、原子吸收光谱法的线性回归方程分别为y=0.2049x- 0.0188(R2=0.9985)、y=0.0755x+0.0071(R2= 0.9994)。根据ICHQ2的原则,可计算得比色法的检出限为0.090 mg/L;原子光谱法的最低检出限为0.012 mg/L。整体上,原子吸收光谱法的线性更好,检出限更低。
2.1.2 准确度与精密度 准确度与精密度是方法学考察的重要指标。准确度指的是测量值与真实值的接近程度,通常以回收率来表示;精密度是指同一个数值,多次独立测量,各测量值的一致程度,通常以相对标准偏差表示。
(1)准确度:如表3,在考察的浓度区间内,比色法的回收率在61.5%~90.4%之间,平均值为79.6%;原子吸收光谱法的回收率在86.4%~95.7%之间,平均值为93.2%。可知,原子吸收光谱法的准确度更高。此外,对于比色法,回收率随铁离子浓度降低而减小,当铁离子浓度为1 mg/L时,回收率小于70%,已不能准确定量。
(2)精密度:由表3可知,比色法的相对标准偏差在0.444%~2.939%之间,原子吸收光谱的相对标准偏差在0.322%~3.929%之间,均小于5%,说明两种方法的精密度较高。方法的精密度还与铁离子的浓度有关。铁离子浓度分别为5、2 mg/L时,比色法和原子吸收光谱法的相对标准偏差最低。
2.2 DOM对两种方法测定铁离子的影响
2.2.1 DOM对检测时长的影响 本研究结果表明,当溶液中铁离子与DOM共存时,DOM对原子吸收光谱法的测定时长影响不大,但显著增加了比色法的测定时长。如图2所示,无DOM的铁离子测定,在0.5 h时即达到显色稳定,而含DOM铁离子至少需12 h后才达到显色稳定。这使比色法的整体时长增加11.5 h。此外,显色稳定后,含DOM下的吸光度远小于无DOM,这说明DOM也影响了比色法的准确性。
2.2.2 DOM对铁离子检测准确度、精密度的影响(1)DOM对不同浓度铁离子检测的影响。准确度:由图3可知,当DOM与铁离子共存时,可使比色法的回收率降低28.3%~44.4%,严重影响了比色法的准确性。其中对1、10 mg/L铁离子的测定影响最大,对2 mg/L铁离子影响最小。整体上,DOM对比色法准确性的降低作用呈现V型曲线;相反,对于原子吸收光谱法,DOM只使10 mg/L铁离子的回收率减小3.4%,而一定程度上增加了1~5 mg/L鐵离子的回收率(1.1%~ 7.0%),这说明DOM对原子吸收光谱还存在着一定正的基质效应。
精密度:DOM均增加了两种方法的相对标准偏差(图3),其中对比色法增加数值更大,说明DOM对比色法精密度的影响更大。此外,DOM对低浓度铁离子(1 mg/L)测定的精密度影响最大,可分别使比色法和原子吸收光谱法相关标准偏差增加22.2%、8.6%。
(2)不同浓度DOM对铁离子检测的影响。 准确度:由图4可知,当DOM与铁离子共存时,随着DOM浓度的增加,比色法的回收率呈现出现先急剧下降后平缓的指数函数趋势(y= 78.639e?0.006x,R2=0.8748)。当DOM浓度小于10 mg/L时,比色法的回收率即小于70%。DOM浓度为100 mg/L时,回收率只有46.0%,严重影响了比色法的准确度。相反,原子吸收光谱法的回收率受DOM影响不显著。
精密度:如图4,比色法的相对标准偏差随DOM浓度增加呈现出先增加后减少的一元二次函数趋势(y=0.0028x2+0.3327x+0.1438,R2=0.8550)。当DOM浓度为50 mg/L时,比色法的标准偏差最大(11.5%),精密度最低。原子吸收光谱法的精密度受DOM影响不显著,相对标准偏差均小于5%。
2.3 DOM影响铁离子测定的原因分析
综上可知,DOM极大地影响了比色法的准确度和精密度。因比色法测定铁离子过程已扣除了DOM的背景吸光度,根据比色法的原理[16],我们猜测DOM可能影响了其络合过程而影响了方法的准确度和精密度。为此,我们测定了DOM与铁离子/Phen络合物的红外吸收光谱和荧光光谱特征。
2.3.1 三维荧光光谱特征 如图5,Phen在Ex/Em=(285~363) nm/(331~427)nm处有一个强而尖锐的特征荧光峰;DOM在Ex/Em=(335~620) nm/(362~692) nm有一个类腐殖酸荧光峰[17];当DOM与Phen共存时,可顯著观察到Phen的荧光峰强度降低73.4%,这表明Phen与DOM中的类腐殖酸物质发生了强有力络合作用[18]。当铁离子
2.3.2 红外光谱特征 由图6可知,本研究所选的堆肥DOM在3390、1654、1380、1070、642 cm?1含有显著的吸收峰,说明该DOM是一种既含苯环、酚羟基等芳香基团,也含有甲基、氨基、羧基、羟基等亲水基团的有机质[11-14, 20]。分析DOM-Fe络合物的红外光谱信息:DOM络合铁离子后,3400~3100 cm?1和642 cm?1处的强度下降,并发生一定的红移,说明铁离子与DOM的羟基、氨基发生了氢键结合[15, 20];DOM络合Phen后,3400~3100、1070、642 cm?1的强度发生了明显下降,说明Phen与DOM的羟基、羧基、氨基存在着氢键结合;这与DOM的极性组分特征一致(表1),HOA组分在DOM中的含量最高,达49.61%,是一种与金属离子或苯类物质结合作用均较强的物质[15, 21]。1654 cm?1处的吸收峰也发生了明显的下降,说明Phen与DOM存在苯环之间的π-π共轭作用[22-23],这与表1中DOM的芳香性参数(碳/氢)一致,所用的堆肥DOM是一种芳香性较高的有机质[21]。
3 讨论
3.1 DOM影响比色法测定铁离子原因分析
比色法测定铁离子的原理是Fe与Phen生成橙红色络合物,通过对络合物的比色而间接获得Fe的含量[16]。本研究发现DOM的腐殖酸类物质能通过氢键结合与铁离子发生络合作用。这与前人的研究结果一致:DOM中的腐殖酸类物质通常含有大量的羧基、羟基、酚羟基等活性官能团[12-14],Fe、Hg、Cu等顺磁金属能与DOM的这官能团发生络合生成多齿螯合物而使DOM荧光性发生淬灭[2, 3, 11, 19]。Fujii等[2]认为DOM的芳香性越大、含氧酸性官能团越多,与金属离子的结合能力越强;形成的多齿配体中若含有O/N配体,配合物越稳定。邬钰等[4]也发现DOM中的多种酚酸物质能与Fe发生强有力的络合。含苯环的芳香类物质也能与DOM发生结合。研究表明,多环芳烃能与DOM发生NH-π和π-π结合[18, 22-23]。这与本研究结果相似。Phen是一种螯合能力很强的双齿杂环化合物配体,DOM中的羟基、羧基、氨基、苯环等与Phen发生氢键、π-π共轭结合。因此,在比色过程中,Fe、DOM、Phen三者将发生竞争络合而减少Phen与Fe之间的络合,最终影响测定。本研究结果中“DOM浓度越高或铁离子浓度越低,检测受影响越大”的现象也从侧面证明了这一点,即DOM物质的量足够时,可提供的络合位点更多,与Phen或Fe的络合程度则越大[24]。此外,DOM中的Cu2+、Mn2+、Zn2+也可能是影响比色法测定的重要因素,后者可在Phen/Fe的络合过程中形成空间位阻[9-10]。
为此,在对DOM介质下的铁离子进行比色法测定时,应对样品进行去除DOM前处理,或挑选一种对铁离子选择性较高的显色剂。
3.2 DOM影响原子吸收光谱法测定铁离子的原因分析
与比色法不一样,原子吸收光谱法是基于待测元素基态原子蒸汽对其特征辐射谱线的吸收程度而定量的一种仪器分析方法[25]。本研究中,DOM对原子吸收光谱法的影响不大,可能是因为不同元素的原子结构和外层电子排布不同,对辐射谱线的吸收具有选择性[26],溶液中的DOM组分对其影响有限。DOM对它具有一定的基质效应,一方面可能是DOM中也含有铁元素,使测定结果偏大;另一方面是DOM与铁离子生成了更稳定的络合物,降低了铁的原子化效果,使测定结果偏低[10]。
4 结论
(1)对于溶液中铁离子的测定,原子吸收光谱法与比色法的精密度相当,但准确度更高(回收率:86.4%~97.8%),检出限更低(0.012 mg/L)。
(2)DOM對原子吸收光谱法测定铁离子的影响不明显,而显著降低了比色法的准确度、精密度、检测时长。随着DOM浓度的增加,比色法的准确度降低,呈现出指数函数趋势;对精密度的降低,呈现出先增大后减小的一元二次函数趋势。此外铁离子浓度越低,受DOM的影响更大。
(3)在DOM存在的溶液介质中,DOM影响比色法的机制主要是通过氢键结合或π-π共轭作用与铁离子、Phen发生络合作用,减少了铁离子与Phen的络合程度而导致的。
参考文献
Lin M, Hu X, Pan D, et al. Determination of iron in seawater: from the laboratory to in situ, measurements[J]. Talanta, 2018, 188: 135-144.
Fujii M, Dang T C, Bligh M W, et al. Effect of natural organic matter on iron uptake by the freshwater cyanobacterium Microcystis aeruginosa[J]. Environmental Science & Technology, 2014, 48(1): 365-374.
Fujii M, Imaoka A, Yoshimura C, et al. Effects of molecular composition of natural organic matter on ferric iron complexation at circumneutral pH[J]. Environmental Science & Technology, 2014, 48(8): 4414-4424.
邬 钰, 向 武, 傅先芳, 等. 东北哈尼泥炭沼泽中酚酸的组成、酚铁相互作用及其环境意义[J]. 地球科学, 2016, 41(4): 683-691.
Zhu Y, Hu X, Pan D, et al. Speciation determination of iron and its spatial and seasonal distribution in coastal river[J]. Scientific Reports, 2018, 8(1): 2576.
Lin F, Cai J, Li Y, et al. Constituting fully integrated colorimetric analysis system for Fe(III) on multifunctional nitrogen-doped MoO3 / cellulose paper[J]. Talanta, 2018, 180: 352-357.
Kang J H, Kim C. Colorimetric detection of iron and fluorescence detection of zinc and cadmium by a chemosensor containing a bio-friendly octopamine[J]. Photochemical & Photobiological Sciences, 2018, 17(4): 442-452.
Sahraeian T, Sereshti H, Rohanifar A. Simultaneous determination of bismuth, lead, and iron in water samples by optimization of usaeme and ICP-OES via experimental design[J]. Journal of Analysis & Testing, 2018, 2:98-105.
Braunschweig J, Bosch J, Heister K, et al. Reevaluation of colorimetric iron determination methods commonly used in geomicrobiology[J]. Journal of Microbiological Methods, 2012, 89(1): 41-48.
Paipa C, Mateo M, Godoy I, et al. Comparative study of alternative methods for the simultaneous determination of Fe3+, and Fe2+, in leaching solutions and in acid mine drainages[J]. Minerals Engineering, 2005, 18(11): 1116-1119.
Poulin B A, Ryan J N, Aiken G R. Effects of iron on optical properties of dissolved organic matter[J]. Environmental Science & Technology, 2014, 48(17): 10098-10106.
Lerman I, Chen Y, Xing B, et al. Adsorption of carbamazepine by carbon nanotubes: Effects of DOM introduction and competition with phenanthrene and bisphenol A[J]. Environmental Pollution, 2013, 182(6): 169-176.
Nebbioso A, Piccolo A. Molecular characterization of dissolved organic matter (DOM): a critical review[J]. Analytical & Bioanalytical Chemistry, 2013, 405(1): 109-124.
Zhou J, Chen H, Huang W. Effects of rice straw-derived dissolved organic matter on pyrene sorption by soil[J]. Environmental Toxicology and Chemistry, 2010, 29(9): 1967-1975.
Wu D, Yun Y, Jiang L, et al. Influence of dissolved organic matter on sorption and desorption of MCPA in ferralsol[J]. Science of the Total Environment, 2018, 616-617: 1449-1456.
Carpenter C E, Ward R E. Iron Determination by Ferrozine Method[M]// Nielsen S S. Food Analysis Laboratory Manual, Cham: Springer, 2017: 157-161.
Qin C, Liu H, Liu L, et al. Bioavailability and characterization of dissolved organic nitrogen and dissolved organic phosphorus in wastewater effluents[J]. Science of the Total Environment, 2015, 511: 47-53.
Wang L, Li H, Yang Y, et al. Identifying structural characteristics of humic acid to static and dynamic fluorescence quenching of phenanthrene, 9-phenanthrol, and naphthalene[J]. Water Research, 2017, 122: 337-344.
趙 萱, 成杰民. 白洋淀沉积物中溶解有机质荧光特性及其与铜的相互作用[J]. 农业环境科学学报, 2012, 31(6): 1217-1222.
Oren A, Chefetz B. Sorptive and desorptive fractionation of dissolved organic matter by mineral soil matrices[J]. Journal of Environmental Quality, 2012, 41(2): 526-533.
吴东明, 任常琦, 李勤奋, 等. 溶解性有机质对铁铝土吸附2,4-D的影响[J]. 中国环境科学, 2018, 38(3): 1090-1098.
占新华, 周立祥, 杨 红, 等. 水溶性有机物与多环芳烃结合特征的红外光谱学研究[J]. 土壤学报, 2007, 44(1): 47-53.
Zhao J, Wang Z, Ghosh S, et al. Phenanthrene binding by humic acid-protein complexes as studied by passive dosing technique[J]. Environmental Pollution, 2014, 184(1): 145-153.
Gledhill M, Gerringa L J A. The effect of metal concentration on the parameters derived from complexometric titrations of trace elements in seawater[J]. Frontiers in Marine Science, 2017, 4: 251-565.
Welz B, Vale M G R, Pereira ? R, et al. Continuum source atomic absorption spectrometry: past, present and future aspects-a critical review[J]. Journal of the Brazilian Chemical Society, 2014, 25(5): 799-821.
Akram S, Najam R, Rizwani G H, et al. Determination of heavy metal contents by atomic absorption spectroscopy (AAS) in some medicinal plants from Pakistani and Malaysian origin[J]. Pakistan Journal of Pharmaceutical Sciences, 2015, 28(5): 1781-1787.
