二氧化碳-氮气混合气体在微粉硅胶中生成水合物的实验研究*
2019-09-05梁德青
刘 军,梁德青
(1.中国科学院广州能源研究所,广州 510640;2.中国科学院天然气水合物重点实验室,广州 510640;3.广东省新能源和可再生能源研究开发与应用重点实验室,广州 510640;4.中国科学院大学,北京 100049)
0 引 言
全球的能源供应目前仍主要来源于化石燃料的燃烧,燃烧化石燃料释放大量的N2与CO2,导致严重的温室效应[1]。为降低温室效应,改善人类居住环境,人们提出了将CO2分离,用于置换海底的可燃冰,封存在海底[2]。1 m3的可燃冰(水合物)可以储存约160 m3的CO2,能有效缓解环境问题[3-4]。
基于水合物法分离N2与CO2混合气的技术具有重大的研究价值,但在生成水合物的过程中,由于水合物阻碍了气液进一步的接触,导致水合物的生成效率降低[5]。为了增大水合物生成过程中气液接触表面,微粉硅胶(silica gel)作为一种多孔介质,被用于促进水合物的生成[6]。
ZHONG等[7-9]研究了在微粉硅胶中利用水合物法分离CO2/H2混合气,在分离CO2/H2混合气的过程中,水合物中CO2含量占客体组分的比例能够达到98mol%,分离效果较好。因此,在微粉硅胶中生成水合物,进而分离N2与CO2混合气具有重要研究价值。早在2005年,SEO等[10]最先利用在微粉硅胶中生成水合物分离N2/CO2混合气,利用三步分离的方法,CO2占水合物中客体组分含量的比例最高能够达到96mol%。ADEYEMO等[11]在实验中添加热力学促进剂THF,虽然能降低水合物生成压力,但是同样降低了相对气体消耗量。
然而微粉硅胶使水合物的相平衡曲线向左移动,增大了水合物的生成压力[12-14]。在水合物的生成工艺中,压缩气体的能耗占所有能耗的50% ~80%[13]。为了降低水合物的生成压力,人们采用添加水合物生成热力学促进剂(THF/TBAB),虽然热力学促进剂能降低水合物的生成压力,但是热力学促进剂本身占据了水合物的大笼子,降低了相对气体消耗量[15-16]。为了能有效降低水合物生成压力,而不降低水合物生成相对气体消耗量,可以采用降低温度到冰点以下的方式[17]。在纯水生成水合物的过程中,水在冰点以下结成块状的冰,阻碍了气冰的进一步接触,限制了人们在冰点以下研究水合物的生成效果[18]。然而在微粉硅胶中,水结冰不会阻碍气冰的接触,可有效促进水合物的生成[19]。
为降低生成水合物所需能耗,并快速大量地生成水合物,本工作将温度设定在冰点以下,开展在微粉硅胶中N2与CO2混合气水合物的生成研究。分析反应釜中气体组分随时间的变化关系,水合物中气体组分与水合物生成驱动力之间的关系,生成水合物的气体消耗量与消耗速率随压力、温度变化关系。
1 实验部分
1.1 实验材料
CO2(20mol%)与N2(80mol%)的标准混合气购买于佛山华特气体有限公司。微粉硅胶(silica gel)由加拿大的Silicycle公司提供,为球形颗粒,具体参数如表1中silica gel 1所示。实验用水为自制的去离子水,电阻为18 mΩ·cm。

表1 微粉硅胶参数Table 1 Parameters of the silica gel
1.2 实验装置
实验装置如图1所示。装置主要包括缓冲罐与反应釜两部分,缓冲罐的体积为1 165 mL,反应釜的体积为505 mL。缓冲罐与反应釜用316不锈钢制成,最大的承压能力为20 MPa。缓冲罐与反应釜被放置在恒温的水槽中,恒温水槽的温度控制范围是-20~100℃,控制温度的精度为 ±0.1℃。反应釜内设置两个PT100热电偶,温度的测量精度为 ±0.1℃,一个用于测量气体的温度,一个用于测量微粉硅胶内部的温度,反应釜内的压力传感器型号为CYB-20S,测量的精度为 ±0.02 MPa。缓冲罐内设置了一个温度传感器和一个压力传感器,温度传感器与压力传感器的型号与测量精度跟反应釜中的相同。反应釜与缓冲罐之间用两个阀门和一段距离为30 mm的管线连接,管线的内部直径为3 mm,相比于缓冲罐与反应釜的体积,连接管线的体积可以忽略不计。所有的传感器都连接到了安捷伦采集仪上采集数据,采集数据的时间间隔为10 s。气相色谱的型号为FULI 9790。
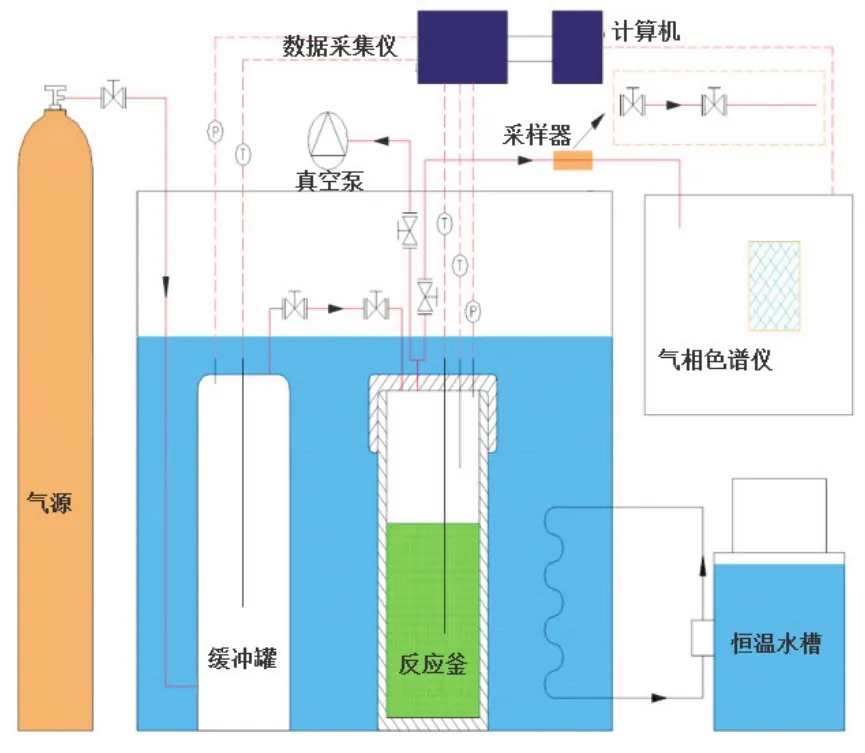
图1 在微粉硅胶中生成水合物装置原理图Fig.1 Schematic diagram of apparatus for hydrate formation in silica gel bed
1.3 实验过程
配制含水率为100% 的饱和微粉硅胶。先将微粉硅胶在真空干燥箱中干燥24 h,去除微粉硅胶中含有的1%~2%水。然后将等体积的微粉硅胶孔和去离子水混合,在离心机中以3 000 r/min的转速离心3 min,在宏观上微粉硅胶颗粒之间无自由水,颗粒之间可以相对滑动。然后取一定质量的饱和微粉硅胶放入热重分析仪,温度从常温升高到200℃,微粉硅胶中的水蒸发导致微粉硅胶质量减少。重复上述步骤,发现相同质量的饱和微粉硅胶中的水的减少量相同,说明水已经均匀地扩散到微粉硅胶的孔隙中。
将饱和微粉硅胶放入反应釜前,先用去离子水洗涤反应釜三次,并用N2吹扫干净。然后将饱和的微粉硅胶装入反应釜,封闭反应釜,将反应釜抽真空。然后重复向反应釜中注入低于1 MPa的实验气体三次,并抽真空。向缓冲罐中注入充足的实验气体,控制水浴温度,将反应釜与缓冲罐的温度降低至实验设定温度。待反应釜与缓冲罐中的温度与压力稳定后,先记录缓冲罐中的温度与压力,然后打开缓冲罐与反应釜之间的阀门,向反应釜中充入一定压力的实验气体,关闭反应釜与缓冲罐之间的阀门,水合物开始生成。等缓冲罐中的温度与压力再次稳定时,第二次记录缓冲罐的温度与压力。在水合物的生成过程中,取6次气体进行组分含量测定。
在水合物生成完成后,迅速放出反应釜中气体,并将反应釜抽真空。将反应釜升温至30℃,水合物全部分解,利用气袋收集反应釜中所有的分解气,最后利用气相色谱分析仪分析分解气的气体组分。
1.4 计算
实验采用计算注气前后缓冲罐内气体的减少量作为反应釜内初始进气量n0。如式(1)~ 式(3)所示。
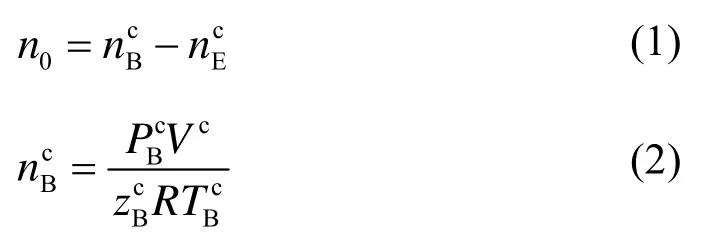

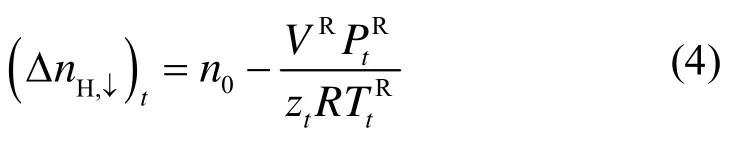
在任意时刻,反应釜中生成水合物的相对气体消耗量NGt为反应釜内消耗气体的摩尔量与反应釜中水的摩尔量之比,如公式(5)所示。

式中:nH2O是反应釜中水的摩尔量。
水转化成水合物的转化率为消耗的气体摩尔量乘以水合数6.62与加入到反应釜中水的摩尔量之比,如公式(6)所示。
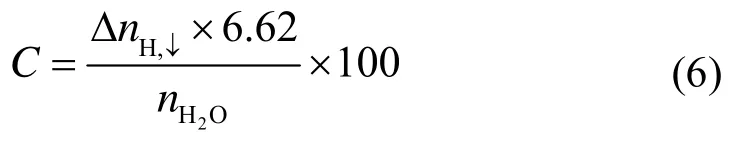
式中:C为水的转化率,mol%;ΔnH,↓是水合物生成结束后反应釜内的气体消耗量。
在水合物生成前30 min的相对气体消耗速率NR30可由前30 min的气体消耗量、时间及反应釜中水体积计算获得,如公式(7)所示。
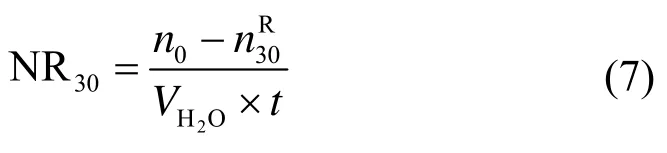
CO2在水合物中分流分率,如公式(8)所示。
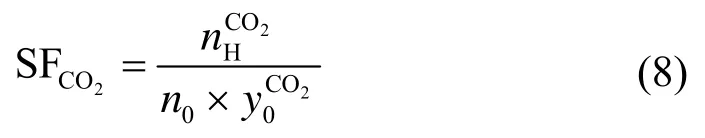
生成N2与CO2混合气水合物的分离系数SF,如公式(9)所示。
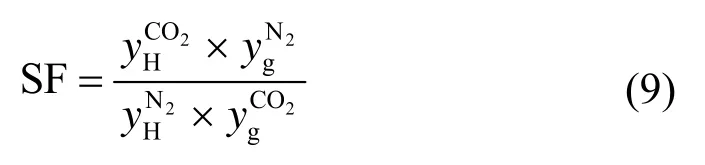
2 结果与讨论
2.1 温度与压力对N2与CO2混合气水合物气体消耗量的影响
在100%含水率的50 nm微粉硅胶中生成N2与CO2混合气体水合物的实验中,加入反应釜的微粉硅胶中含有水的质量为 (54.4 ± 0.1)g,实验初始压力分别为8.0 MPa、7.0 MPa和6.0 MPa,温度分别为 -5℃、-10℃、-15℃和-20℃,进行N2与CO2混合气水合物生成实验。为保证水合物的充分生成,实验持续大约24 h。
在温度为 -20℃,初始压力分别为8.0 MPa和7.0 MPa的条件下,N2与CO2混合气水合物生成过程中,反应釜内的温度与压力变化情况如图2所示。从图中可以看出,无法区分出N2与CO2混合气水合物的成核阶段与水合物的成长阶段,说明在向反应釜内注入气体结束后,N2与CO2混合气水合物迅速成核与成长,水合物生成的诱导时间在1 min以内。反应釜内气相与微粉硅胶相的初始设定温度都为-20℃,在图2中,气相与微粉硅胶相的初始温度都大于 -20℃。说明向反应釜内注入气体的过程中,反应釜中的气相与微粉硅胶相的温度具有不同程度的提升。在注气结束后,气相温度迅速恢复到设定温度 -20℃。微粉硅胶中的温度则缓慢下降,大约在100 min,恢复到设定温度 -20℃,这是由于微粉硅胶的导热率较低和水合物生成放热导致的[21]。
不同温度和压力下,反应釜中的N2与CO2混合气消耗量随时间的变化情况如图3所示。可以看出,在初始压力分别为6.0 MPa和7.0 MPa时,温度越低,反应釜内的气体消耗量越大。当初始压力为8.0 MPa,温度为 -10℃、-15℃和 -20℃时的气体消耗量基本相同,明显大于 -5℃时的气体消耗量。在各个实验条件下,气体消耗量随时间变化的斜率逐渐减小,说明反应釜内的气体消耗速率在逐渐降低。
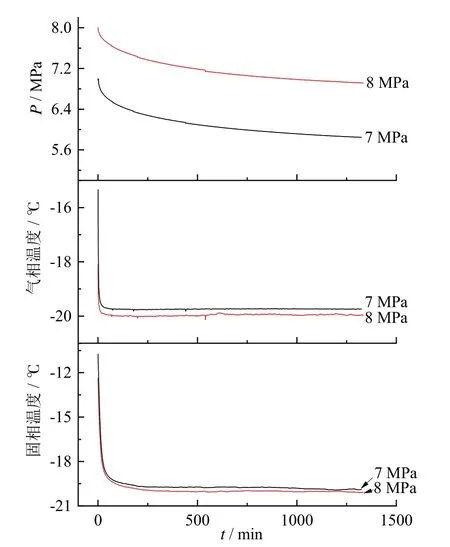
图2 N2与CO2混合气体水合物生成过程中反应釜中温度与压力的变化Fig.2 Evolution of P and T during the N2/CO2 mixed gas hydrate formation process in the reactor
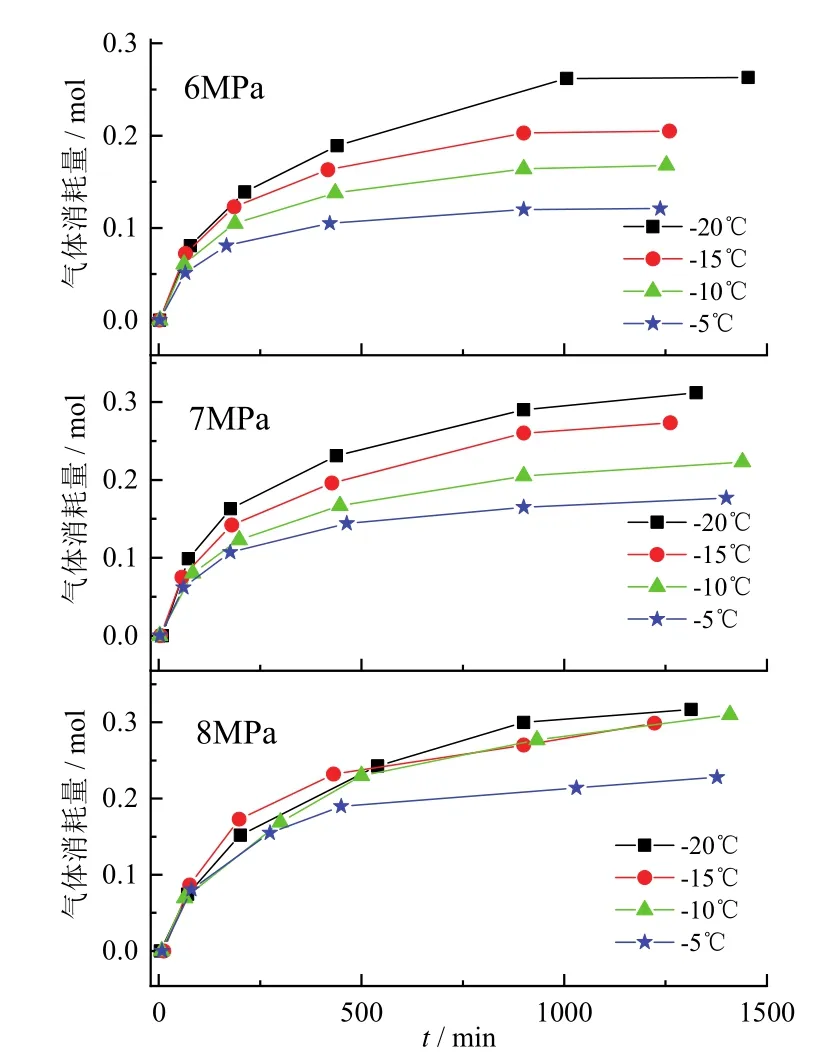
图3 不同初始压力、温度下反应釜内混合气气体消耗变化图Fig.3 Evolution of mixed gas uptake at different initial pressures and temperatures in the reactor
反应釜内最终的气体消耗量与温度、压力之间的关系如图4所示。从图中可以看出,在相同的温度下,压力越大,N2与CO2混合气水合物生成驱动力越高,气体消耗量越大。在相同的初始压力下,压力为6.0 MPa或7.0 MPa时,温度越低,N2与CO2混合气水合物气体消耗量越大。压力为8.0 MPa时,温度从 -5℃降到 -10℃,气体消耗量明显增加,继续降温到 -20℃,N2与CO2混合气水合物的气体消耗量略微下降。
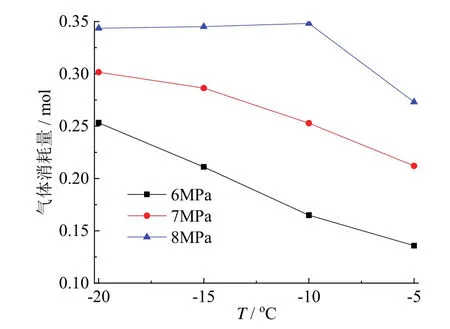
图4 反应釜中气体消耗量与温度、压力关系图Fig.4 Effect of temperature and pressure on gas uptake in the reactor
水的转化率与相对气体消耗量NGt与温度、压力的关系如图5。可以看出,N2与CO2混合气水合物相对气体消耗量NGt的最大值为0.115 (mol/mol),低于临界的水合物相对气体消耗量。梁德青等[19]研究了微粉硅胶生成生物沼气水合物的过程,用到的微粉硅胶的参数如表1中的silica gel 2所示,用到的生物沼气组分为CO2/CH4(40mol%/60mol%),压力为2.6~5.2 MPa,温度为 -10~-2℃,生成水合物的水合数为6.62。本文中用到的水合数与梁德青等[19]在微粉硅胶生成生物沼气水合物的水合数相同,生成N2与CO2混合气水合物水的转化率最大约为78mol%,最低约为30mol%。水的转化率与相对气体消耗量随温度和压力变化的规律与气体消耗量相同。
N2与CO2混合气水合物生成前30 min中的相对气体消耗速率NR30与完成90%的气体消耗量所需的时间T90随温度、压力变化的关系如图6所示。从图中可以看出,初始压力为7 MPa与8 MPa时,T90相差不大,均明显大于初始压力为6.0 MPa下所需的T90。从整体来看,N2与CO2混合气水合物生成前30 min中的相对气体消耗速率NR30与初始压力没有明显的关系,NR30随着温度的升高而逐渐降低。NR30的最大值约为22 mol/(min·m3),低于梁德青等[19]在研究生成生物沼气水合物的NR30的最大值156.83 mol/(min·m3)。
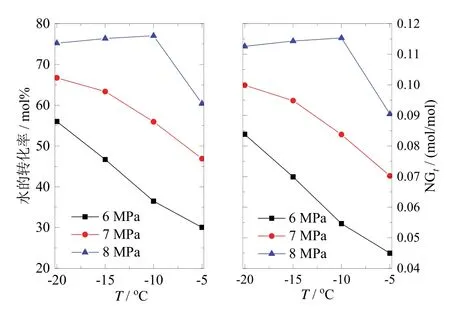
图5 反应釜中水的转化率与相对气体消耗量NGt 随温度、压力变化的关系Fig.5 Effect of temperature and pressure on water conversion and normalized gas uptake NGt
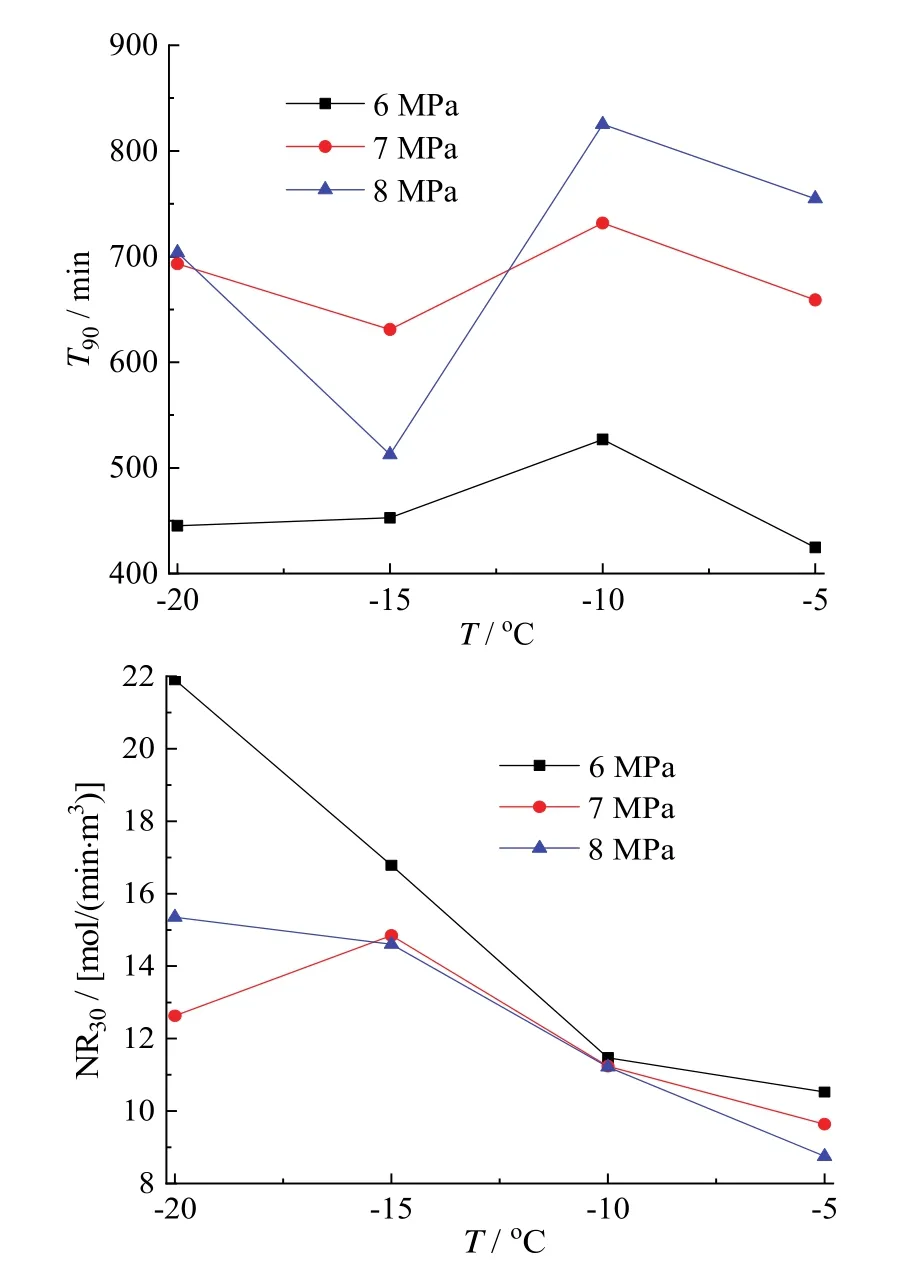
图6 相对气体消耗速率NR30与T90随压力、温度变化的关系Fig.6 Effect of temperature and pressure on T90 and normalized rate of gas uptake NR30
表2归纳了相对气体消耗量NGt、相对气体消耗速率NR30、水的转化率以及T90与温度、压力之间的关系。可以看出,生成N2与CO2混合气水合物的水的转化率范围为30.03%~77.02%,NGt范围为0.044~0.115 (mol/mol),分别低于文献[19]中生物沼气水合物的水的转化率与相对气体消耗量[19]。NR30范围为8.74~21.90 mol/(min·m3),低于生物沼气水合物的相对气体效率速率。生成90%的N2与CO2混合气水合物所需的时间为424.7~825.1 min,长于生成90%的生物沼气水合物所需时间[19]。可见,在微粉硅胶中生成N2与CO2混合气水合物的储气效果低于生物沼气水合物。
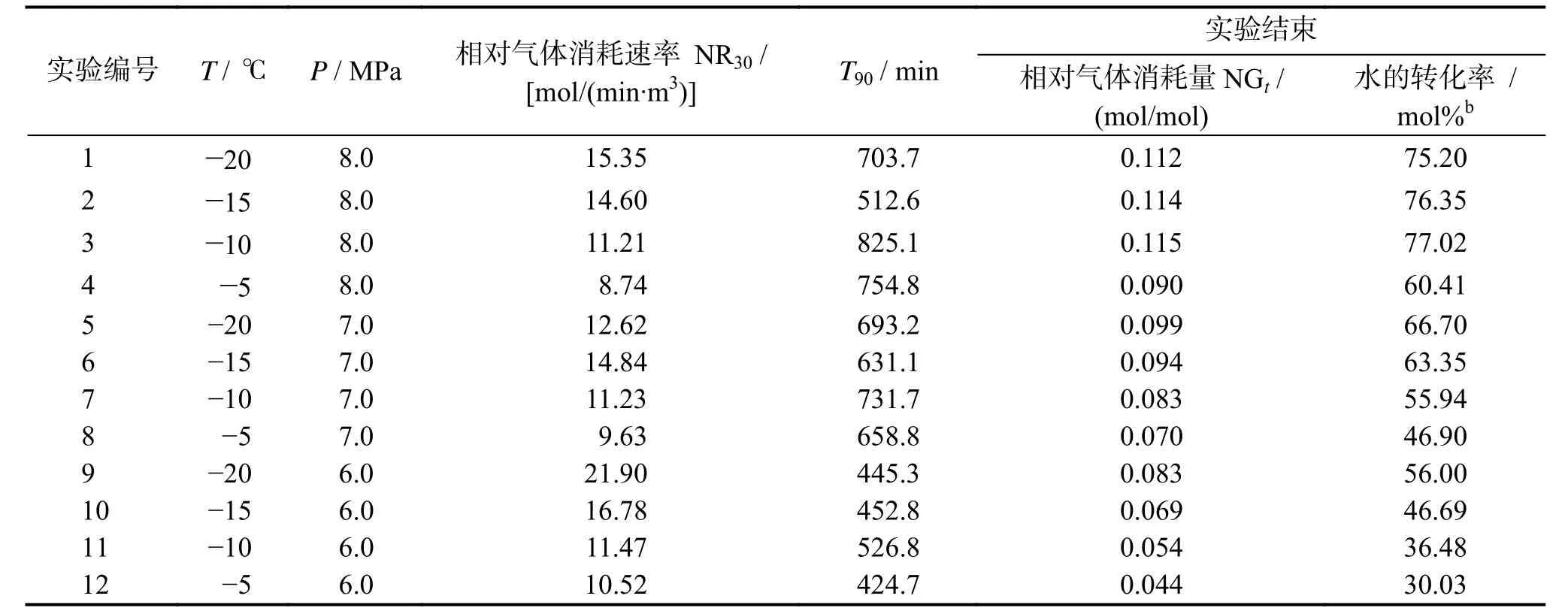
表2 不同压力和温度下50 nm微粉硅胶中生成N2与CO2混合气水合物的储气效果aTable 2 Gas storage efficiency of N2/CO2 mixed gas hydrate at different pressures and temperatures in the 50 nm silica gel
2.2 温度与压力对N2与CO2混合气水合物的气体分离效果的影响
初始压力为8.0 MPa时,不同温度下反应釜中的N2与CO2气体组分随时间的变化关系如图7所示。从图中可以看出,在反应釜中,N2的组分随着水合物的生成不断增加,CO2的组分随着水合物的生成不断降低,说明生成水合物优先吸收CO2气体。在开始生成水合物时,由于水合物生成速率较快,反应釜中气相组分变化速率也相对较快,反应釜中气体组分的变化速率随着时间的推移而逐渐减慢,这也是由于水合物生成速率减慢的缘故。从图4中可以发现,在8.0 MPa,-20℃、-15℃和 -10℃温度下的气体消耗量明显大于温度为 -5℃的气体消耗量。在图7中,-20℃、-15℃和 -10℃下的两种气体组分变化明显大于温度为 -5℃的气体组分变化。说明生成水合物的气体消耗量对反应釜中剩余气体组分变化具有重要的影响。在图7中,反应釜内CO2组分不断减少,N2组分不断增加,导致相同温度下CO2-N2混合气气体水合物的相平衡压力不断增大,不利于水合物的生成。
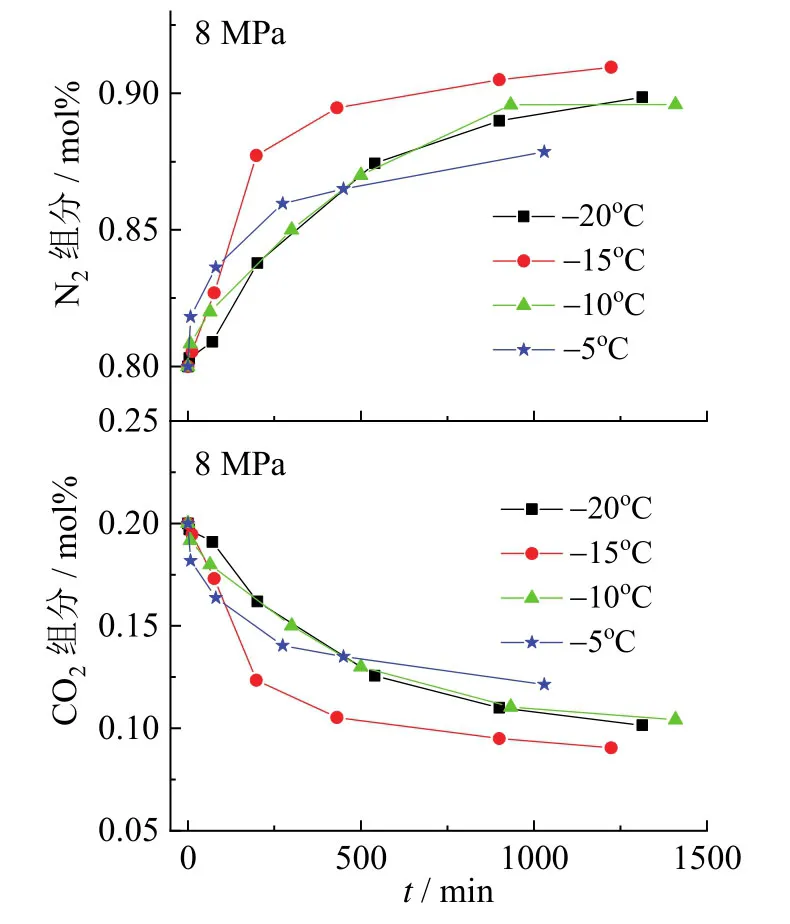
图7 水合物生成过程中反应釜内气体组分变化情况Fig.7 Evolution of gas compositions of N2 and CO2 in gas phase during hydrate formation in the reactor
在N2与CO2混合气水合物生成完成之后,反应釜中剩余N2的组分与温度、压力之间的关系如图8所示。从图中可以看出,反应釜中剩余N2组分的变化范围为85.6mol%~90.9mol%。在温度高于 -15℃时,相同压力下,反应釜中剩余N2组分随着温度的降低而增加,主要原因是降低温度增大了气体消耗量,水合物中消耗了更多CO2气体,反应釜则剩余更多的N2。当温度高于 -15℃时,相同温度下,压力越高,反应釜中剩余N2组分越多。压力增大导致了反应釜中初始气体含量增加,也可能导致水合物中CO2的组分减少,这都不利于增大反应釜中剩余N2的组分,然而压力增加会导致生成水合物的量增加,这有利于增加反应釜中剩余N2的组分,说明生成水合物的气体消耗量对反应釜中气体的组分变化起到主要作用。而在 -20℃,三个压力下反应釜中剩余N2组分比较接近,这是压力导致的三个变化因素共同造成的结果。
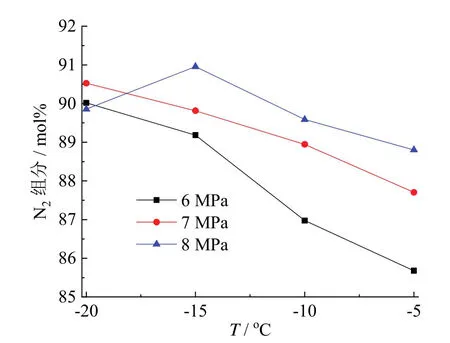
图8 水合物生成完成后反应釜中剩余N2组分与温度、压力之间的关系Fig.8 Effect of temperature and pressure on N2 proportion in equilibrium gas after hydrate formation finished in the reactor
生成的水合物中CO2组分与压力、温度之间的关系如图9所示。可以看出,在8.0 MPa压力下,温度对水合物中的CO2组分影响较小,CO2组分从20.0mol% 提高到了55.8mol%~58.0mol%。在压力为6.0 MPa的情况下,温度越高,水合物中CO2组分的含量越大,CO2组分从20.0 mol%提高到了57.3mol%~65.7mol%。而在压力为7.0 MPa时,这种规律并不完全成立,-10℃时水合物中CO2组分的含量小于 -15℃下的含量。在温度为 -15℃和 -5℃时,相同温度下,压力降低有助于提高水合物中CO2组分的含量,而在 -20℃与 -10℃时,这种规律并不完全适用。
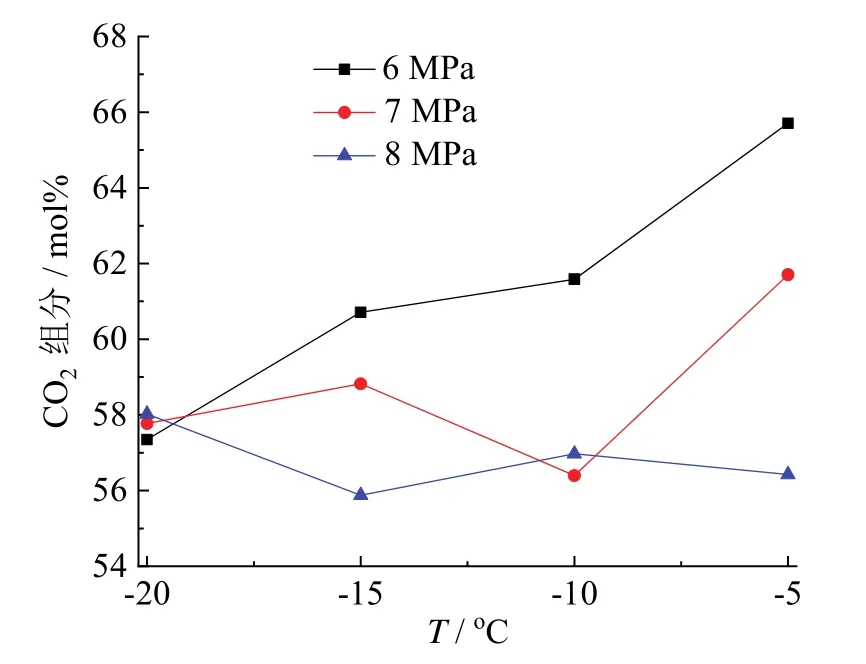
图9 水合物生成完成后水合物中CO2组分与温度、压力的关系Fig.9 Effect of temperature and pressure on CO2 proportion in the hydrate after hydrate formation finished
表3归纳了剩余气体中N2组分、水合物中CO2组分、分离系数SF以及CO2气体储存在水合物中的分流分率SFCO2与温度、压力之间的关系。从表中可以看出,剩余气体中N2的组分主要集中在89mol%~91mol%。生成N2与CO2混合气水合物中CO2的组分主要集中在56mol%~60mol%,只有实验序号8、10、11和12中的CO2组分大于60mol%,这几组实验的温度较高或者压力较低,生成水合物的驱动力较低,导致了水合物中CO2组分的上升。实验12中压力最小、温度最高,生成水合物驱动力最小,生成的水合物相对气体消耗量最小,生成的水合物中的CO2组分却最大为65.70mol%,最终导致了水合物中CO2分流分率最小为36.22%。说明虽然实验12得到的水合物中CO2组分含量最高,但CO2的封存率也最小。水合物中CO2的分流分率主要的分布范围为47mol%~57 mol%,说明利用水合物一步法分离N2与CO2混合气时,大约有50mol%的CO2无法分离出来。本文中CO2组分从20mol%提高到了60mol%左右,在文献[19]进行生物沼气水合物的大部分实验中,CO2组分从40mol%提高到了60mol%左右。本文中的分离系数范围为10.26 ~13.07,在梁德青等[19]进行生物沼气水合物的大部分实验中,分离系数范围是2.74~5.64。因此,在微粉硅胶中,生成N2与CO2混合气水合物的分离效果整体优于生物沼气水合物。
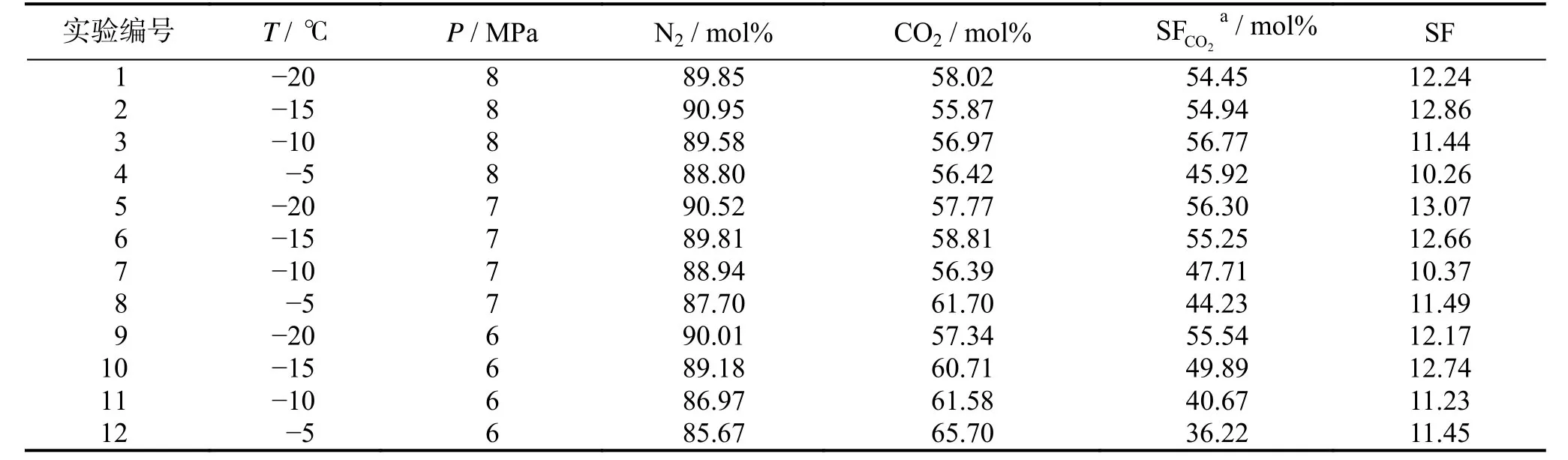
表3 不同压力、温度下50 nm微粉硅胶中生成N2与CO2混合气水合物的分离效果Table 3 Separation efficiency of N2/CO2 mixed gas hydrate at different pressures and temperatures in the 50 nm silica gel
3 结 论
在N2与CO2混合气生成水合物实验中,向反应釜注入N2与CO2混合气后,反应釜内直接生成N2与CO2混合气水合物,水合物诱导时间小于1 min。由于水合物生成是放热反应,微粉硅胶中的温度大约需要100 min恢复到实验设定温度。水合物的生成速率随着时间的推移逐渐降低,温度越低,压力越高,气体消耗量越大。
在 -10℃和8.0 MPa的条件下,生成水合物的相对气体消耗量最大为0.115 mol/mol,水的转化率最大为77.02mol%。前30 min的相对气体消耗速率与压力无关,最大值为21.90 mol/(min·m3),生成90mol% 的N2与CO2混合气水合物需要的时间范围为424.7~825.1 min。
气体消耗量越大,反应釜中剩余N2组分含量越大,最大值为90.95mol%。水合物生成驱动力越小,水合物中CO2组分含量越大,最大值为65.70mol%。分离系数范围为10.26~13.07。
