EDTA络合滴定法测定黄铜中高含量锌
2019-09-03李冬梅程晓寅张学彬
李冬梅,程晓寅,张学彬
(1宁波市食品检验检测研究院,浙江 宁波315048;2宁波市产品质量检验研究院,浙江 宁波315048)
1 前言
黄铜是制造机械零件的良好材料,常用于制造阀门、散热器和空调内外机连接管等。黄铜主要成分为铜、锌,锌含量高达5%~35%,同时含有少量的铅、锡、铁、铝和其它杂质等元素。GB/T 5231—2012对高含量锌的要求以“余量”显示,而对杂质含量有具体要求。在日常检验分析中,黄铜中各杂质元素含量通过GB/T 5121.1~26—2008分别测定,操作步骤复杂烦琐,试剂消耗多,测试速度慢,检测流程长,不能满足大批量检测及快速检测的要求;而且有时杂质成分无法确认测定,杂质含量只能采用100%减去铜、锌及已规定元素含量的方法求得。然而目前黄铜合金中高含量锌的测定方法有:GB/T 5121.11—2008[1]标准规定的4-甲基-戊酮-2萃取分离-Na2EDTA[A1]滴定法,其锌的测定范围为0.000 05%~6.00%;GB/T 5 121.27—2008[2]标准规定锌的测定范围为0.000 05%~7.00%,均不能满足黄铜中高含量锌(5%~35%)的测定。
EDTA络合滴定法因使用仪器简单、试剂用量少、操作简单、准确性好,广泛应用于工矿企业的生产和质量控制等,在铝锌合金[3]以及精锌矿物[4]等物料分析中的应用已有报道。李山[5]等人采用2-(5氯-2-吡啶偶氮)-5-二乙基氨基酚作指示剂络合滴定连续测定铜和锌,刘和连[6]等人采用硫酸钠掩蔽,1-2(吡啶偶氮)-2-萘酚(PAN)作指示剂,EDTA滴定法测定黄铜中铜和锌,杨桂珍[7]等人通过离子交换分离,用EDTA定法测定了黄铜中锌含量。采用硫酸钾和氯化钡沉淀分离Pb后,再以氟化钾和硫脲作掩蔽剂,以二甲酚橙做指示剂,利用ETDA标准溶液滴定黄铜中高含量锌。实验中对酸溶条件、指示剂和酸度、干扰离子的掩蔽、六次甲基四胺的用量及方法的可靠性进行了研究,结果表明该方法能满足实际样品中高含量锌的分析要求。
2 实验部分
2.1 试剂
盐酸;盐酸(1+1);过氧化氢(30v/v%);氯化钡溶液10 g/L;硫酸钾溶液50 g/L;氟化钾溶液100 g/L;硫脲溶液100 g/L。六次甲基四胺缓冲溶液(pH=5.5),称取150 g六次甲基四胺于烧杯中,加入100 mL水、30 mL盐酸,溶解后移入500 mL容量瓶中,定容,摇匀。二甲酚橙指示剂5.0 g/L;EDTA标准溶液0.02 mol/L,称取8 g乙二胺四乙酸二钠于1 000 mL烧杯中,加水微热搅拌溶解,冷却至室温,移入试剂瓶中,用水稀释至约1 L,摇匀,放置3 d后标定。金属锌≥99.99%,使用前用0.1 mol/L盐酸溶液清洗1 min,再用水和丙酮冲洗,并在50℃烘箱中烘干。
国 家 标 准 物 质 :GBW(E)020015、684A、ZBY9041a和ZBY9221黄铜标准物质除另行说明,实验室用试剂均为分析纯水,水均为符合GB/T 6682—2008规定的三级以上的蒸馏水。
2.2 EDTA标准滴定溶液的标定
称取0.2 g金属锌置于150 mL烧杯中,用少量水湿润,盖上表面皿,用滴管从烧杯口加入1:1盐酸5 mL,低温溶解,取下冷却,用少量水吹洗表面皿和杯壁,小心地将溶液转移至250 mL容量瓶中,用纯水稀释至标线,摇匀。移取25 mL锌标准溶液于150 mL锥形瓶中,加水50 mL,3~4滴二甲酚橙指示剂,10 mL六亚甲基四胺溶液,用EDTA标准溶液滴定,溶液由红紫色变为纯黄色即为终点。同时做空白实验。根据公式(1)计算EDTA标准溶液对锌的滴定度:

式中:f为单位体积EDTA标准滴定溶液相对于锌的滴定度,g/mL;mZn为称取金属锌质量,g;V1为标定时消耗EDTA标准滴定溶液的体积,mL;V0为标定时滴定空白实验溶液所消耗Na2EDTA标准滴定溶液的体积,mL。
2.3 实验方法
称取0.05~0.15 g(精确至0.000 1 g)的试样于300 mL三角瓶中,盖上表面皿;加入5 mL盐酸(1+1),盖上表面皿,逐滴加入1 mL过氧化氢(30%),放置。待试样完全溶解后,在通风橱内加热至大量小气泡冒出,从加热器上移去三角瓶,反应平稳后继续加热除去剩余的过氧化氢,溶液中小而密的气泡(O2)变少至无,继续出现大而少的气泡(水蒸汽),再加热浓缩至2~3 mL左右(切勿蒸干),取下冷却。加入3 mL氯化钡溶液及硫酸钾溶液20 mL,摇匀。加氟化钾溶液20 mL,摇匀。加硫脲溶液10 mL,摇匀。加pH 5.5六次甲基四胺缓冲溶液10 mL,滴加二甲酚橙指示剂3~4滴,用EDTA标准溶液滴定,溶液由红紫色变为纯黄色为终点,15 s不褪色。随同试样做空白实验,滴定消耗EDTA标准溶液的体积小于0.02 mL,含量可忽略不计。二甲酚橙指示剂的配置时间不宜过长,防止影响终点的判定。
2.4 结果计算
按式(2)计算试样中锌含量:

式中:V2为滴定锌时所消耗EDTA标准溶液的体积,mL;V0为滴定空白实验中锌所消耗EDTA标准溶液的体积,mL;f为EDTA标准溶液的浓度,mol/L;mCu为试样的重量,g;65.38为锌的摩尔质量,g/mol。
3 结果与讨论
3.1 溶样条件的选择
称取0.1 g黄铜标准样品(ZBY9041a),对溶样条件进行了选择和优化。实验选择盐酸进行溶样,并对不同浓度盐酸的溶样效果进行比较。实验发现,与盐酸相比,盐酸(1+1)对样品的分解速度较快。采用盐酸(1+1)分解样品的过程中,滴加少量过氧化氢,可缩短大量溶样时间。盐酸(1+1)的用量实验表明:当其用量为4~7 mL时,样品溶解完全,锌的测定值与认定值一致,因此,实验优先选用5 mL盐酸(1+1)并滴加1 mL过氧化氢溶样。
3.2 指示剂用量
二甲酚橙指示剂的用量直接影响滴定终点的判断。随着滴定剂的逐滴加入,溶液的颜色逐渐从红紫色逐步到橙,红的成分继续减少,直至终点的黄色。二甲酚橙指示剂过量,溶液仍是黄色,终点易过。因此,以实验方法的加入量为最佳,当溶液从红紫色变至橙色时,说明已快到终点,要1滴多摇,使硫酸铅钡沉淀溶解吸附的Zn2+,此时会出现返色(又变红),直到加1滴或半滴,摇动后出现不带红的黄色(或略带米色,溶液中有白色沉淀),并能保持30 s即为终点。实验表明,3~4滴二甲酚橙均可得到明显终点,锌的测定值与认定值一致。实验选用加入4滴二甲酚橙指示剂。
3.3 酸度选择
采用EDTA标准溶液滴定锌时,要求pH>4。而二甲酚橙指示剂在pH>6.3时为红色,在pH<6.3时其为黄色,pH=6.3时呈中间颜色,二甲酚橙与金属离子锌形成的络合物是红色,故滴定锌时溶液酸度应选择在4<pH<6.1条件下,发生以下反应:MIn+H2Y2-→MY+H2In4-。
测定Zn2+的适宜酸度为pH=5.5终点时,溶液从红紫色变为纯黄色。同时在pH5.5条件下对ZBY9041a黄铜标准样品进行滴定,锌的测定值与认定值一致。实验选用PH=5.5的酸度条件。
3.4 干扰离子的掩蔽
黄铜合金中干扰锌含量测定的离子主要Cu2+、Pb2+、Sn4+、Fe3+、Al3+等。在实验条件下对Cu2+、Pb2+、Sn4+、Fe3+、Al3+等离子进行了掩蔽。
3.4.1 Pb2+的掩蔽
在微酸性溶液中,加入适量的氯化钡和硫酸钾溶液,使生成硫酸钡沉淀,溶液中共存的铅也一起以PbSO4沉淀析出;当Ba2+的量超过Pb2+量10倍以上时,Pb2+即会全部渗入硫酸钡晶格中去,形成相当稳定的硫酸铅钡混晶沉淀,这种沉淀比单纯的硫酸铅沉淀稳定得多。实验选用氯化钡和硫酸钾溶液作为Pb2+的掩蔽剂。实验表明,加入3 mL氯化钡溶液和20 ml硫酸钾溶液,可完全掩蔽Pb2+。本实验中加入3 mL氯化钡溶液和20 mL硫酸钾溶液。
3.4.2 Cu2+的掩蔽
黄铜中含铜量占60%左右。熟知硫脲是铜的良好掩蔽剂,在一定酸度(pH=2~6)下,把Cu2+还原成 Cu+,8Cu2++CS(NH2)2+5H2O=8Cu++CO(NH2)2+SO42-+10H+。同时,硫脲与Cu+形成络合物(lgβ=15.4),从而掩蔽Cu2+,达到与锌的分离。
实验选用硫脲作为Cu2+的掩蔽剂,在pH=5.5条件下掩蔽Cu2+,而且其他离子在此条件下大都不与硫脲作用,从而提高了测定结果的准确度。已知Cu(Ⅰ)-硫脲络合物的稳定常数为良lgβ=15.4,Zn(Ⅱ)-EDTA络合物的稳定常数为lgβ=16.5,在pH=5.5时,该络合物的酸效应系数lgαY(H)=5.51,因此,条件稳定常数可根据公式 lgK'=lgβ-lgαY(H)算出;Cu(Ⅰ)-硫脲的条件稳定常数lgK'=9.89;Zn(Ⅱ)-EDTA的条件稳定常数lgK'=10.99;上述的条件稳定常数远大于8,故Cu能被硫脲全部掩蔽,锌能被EDTA准确滴定。实验表明,在pH=5.5条件下,加入10 mL硫脲溶液,在1 min中可完全掩蔽Cu2+。
3.4.3 Sn4+、Fe3+、Al3+的掩蔽
F-与Sn4+、Fe3+、Al3+等生成稳定的络合物(SnF62-、FeF63-、AlF63-)。实验选用氟化钾作为Sn4+、Fe3+、Al3+等离子的掩蔽剂。实验表明,当加入的氟化钾溶液到18 mL时,锌的测定结果趋于稳定,掩蔽Sn4+、Fe3+、Al3+的目的已经达到。为完全除去Sn4+、Fe3+、Al3+的干扰,本实验中加入20 mL氟化钾溶液。
3.5 六次甲基四胺的用量
以二甲酚橙作指示剂,10~25 mL六次甲基四胺溶液均能控制体系的pH在5~6,均可得到满意结果。采用加入15 mL六次甲基四胺缓冲溶液。
3.6 精密度实验
为了考察方法的精密度,对锌含量不同的黄铜进行了10次测定,计算平均值和相对偏差(RSD),结果见表1。从表1可以看出锌的RSD为0.17%~0.22%,方法具有较好的精密度。
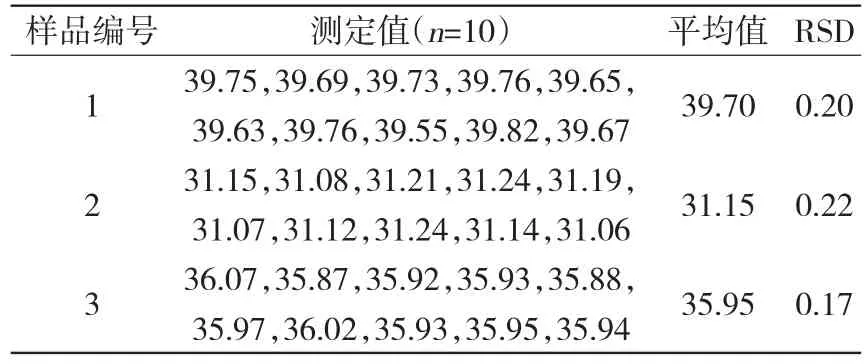
表1 精密度实验结果 %
4 样品分析
按照实验方法,对 GBE(E)020015、684A、ZBY9041a和ZBY9221四种黄铜标准物质中锌含量进行测定,并将测定值与标准物质的认定值进行对照,结果见表2。从表2的结果可以看出,锌测定结果均在认定值允许的误差范围内,结果准确。
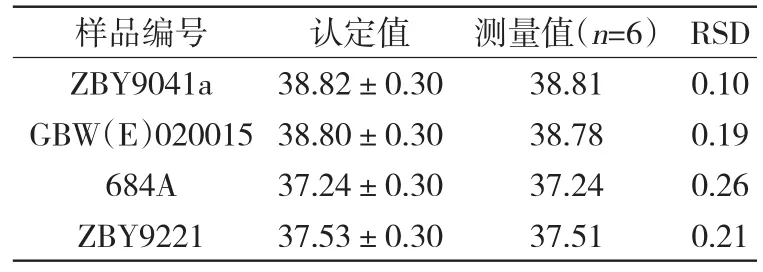
表2 黄铜标准物质中锌的测定结果 %
由于锰、镍、镉含量高时,滴定终点不明显,难以控制,所以本方法不适于镍、锰及镉含量高的铜合金样品。
5 结语
采用盐酸、过氧化氢溶样,用硫酸钾和氯化钡沉淀分离Pb,用氟化钾掩蔽Sn4+、Fe3+、Al3+,用硫脲掩蔽Cu2+,在pH=5.5六次甲基四胺溶液中,以二甲基橙为指示剂,用ETDA络合滴定测定其含锌量。方法能够满足实际样品中高含量的准确度和精密度要求,可用于实际样品的分析和质量控制。
