基于超高效液相色谱—飞行时间质谱联用的冠心病非靶向代谢组学分析及代谢标记物的探索
2019-09-02刘倩倩王春玥宋晨曦李一平伏蕊朱成刚窦克非
刘倩倩,王春玥,宋晨曦,李一平,伏蕊,朱成刚,窦克非
冠状动脉粥样硬化性心脏病(冠心病)是最常见的心血管疾病,但其确切的发病机制至今仍不明确[1-3]。在过去十年里,关于动物及人类代谢组学方面的研究均取得巨大进步,通过联合使用靶向及非靶向的方法,代谢组学已经识别出多种不同心血管疾病相关的代谢物指标[4-6]。目前针对冠心病的靶向代谢组学研究开展较多,但能够反映冠心病患者整体内环境的代谢标志物及发病机制为导向的非靶向代谢组学研究却开展得十分有限。因此,本研究借助超高效液相色谱—飞行时间质谱联用(ultra-high performance liquid chromatography coupled to quadruple time-of-flight mass spectrometry,UHPLC-QTOF/MS)的非靶向代谢组学方法分析了严重冠状动脉狭窄的冠心病患者和冠状动脉造影正常者之间的血浆代谢物差异。
1 资料与方法
研究对象:本研究入选了2011年6月至2015年3月于中国医学科学院阜外医院接受择期经皮冠状动脉介入治疗或冠状动脉造影的住院患者300例,并分为两组,即冠心病组(n=150),患者冠状动脉严重狭窄(狭窄≥80%);和年龄与性别 1:1 匹配的冠状动脉造影正常(狭窄≤20%)的对照组(n=150)。并利用UHPLC-QTOF/MS的非靶向代谢组学方法,分析两组患者血浆代谢图谱并挖掘两组间差异性最显著的代谢物(图1)。本研究经阜外医院伦理委员会批准,入组患者及其家属均签署了知情同意书。
样本采集和处理:造影前采集空腹静脉血置于肝素抗凝管中,4℃ 2 300 rpm离心10 min后取上清,12 000 rpm离心15 min后取400 μl分装至冻存管,-80℃条件下保存直至上机检测。
UHPLC-QTOF/MS检测:运用UHPLC-QTOF/MS的代谢组学检测方法,并利用阳离子相和阴离子相两种电离模式联合检测,对血清进行一级、二级离子检测。色谱条件:序列中每隔8个检测样本插入一个空白样本(75%乙腈溶液)和一个质量控制(QC)样本,进样量为4 μl。色谱柱为Waters ACQUITY UHPLC HSS T3(2.1×100 mm,1.7 μm);流动相A为0.1% 甲酸溶解于水(阳离子相)或0.5 mM氟化铵阴离子相)溶解于水;流动相B为0.1%甲酸溶解于乙腈溶液(阳离子相)或乙腈溶液(阴离子相)。质谱条件:质量扫描范围:50~1 200 mz;扫描速率:4质谱/s。鞘气温度:400℃;干燥气温度:250℃;鞘气流速:12 L/min;干燥气流速:16 L/min;喷雾电压:20 psi (阳离子模式)或40 psi(阴离子模式);喷嘴电压:0 V。
数据预处理与分析:首先使用ProteoWizard将质谱原始数据转换为mzXML格式,然后使用 XCMS(xcms4dda、xcms4 lipid)程序对数据进行处理,并检索自建库并获得矩阵数据表,矩阵数据表中包括质荷比(m/z)、保留时间(RT)、峰面积。使用CAMERA软件对XCMS处理过的数据进行峰筛选,其后利用LOESS回归模型对QC样本进行归一化处理,与 QC匹配度低于80%的数据被弃去。
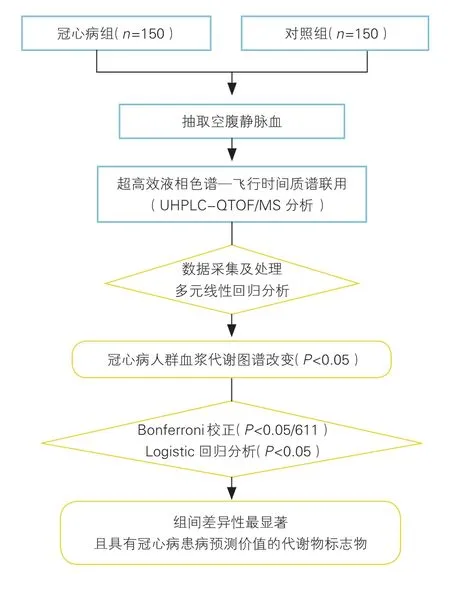
图1 临床研究技术路线
统计学分析方法:所有数据应用 SAS 9.4 软件进行分析。连续变量用均数±标准差表示,并用t检验进行比较。分类变量用频数及百分比表示并以卡方检验进行比较。利用多元线性回归模型,分析校正传统冠心病危险因素和检测批次等因素后冠心病组与对照组之间血浆显著性差异代谢物小分子。利用Bonferroni校正,将显著性差异的阈值设置为P<8.2×10-5(0.05/611)以减少假阳性错误概率。利用Logistic 回归模型分析代谢物与疾病发生风险的相关性。P<0.05为差异有统计学意义。
2 结果
两组患者临床基线资料的比较(表1):冠心病组和对照组患者的体重指数组间差异无统计学意义;相较对照组,冠心病组患者高血压、糖尿病、高脂血症、吸烟及冠心病家族史比例均明显更高(P均<0.05)。
冠心病患者血浆代谢组学变化(图2):本研究对冠心病组和对照组之间的差异代谢物进行了多元线性回归分析。

图2 105个冠心病人群血浆差异小分子代谢物成分分类图
在校正传统冠心病危险因素(年龄、性别、体重指数、吸烟)和检测批次后,共筛选出105个两组间差异显著的代谢物,其中包含84种已知代谢物和21种未知代谢物。组间显著性差异代谢物主要包含51 种甘油磷脂类、10 种肉毒碱、8 种游离脂肪酸、5 种胆汁酸代谢产物、3 种氨基酸类以及7 种未统一分类代谢物,其中脂质代谢异常(甘油磷脂类、肉毒碱、游离脂肪酸)占总代谢状态改变的65.74%,是总代谢状态改变的主要原因,这验证了既往研究所报道的脂质代谢异常在冠心病发病机制中的重要作用。
最具预测性的冠心病相关的血浆代谢物(表2):经过多元线性回归分析及Bonferroni校正后,从上述105种差异代谢物中筛选出5种差异最为显著的血浆代谢物(P均<0.05),即棕榈酸、亚油酸、脂酰肉毒碱(14:1)、石胆酸、磷脂酰甘油(20:3/2:0)。校正危险因素后,Logistic 回归模型分析结果显示,这5种代谢物与冠心病发病风险显著正相关(OR=2.791~7.237)。

表2 5种组间差异性最显著的代谢物及其与冠心病患病风险的关联
3 讨论
本研究借助UHPLC-QTOF/MS的非靶向代谢组学方法分析了冠心病患者和冠状动脉造影正常者之间血浆代谢物水平的差异。研究一共筛选出105个差异性代谢物,其中脂质代谢(磷脂、肉毒碱、游离脂肪酸)占总代谢状态改变的65.74%,并从中筛选出5种差异最为显著的血浆代谢物,其在冠心病组均显著高于对照组,且与冠心病发病风险显著正相关,OR值范围从石胆酸的 2.791到棕榈酸的7.237。
冠心病组患者血浆棕榈酸水平显著高于对照组,是冠心病相关性最高的代谢物之一,同时也是冠心病发病风险预测能力最高的代谢物(OR=7.237,95% CI:2.390~21.912,P=0.0001),这与既往多项研究结果一致[7-8]。近期一项临床试验Meta分析结果显示,棕榈酸(16:0)可以显著增加总胆固醇及低密度脂蛋白(LDL)水平[9]。另外一项体外实验也验证了棕榈酸可以通过触发炎症相关信号通路而引起内皮细胞功能紊乱,从而具有诱发动脉粥样硬化形成的潜力[10]。
本研究中,亚油酸血浆水平每升高1个单位,冠心病的患病风险就增加6.133倍(95% CI:2.367~15.893,P=0.0005)。最近研究发现,作为日常生活中最常见的ω-6多不饱和脂肪酸的亚油酸摄入增加后会提高5年内全因死亡风险、心血管疾病包括冠心病的发病风险[11],这与本研究结果也是一致的。至于亚油酸水平增加引起心血管发病的机制,有研究证实与氧化型油酸代谢物(oxidized linoleic acid metabolites,OXLAMs)的升高有关,而OXLAMs具有诱使巨噬细胞转化为泡沫细胞及内皮细胞功能紊乱的作用导致动脉粥样硬化形成[12-15]。
本研究也进一步验证了磷脂酰甘油(20:3/2:0)与冠心病的强相关性。目前较少研究关注过磷脂酰甘油这一亚类的甘油磷脂,本研究首先报道了人血浆中磷脂酰甘油(20:3/2:0)水平与冠心病患病风险正相关的结果(OR=3.938,95% CI:1.891~8.204,P=0.0001)。早前有研究发现在动脉粥样硬化大鼠模型的血浆中磷脂酰甘油类水平显著升高[16],这也间接验证了本文的研究结果。
几乎所有有关冠心病的代谢组学研究都报道过肉毒碱类代谢物在冠心病人群与对照人群中的差异,本研究中也发现了一种中链的脂酰肉毒碱(14:1)与冠心病患病风险显著相关(OR=3.379,95%CI:1.913~5.967,P<0.0001)。有研究发现血浆中肉毒碱水平的升高与巨噬细胞脂质代谢过程中β氧化功能不全有关,而巨噬细胞脂质超载向巨噬泡沫细胞转化在动脉粥样硬化的形成中起到至关重要的作用[17]。
目前关于石胆酸与血管病变的研究并不多,本研究首先发现血浆石胆酸水平的升高与冠心病患病风险呈正相关(OR=2.791,95% CI:1.74~4.477,P=0.0003)。Charach等[18]通过粪便代谢组学检测发现冠心病患者排泄胆汁酸的能力下降,因此不能摆脱体内过高的脂质负荷,这也可以解释本研究结果中冠心病患者血浆中石胆酸的堆积。多项研究发现瘀胆症的患者体内石胆酸的堆积能够引起肝组织炎症反应,相关体外实验显示石胆酸能够通过激活核因子-κB(NF-KB)和P38丝裂原活化蛋白激酶(p38 MAPK)相关炎症通路而诱导血管内皮细胞功能障碍[19],间接提示石胆酸可能具有致动脉粥样硬化的作用。
本研究局限性:本研究为单中心病例对照研究,虽然借助先进的代谢组学手段挖掘出许多代谢标志物与冠心病患病之间的关联,但尚不能为其因果性提供依据,因此还需要在前瞻性队列研究以及细胞及动物的相关干预实验中进行验证。
综上所述,本研究借助UHPLC-QTOF/MS的非靶向代谢组学方法分析了严重冠状动脉狭窄冠心病患者和冠状动脉造影正常者之间血浆代谢物水平的差异。本研究不仅提供了更全面的冠心病血浆代谢图谱改变,还首次挖掘出了石胆酸和磷脂酰甘油(20:3/2:0)这两种与冠心病病理生理过程有强关联的潜在生物标志物,为从整体水平探索冠心病动脉粥样硬化病理生理机制及寻求新的治疗途径供了依据。
利益冲突:所有作者均声明不存在利益冲突
