还原棕BR的间接电化学还原染色机理
2019-08-29樊增禄
于 翔,王 雅,李 庆,樊增禄
(西安工程大学 环境与化学工程学院,陕西 西安 710048)
0 引 言
还原染料是纤维素纤维染色的重要染料之一[1],但需用连二亚硫酸钠在高浓度烧碱溶液中将其还原成水溶性的还原染料隐色体钠盐,才能实现对纤维的上染[2-4]。因而导致染色废水中存在大量的Na2SO4、Na2SO3和Na2S2O3等含硫化合物,给生态环境和废水处理造成巨大压力[5-6]。作为全球第一纺织大国,我国每年因还原染料染色消耗的保险粉数以万吨,由此产生的水污染危害巨大,研发环境友好的还原染料染色新技术意义重大[7-8]。
自19世纪起,学者们就开始寻求新的还原染料还原方法,如电化学方法、催化氢化以及生物方法等,但目前这些方法都还处于实验室研究阶段,其中电化学还原方法,包括直接和间接电化学还原,备受关注[9-11]。直接电化学还原是染料直接从阴极获得电子被还原成可溶的染料隐色体,但是固体染料和电极接触不够充分,效率比较低,染料不能充分还原。间接电化学还原是在电化学还原体系中引入一种电子介体,它是一种可逆的氧化还原物质,能从阴极获得电子,然后把电子传递给染料而使之还原。给出电子的介体能重新在阴极获得电子,如此重复循环,使染料不断还原。所用电子介体是水溶性的,可以和染料充分接触,染料还原效率很高[12-14]。考虑到还原染料的还原电位在-1 000 mV~-650 mV之间,具有足够低还原电位的电子介体的选择十分重要。研究结果表明,Fe(II)的三乙醇胺(TEA)配合物在碱性溶液中的还原电位可达到-1 050 mV,因此Fe(II)/Fe(III)与TEA构成的氧化-还原型配合物体系适合于对还原染料进行间接电化学还原。Fe(II)与Fe(III)之间可以实现有效的电子传递,足够低的还原电位足以还原所有的还原染料,且不需添加其他还原剂[15-17]。目前,还原染料的电化学还原效能还无法与化学还原剂相媲美,染料还原仍不够充分,染色效果仍需改进。其中,TEA与FeSO4·7H2O的配位数以及还原染料电化学还原染色的机理等关键问题的研究更是鲜见报道。
本研究在三电极体系下,将还原棕BR的间接电化学还原染色体系与电化学工作站相连接,采用循环伏安法研究还原棕BR的电化学还原过程和最佳还原pH值,以及TEA与FeSO4·7H2O摩尔比对染色体系的电导率、还原电位及还原棕BR电化学还原染色效果的影响。
1 实 验
1.1 材料、试剂与仪器
1.1.1 材料 纯棉漂白机织物,27.8 tex/27.8 tex,236(根/10cm)×142(根/10cm)。
1.1.2 试剂 硫酸铁(Fe2(SO4)3,分析纯,天津市福晨化学试剂厂),硫酸亚铁(FeSO4·7H2O,分析纯,天津市河东区河岩试剂厂),氢氧化钠(NaOH,分析纯,天津市河东区河岩试剂厂),三乙醇胺(TEA,分析纯,天津市河东区河岩试剂厂),保险粉(Na2S2O4,分析纯,天津市河东区河岩试剂厂),土耳其红油(化学纯,上海试剂二厂),无水碳酸钠(Na2CO3,分析纯,郑州派尼化学试剂厂),还原棕BR(工业品,浙江亿得化工有限公司)。
1.1.3 仪器 CHI660C型电化学工作站(上海辰华仪器公司),KQ3200型超声波清洗器(昆山市超声仪器有限公司),78HW-1型数显恒温磁力搅拌器(常州国华电器有限公司),HB17300SC2A型恒流稳压电源(天津市无线电元件三厂),868型台面式pH/ISE测试仪(美国奥立龙公司),Color i7型分光测色仪(美国X-Rite公司),HH-S4型数显恒温水浴锅(北京科伟永兴仪器有限公司),Y571B型摩擦色牢度仪(宁波纺织仪器厂),SW-12A型耐洗色牢度试验机(无锡纺织仪器厂)。
1.2 实验装置
还原棕BR间接电化学还原染色装置如图1所示。还原棕BR对棉织物进行电化学无盐染色时所用石英玻璃电解槽可分为阳极区和阴极区,两极通过导线与恒压稳流电源相连接,其中阳极区的容积为25 mm×60 mm×70 mm,阴极区的容积为100 mm×60 mm×70 mm,2个区间用6 cm×6 cm的Nafion膜隔开。其中,阳极为网状铜镍合金电极(10 cm2);阴极为铜片(10 cm2~30 cm2);参比电极为218型饱和银/氯化银电极;指示电极为213型铂电极。
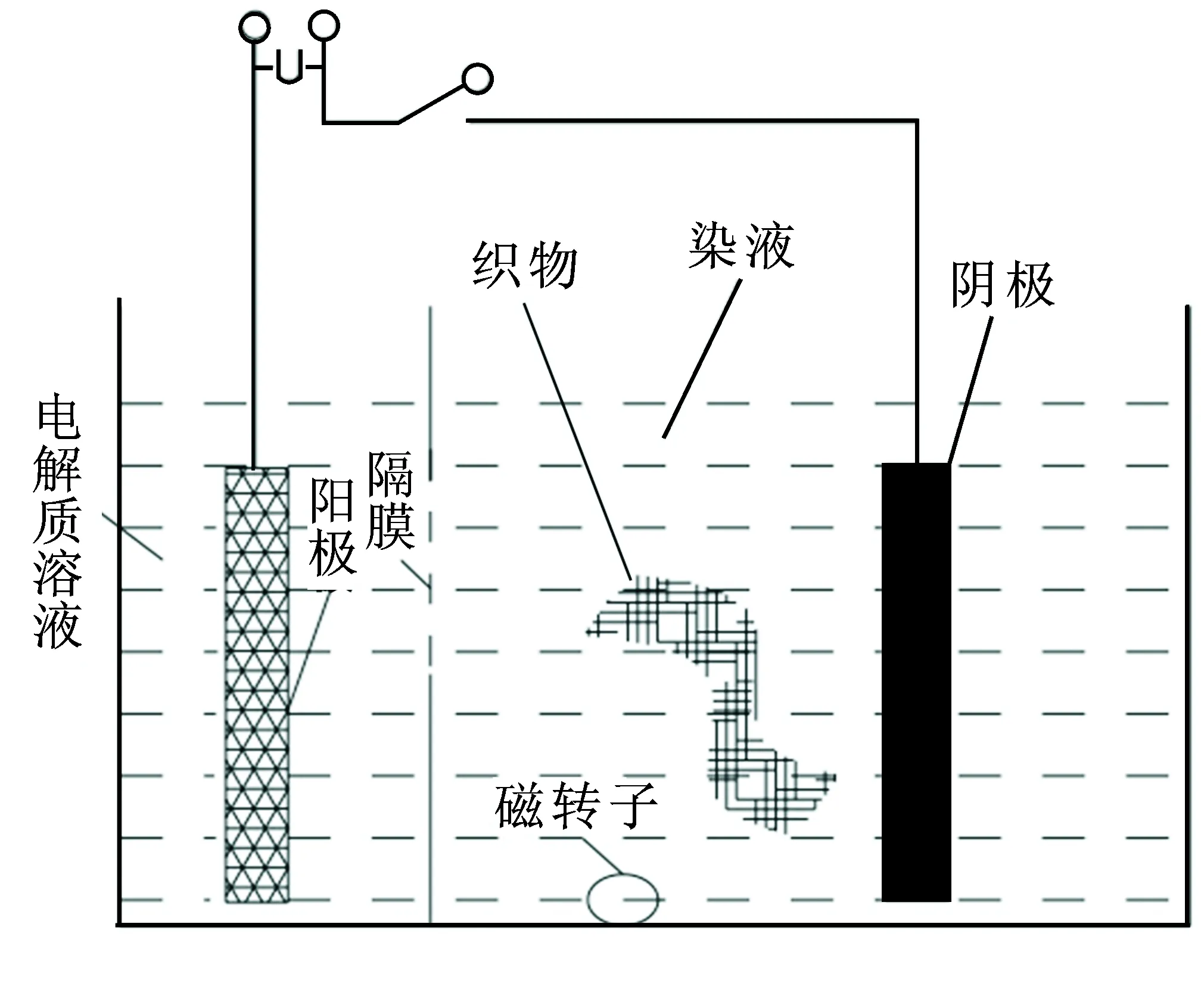
图 1 还原棕BR电化学无盐染色装置Fig.1 Electrochemical salt-free dyeingdevice for vat brown BR
1.3 染色工艺
1.3.1 还原棕BR间接电化学还原染色 间接电化学还原染色体系中,阳极区和阴极区的试剂和染料组成如下:
(1) 阳极区 35 g/L的H2SO4溶液。
(2) 阴极区 阴极区染色溶液体系如表1所示。
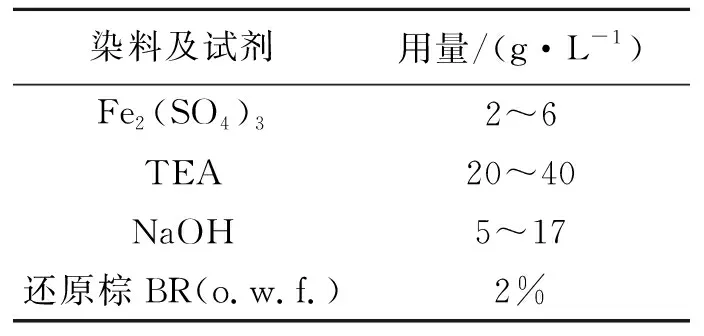
表 1 阴极区的染色体系组成
注:浴比为100∶1
还原棕BR对棉织物的间接电化学染色工艺流程如图2所示。染色工艺参数如下[11]:还原棕BR间接电化学还原染色的最佳外加电压为3 V,NaOH质量浓度为8 g/L,TEA为30 g/L,Fe2(SO4)3为5 g/L。阴极的电极面积为25 cm2,最佳染色时间为70 min,染色温度为40 ℃。

图 2 还原棕BR的间接电化学还原染色工艺流程Fig.2 Process of indirect electrochemical reduction dyeing for vat brown BR
1.3.2 还原棕BR的传统浸染染色 还原染料的还原(还原棕BR的用量为棉织物总质量的2%,Na2S2O4为10 g/L、NaOH为12 g/L)→加入纯棉织物,染色温度为60 ℃→氧化(空气中氧化)→水洗→皂煮→水洗→烘干。
1.4 性能测试
1.4.1 还原电位 选取面积10 cm2的网状铜镍合金为阳极,25 cm2的铜片为阴极,并将阳、阴电极通过导线分别与pH/ISE测试仪的正、负极连接。在染色过程中调节外加电压,并通过pH/ISE测试仪监测还原电位,待电位数值稳定后记录数据。
1.4.2K/S值及匀染性 采用分光测色仪测定染色后纯棉织物的K/S值。将染色后织物折叠三层,在正、反面分别随机选取4个点测试,取8次测试的平均值,计为K/S值。
1.4.3 色牢度 依据GB/T 3920—2008《纺织品 色牢度试验 耐摩擦色牢度》、GB/T 3921—2008《纺织品 色牢度试验 耐皂洗色牢度》、GB/T 251—2008《纺织品 色牢度试验 评定沾色用灰色样卡》分别测试评定染色后棉织物的耐擦色牢度,皂洗色牢度等。
1.4.4 铁胺配合物的电化学行为 本课题组前期研究[18]证实,还原棕BR进行电化学还原染色时,染色体系中各电解质溶液的最佳质量浓度配比为Fe2(SO4)3∶NaOH∶TEA=5∶8∶30。文中,先配置一定浓度的铁胺配合物溶液,向溶液中通入氮气15 min以去除氧气。在三电极体系下,采用循环伏安法[19]和方波伏安法[20]探究银电极上发生的电化学行为。
1.4.5 染色体系的电化学行为 将阴极区作为电化学染色区域,染色体系中的电解质溶液中含有Fe2(SO4)3、TEA、NaOH和还原棕BR,质量浓度分别为5 g/L、30 g/L、8 g/L和0.2 g/L。阳极区的H2SO4溶液浓度为35 g/L。在染色区域,待还原棕BR被电化学体系完全还原后,取出少量电解液并稀释,向溶液中通入氮气15 min以去除氧气。在三电极体系下,以Ag电极为工作电极,采用循环伏安法和方波伏安法研究染色体系的电化学行为。
2 结果与讨论
2.1 染色体系及染色过程中的电化学行为
2.1.1 在银电极的电化学行为 将一定配比的NaOH和TEA混合溶液作为空白底液,采用银电极测试空白底液、铁胺配合物(TEA/FeSO4·7H2O)和染色体系(空白底液+铁胺配合物)的循环伏安曲线,结果见图3。
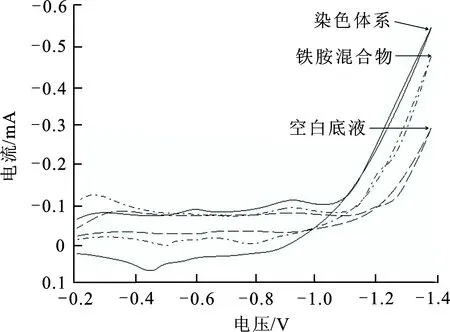
图 3 银电极上的循环伏安曲线Fig.3 Cyclic volt-ampere curves on thesilver electrode
从图3得知,当铁胺配合物溶液中加入还原棕BR后,电势从-0.2 V向负方向扫描至-1.4 V,之后回扫至-0.2 V,在-0.4 V与-0.6 V附近出现一对准可逆的氧化还原峰,-1.0 V附近出现一个不可逆还原峰,-1.1 V附近电流开始逐渐上升,发生了析氢反应,析氢电位比加入染料前增大。染料在银电极上没有出现电流响应,可能是由于染料不溶于水很难接近电极表面,因此还原峰应该是铁胺配合物的还原峰。说明还原棕BR的还原极可能是通过间接电化学还原方式实现的,即电极向铁胺配合物转移电子,然后铁胺配合物向还原棕BR的固体颗粒传递电子,获得可溶于水的染料隐色体。
2.1.2 扫描次数对循环伏安曲线的影响 同一染色体系中加入还原棕BR并进行多次间接电化学还原染色后,为了验证该过程中染料和铁胺配合物与电极间的电化学行为及其可能的变化情况,在上述染色体系下进行了5次连续扫描,获得了相应的循环伏安曲线,如图4所示。
从图4可知,在染色体系中加入还原棕BR(加入初始为悬浮体状态)后,连续扫描5次,所获得的循环伏安曲线的峰形和峰电流数值基本没有发生变化。说明在染色体系中加入还原棕BR后,铁胺配合物和还原棕BR均没有被吸附在银电极上,也没有发生聚集现象。这一现象对后续棉织物在该染色体系中的染色是十分有利的。
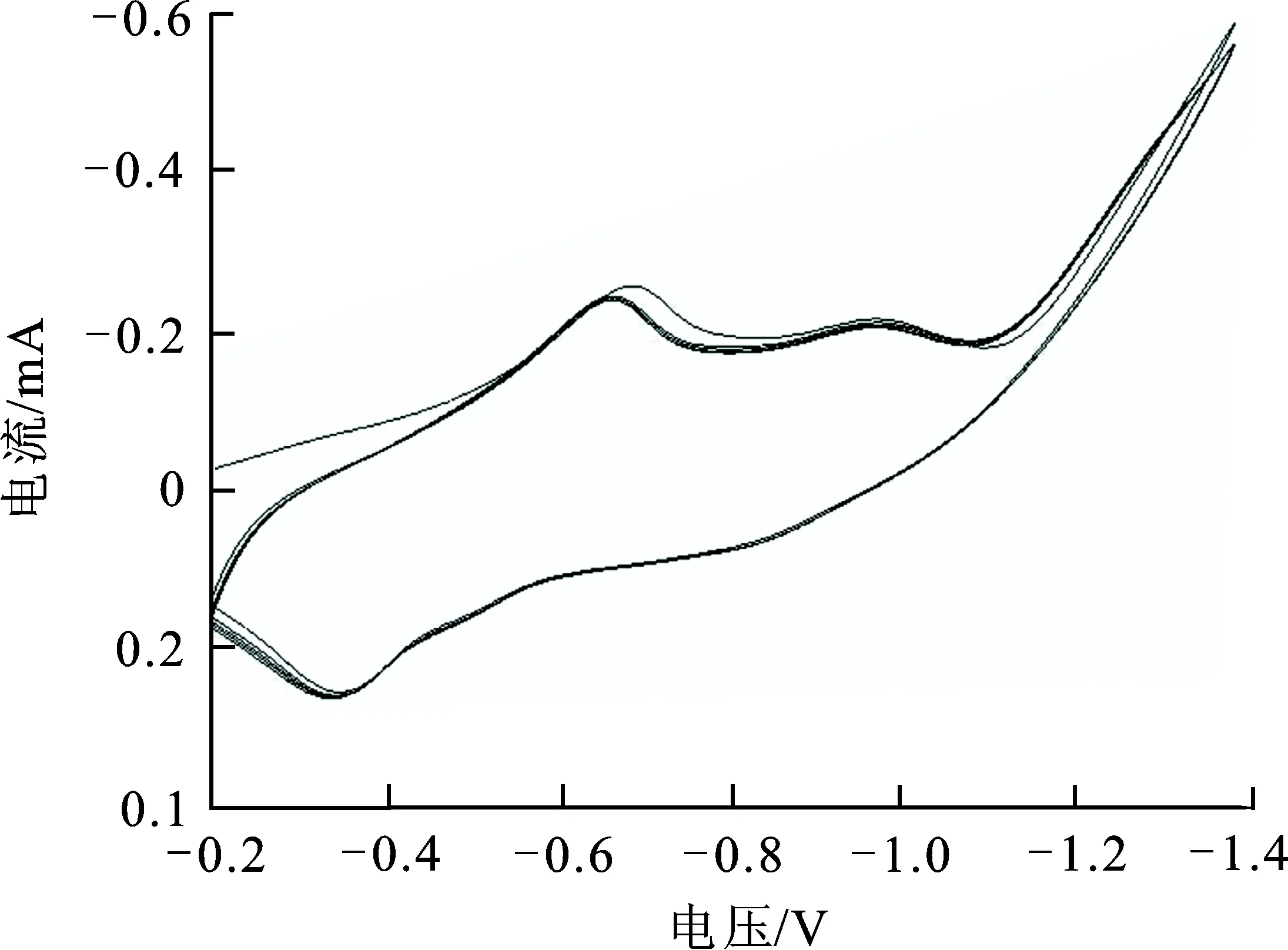
图 4 扫描次数对循环伏安曲线的影响Fig.4 The influence of scanning times on cyclic voltammetry curves
2.1.3 pH值对峰电位和峰电流的影响 考虑到还原棕BR在电化学还原染色过程中,铁胺配合物作为电子传递介质,其电子传递效能的高低对还原棕BR的还原至关重要,本研究在电位扫描速率为50 mV/s时,通过循环伏安扫描探析pH值对铁胺配合物的氧化还原峰电流的影响,结果如图5所示。
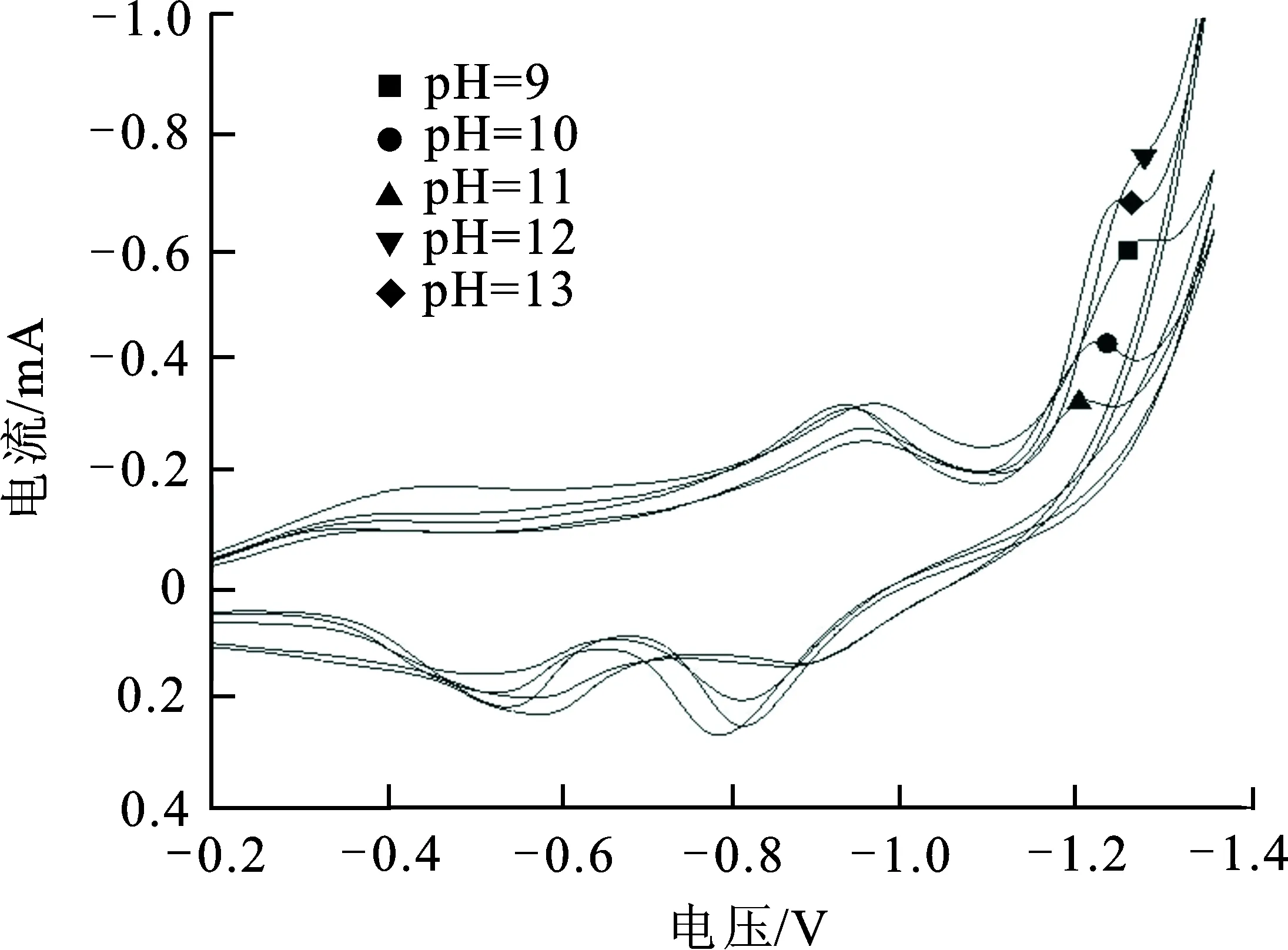
图 5 铁胺配合物在不同pH值下的循环伏安曲线
从图5可知, 当染色体系的 pH 值从9增加到11时, 铁胺配合物的氧化峰电流呈现逐渐增大的趋势, 即pH值增加时, 铁胺配合物的给电子能力更强。 当pH值大于11时, 随着pH值的增加, 铁胺配合物的氧化峰电流发生了一定程度的减小, 很可能是由于随着pH值的增加, 发生了OH-和TEA与 Fe(II) 或 Fe(III) 之间的配位竞争。 从实验现象观察, 此时体系中的 Fe(II)/Fe(III) 发生了沉淀反应, 必然会降低铁胺配合物的得失电子能力, 使电流效应减弱。 因此, 该氧化-还原体系的最佳pH值为11。
2.2 配位数和还原电位的测定及对染色效果的影响
2.2.1 配位数的测定 通过测试铁胺配合物溶液的电导率研究其配位数,即固定NaOH物质的量(0.02 mol)及FeSO4·7H2O物质的量(0.001 07 mol),变化TEA物质的量,测试不同n(TEA)∶n(FeSO4·7H2O)下染色体系(TEA+FeSO4·7H2O+NaOH)的电导率G,结果见表2。
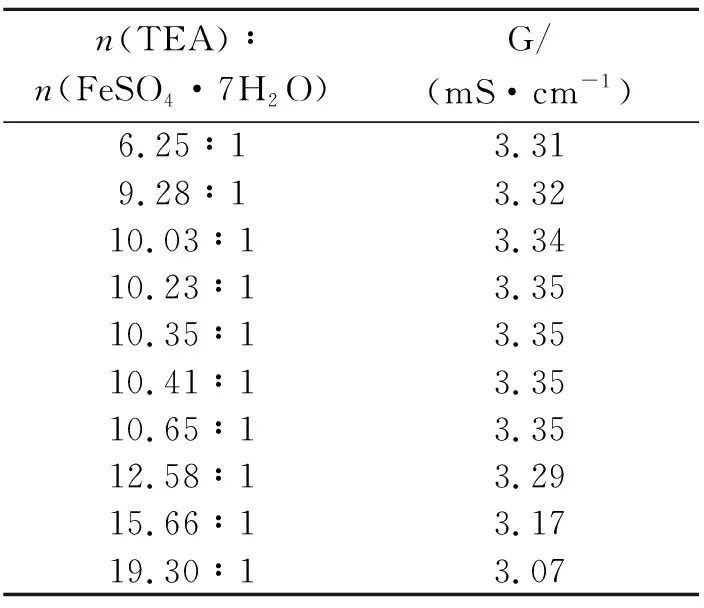
表 2 TEA与FeSO4·7H2O的配比对染色体系电导率的影响
从表2可知,随着染色体系中TEA与FeSO4·7H2O的物质的量之比从6.25∶1增大到10.65∶1,染色体系的电导率G逐渐增大,并逐渐稳定在3.35 mS/cm,继续再增加TEA的量,电导率又逐渐降低。表明在染色体系中,一个Fe2+离子大概可与11个TEA分子配位,形成配位化合物。当n(TEA)∶n(FeSO4·7H2O)从10.65∶1增加到19.30∶1时,过量的TEA使FeSO4·7H2O几乎完全配位,溶液中几乎无游离态的Fe2+存在,因此染色体系的电导率降低。并且在此过程中,体系一直处于澄清状态,说明TEA对Fe2+的配位竞争能力超过了NaOH对Fe2+的沉淀反应能力。当n(TEA)∶n(FeSO4·7H2O)从10.65∶1降至6.25∶1时,Fe2+未能完全参与配位反应,游离的Fe2+会与OH-结合,生成Fe(OH)2沉淀,因此电导率又下降。从实验现象观察,染色体系伴有微弱的浑浊现象。结合测试结果以及参考文献[21],推测TEA与Fe2+的物质的量的最佳配比应为11∶1,即该反应的配位数为11。
2.2.2 TEA与FeSO4·7H2O的配比对染色效果的影响 从2.2.1的结果可知,TEA与FeSO4·7H2O的配比将影响染色体系的电导率,并可能影响还原棕BR的还原染色效果。因此,单因素变化TEA与FeSO4·7H2O的配比,研究其对还原棕BR染色后棉织物K/S值的影响,结果见图6。
从图6可知,随着TEA与FeSO4·7H2O的摩尔比逐渐增加,还原棕BR染色后棉织物的K/S值呈先增加后减少的趋势。在n(TEA)∶n(FeSO4·7H2O)为15∶1时,染色后棉织物的K/S值最大,且发现通过电导率测试确定的TEA与Fe2+的最佳配比(11∶1)并不能使还原棕BR在电化学还原染色中达到最佳的染色效果。可能是因为在染色过程中棉织物的加入以及磁子的搅拌作用,使得TEA与Fe2+的配位受到了干扰,因而需要加入更多的TEA才能达到原先的配位效果[18]。
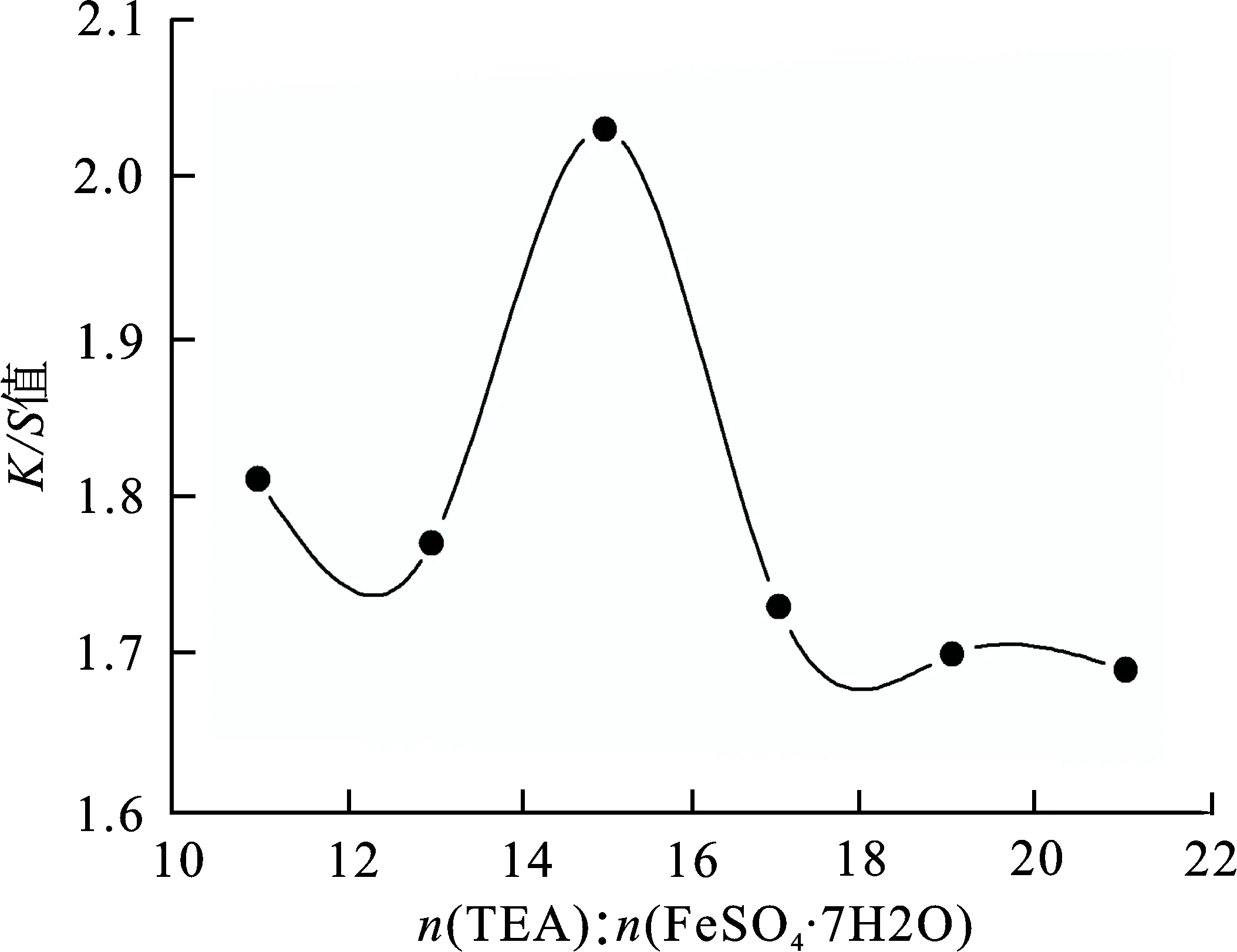
图 6 n(TEA):n(FeSO4·7H2O)对还原棕BR染色效果的影响
2.2.3 TEA与FeSO4·7H2O的配比对还原电位的影响 染色体系还原电位的高低直接决定了还原棕BR的不溶性悬浮体能否被还原成可溶性的隐色体,进而实现在棉织物上的上染。因此,分别分析不同n(TEA):n(FeSO4·7H2O)对染色体系还原电位的影响,结果见图7。

图 7 n(TEA):n(FeSO4·7H2O)对染色体系还原电位的影响
从图7可知,当n(TEA)∶n(FeSO4·7H2O)≤15时,染色体系的还原电位基本保持不变。但当n(TEA)∶n(FeSO4·7H2O)>15时,染色体系的还原电位迅速下降。结合2.2.1和2.2.2中的结果不难发现,此时染色体系的电导率显著降低,还原棕BR对纯棉织物的染色效果也明显变差。由此可见,当TEA与FeSO4·7H2O的摩尔比大于15时,电化学还原染色体系电导率下降和还原电位降低直接引起电子传递效率下降,还原棕BR分子得电子变得困难,其被还原为可溶性隐色体的效率下降,继而导致对棉织物的上染率降低,染色效果变差。
2.2.4 间接电化学还原与传统工艺染色效果比较 在本研究中还将经间接电化学还原染色方法和传统浸染方法染色后棉织物的各项色牢度进行了比较,结果如下表3所示。

表 3 2种染色方法的色牢度比较
从表3可知,经间接电化学还原染色方法染色后棉织物的各项色牢度与传统浸染染色方法染色后棉织物的色牢度基本相当。
3 结 论
(1) 还原棕BR还原染色是通过间接电化学还原方式实现的,即阴极将电子传递给铁胺配合物,然后还原棕BR从铁胺配合物获得电子,被还原为隐色体。染料并非通过在阴极上吸附而直接获得电子。
(2) 体系进行间接电化学还原染色的最佳pH值为11。TEA与FeSO4·7H2O物质的量配比为11∶1时,染色体系可获得最高电导率;n(TEA)∶n(FeSO4·7H2O)为15时,染色体系可获得最高还原电位,还原棕BR可获得最佳染色效果。
(3) 经间接电化学还原染色方法染色后棉织物的各项色牢度与传统染色方法基本相当。
