体质量指数对胃癌根治术病人远期预后的影响
2019-08-26陈杰李政焰季刚王士祺白槟赵青川
陈杰,李政焰,季刚,王士祺,白槟,赵青川
(1.第四军医大学西京消化病医院消化外科 国家消化系统疾病临床医学研究中心,陕西 西安710032;2.中国人民解放军77675部队50分队,西藏 林芝 860000)
胃癌是常见的消化道恶性肿瘤,2018年在全球范围内新发癌症中发病率占第5位、死亡率占第3位,在新增1 810万癌症病例中,亚洲病人占据近50%,960万癌症死亡病人中,亚洲病人占近70%[1]。外科手术仍是临床上唯一可能治愈胃癌的医疗手段。
体质量指数(body mass index,BMI)是结合身高和体重来判断人体超重/肥胖与否和程度的指数[2],临床上常用来评估病人的营养状况,对患有肿瘤、糖尿病等伴有代谢相关症候疾病的病人具有尤为重要的参考价值。目前WHO 将30 kg/m2>BMI≥25 kg/m2定义为超重,BMI≥30 kg/m2定义为肥胖[3]。我国成人BMI的界值[4-5]:BMI<18.5 kg/m2为体重过低,18.5 kg/m2≤BMI<24 kg/m2为正常体重,24 kg/m2≤BMI<28 kg/m2为超重,BMI≥28 kg/m2为肥胖。
目前关于BMI和胃癌术后远期生存的研究较少,现有研究多来源于欧美和韩国、日本,且结论不一。我国现有对BMI与胃癌术后远期生存情况的研究多以WHO定义的标准,将正常体重与超重以及超重与肥胖分界值分别设置为25 kg/m2及30 kg/m2。然而由于人种差异,这一分界值并不适用于我国,同时现有研究存在样本量较小,随访时间短等缺点。因此,本研究回顾性分析1 973例施行胃癌根治术病人的临床病理资料及随访情况,旨在探讨术前BMI对胃癌根治术后远期预后的影响。
资料与方法
一、一般资料
回顾性收集2009年6月至2013年7月在第四军医大学西京消化病医院消化外科行胃癌根治术1 973例病人的临床资料,所有病人均行根治性胃切除术。进展期病人术后行常规化疗。肿瘤TNM分期依据第8版国际抗癌联盟(UICC)分期标准[6],手术医师切除标本后对切除标本、清扫淋巴结并进行分类,送病理科检测,术后进展期胃癌病人在依据病人病理分期、全身状况、器官功能在术后3~4周开始接受以氟尿嘧啶为基础的辅助化疗方案。本研究通过医院伦理委员会批准,术前所有病人均已签署书面知情同意书。
纳入标准:①原发性胃癌;②年龄20~75岁;③接受根治性胃癌切除手术。排除标准:①姑息性及探查手术治疗者;②病人合并其他部位恶性病变者手术或者术后1个月内死亡者;③胃癌术后复发、残胃癌;④上皮内瘤变者、胃间质瘤、胃溃疡等良性病变者;⑤胃内淋巴瘤、黑色素瘤、肉瘤等恶性病变者;⑥术前接受放化疗的病人;⑦术后失访的病人、资料不全影响判断者。
分组:根据中国成人BMI界值分为4组,体重过低组(BMI<18.5 kg/m2), 体重正常组(18.5 kg/m2≤BMI<24 kg/m2),超重组(24 kg/m2≤BMI<28 kg/m2),肥胖组(BMI≥28 kg/m2)。最终共有1 973例病人纳入研究,其中男性1 478例(74.9%),女性495例(25.1%),年龄(58.3±9.4)岁;体重过低组190例(9.6%)、体重正常组1 205例(61.1%),超重组490例(24.8%),肥胖组88例(4.5%)。病人年龄、性别、吸烟史、术前美国麻醉医师协会(ASA)评分、手术方式、胃切除范围、消化道重建方式、肿瘤细胞分化程度在4组间差异均无统计学意义(表1),但病理分期、肿瘤长径在各组差异具有统计学意义(P<0.01)。如表1所示,体重过低组相比其他3组肿瘤长径长、肿瘤处于Ⅲ期者比例高。
二、评价方法
主要评价术后5年生存情况:由专人负责术后随访,采用门诊复查、电话、信件等方式进行。总生存时间(overall survival,OS)计算方式为从手术到病人以任何原因死亡或末次随访日期,本研究末次随访时间为2018年7月,终止日期为2018年7月31日。无进展生存期(progress free survival,PFS)以手术时间到首次记录到胃癌复发或者转移、死亡或末次随访评估的日期。生存时间的计算以月为单位,超过1个月不足2个月记录为1个月。术后2年内每3个月随访1次,第2年至第5年每6个月随访1次,术后生存超过5年的病人每1年随访一次。

表1 病人一般资料统计
注:表中各项目,除肿瘤长径外 ,余单位均为“例(%)”;近端(吻合方式)包括双通道吻合、食管残胃吻合、空肠间置吻合
三、统计学分析
应用SPSS(24.0版)统计软件进行分析,组间比较采用交叉表检验或单因素ANOVA检验,生存分析采用Kaplan-Meier法进行分析,生存曲线的比较采用Log-rank趋势检验。P<0.05为差异有统计学意义。危险因素的单因素分析采用交叉表法进行分析,多因素分析采用Cox比例风险回归模型,P<0.05为差异具有统计学意义。
结 果
一、各组病人术后5年生存情况比较
体重过低组病人术后5年生存率明显低于其他各组(P<0.01);体重正常组5年生存率低于肥胖组(P=0.042),见图1,体重正常组与超重组、超重组与肥胖组两两比较差异无统计学意义。术后5年PFS与OS结果相似(图2)。相比于其他组,体重过低组病人在术后5年总体死亡率最高,术后5年PFS率也最差,总体生存情况见表2。
二、远期预后的单因素分析及多因素分析
本研究的中位随访时间为64个月(1~113个月),单因素分析结果显示年龄、ASA评分、胃切除范围、肿瘤长径、肿瘤分化程度、BMI、术后化疗、肿瘤TNM分期与胃癌远期预后相关。多因素分析显示,年龄≥60岁、ASA评分≥3分、肿瘤长径≥10 cm、肿瘤印戒黏液未分化、全胃切除、BMI<18.5 kg/m2、肿瘤TNM分期为Ⅲ期是胃癌远期预后的独立危险因素。见表3。
三、亚组分析
按TNM分期对各组病人进行亚组分析。结果显示Ⅰ期病人5年生存率为92.4%,Ⅱ期为66.2%,Ⅲ期为36.6%,见图3。各亚组中体重过低组病人5年生存率均显著低于正常体重组、超重组、肥胖组,差异具有统计学意义(P<0.05),见图4~图6。
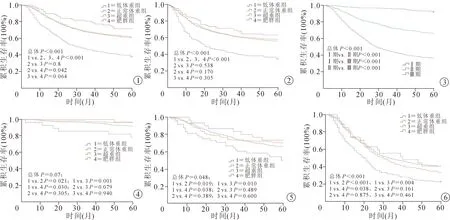
图1 按BMI分组术后5年总体生存情况 图2 按BMI分组术后5年无进展生存情况 图3 按TNM分期术后5年总体生存情况 图4 TNM分期Ⅰ期病人术后5年生存情况 图5 TNM分期Ⅱ期病人术后5年生存情况 图6 TNM分期Ⅲ期病人术后5年生存情况
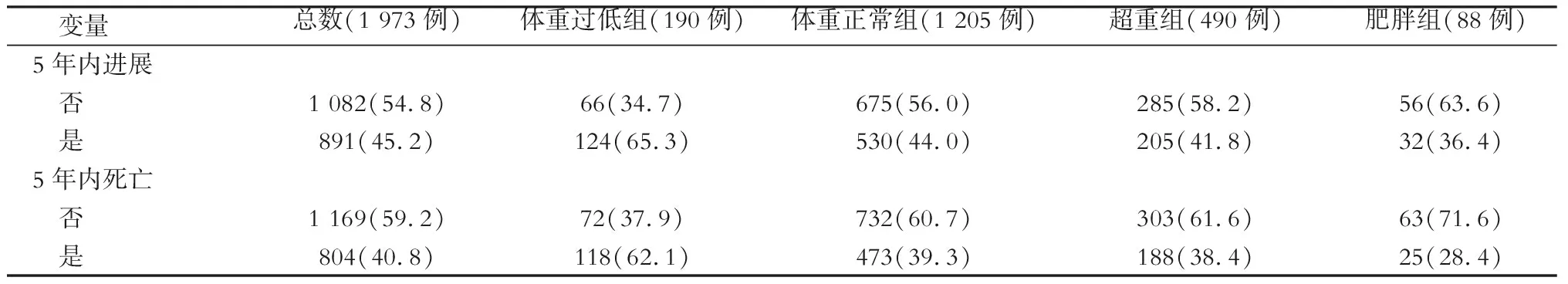
变量总数(1 973例)体重过低组(190例)体重正常组(1 205例)超重组(490例)肥胖组(88例)5年内进展 否1 082(54.8)66(34.7)675(56.0)285(58.2)56(63.6) 是891(45.2)124(65.3)530(44.0)205(41.8)32(36.4)5年内死亡 否1 169(59.2)72(37.9)732(60.7)303(61.6)63(71.6) 是804(40.8)118(62.1)473(39.3)188(38.4)25(28.4)

表3 胃癌术后5年生存的危险因素的单因素和多因素分析
注:HR.风险比
讨 论
胃癌是中国癌症总体发病率第2位、死亡率第3位的恶性肿瘤[7],由于肿瘤位置的特殊性、机械因素(梗阻等)、心理社会因素、手术与化疗等医疗等相关因素共同作用,胃癌对病人营养状况的影响在各类肿瘤中尤为突出[8]。超重和肥胖是正逐渐成为一个全球性、社会性问题[9]。通常人们会认为肥胖对健康不利,会导致严重的健康后果。过高的BMI可引起多种慢性疾病[10-12],如心血管疾病、糖尿病、骨关节炎发病风险增加,某些癌症[13-16]如:结肠癌、肾细胞癌、子宫内膜癌、乳腺癌等。BMI是通过体重与身高的平方的比值来评估人体营养状况的一种指标。BMI过低提示营养不良,而BMI过高则会因为腹壁过厚、脂肪过多导致胃癌手术难度增加[17]。
目前研究多集中于BMI对手术近期疗效的影响,受样本量、种族差异、经济医疗条件等因素的影响,BMI与胃癌病人远期预后的相关性仍存争议。Bickenbach等[18]研究认为,高BMI(BMI>25 kg/m2)是胃癌术后并发症增加的预测因素但不是远期生存的预测因素。Dhar等[19]对787例胃癌病人研究认为高BMI不利于胃癌淋巴结清除,进而影响病人预后,高BMI的病人胃癌复发的风险是低BMI病人的1.85倍,认为BMI是术后复发的独立危险因素。Tokunaga等[20]的研究结果显示BMI≥25 kg/m2的进展期胃癌病人5年生存率明显高于BMI<25 kg/m2病人(81.5% 比74.1%)。Kruhlikava等[21]研究认为BMI>30 kg/m2或者BMI<18.5 kg/m2并不影响食管胃结合部癌病人远期生存情况。Chen等[22]的1 249例胃癌病人单中心队列研究显示BMI≥25 kg/m2病人术后5年生存率最高为60.7%,正常BMI(18.5 kg/m2 胃癌是消化道最常见的恶性肿瘤,由于肿瘤消耗、摄入减少等因素影响,易导致体重减轻,胃切除术由于胃容量减少和激素变化而进一步导致体重减轻[25]。Kiyama等[26]研究显示胃癌术后病人体重通常会下降5%至19%,胃切除术后6~18个月左右BMI变化值达到最低,进而趋于稳定或增长[27]。Arques等[28]的研究认为术前高BMI的病人的营养状况较低BMI病人好。本研究显示术前低BMI病人TNM分期较晚,术后可能随着BMI进一步降低,出现营养状况进一步下降,进而影响病人预后。 韩国学者 Lee等[29]近期一项大样本回顾性研究显示低BMI组(<18.5 kg/m2)病人远期生存率显著低于正常BMI组(18.5 kg/m2≤BMI<23 kg/m2)。此外,其研究发现超重组(23 kg/m2≤BMI<25 kg/m2),轻度肥胖组(25 kg/m2≤BMI<28 kg/m2),中度肥胖组(28 kg/m2≤BMI<30 kg/m2)远期生存率高于正常BMI组。本研究结果显示:术前体重过低组病人的5年生存率显著低于体重正常组,这一结论也与 Lee等的结论一致。然而,本研究中并未发现超重及肥胖组与正常体重组病人的生存差异。与其他研究不同,本研究按照中国成人BMI界值进行分组,发现术前低BMI是胃癌根治术病人远期预后不良的危险因素。但本研究结果显示超重或者肥胖病人与体重正常病人5年生存率差异无统计学意义,并不能得出高BMI是术后远期生存的保护性因素的结论。从疾病角度来看,低BMI是疾病发展的果而不是因,病人术前低BMI提示病人因肿瘤消耗而导致营养状态不佳,应考虑积极给予营养支持,以期改善其预后。 这项研究也存在一些不足之处:第一,未将术前3个月至1年以及术后1年BMI变化纳入研究,不能得出完整的BMI变化对胃癌根治术病人远期预后的影响;第二,研究为单中心研究,纳入的病例数量有限,结论仍需多中心、大样本研究进一步证实;第三,本研究分析了术前BMI对胃癌根治术病人远期预后的影响,但由于肿瘤消耗带来的肌肉减少的状况广泛存在,单纯的BMI不足以准确判断病人营养状况,需进一步探究身体肌肉含量对胃癌根治术病人远期预后的影响。 综上所述,术前低BMI是胃癌病人远期预后不良的独立危险因素,即使相同的TNM分期亦有此规律。低BMI病人围手术期应予以充分营养支持以改善病人远期预后。
