成年先天性心脏病致大面积脑梗死一例报道并文献复习
2019-08-23章林杜少辉杨珣张强杨嘉敏骆沁文李少锋
章林,杜少辉,杨珣,张强,杨嘉敏,骆沁文,李少锋
大动脉粥样硬化、小动脉闭塞及心源性栓塞均是脑梗死的常见病因。近年来随着手术及护理学发展,先天性心脏病手术率及早期存活率升高,而成年先天性心脏病致脑梗死者较少见,其实先天性心脏病对神经系统的损伤是持续性的,其可影响患者生活质量、学业成绩及独立生活能力,因此需提高临床工作者对该病的重视和认识。本文报道1例成年先天性心脏病致大面积脑梗死患者慢病进行文献复习,以提高临床医生对成年先天性心脏病致脑梗死的认识。
1 病例简介
患者,女,26岁,因“言语不能伴右侧肢体无力2 d”于2018-04-25入住深圳市第二人民医院,家属代述患者2 d前睡醒时突发言语不能、右侧肢体无力,可扶墙站立,无恶心、呕吐,无肢体抽搐,遂由家属送至医院就诊,行颅脑磁共振成像(MRI)检查结果示左侧颞叶、顶叶大面积急性梗死,后转至病房住院治疗。既往有先天性心脏病病史,未系统治疗,未婚,无性病及冶游史,否认烟酒嗜好,否认家族遗传史。入院查体:体温36.2 ℃,脉搏82次/min,呼吸20次/min,血压93/50 mm Hg(1 mm Hg=0.133 kPa)。肺部听诊无异常,胸骨左缘可闻及3/6级收缩期吹风样杂音,腹部查体无特殊。神经系统查体配合欠佳,意识清晰,完全运动性失语,两侧瞳孔等大等圆,直径3 mm,对光反射灵敏,眼球活动正常,无眼震,右侧鼻唇沟变浅,伸舌偏右。右上肢肌力0级,右下肢肌力0~1级,左侧肢体活动可,右侧肢体肌张力减弱,腱反射可引出,右侧巴氏征、查多克征(+),左侧肢体病理征(-),颈软无抵抗,克氏征(-)。两侧锁骨上区及颈动脉听诊区未闻及血管杂音。双手可见杵状指。美国国立卫生研究院卒中量表(NIHSS)评分11分,Barthel指数(BI)评分20分,洼田饮水试验1级,改良Rankin量表(mRS)4级。急诊动脉血气分析结果示动脉血二氧化碳分压为21.8 mm Hg,动脉血氧分压为59.2 mm Hg,实际剩余碱为-8.2 mmol/L,实际碳酸氢根为14.2 mmol/L,标准剩余碱为-9.6 mmol/L,标准碳酸氢根为17.8 mmol/L,二氧化碳总量为12.4 mmol/L。血常规、血生化、自身免疫等未见明显异常。动态心电图检查结果示窦性心律不齐;交界性逸搏、室性逸搏;偶发多源房性期前收缩、室性期前收缩;部分时间ST-T段改变;心率变异性增高。心脏彩超检查结果示先天性心脏病;室间隔缺损(肌部),缺损处可见双向血流信号;肺动脉内径增宽;肺动脉瓣重度狭窄;右心室流出道轻度狭窄。颅脑CT检查结果示左侧颞叶、顶叶大面积梗死,见图1A、1B。头颈部CT血管造影检查结果示左侧大脑中动脉狭窄、闭塞。脑电图未见异常。诊断:(1)脑梗死(左侧颞叶及顶叶,心源性栓塞型);(2)先天性心脏病:室间隔缺损(肌部)、肺动脉瓣狭窄(重度);(3)左侧大脑中动脉重度狭窄或闭塞;(4)心律失常:交界性逸搏、室性逸搏。给予患者改善血液循环、清除氧自由基、营养神经、抗血小板聚集、抗凝等治疗。患者出院时右侧肢体肌力稍恢复,言语不清好转。
2 讨论
先天性心脏病是青少年脑梗死的常见原因,其中室间隔缺损并发脑梗死较少见。SHUIAB[1]于1989年首次报道1例室间隔缺损并脑梗死患者,推测其发病原因为栓塞。陈世保等[2]于2018年报道了1例室间隔缺损并发脑梗死患者,其发病原因可能是患者出现艾森门革综合征后机体处于慢性缺氧状态,刺激红细胞生成素增多,导致血红蛋白及红细胞比容(HCT)持续升高,进而发展为继发性红细胞增多症。本例患者发生先天性心脏病并发脑梗死的机制可能如下:(1)患者幼年时有运动耐力低下表现,且血气分析结果显示低氧血症,有杵状指,提示患者脑部持续性缺氧;(2)患者动态心电图检查结果示心律失常,可间接影响脑部血供;(3)心脏彩超检查结果示患者室间隔缺损处双向血流信号,且由无青紫型转变为有青紫型,提示艾森门革综合征。
先天性心脏病患者致脑损伤的原因较复杂,但主要包括胎儿时期脑损伤、脑血流改变、颅内分子生物学指标变化、血栓形成及手术因素。而既往研究表明,手术前检查发现约50%的先天性心脏病患者在新生儿期即有神经系统发育不良表现[3]。
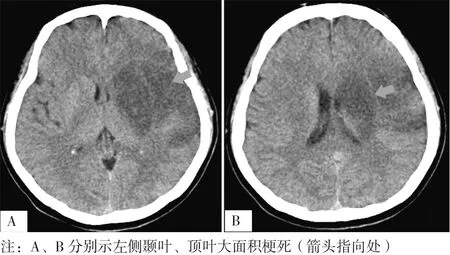
图1 颅脑CT检查结果Table 1 Craniocerebral CT examination results
2.1 胎儿时期脑损伤 先天性心脏病患者的脑损伤在胎儿时期已存在,主要是先天性心脏病使胎儿血流动力学改变,脑血流减少,脑氧供降低,进而使脑细胞生长及成熟受限,发生白质病变。先天性心脏病胎儿MRI检查结果示总脑容量(经孕龄及体质量调整)减少、脑代谢异常、皮质发育延迟[4]。通过评估先天性心脏缺陷患者术前大脑发育情况发现,超过20%的患者有40%~50%的白质损伤[5-6]。
研究表明,先天性心脏病患者大脑成熟度低是围术期脑损伤及神经发育障碍的重要危险因素[7-8]。一项有关青少年大动脉转位的研究结果显示,白质微观结构的区域变化与计算力、注意力、执行功能、视觉和空间技能以及记忆减退有关[9]。HEINRICHS等[10]发现32%行大动脉转位术的患者存在中重度白质损伤,且损伤程度越重则患者神经发育障碍越严重。
2.2 脑血流改变 脑血流变化在青紫型及非青紫型先天性心脏病患者中有不同机制:青紫型先天性心脏病是由右向左分流,体循环中混有静脉血液,致动脉血中氧浓度降低,机体长期处于缺氧状态,导致智力发育障碍、晕厥、头晕、头痛等。非青紫型先天性心脏病由左向右分流,肺血多,易致心功能异常及充血性心力衰竭,可形成脑水肿及脑缺血缺氧性改变。另外心脏结构及血流动力学改变可致心律失常,进而影响脑血供[11]。夏礼勤等[12]对66例先天性心脏病患儿进行脑血流图(REG)检查结果示,脑血流异常发生率较高(80.3%),其中青紫型先天性心脏病中重度脑血流异常比例更高,REG检查结果示波幅、流入容积速度降低,且其脑血流下降程度与动脉血氧分压及血液黏度有关[12]。
2.3 颅内分子生物学指标变化
2.3.1 N乙酰天门氨酸(NAA)降低 MILLER等[13]对先天性心脏病患儿及健康对照者行磁共振波谱检查结果示,先天性心脏病患儿NAA峰较健康对照者降低,而NAA降低提示神经元未成熟,也反映慢性缺氧对神经元损伤;弥散成像结果示先天性心脏病患儿脑组织水分含量较多,提示神经元及神经胶质细胞发育均不成熟。
2.3.2 乳酸升高、谷氨酸代谢异常 张斯琴等[14]通过分析25例青紫型先天性心脏病患者磁共振质子波谱检查结果发现,青紫型先天性心脏病患者乳酸升高,提示患者脑能量代谢异常。一项针对新生儿缺氧缺血性脑病的研究显示,在病变早期即可观察到乳酸峰,且乳酸峰与症状呈正相关,经治疗后乳酸峰回落,此外谷氨酸等兴奋型氨基酸代谢异常,而这些异常对神经元具有毒性作用[15]。
2.4 血栓形成
2.4.1 血栓形成和继发性出血 青紫型先天性心脏病患者低氧血症慢性期HCT逐渐增加,于2周后高于参考范围,导致血流瘀滞及全身各器官血栓形成,进一步促进脑栓塞,增加肺出血和脑出血发生风险[16]。
2.4.2 艾森门革综合征 房间隔缺损、室间隔缺损为左向右分流,而当肺动脉高压发展至器质性肺动脉阻塞性疾病时出现右向左分流,皮肤黏膜由无青紫发展为有青紫时即为艾森门革综合征[17]。邢西迁等[18]通过分析4例艾森门革综合征患者发现,均无静脉血栓形成的危险因素,且D-二聚体阴性,下肢静脉彩超检查结果未见血栓形成,但心脏彩超检查结果示肺动脉压升高、肺部血管增的强影像学特点均提示肺动脉近端或较大分支有层状附壁血栓形成,提示艾森门革综合征致肺动脉栓塞具有隐匿性、渐进性等,易漏诊;原因可能是肺动脉高压导致肺动脉血流减慢,而机体缺氧可刺激骨髓造血细胞生成,使代偿性红细胞生成增多致血液黏度增加,导致肺动脉血栓形成。
2.5 手术导致脑损伤 脑血管疾病是先天性心脏病患者术后较常见且严重的并发症之一。既往研究结果表明,成年人心脏术后脑梗死发生率为2%~6%,儿童心脏术后脑梗死发生率为0.54%[19]。虽然儿童心脏术后脑梗死发生率较低,但脑梗死是儿童死亡的十大原因之一[20]。先天性心脏病术后并发脑梗死可能的机制为创伤造成全身炎性反应,导致血容量改变、血压波动、继发高凝状态及各种性质栓子形成[21]。
