慢性肾脏病不同分期患者血清多项骨代谢指标变化与成纤维细胞生长因子23的相关性分析*
2019-08-20尹爱萍
杨 雄,尹爱萍
(1.神木市医院综合内科,陕西神木 719300;2.西安交通大学医学院,西安 710061;3.西安交通大学第一附属医院肾内科,西安 710061)
慢性肾脏病(chronic kidney disease,CKD)是由多种因素导致的肾脏慢性结构改变及功能障碍性疾病,其治疗难度大,临床发病率高,多为肾脏急性病症未经控制转归导致[1],严重地危害了患者的生存质量。随着CKD病情发展,患者容易引发钙磷代谢和骨代谢紊乱(chronic kidney disease-mineraland bone disorder,CKD-MDB),因而引发继发性甲状旁腺功能亢进,甚至导致骨骼病变、甲状旁腺肿瘤以及严重心血管事件,威胁患者生命安全[2]。因此,对于CKD-MDB患者来说良好的预测和评价标志物对于其早期诊断和治疗至关重要。成纤维细胞生长因子23(fibroblast growth factor 23,FGF23)为骨成纤维细胞和骨细胞合成的内分泌荷尔蒙因子,其对于25羟基维生素D(25-hydroxyvitamin D,25-OH-VD)及血磷(serum phosphate,P)等有重要的调控作用[3-4]。研究显示,血清FGF23升高预示着CKD患者预后不良,且随着其浓度升高,其对于肾脏等靶器官的毒性效应逐渐加重[5-6]。因此,对于不同分期CKD患者矿物质骨代谢指标和FGF23水平进行检测对于CKD诊断、治疗和预后具有独立预测作用。本研究对神木市医院综合内科2016年1月~2018年12月收治的100例CKD 3~5期患者矿物质骨代谢指标变化及与FGF23的相关性进行了研究,取得了一定的进展,具体如下。
1材料与方法
1.1 研究对象 见表1。选取神木市医院2016年1月~2018年12月收治的100例慢性肾脏病患者,所有患者均符合国际改善全球肾脏病预后组织(kidney disease improving global outcomes,K/DIGO)指南中关于CKD的诊断标准[7],纳入标准:①所有患者均对本研究内容充分知情并签署知情同意书;②血清甲状旁腺激素(serum parathyroid hormone,iPTH)>1 000pg/ml;③存在维生素D不足或缺乏;④临床资料完善;⑤CKD分期3~5期。排除标准:①并发恶性肿瘤患者;②应用糖皮质激素、免疫抑制剂或免疫调节剂等治疗者;③慢性肾功能不全或急性肾损伤患者;④认知功能障碍者;⑤中途退出研究者。本研究事先征得我院伦理委员会批准通过。其中,CKD 3期(n=33),CKD 4期(n=32),CKD 5期(n=35),患者的性别、年龄、疾病类型比较,差异均无统计学意义(F=0.55,P=0.929;χ2=1.035,P=0.372;F=0.62,P=0.96)。
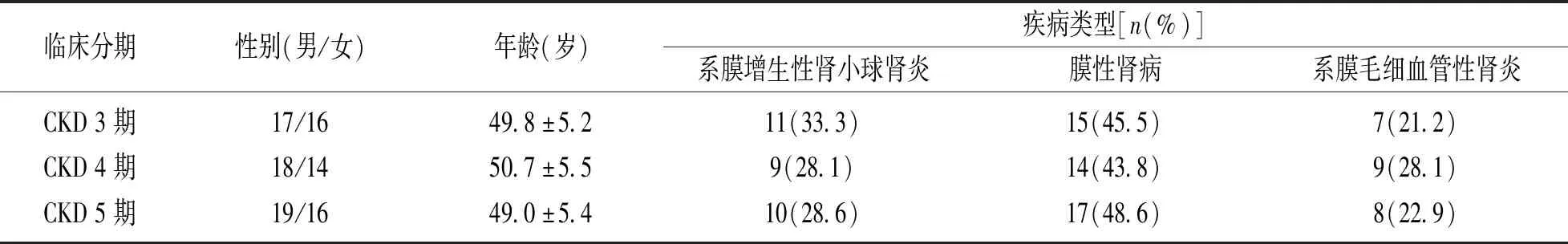
表1 不同CKD分期患者临床一般资料比较
1.2 试剂和仪器 高速离心机购于广州吉迪仪器有限公司,日立7600全自动生化分析仪购于北京泰林东方商贸有限公司;酶联免疫吸附实验试剂盒购自美国Immutopics公司;放射免疫试剂盒购自天津九鼎医学生物工程有限公司。
1.3 方法 所有患者于入院后次日清晨空腹状态下抽取5 ml静脉血,4 000 r/min离心5 min获取血清,于-20℃冰箱中保存待测。检测血钙(serum calcium,Ca)、磷(P)、血镁(blood magnesium,Mg)、全段甲状旁腺激素(iPTH)、骨钙素(Osteocalcin,OC)、骨型碱性磷酸酶(bone serum bone specific alkaline,BSALP)、抗酒石酸酸性磷酸酶5b(tartrate-resistant acid phosphatase-5b,TRACP-5b)、lotho蛋白、FGF23和25羟基维生素D(25-OH-VD)水平。其中,FGF23,BSALP,TRACP-5b,lotho蛋白和25-OH-VD检测采用酶联免疫吸附实验(enzyme-linked immunosorbent assay,ELISA)法;骨钙素检测采用放射免疫法(radioimmunoassay,RIA)检测,所有操作严格按照试剂盒说明书进行。
2结果
2.1 各组慢性肾脏病相关指标水平比较 见表2。随着CKD患者分期升高,血P,血Mg,iPTH,OC,BSALP,TRACP-5b及FGF23的水平均显著升高(均P<0.001),而血Ca,Klotho蛋白和25-OH-VD均显著降低(均P<0.001),CKD 4期和CKD 5期患者与CKD 3期相比和CKD 5期与CKD 4期相比,差异均具有统计学意义(F=9.924,P=0.006<0.05,F=6.657,P=0.019<0.05)。
表2 各组慢性肾脏病相关指标水平比较
2.2 FGF23与各指标的相关性分析 见表3。CKD 3~5期患者FGF23平均浓度水平与疾病类型、临床分期、血P,Mg,iPTH,OC,BSALP,TRACP-5b存在正相关性,差异均具有统计学意义(r=0.948~10.994,均P<0.05),而与血Ca、Klotho蛋白、25-OH-VD存在负相关性,差异均具有统计学意义(r=-6.755~-2.063,均P<0.05)。

表3 FGF23与各指标相关性分析
2.3 FGF23与各指标多元回归分析 见表4。以CKD 3~5期患者FGF23平均浓度作为因变量,表3中明显相关因素作为自变量进行回归分析显示,血Ca,P,Mg和iPTH为FGF23的独立影响因素,差异具有统计学意义(B=-0.533~6.075,SE=0.069~0.286,χ2=-6.844~8.436,allP<0.05)。

表4 FGF23与各指标多元回归分析
3讨论CKD是我国发病率较高的一种慢性进展性疾病,以老年患者居多。随着我国社会老龄化的加剧,导致CKD患病率逐年增加。贫血、高血压、钙磷代谢异常、代谢性酸中毒及营养不良等并发症不断出现[8]。不同CKD分期患者临床症状存在一定的差异。其中,钙磷代谢异常在CKD 3~5期患者中更为常见,钙磷代谢异常会导致患者机体多系统受损,严重影响了患者的预后。研究显示,矿物质骨代谢情况与CKD患者的病情存在明显相关性,对于矿物质骨代谢的指标评估有助于人们了解CKD患者病情发展情况[9]。
张丽娜等[10]研究显示,随着CKD患者分期升高,其血Ca,P水平显著降低,而iPTH等存在明显上升,这与本研究的结果相一致。之前的研究表明,CKD患者由于肾功能降低,导致活性维生素D生成不足,引起磷排泄量明显下降[11]。同时,肾功能降低导致α-1-羟化酶表达明显降低,导致骨化三醇的合成明显减少,而骨化三醇与尿液中Ca的重吸收有着密切联系,直接导致了血液中Ca的含量明显下降。RANKL-RANK-OPG骨调节轴参与骨细胞凋亡及骨钙的交换。CKD患者中过度升高的iPTH会导致RANKL表达增加,导致骨细胞生存时间降低,引起骨量丢失[12]。
研究显示,FGF23的主要作用是参与矿物质代谢,其能够减少肾脏对磷的重吸收作用。PTH和25-OH-VD在磷代谢的调节中发挥着关键作用[13]。PTH能够降低肾近曲小管PiT1,NPT2a和NPT2c对于P的重吸收,起到防止机体发生高磷血症的作用。25-OH-VD能够增加小肠吸收磷的效率,促使血清磷浓度增加。因此,PTH和25-OH-VD与FGF23可能存在一定的相关性。肾脏是FGF23发挥生理作用的主要靶器官,而在CKD患者中存在血清FGF23水平明显升高的情况,且其升高时机相对于PTH更加提前[14]。本研究结果显示,在CKD患者中FGF23显著升高,且随患者病情加重FGF23水平不断升高,与既往多数研究结果相符。心血管疾病是CKD患者死亡的主要原因,研究显示CKD患者FGF23升高与心血管疾病风险有着密切关系[15]。研究认为,FGF23可以作为CKD患者不良预后的可靠指示物[16-17]。FGF23升高的原因与CKD肾功能损伤有关。FGF23对于矿物质代谢的影响与PTH有着密切关系,FGF23能够通过丝裂原活化蛋白激酶(MARK)通道抑制甲状旁腺分泌功能,FGF23与FGFR-α Klotho结合形成复合物,该复合物能诱导早期生长反应因子1的表达,从而抑制PTH表达[18]。
本研究结果显示,血P,Mg,iPTH,OC,BSALP,TRACP-5b与FGF23存在明显正相关性,而血Ca,Klotho蛋白,25-OH-VD与FGF23存在明显负相关性。多元回归分析结果显示,血Ca,P,Mg,iPTH为FGF23的独立影响因素。最近研究显示,FGF23升高是导致CKD患者肾功能减退时PTH和25-OH-VD等异常变化的主要因素[19-20]。而FGF23增加却不能抑制PTH的分泌,本研究推测这可能与α Klotho-FGFR1c表达降低导致甲状旁腺对FGF23产生抵抗作用有关。综上所述,CKD 3~5期患者矿物质骨代谢紊乱逐渐加重,其与FGF23存在着明显相关性,FGF23可作为CKD患者骨代谢紊乱的有效指示因子。
