大豆磷脂酰胆碱细菌内毒素检查方法考察
2019-08-15肖婧薇王文佳何华红
肖婧薇,王文佳,何华红,李 薇
(广东省广州市药品检验所医疗器械及药包材<药理>室,广东 广州 510610)
大豆磷脂酰胆碱是大豆磷脂的主要活性成分,大豆磷脂作为天然乳化剂、增溶剂、分散剂广泛应用于药物注射剂中[1-2],故大豆磷脂酰胆碱也是一种用于注射剂的药用辅料。注射剂直接注入人体,其细菌内毒素的含量或限值有严格规定,所用辅料也必须符合相应规定。2015年版《中国药典》尚未将大豆磷脂酰胆碱作为药用辅料收载,本研究中参照2015年版《中国药典(四部)》通则1143[3]154-157“细菌内毒素检查法”,全面考察了大豆磷脂酰胆碱的细菌内毒素检查方法,以进一步控制注射剂质量。现报道如下。
1 仪器与试药
仪器:TW12型六孔恒温水浴(德国Julabo公司);MS3basic型旋涡混合器(德国IKA公司);LKL164-03型内毒素定量仪(英国Lab Kinetics公司);2-16KL型低温高速离心机(德国Sigma公司)。
试药:大豆磷脂酰胆碱(德国Lipoid GmbH,批号为579010-1150055-13,579010-1160058-15,579010-1160059-05,规格为原料,含量为98%);细菌内毒素工作标准品(中国食品药品检定研究院,批号为150601-201580,规格为每支80 EU);细菌内毒素检查用水(BET水,批号为1606290,规格为每支100 mL),鲎试剂 A(TAL,批号分别为 1606142,1607201,规格为每支0.1mL,灵敏度分别为0.25EU/mL和0.06EU/mL),鲎试剂 C(KCA,批号为1709140,规格为每支1.25 mL,灵敏度为50~0.005 EU/mL),均购自湛江安度斯生物有限公司;鲎试剂B(TAL,福州新北生物有限公司,规格为每支 0.1 mL,批号分别为 16031712,16020712,灵敏度分别为0.25 EU/mL和0.06 EU/mL)。
2 方法与结果
2.1 细菌内毒素限值
各国药典均未收载该品种,而在厂家所附标准中,细菌内毒素限值为每1 g大豆磷脂酰胆碱含内毒素的量应小于6 EU。该品种是大豆磷脂的主要活性成分,其在药物制剂中的功能和用途与大豆磷脂相似,2015年版《中国药典(四部)》收载的大豆磷脂(供注射用)[3]468-470的细菌内毒素限值为每1 g大豆磷脂含内毒素的量应小于2.0 EU。综合考虑,本研究限值确定为2.0 EU/g。
2.2 细菌内毒素含量检测(凝胶法)
2.2.1 鲎试剂灵敏度复核试验
按2015年版《中国药典(四部)》通则1143“细菌内毒素检查法”进行鲎试剂标示灵敏度(λ)复核。结果4批鲎试剂λc为0.5~2.0 λ,符合进行细菌内毒素检查的规定。详见表1。

表1 TAL灵敏度复核试验结果(凝胶法)
2.2.2 干扰预试验
最小质量浓度计算:最小有效稀释浓度C=λ/L,L=2.0 EU/g。目前用于药品检验的市售鲎试剂灵敏度一般为0.25~0.03 EU/mL,因此相对应的最小有效质量浓度为 125.00,62.50,31.25,15.62 g/L。
溶液制备:取3批样品,用BET用水溶解制成质量浓度为125 g/L的供试品溶液,置旋涡振荡器振荡5 min使充分混匀,再稀释成3个质量浓度梯度的系列溶液,标记为供试品管(NPC系列);取NPC系列溶液,加入细菌内毒素,制得每个稀释度中含2 λ细菌内毒素的供试品溶液,标记为供试品阳性对照管(PPC系列)。
操作步骤:取灵敏度为0.25 EU/mL的2个不同厂家的TAL,每个质量浓度的NPC和PPC各做2管,同时做细菌内毒素阳性对照(PC)和BET用水阴性对照(NC)各2管。结果3批样品质量浓度在62.5 g/L及以下时对2个厂家鲎试剂与细菌内毒素的反应均无干扰作用。详见表2。
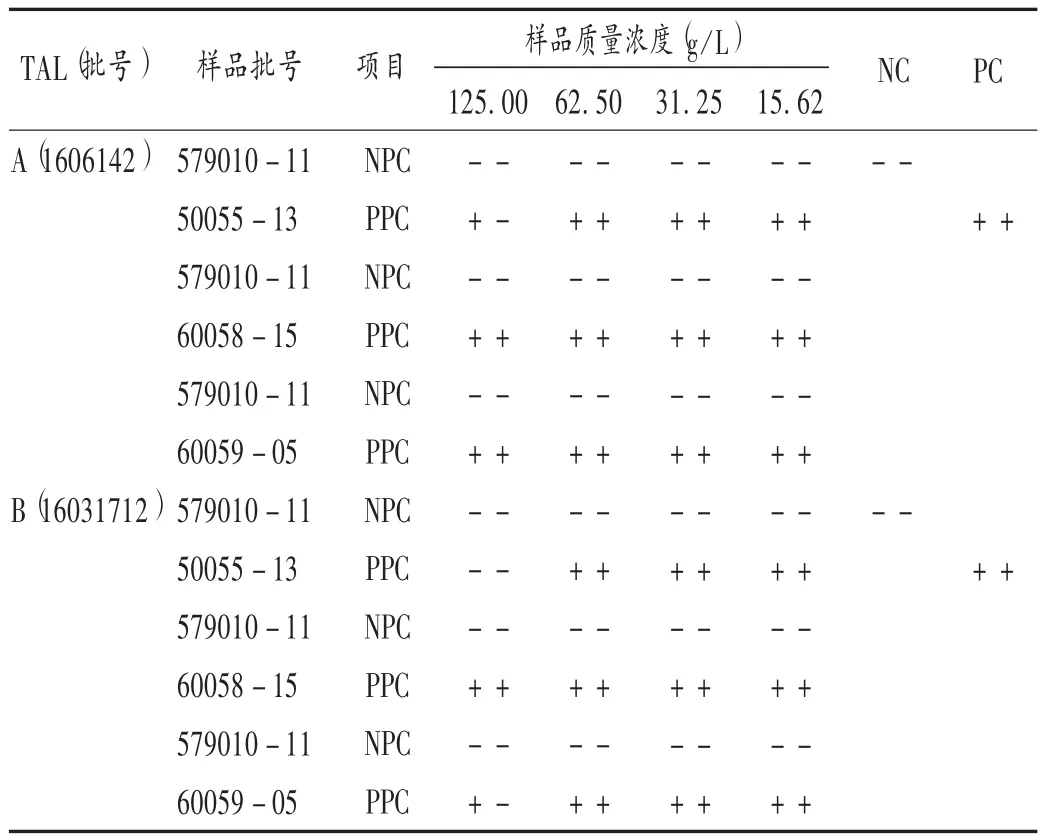
表2 样品干扰预试验结果(凝胶法)
2.2.3 正式干扰试验
取3批样品适量,分别用BET用水制成质量浓度为 62.5 g/L 的溶液,并制成含 2 λ,1 λ,0.5 λ,0.25 λ细菌内毒素的供试品溶液,取灵敏度为0.25 EU/mL的2个厂家的鲎试剂,按2015年版《中国药典(四部)》通则1143中的“干扰试验”项下方法试验。以BET用水进行对照。结果内毒素标准溶液反应终点浓度的几何平均值(Es)和供试品溶液反应终点浓度的几何平均值(Et)均在0.5 λ~2.0 λ范围内,3批样品质量浓度为62.5 g/L时对2个厂家鲎试剂与细菌内毒素的反应均无增强或抑制的干扰作用。故大豆磷脂酰胆碱(94%)的最大不干扰质量浓度为62.5 g/L。详见表3。

表3 样品干扰试验结果(凝胶法)
2.2.4 样品细菌内毒素检查
按2015年版《中国药典(四部)》通则1143中的“细菌内毒素检查法”,用灵敏度为0.06 EU/mL的鲎试剂分别对3批样品进行细菌内毒素检查,结果3批样品的细菌内毒素检查结果均符合规定。详见表4。
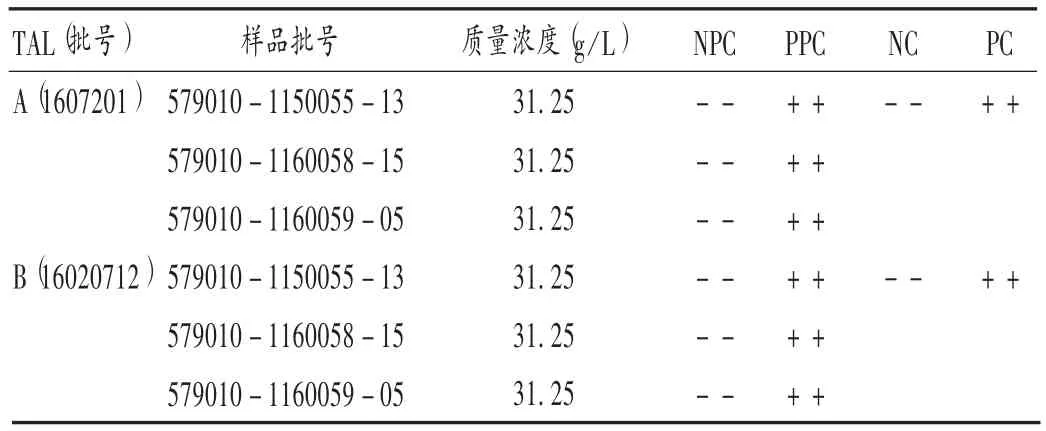
表4 样品细菌内毒素检查结果(凝胶法)
2.3 细菌内毒素含量检测(显色基质法)
2.3.1 标准曲线的可靠性试验
取1支细菌内毒素工作标准品,加入1 mL BET用水溶解,再稀释成浓度分别为 10,1,0.1,0.01 EU/mL的系列溶液,各取0.1 mL,分别与0.1 mL鲎试剂混匀,每个浓度平行做3支管,置内毒素定量仪中,在(37±1)℃下进行检测。以BET用水作阴性对照。结果回归方程为lgTg=2.881 3-0.308 0 lgC(r=-0.999 6),阴性对照的反应时间大于标准曲线最低点的反应时间,各反应点平行管之间的变异系数(CV)均小于10%,表明标准曲线可靠,试验方法成立。详见表5。
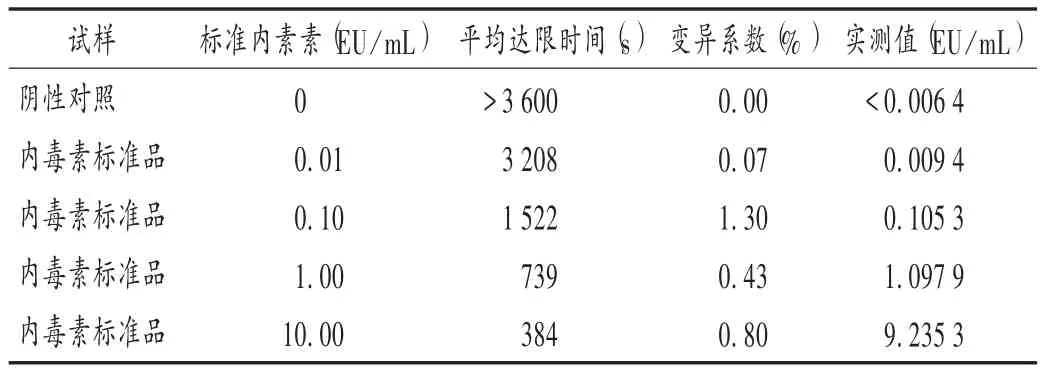
表5 标准曲线可靠性试验结果(显色基质法)
2.3.2 干扰试验
标准曲线最低点的浓度为0.01 EU/mL,故最小有效稀释质量浓度为5 g/L。取3批样品适量,用BET用水溶解成质量浓度为125 g/L的溶液,置旋涡振荡器振荡5 min,稀释成质量浓度为 62.5,31.25,15.6 g/L的系列梯度溶液,作为供试品溶液(A液);另外,制成含0.5 EU/mL细菌内毒素的供试品溶液(B液),充分振荡,215×1g离心 5 min,立即取上清液,分别取0.1 mL与0.1 mL鲎试剂混匀,每个质量浓度平行做2支管,于内毒素定量仪中进行检测。结果3批样品质量浓度在62.5 g/L及以下时,细菌内毒素的回收率在50%~200%之间,表明样品对动态显色法下鲎试剂与细菌内毒素的反应无干扰作用。详见表6。
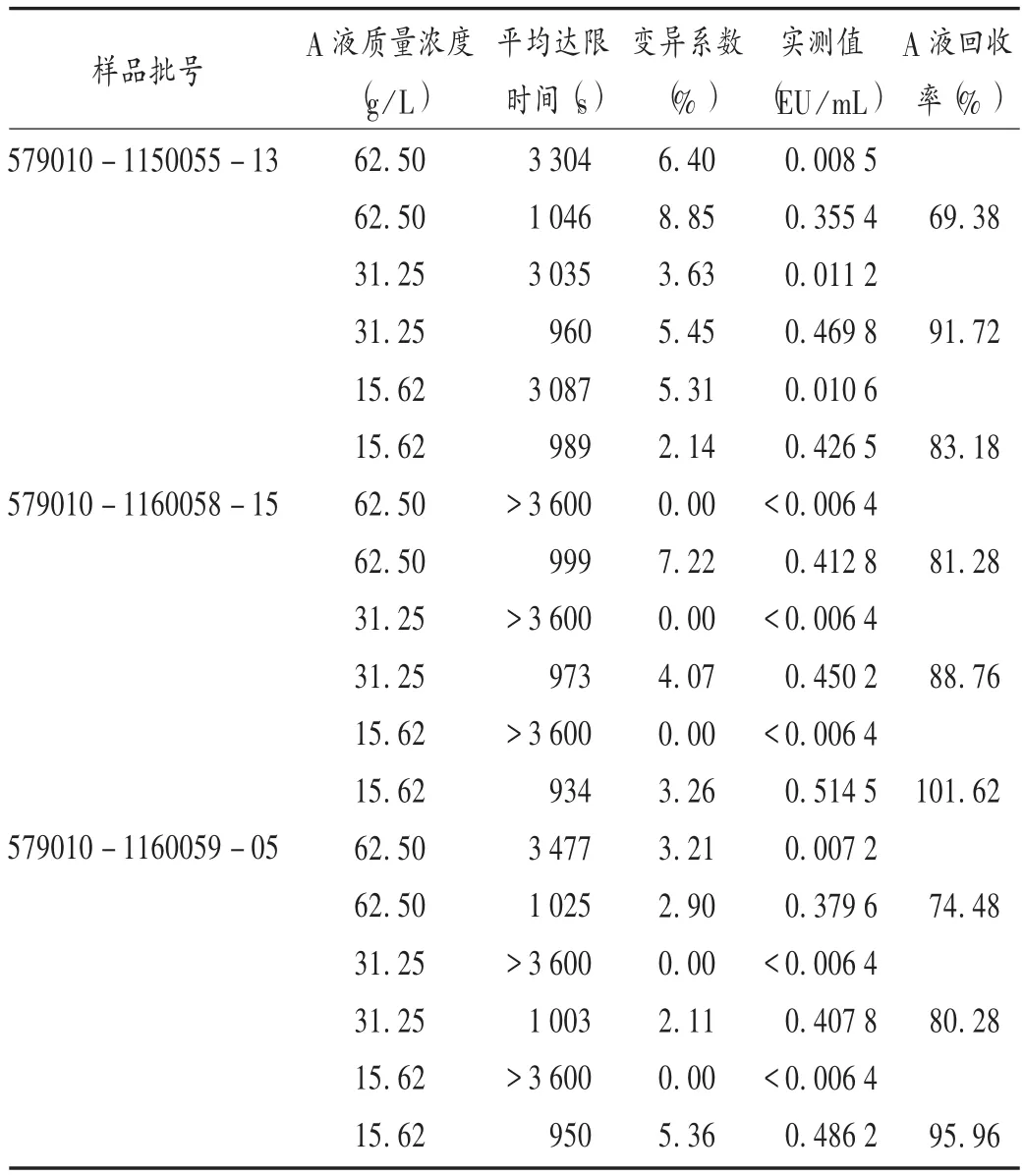
表6 样品干扰试验结果(显色基质法,n=2)
2.3.3 内毒素回收试验
3批样品各称取4份,分别用含细菌内毒素0,0.1,0.2,0.4 EU/mL的BET用水溶解成质量浓度为110 g/L的溶液(每1 g大豆磷脂酰胆碱对应的内毒素含量为0,0.9,1.8,3.6 EU),充分振荡 5 min,用 BET 用水稀释1倍,振荡均匀,215×1g离心5 min,立即取上清液进行检测。结果3批大豆磷脂酰胆碱均未检出细菌内毒素,内毒素加入量为0.05,0.10,0.20 EU/mL时的回收率均为75% ~112%,表明供试品溶液制备过程中的离心处理不会影响细菌内毒素的检出。详见表7。
3 讨论
近年来,由于药用辅料的问题导致的药品严重不良反应或影响用药安全的事件层出不穷[4-6],究其原因主要为质量标准不完善、使用方法不规范[7]。2015年版《中国药典》中药用辅料标准收载量仅270种,其中供注射用药用辅料23种,与美国药典、欧洲药典中1 000多种的收载量比相差较大,因此,药用辅料质量标准的提高和完善迫在眉睫。大豆磷脂酰胆碱作为药用辅料的新品种,其质量标准的研究和制订更应受到重视。对注射剂常用药用辅料应进行相应的安全性检查,而细菌内毒素检查是其安全性检查中必不可少的一项[3]400-402。
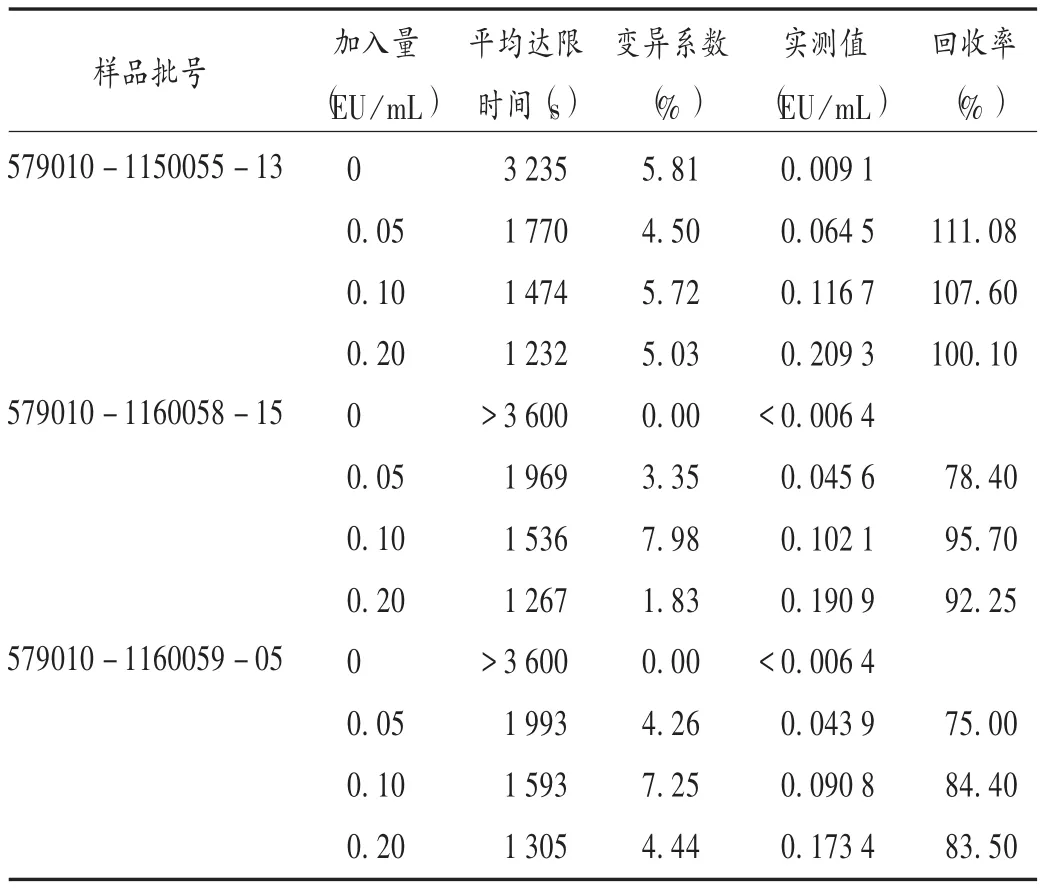
表7 回收试验结果(显色基质法)
2015年版《中国药典》收载的细菌内毒素检查法包括凝胶法和光度测定法,供试品检测时可使用其中任意一种方法,但当结果有争议时凝胶法为仲裁方法[3]154-157,因此本研究中首先采用凝胶法考察大豆磷脂酰胆碱细菌内毒素检查的可行性。结果表明,大豆磷脂酰胆碱质量浓度在62.5g/L及以下时对2个厂家生产的鲎试剂无干扰作用,但使用灵敏度为0.125~0.03 EU/mL的凝胶法鲎试剂对该品种的细菌内毒素进行定性检查,且限值可定为2.0 EU/g。
细菌内毒素检查法的光度测定法包括浊度法和显色基质法,结果可准确反映细菌内毒素的含量,对生产过程和最终产品的质量控制意义重大。大豆磷脂酰胆碱不能完全溶于水,在本试验浓度下,样品与水只能形成混悬液。混悬液的反应体系对2.2项试验反应并无影响,但对2.3项试验中吸光度的检测有一定影响,因此将供试品溶液离心,取上清液进行检测。为了考察萃取处理是否会影响细菌内毒素的检出,在配制供试品时添加细菌内毒素标准品进行外加内毒素回收试验[3]154-157。在该情况下,一般会采取特殊方法来制备供试液,如增溶[8]、萃取[9-10]、过滤[11]等,再进行外加内毒素回收试验,以考察处理方法是否会影响内毒素的检出。本研究中,前期曾尝试过加入乙醇以增加溶解性,但效果不佳,也曾尝试过微膜滤过以去除混悬液中的颗粒,但极易堵塞滤头。最后经试验证实,采用振荡混匀并离心取上清液的操作可行。但得到的供试液并非澄清透明,仍有轻度混浊,会影响浊度法中浊度的测定,而显色基质法是通过测定呈色团的吸光度来反应内毒素的含量,因此不会影响检测结果,可进一步进行干扰试验和回收试验。经考察,大豆磷脂酰胆碱在质量浓度62.5 g/L及以下时对试验结果无干扰作用,且供试液制备过程中的萃取操作不会对供试品本底细菌内毒素造成影响,可采用动态显色法鲎试剂对该品种进行细菌内毒素的定量检测。
综上所述,凝胶法与动态显色法均可用于大豆磷脂酰胆碱的细菌内毒素检查,本研究结果为该品种细菌内毒素检查方法的制订提供参考。但本试验样品量较少,要制订相关质量标准还需更多批次的试验数据加以验证。
