经导管主动脉瓣置换术治疗重度主动脉瓣狭窄合并重度二、三尖瓣关闭不全1例
2019-08-13夏成雨徐承义陈雨意
夏成雨 徐承义 陈雨意 苏
1 临床资料
患者 男性,68岁。因“活动时胸闷、气喘2年,加重3个月,晕厥1次”于2018年6月28日入住武汉亚洲心脏病医院。否认既往病史。入院查体:一般情况可,脉搏96次/分,血压96/71 mmHg(1 mmHg=0.133 kPa);颈静脉不充盈,双肺呼吸音清;心界不大,心率96次/分,律齐,胸骨右缘第2肋间可闻及收缩期3/6级喷射样杂音,向颈部传导,心尖部闻及收缩期3/6级吹风样杂音,向左腋下传导;腹平软,无压痛、反跳痛,肝、脾肋下未触及,肠鸣音正常;四肢脉搏细弱,双下肢无水肿。入院心电图示:窦性心律,完全性右束支传导阻滞,V1~V3导联ST段压低,V1导联T波倒置,V2导联T波双向(图1)。超声心动图示:三叶式主动脉瓣,主动脉瓣和瓣环钙化伴重度狭窄,开口面积0.4 cm²,峰值流速4.4 m/s,平均压差40 mmHg,峰值压差76 mmHg;二尖瓣稍厚、回声增强,收缩期瓣叶对合不良,左心房侧见重度反流信号;三尖瓣回声正常,收缩期右心房侧见重度反流信号(图2A),反流速度4.4 m/s,反流压差79 mmHg,肺动脉收缩压94 mmHg;左心室射血分数49%。实验室检查示:N末端B型脑钠肽前体(N-terminal pro-brain natriuretic peptide,NT-proBNP)14 898 pg/ml,电解质及肝、肾功能均在正常范围。主动脉CT血管造影示:主动脉瓣环、窦部、窦管交界直径分别约为25.5 mm、35.5 mm、29.7 mm,升主动脉管径约43.9 mm,主动脉瓣叶明显增厚、钙化,左、右冠状动脉瓣交界粘连。入院诊断:主动脉瓣重度狭窄并轻度关闭不全,二尖瓣、三尖瓣重度关闭不全,重度肺动脉高压,纽约心脏病协会(New York Heart Association, NYHA)心功能分级Ⅲ级。美国胸外科医师协会评分8分,两位心胸外科医师评估认定外科手术高危。
患者于导管室,全麻下、经食管超声心动图引导下行经导管主动脉瓣置换术(transcatheter aortic valve replacement,TAVR),经右侧颈内静脉入径留置临时起搏器至右心室心尖部。选右侧股动脉,Seldinger's法穿刺送入4 F动脉血管鞘,造影确认穿刺点位置良好。以右侧股动脉为主入径,先行置入2把proglide血管缝合器(雅培,美国)预处理后,置入10 F动脉鞘,沿右侧10 F股动脉鞘送入5 F AL2导管至升主动脉,交换直头导丝(可控导丝V18)跨主动脉瓣至左心室,将AL2导管沿导丝送至左心室,经AL2导管交换超硬导丝(Amplatz Super Stiff)至左心室,撤出AL2导管;撤出10 F血管鞘,沿超硬导丝置入20 F导引鞘(导引鞘-SDV,戈尔);经左侧股动脉入径送猪尾导管至升主动脉窦底;选工作体位,经动脉鞘送入球囊(20 mm×40 mm,NUMED)至主动脉瓣环水平,快速起搏(180次/分)并行瓣膜预扩张(图3A),退出球囊,沿超硬导丝送入已预装的VENUS-A L23瓣膜支架(杭州启明)至主动脉瓣处,根据猪尾导管造影调整位置良好,部分释放后快速起搏,逐步释放瓣膜支架,造影显示支架位置固定良好;造影以及经食管超声心动图提示瓣膜支架扩张不全,瓣膜轻度反流,经超硬导丝送球囊(22 mm×40 mm,NUMED)至瓣膜支架内行球囊后扩张;经猪尾导管在主动脉瓣根部造影,未见瓣膜反流(图3B)。术中经食管超声心动图评估效果满意。退出导丝,proglide缝合右侧股动脉,保留临时起搏器,余穿刺点加压包扎。术后送回冠心病重症监护室密切观察。
患者围术期未发生明显手术并发症。术后24 h内患者临床心功能显著改善,至NYHA心功能分级Ⅰ级。超声心动图示:人工瓣膜状态良好,前向血流速度2.6 m/s,峰值压差27 mmHg,平均压差9 mmHg,轻微至轻度瓣周漏,二尖瓣轻度反流,三尖瓣反流消失(图2B)。NT-proBNP水平下降至1355 pg/ml。随访45 d显示:NYHA心功能分级Ⅰ级;超声心动图提示主动脉瓣人工瓣膜状态良好、最大跨瓣压差19 mmHg,轻微瓣周漏,二尖瓣、三尖瓣轻微反流;NT-proBNP下降至441 pg/ml(表1)。
2 讨论
TAVR是近年来治疗主动脉瓣狭窄的新兴方法,其良好的安全性和有效性已得到大量研究证实。TAVR的主要适应人群为外科手术禁忌、预期寿命超过1年、症状性钙化性重度主动脉瓣狭窄的患者[1]。二尖瓣反流为主动脉瓣狭窄患者的常见合并症,在行外科主动脉瓣膜置换术的患者中高达2/3患者合并有不同程度的二尖瓣反流[2]。虽然国内部分专家共识将联合瓣膜病变列为TAVR的禁忌证[3],但是国外多项临床研究和荟萃分析表明TAVR术后多数二尖瓣反流可不同程度地改善,其改善程度与瓣膜有无器质性病变、心室及瓣环的重构以及恢复时间相关[4-7]。
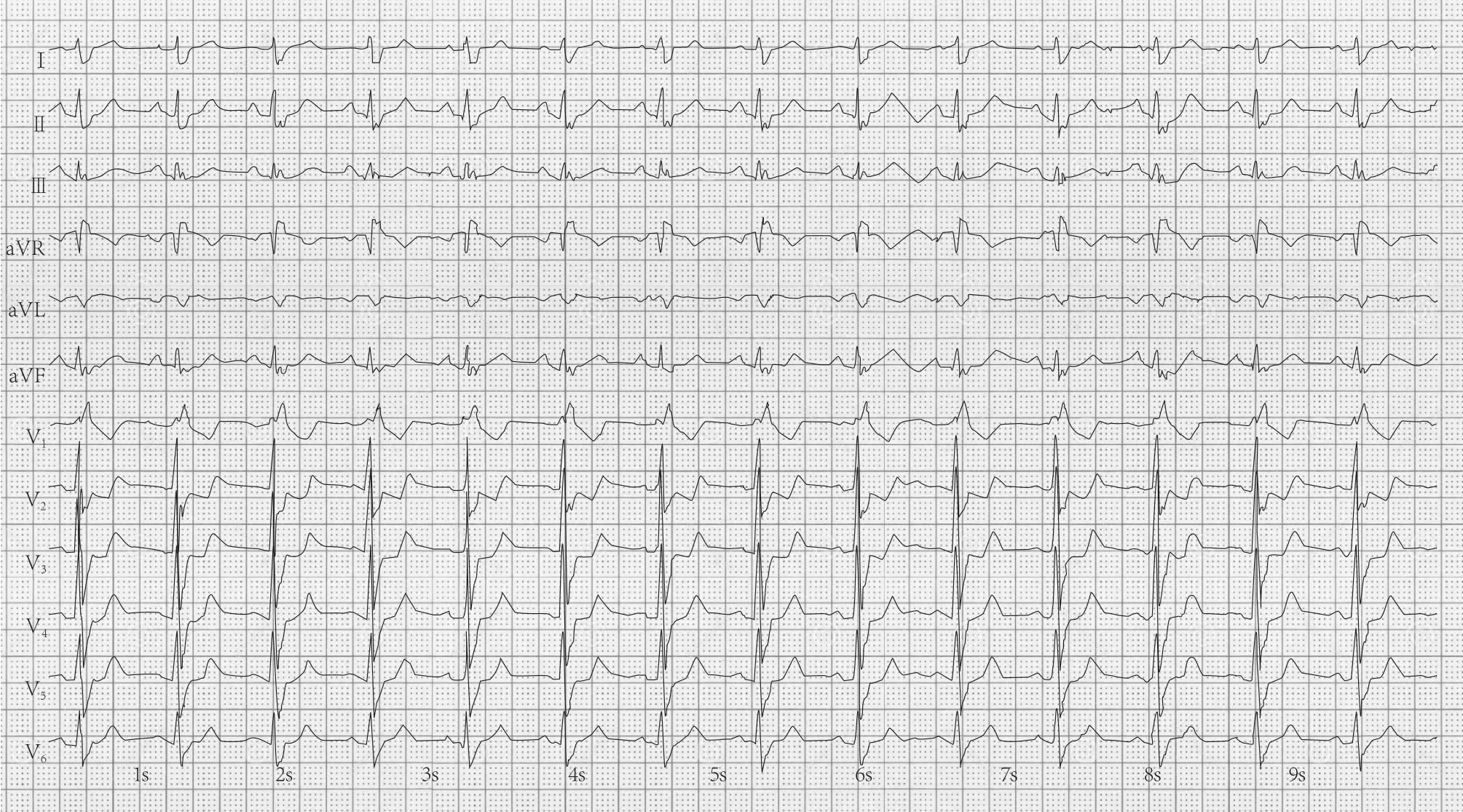
图1 入院心电图,V1~V3导联ST段压低,V1导联T波倒置,V2导联T波双向
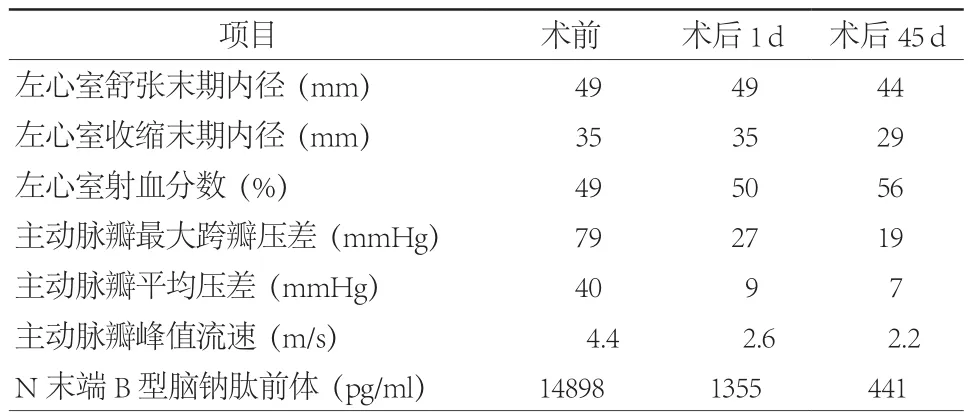
表1 患者术前、术后相关指标变化
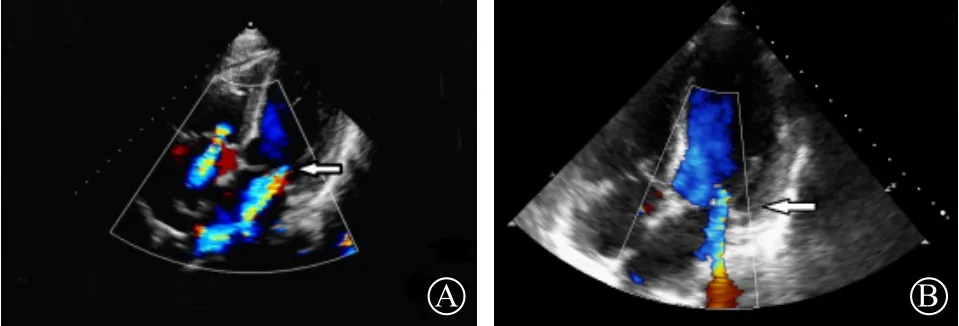
图2 超声心动图 A.术前二尖瓣重度反流伴三尖瓣反流;B.术后二尖瓣轻度反流、三尖瓣反流消失(箭头所示)

图3 经导管主动脉瓣置换术过程造影图像 A.瓣膜置入前球囊预扩张;B.瓣膜准确释放,造影未见瓣膜反流
二尖瓣瓣膜本身的病变对二尖瓣远期预后有重要影响。对于本身存在器质性二尖瓣瓣膜病变的患者,如瓣膜病变的基础病因不能得到控制,则会持续损伤二尖瓣瓣膜,即使术后患者二尖瓣恢复良好,其远期仍有进一步加重二尖瓣反流的可能。其中,对于二尖瓣存在钙化病变的患者,瓣叶的钙化程度对评估患者术后二尖瓣反流改善程度具有重要价值。钙化程度越低,其对二尖瓣运动的限制和约束也越小,术后二尖瓣反流改善越显著[8]。瓣膜功能性反流是指瓣膜存在反流,但没有器质性病变,所以功能性二尖瓣反流通常预后较好[8]。
不同患者二尖瓣反流的恢复时间不同。一项纳入4839例患者的Meta分析表明,在随访1年时间内,大部分患者二尖瓣反流持续改善[7]。也有研究观察到患者的左心室收缩期内径和舒张期内径相应缩小[8],这说明瓣膜反流远期持续改善可能得益于术后心室的慢性重构。本例患者二尖瓣及三尖瓣反流在TAVR后24 h内就得到显著改善,可能与解除主动脉狭窄后左心室及肺动脉内压力迅速减小有关。
本例患者二尖瓣及三尖瓣重度关闭不全,无严重器质性二尖瓣、三尖瓣瓣膜病变,属于功能性反流。主动脉重度狭窄引起左心室、左心房以及肺动脉压力的增高可能是导致二尖瓣及三尖瓣重度关闭不全的原因,故在解除主动脉狭窄后瓣膜反流能够得到迅速且良好的恢复。
最后,主动脉瓣重度狭窄合并多个瓣膜严重反流时,外科治疗应作为首选治疗手段[9]。对于外科高危的主动脉狭窄患者,如果合并二尖瓣功能性反流,TAVR也许可以作为一种尝试的治疗手段。现阶段虽无明确指南和专家共识可循,但相信这些问题将随着技术进步、经验的积累以及其他微创治疗手段(如二尖瓣钳夹术、经导管二尖瓣修复术)的发展而逐步得到解决, TAVR的适应证可能也将不断得到拓展。
