柚皮素自微乳不对称膜渗透泵胶囊的制备及体外评价
2019-08-02王章姐刘自平
王章姐,刘自平,许 燕,尹 伟
安徽新华学院药学院,合肥 230088
柚皮素(naringenin)是柚皮苷的苷元,属二氢黄酮类化合物,广泛存在于蔷薇科植物的花蕾中,具有抗菌、抗炎、抗氧化、抗肿瘤、降血脂、解痉和利胆等多方面药理作用。柚皮素几乎不溶于水,常规口服剂型生物利用度较低、半衰期短,可通过改进其口服剂型,提高水溶性,延长半衰期,从而达到提高生物利用度的目的[1-3]。
1982年,日本学者Kawashima发明了球晶造粒技术(spherical crystallization technique),并用该技术在液相中通过一个步骤即完成了水杨酸的结晶、析出和凝聚成粒等过程[4]。该技术流程简单、所用设备少,简化了传统制粒工艺,改善了药物颗粒的粉体流动性、填充性和压缩成形性,制成的颗粒可直接用于压片。球晶造粒技术关键在于溶剂系统的选择,原则上为3溶剂系统:架桥剂、良溶剂和不良溶剂,根据药物的理化性质有时不需架桥剂,仅采用良溶剂和不良溶剂系统就可完成。选择合适的溶剂系统,将自微乳作为主药,利用球晶造粒技术将其在液相中一步固化成粒,可构建出稳定性高、载药量大的固体自微乳释药系统。
渗透泵制剂因其显著的释药特性,已经成为理想的一种控释制剂。其释药动力来源于渗透泵膜内外的渗透压差,在机体内不易受酸、碱、酶及食物等因素的影响,能维持长时间恒速释药,表现为零级释药特征[5]。不对称膜(asymmetric membrane,AM)是指一种断面结构不相对称的半透膜,由基底层和表皮层两部分组成。其中,基底层较厚且具有疏松的海绵状多孔,主要起支撑和抗压作用,其厚度决定膜的机械强度;表皮层为活性控释层,薄且致密,可控制水分渗透、减少时滞时间、促进药物释放[6]。以AM作为半透膜制成新型渗透泵制剂,可显著提高难溶性药物的释放速率,且具有高选择性、高渗透性、高水通量以及良好体内外相关性的特点[7]。本研究运用球晶造粒技术和不对称膜技术制备柚皮素自微乳不对称膜渗透泵胶囊,可提高难溶性药物柚皮素的水溶性和生物利用度,保证药物在低渗透压和低溶解度条件下完全释药,解决难溶性药物制成渗透泵释药不完全的问题,制剂工艺简单,使得自微乳渗透泵控释胶囊在缓控释领域有广泛的应用前景。
1 仪器与材料
1.1 仪器
CHY-C2A薄膜测厚仪,济南兰光机电技术有限公司;AS3120型超声清洗器,Autoscience公司;CP2115D电子天平,Satorius公司; 85-2 恒温磁力搅拌器,金坛市金分仪器有限责任公司;HH-S2恒温水浴锅,江苏省金坛市环宇科学仪器厂;ZEN 3690 Malvern粒径电位测定仪,英国马尔文仪器有限公司;HT7700-SS 透射电子显微镜,日本日立公司;Agilent 1100 高效液相色谱仪;美国安捷伦公司;Agilent G1315A 紫外检测器,美国安捷伦公司;XB C18色谱柱(Welch ,250 mm×4.6 mm,5μm); Heraeus Multifuge X1R 离心机,赛默飞世尔科技公司;ZRS 8G智能溶出仪,天津大学无线电厂。
1.2 材料与试剂
柚皮素原料,批号20160725,质量分数98%,成都康辉生物科技有限公司;柚皮素对照品,中国药品生物制品检定所,批号120546-201409,质量分数99%;醋酸纤维素(CA),中国医药集团上海化学试剂公司);乙基纤维素(EC,10cp),卡乐康公司;微粉硅胶(SiO2),安徽山河药用辅料有限公司;十二烷基硫酸钠(SDS),安徽山河药用辅料有限公司;硬脂酸镁(MS),安徽山河药用辅料有限公司;滑石粉,安徽山河药用辅料有限公司;水为超纯水;乙腈、甲醇为色谱纯;其余试剂均为分析纯。其他试剂均为分析纯。
2 方法与结果
2.1 含量测定条件与方法
2.1.1 色谱条件
色谱柱为C18柱(300 mm×3.9 mm,4 μm),流动相为甲醇:水:冰醋酸(49∶50∶1),检测波长288 nm,体积流量1.0 mL/min,柱温40 ℃,进样量20 μL。
2.1.2 标准曲线制备
分别精密量取柚皮素对照品储备液0.5、1、1.5、2、2.5 mL,置20 mL容量瓶中,加甲醇定容,摇匀得质量浓度为25.5、51.0、76.5、102、127.5 μg/mL的对照品溶液,分别取上述对照品溶液20 μL注入高效液相色谱仪,记录色谱峰面积,以峰面积积分值(Y)对柚皮素质量浓度(X)作线性回归,得回归方程为y=70 368x-46 758,R2=0.999 9,表明柚皮素在25.5~127.5 μg/mL线性关系良好。
2.1.3 释放度测定
参照《中华人民共和国药典》2015年版第四部通则0931释放度测定第二法,采用溶出度测定第一法的装置[9],测定柚皮素自微乳不对称膜渗透泵胶囊的体外累积释放度。释放介质为经脱气处理的双蒸水900 mL(含0.5%SDS),转速75 rpm,释放介质温度恒定在(37±0.5)℃。于2、4、6、8、10、12、14、16、18、20、22、24 h分别取样5 mL,并补充等体积同温释放介质,用0.45 μm微孔滤膜滤过,取续滤液稀释至适宜浓度,于288 nm处测定峰面积,计算药物累积释放度。
2.2 柚皮素自微乳的制备
在前期研究基础上[8],精密称取51 g聚山梨酯80,33 g PEG400,16 g油酸乙酯,混匀后加入35 g柚皮素原料,置超声清洗仪中超声振荡使柚皮素充分溶解,即得柚皮素自微乳。
2.3 柚皮素固体自微乳的制备
运用球晶造粒技术制备柚皮素固体自微乳,将盛有不良溶剂的烧杯置恒温水浴锅中,精密称取处方量的柚皮素自微乳,溶于良溶剂和架桥剂溶液中,再加入一定量的分散载体形成均匀混悬液,在恒温、搅拌的条件下倒入盛有不良溶剂的烧杯中,持续恒温搅拌30 min,即得。
2.4 球晶造粒技术筛选固体自微乳处方
2.4.1 分散载体的考察
固定其他处方和工艺条件,分别选择滑石粉、微粉硅胶、硬脂酸镁为分散载体,考察其对柚皮素固体自微乳成球性的影响。由表1可知,滑石粉不易成球,微粉硅胶和硬脂酸镁均可成球,但成球形态有所差异,微粉硅胶成球效果优于滑石粉和硬脂酸镁,选择微粉硅胶作为分散载体。

表1 分散载体对于成球性的影响Table 1 The effects of dispersion carriers on the microspheres
2.4.2 不良溶剂用量考察
根据预实验结果,选择液体石蜡作为不良溶剂,以产率为指标,考察其用量。由实验可知,液体石蜡体积在100 mL和125 mL时得球率相对较高,且两者相差不大,故选择液体石蜡体积为100 mL。
2.4.3 良溶剂用量考察
根据预实验结果,选择无水乙醇作为良溶剂,以产率为指标,考察其用量,选择利于成球的最佳良溶剂系统。从实验结果可以看出,当无水乙醇用量为7 mL时自微乳浓度达到饱和状态,收率最高,故乙醇最佳用量选择7 mL。
2.4.4 系统温度的考察
系统温度会影响自微乳的稳定性,同时对成球性也有一定的影响,根据预实验,设定系统温度的范围18~40 ℃,选择有利于成球的最佳温度。通过实验可知,反应温度对于收率影响比较显著,温度在25 ℃时收率最高,故选择25 ℃作为系统温度。
2.4.5 搅拌时间的选择
以产率为指标,考察搅拌时间对制备柚皮素固体自微乳的影响。当搅拌时间为30 min时,成球率有较大提升,继续增加搅拌时间至40、50 min 收率基本无变化,因此设定搅拌时间为30 min。
2.4.6 搅拌速度的选择
考察不同转速对成球性能的影响。当转速在300~500 rpm时收率变化不大,转速在400 rpm时相对较高,且随着搅拌速度的加快,颗粒直径逐渐变小,产率略有下降,所以选择400 rpm作为搅拌速度。
2.5 柚皮素固体自微乳的质量评价
2.5.1 柚皮素固体自微乳形态
取柚皮素固体自微乳约1 g,于37 ℃水浴加入100倍同温蒸馏水,在100 rpm转速下制备成微乳,滤膜过滤后,取适量柚皮素微乳,滴至覆有碳膜的铜网上,用2%磷钨酸(氢氧化钠调节pH至7.0)负染,自然挥干,用滤纸吸干铜网边缘多余染液,于透射电镜(TEM)下观察微乳形态,结果见图1(A),微乳非连续相粒子呈球形乳滴,分布较为均匀。
2.5.2 柚皮素固体自微乳粒径分布
取“2.5.1”项下所得微乳,过滤后用激光粒径电位测定仪,粒径分布图见图1(B)。由图可知,柚皮素固体自微乳乳化后其粒径为14.89 nm。

图1 柚皮素固体自微乳透射电子显微镜及粒径分布图Fig.1 TEM and particle size distribution of naringenin solid self-microemulsifying
2.5.3 柚皮素固体自微乳流动性考察
2.5.3.1 休止角
将漏斗水平放置于平面上,取一定量待测物,在一定振动频率下使柚皮素固体自微乳通过漏斗均匀流出,直至获得最高的圆锥体,测量圆锥体斜面与平面的夹角,即得休止角,重复5次,取其平均值,由表2可以看出,休止角小于30°,其流动性较好。
2.5.3.2 卡式指数
取待测柚皮素固体自微乳,在一定振动强度下使待测物均匀由漏斗流入10 mL量筒中,精确称重,计算松密度ρ0;采用轻敲法使其在量筒中处于最紧实状态,计算振实密度ρf。通过公式C=(1-ρ0/ρf)×100%计算卡式指数,重复测定5次,结果见表2。由结果可知,卡式指数在15%~25%之间,表明其可压性和填充性较好。
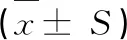


项目名称Project name结果Results休止角Angle of rest28.6±1.3卡式指数Card index19.38±0.82
2.6 不对称膜渗透泵胶囊壳的制备
本实验采用浸入沉淀法进行湿法相转移实现不对称膜的制备,根据前期预实验结果及相关文献,以醋酸纤维素为成膜材料,丙酮:无水乙醇(4∶1)为混合溶剂,甘油为致孔剂[10,11]。称取处方量的醋酸纤维素、致孔剂,加入混合溶剂搅拌溶解混匀,配成囊壳聚合物膜材溶液,用栓模浸入上述溶液中,慢慢退出,再慢慢旋转栓模,以确保聚合物膜材涂布均匀,再将栓模浸入10%的甘油溶液中,待浸入一定时间后,将栓模从甘油中取出,室温下干燥、剥离、剪切得不对称膜渗透泵胶囊壳囊帽和囊体[12]。
2.7 星点设计效应面法优化不对称膜渗透泵胶囊壳制备工艺
2.7.1 实验设计[13]
根据前期预实验和单因素实验的考察,仅确定了影响不对称膜渗透泵囊壳制备工艺的因素及范围,其工艺需进一步优化,本实验选取醋酸纤维素浓度(X1)、栓模浸入聚合物溶液中时间(X2)、栓模浸入淬火液中时间(X3)为考察因素,用薄膜测厚仪测定不对称膜渗透泵胶囊壳厚度,以药物24 h累积释放度(Y1)和不对称膜渗透泵胶囊壳厚度(Y2)为评价指标,采用星点设计效应面法优化不对称膜渗透泵胶囊壳的制备工艺,因素水平见表3,试验设计与结果见表4。
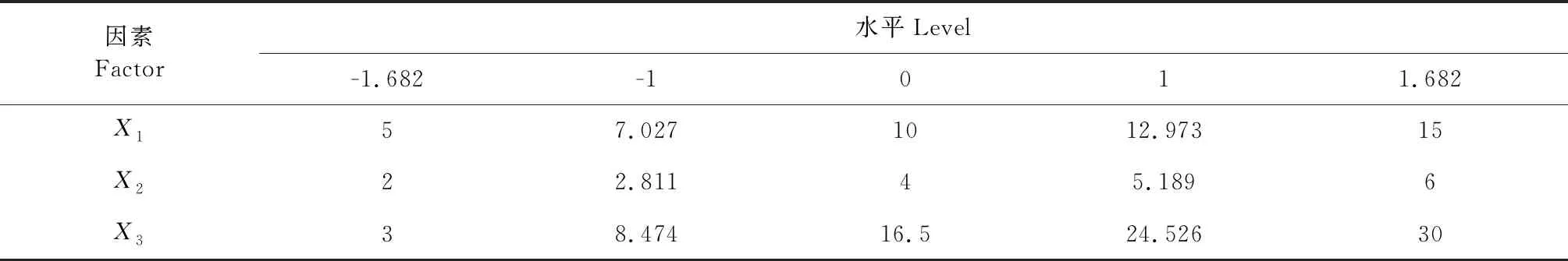
表3 因素水平表Table 3 Factors and levels
表4 实验设计与结果 Table 4 Arrangement and results
续表4(Continued Tab.4)

序号No.X1(%)X2(min)X3(min)Y1(%)Y2(mm)1015416.581.480.5751110216.586.50.2751210616.581.550.26213104387.850.564141043092.520.64915~2010416.595.790.27
2.7.2 模型拟合

2.7.3 效应面优化
采用Design Expert 8.0软件绘制不同影响因素对于响应值的三维曲线,分别固定醋酸纤维素浓度、栓模浸入聚合物溶液中时间、栓模浸入淬火液中时间3个影响因素其中之一,考察其他2个因素对药物累积释放、不对称膜渗透泵胶囊壳厚度的效应曲面图,结果见图2。根据方程和响应面图确定不对称膜渗透泵胶囊壳最佳工艺是: 醋酸纤维素浓度为9.44%,栓模浸入聚合物溶液中时间3.77 min,栓模浸入淬火液中时间15.86 min。
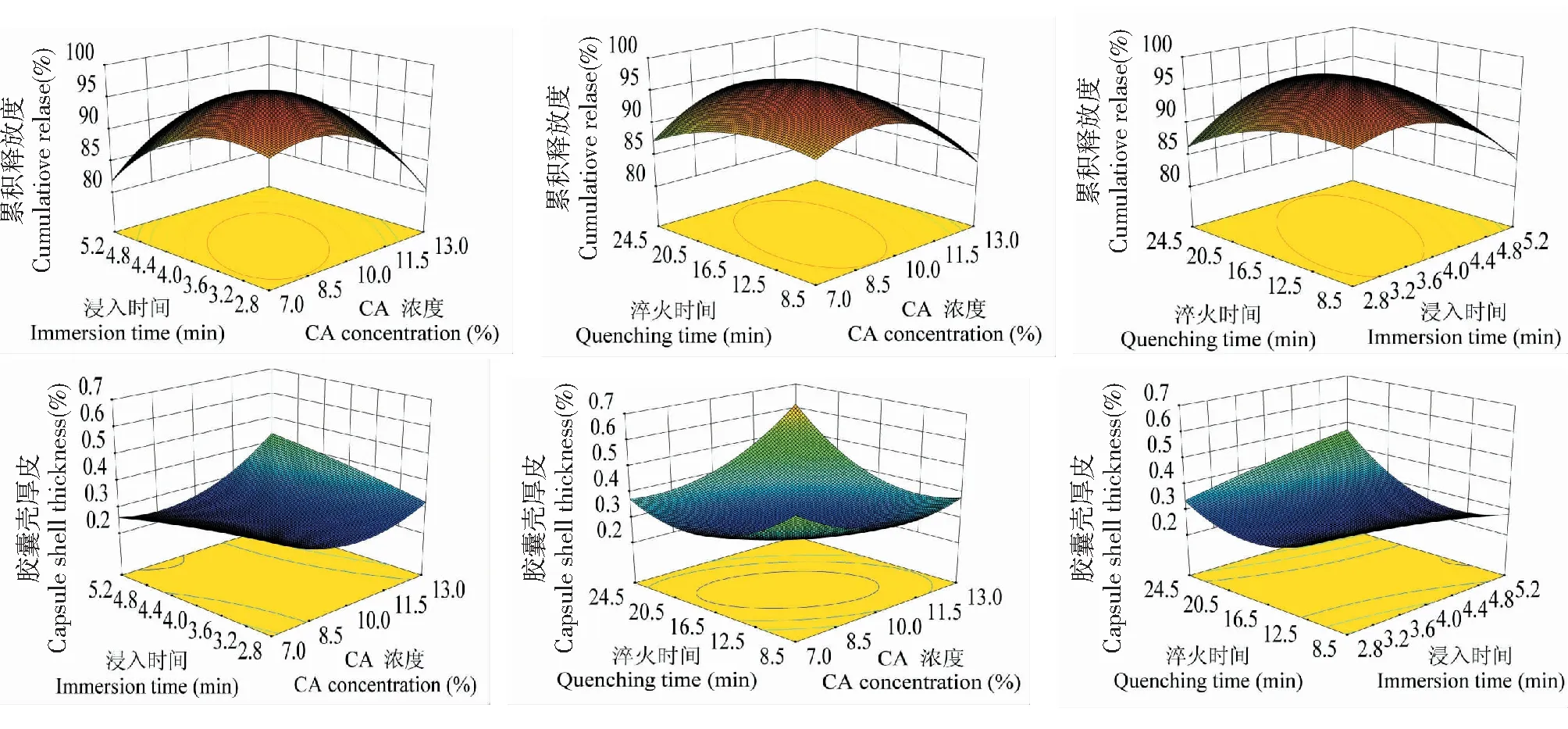
图2 药物累积释放度,胶囊壳厚度的效应面的三维图Fig.2 Response surface plot (3D) of cumulative drug release and capsule shell thickness
2.8 验证试验
根据优化的最佳制备工艺:取80 mL丙酮与20 mL无水乙醇混合,作为混合溶剂;称取10 g甘油置上述混合溶剂中搅拌溶解,再加入9.44 g醋酸纤维素,配成囊壳聚合物膜材溶液;用栓模浸入囊壳聚合物膜材溶液中3.77 min,慢慢退出,再慢慢旋转栓模,以保证聚合物膜材涂布均匀,将栓模浸入10%甘油溶液中15.86 min,将栓模从甘油中取出,室温下干燥,栓模上剥离,剪切得不对称膜渗透泵胶囊壳囊帽和囊体;称取柚皮素固体自微乳,按“2.9”项下的方法制备胶囊,测定其药物累积释放度与囊壳厚度,结果见表4。其中偏差=(预测值-实测值) / 预测值。通过验证实验可知,星点设计效应面法所建立的模型预测性良好,方法可行,结果可靠,可较好地应用于不对称膜渗透泵胶囊壳制备工艺的优化。
2.9 柚皮素自微乳不对称膜渗透泵胶囊的制备
取柚皮素固体自微乳适量,直接灌装于不对称膜渗透泵胶囊壳中,灌装后在囊帽与囊体接口处涂上胶液,晾干,即得;胶囊内容物总量为0.25 g,每粒胶囊含柚皮素152.5 mg。

表5 星点设计效应面优化法验证Table 5 Verification of the central composite design-response surface methodology
2.10 装量差异检查
渗透泵胶囊理论装量为0.25 g,混合好的柚皮素固体自微乳用胶囊板手工装3批,每批取10粒,进行装量差异检查,测得平均装量为0.253 8 g,上限为0.265 9 g(+4.8%),下限为0.236 3 g(-6.9%),符合《中国药典》2015版相关规定,故采用1号胶囊,装量为0.25 g。
2.11 体外释药行为的考察
2.11.1 转速对药物释放的影响
按“2.1.3”项下释放度测定法,分别测定制剂在转速为50、100、150 rpm下24 h内的释放度,由图3可显示,不同转速对药物释放基本无影响,可预测制剂在体内释放几乎不受胃肠道蠕动影响。

图3 不同转速对释放的影响Fig.3 Effect of rtation rate on drug release
2.11.2 不同释放介质对药物释放的影响
按“2.1.3”项下释放度测定法,分别测定释放介质为0.1 mol/L盐酸、pH4.5乙酸盐缓冲液、pH6.8和pH8.6磷酸盐缓冲液24 h内的释放行为。结果见图4,由图可知,在不同释放介质中药物的释放几乎无差异,故释放介质的类型不影响释药行为。
2.12 释药模型拟合
采用Origin8.0分别对柚皮素自微乳不对称膜渗透泵胶囊体外释药曲线进行零级模型、一级模型、Higuchi模型拟合,结果见表6。

图4 不同释放介质对释放的影响Fig.4 Effect of media on drug release

模型Model拟合方程Fitting equationR零级模型Zero modelY=3.76t+2.580.999 7一级模型Level 1 modelY=-987 25(1-e0.000 039 6t)0.998 5Higuchi模型Higuchi modelY=24t1/2-320.985 8
由相关系数R可知,体外释放模型拟合接近程度依次为:零级模型>一级模型>Higuchi模型,以零级释药方程拟合时,其R值最大且更接近1,结果表明柚皮素自微乳不对称膜渗透泵胶囊体外释放符合零级释药模型,即柚皮素以恒速释药,达到了设计目的和要求。
2.13 自微乳渗透泵胶囊和柚皮素渗透泵胶囊体外释放行为的比较
将柚皮素按照“2.9”项下方法制备柚皮素渗透泵胶囊,并按“2.1.3”项下方法进行体外释放度考察,结果见图5。由结果可知,柚皮素渗透泵胶囊在24 h内累积释放度仅为21.2%,而其自微乳渗透泵胶囊在同样时间内累积释放度达90%以上。故有必要采用自微乳技术制备柚皮素渗透泵胶囊,从而提高药物的溶解度。
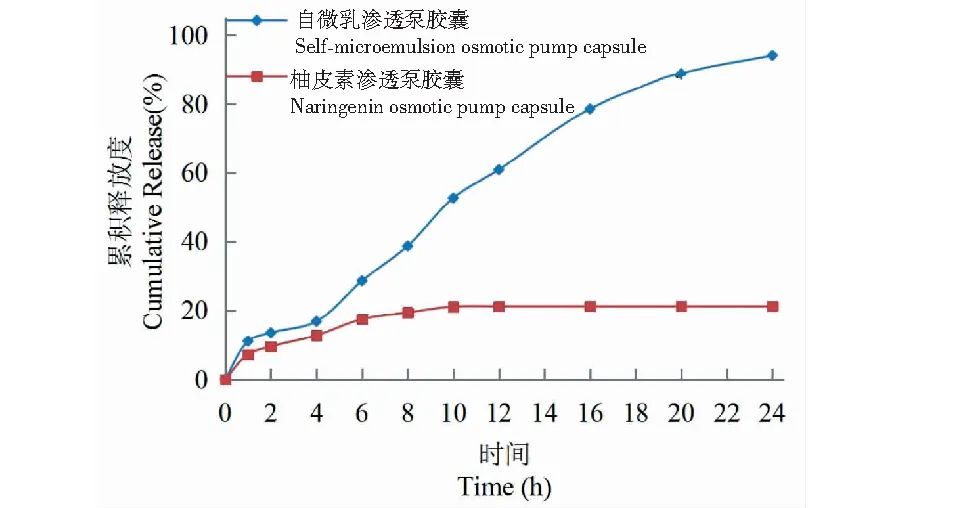
图5 柚皮素渗透泵胶囊与自微乳渗透 泵胶囊体外释药的比较(n=3) Fig.5 Comparison of naringenin release in vitro between osmotic pump capsules and microemulsion osmotic pump capsules (n=3)
3 结论
本实验采用球晶造粒技术固化柚皮素自微乳,工艺简单方便。在球晶造粒过程中使用了微粉硅胶,其主要作用是降低乳滴在固化过程中的粘性,且成球性较好。良溶剂和不良溶剂体系直接影响能否成球,本实验中选择的无水乙醇和液体石蜡作为溶剂系统,成球效果好,得率高。
本研究将自微乳与不对称膜渗透泵胶囊相结合制得新型药物传递系统,可双重解决难溶性药物柚皮素的水溶性和控释制剂释药不完全的问题,显著提高难溶性药物的生物利用度。
以醋酸纤维素浓度、栓模浸入聚合物溶液中时间、栓模浸入淬火液中时间为考察因素,采用星点设计效应面法优化不对称膜渗透泵胶囊壳的制备工艺,其试验次数少、精度高,充分考虑各因素之间的交互作用,运用非线性方程模型拟合,所建立的模型相关系数较高,预测性较好。
本实验所制得的柚皮素自微乳不对称膜渗透泵胶囊,其释药曲线以不同模型进行拟合,通过拟合结果可知,零级模型R值最大且更接近1,说明柚皮素自微乳不对称膜渗透泵胶囊达到了控释制剂的设计要求。但其体内外相关是否良好等需进一步深入研究。
