含替诺福韦的一线HAART方案治疗HIV感染/AIDS患者的疗效及治疗失败的影响因素▲
2019-08-01蒋忠胜苏明华温小凤江建宁
覃 川 蒋忠胜 苏明华 温小凤 江建宁,3
(1 广西医科大学第一附属医院感染性疾病科,南宁市 530021,电子邮箱:quest2009@126.com;2 广西柳州市人民医院感染病科,柳州市 545006;3 广西艾滋病防治研究重点实验室,南宁市 530021)
高效抗逆转录病毒治疗(highly active antiretroviral therapy,HAART)应用于临床后,大多数HIV感染/AIDS患者体内的病毒复制得到抑制,从而降低了AIDS的发病率及死亡率[1]。替诺福韦是核苷类逆转录酶抑制剂中具有代表性的一线抗病毒药物。2010年我国新修订的AIDS诊疗指南及抗病毒治疗规范推荐替诺福韦/齐多夫定+拉米夫定+依非韦伦/奈韦拉平作为一线抗病毒方案[2-3]。目前,对于含替诺福韦的一线HAART方案的抗病毒疗效尚存在争议。本研究主要探讨含替诺福韦的一线HAART方案的疗效,分析HAART方案治疗失败的影响因素,以期为国内HAART临床实践提供循证依据。
1 资料与方法
1.1 临床资料 选择2009年12月至2013年8月,在广西医科大学第一附属医院AIDS抗病毒治疗门诊、柳州市人民医院感染病科AIDS抗病毒治疗门诊采用HAART方案治疗的409例HIV感染/AIDS患者为研究对象。纳入标准:由省级或市级疾控中心经过HIV抗体确认实验确诊;符合《艾滋病诊疗指南(2011年版)》[3]中关于HIV感染或AIDS的诊断标准;年龄≥18岁,接受HAART方案治疗≥24个月,服药依从性≥95%。排除标准:既往接受过HAART方案治疗的非初治患者;初始HAART方案不含替诺福韦,但在采用HAART方案治疗期间换用包含替诺福韦的一线HAART方案患者。409例患者中,男295例,女114例,年龄(43.0±12.0)岁,无停药、死亡及其他原因终止治疗的病例。以初始HAART方案为替诺福韦+拉米夫定+奈韦拉平/依非韦伦的169例患者为替诺福韦组,其中,采用替诺福韦+拉米夫定+依非韦伦方案共168例,替诺福韦+拉米夫定+奈韦拉平方案共1例;以初始HAART方案为齐多夫定/司他夫定+拉米夫定+奈韦拉平/依非韦伦的240例患者为非替诺福韦组,其中采用齐多夫定+拉米夫定+奈韦拉平共63例,司他夫定+拉米夫定+奈韦拉平共66例,齐多夫定+拉米夫定+依非韦伦共40例,司他夫定+拉米夫定+依非韦伦共71例。两组患者的基线资料差异无统计学意义(均P>0.05),见表1。
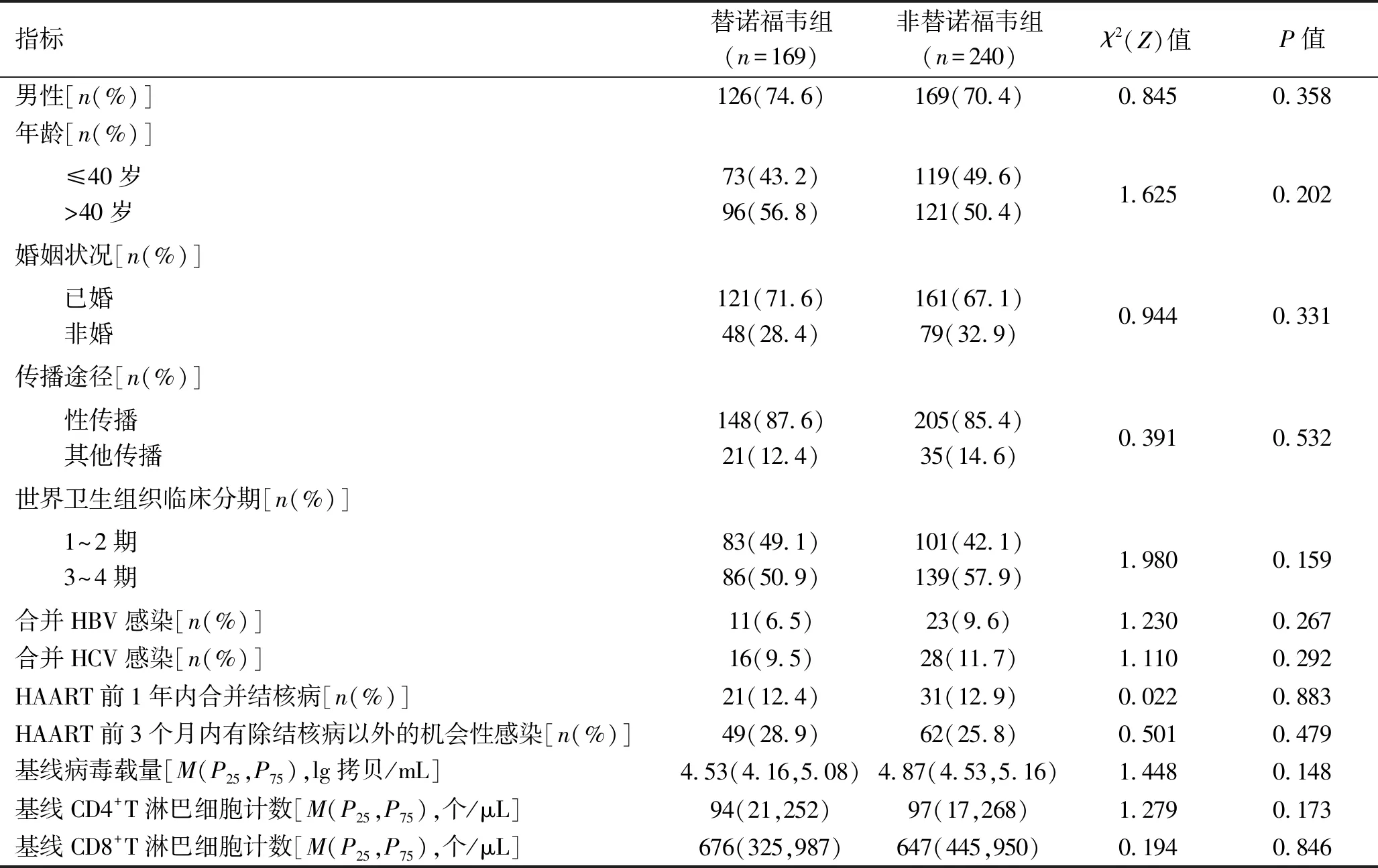
表1 两组的基线资料比较
注:非婚包括离异、丧偶、未婚、分居;其他传播途径包括静脉吸毒、输血传播。
1.2 资料收集 (1)收集所有患者的基线资料,包括一般资料[性别、年龄、婚姻、传播途径、临床分期(世界卫生组织分期法)],是否合并HBV感染、HCV感染、结核病及其他机会性感染,基线CD4+、CD8+T淋巴细胞计数,病毒载量。(2)随访资料:HAART启动后,第1年每3个月检测1次CD4+及CD8+T淋巴细胞计数,第2年每6个月检测1次CD4+及CD8+T淋巴细胞计数;每12个月检测1次病毒载量。记录所有患者治疗24个月内的CD4+及CD8+T淋巴细胞计数、病毒载量及治疗失败情况。病毒载量采用以10为底的对数表示,即病毒载量(lg拷贝/mL)=lg实测病毒载量数值;某时点CD4+T淋巴细胞计数增幅=(随访值-基线值)/基线值×100%。
1.3 治疗失败的标准 参照世界卫生组织的抗病毒治疗指南[4],将治疗失败定义为病毒学和(或)免疫学失败。(1)免疫学失败:HAART启动后,CD4+T淋巴细胞计数连续2次低至或低于基线水平,或连续2次较峰值下降>50%;或HAART时间≥1年,CD4+T淋巴细胞计数仍<100个/μL。(2)病毒学失败:HAART时间≥6个月,病毒载量仍>1 000拷贝/mL(1 000拷贝/mL=3 lg拷贝/mL)。
1.4 统计学分析 采用SPSS 19.0统计软件进行统计学分析。计量资料以M(P25,P75)表示,组间比较采用秩和检验;计数资料以例数(百分比)表示,组间比较采用χ2检验;采用Logistic回归模型分析HAART治疗失败的影响因素。以P<0.05为差异有统计学意义。
2 结 果
2.1 两组患者的治疗失败情况比较 治疗24个月内,共48例患者出现治疗失败,其中病毒学失败30例,免疫学失败29例,同时出现免疫学及病毒学失败11例。替诺福韦组的治疗失败率、病毒学失败率、免疫学失败率均低于非替诺福韦组(均P<0.05),见表2。
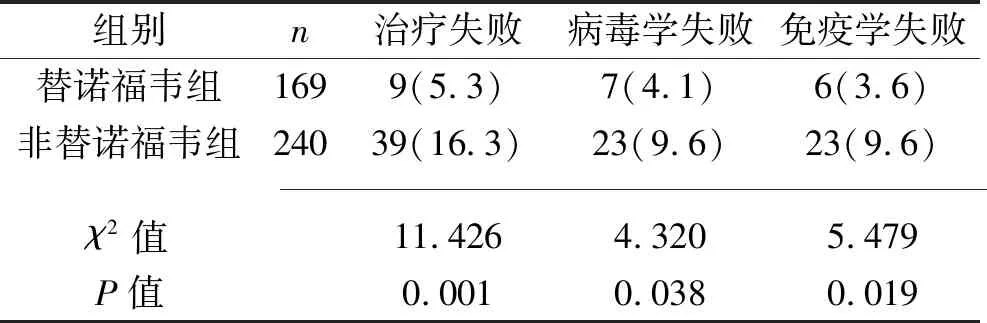
表2 两组的治疗失败情况[n(%)]
2.2 治疗过程中两组患者的免疫学应答情况 两组患者治疗后各时点的CD4+、CD8+T淋巴细胞计数均较基线时升高,且替诺福韦组在治疗第3、6、9、12个月的CD4+T淋巴细胞计数高于非替诺福韦组(均P<0.05)。两组治疗后各时点的CD4+T淋巴细胞计数增幅及CD8+T细胞计数比较,差异均无统计学意义(均P>0.05)。见表3~5。
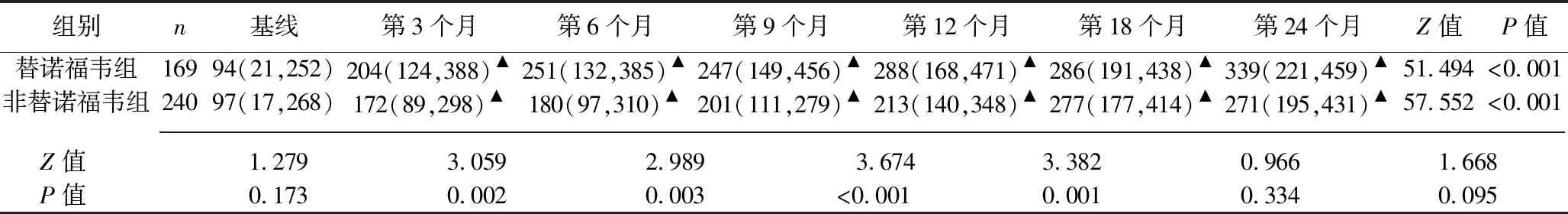
表3 两组CD4+T淋巴细胞计数比较[M(P25,P75),个/μL]
注:与基线相比,▲P<0.05。
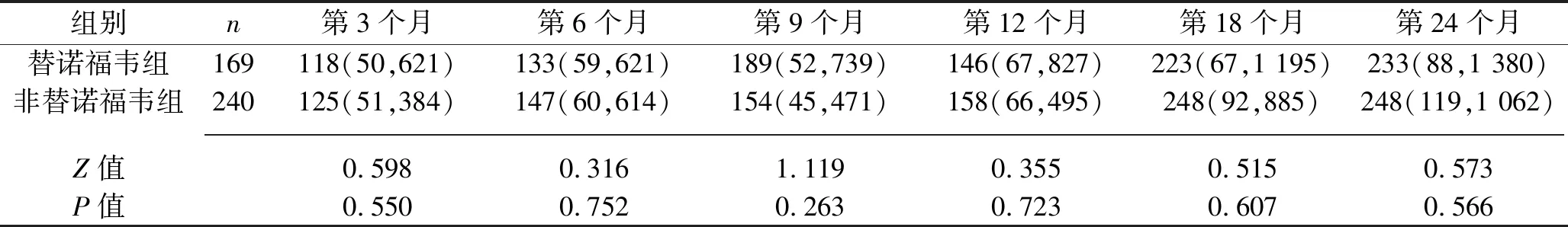
表4 两组CD4+T淋巴细胞计数较基线值增幅比较[M(P25,P75),%]

表5 两组CD8+T淋巴细胞计数比较[M(P25,P75),个/μL]
注:与基线比较,▲P<0.05。
2.3 两组患者的病毒学应答情况 HAART治疗后第12个月及第24个月,两组患者的病毒载量水平均较基线降低(均P<0.05);各时点两组患者的病毒载量水平比较,差异均无统计学意义(均P>0.05)。见表6。
2.4 HAART治疗失败的影响因素 以性别等基线资料为自变量,以HAART治疗失败与否为因变量,纳入Logistic回归模型分析,变量赋值见表7。结果显示,基线CD4+T淋巴细胞计数降低、HAART初始方案未包含替诺福韦是HAART治疗失败的危险因素(均P<0.05),见表8。
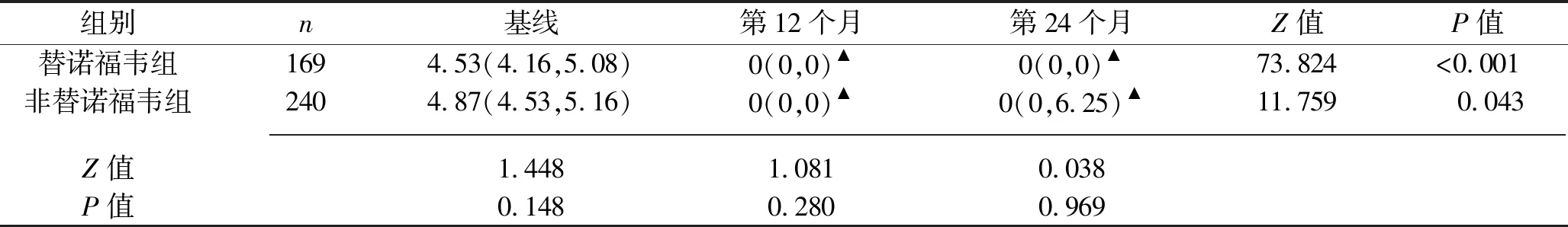
表6 两组患者治疗后病毒载量比较[M(P25,P75),lg拷贝/mL]
注:▲与基线比较,P<0.05。

表7 变量赋值表

表8 HAART治疗失败的影响因素
3 讨 论
既往研究已证实了替诺福韦的有效性、持久性以及安全性[5-6]。替诺福韦的耐药屏障较高,需3种或3种以上胸苷类似物变异才可能引起HIV对替诺福韦耐药[7],且以替诺福韦为基础的HAART方案在抑制病毒方面具有明显优势[6],这使得替诺福韦成为未普及HIV病毒学检测地区首选的一线抗病毒药物[2]。本研究结果显示,替诺福韦组的治疗失败率、病毒学失败率、免疫学失败率均低于非替诺福韦组(均P<0.05);多因素分析结果显示,HAART初始方案包含替诺福韦的患者发生HAART治疗失败的风险低于不包含替诺福韦的患者(P<0.05)。这提示替诺福韦较其他一线抗病毒药物更具优势,与相关研究结果[8-9]相似,原因考虑与替诺福韦的高耐药屏障、高效抑制病毒能力、患者的依从性较高有关。虽然近年来国内外关于含替诺福韦治疗方案的病毒学疗效的研究结果[10-11]不尽相同,但考虑到我国是人口大国,人均资源占有量有限,病毒载量及耐药检测未能广泛普及,因此,在现有条件下替诺福韦仍应作为国内首选的一线抗病毒药物。
对于替诺福韦能否更好地改善CD4+T淋巴细胞计数,目前尚存在争议。相关研究结果显示,以替诺福韦为基础的HAART方案在病毒抑制及免疫学应答上均较其他方案更具优越性[12-13];另有研究结果显示,与含齐多夫定或司他夫定的HAART方案相比,在免疫学应答方面含替诺福韦的HAART方案并无优势[14],这一结果可能与替诺福韦相关的特异性淋巴细胞毒性有关,而这种特异性淋巴细胞毒性在替诺福韦与去羟肌酐合用时更明显[15]。本研究中,治疗后各时间点两组的CD4+T淋巴细胞计数均均较基线升高,而在治疗第3、6、9、12个月时,替诺福韦组的CD4+T淋巴细胞计数高于非替诺福韦组,与相关研究结果[12]相似,提示在HAART启动12个月内,在改善CD4+T淋巴细胞计数方面,含替诺福韦的一线HAART方案效果优于不含替诺福韦的HAART方案。同时,治疗12、24个月时两组病毒载量水平几乎均在检出限下。以上结果对于基线CD4+T淋巴细胞计数低下的抗病毒初治AIDS患者,均具有积极的临床意义。另外,本研究结果显示,治疗后各时间点、两组CD4+T淋巴细胞计数的增幅百分比比较,差异均无统计学意义(均P>0.05),可能是因为在不同条件下,替诺福韦的特异性淋巴细胞毒性对CD4+T淋巴细胞计数的影响程度不同有关。
感染HIV后,体内CD8+T淋巴细胞可大量增殖、活化以发挥其细胞毒性作用。治疗开始后,随着病毒载量的下降及CD4+T淋巴细胞计数的回升,CD8+T淋巴细胞数可逐渐下降[16]。本研究中,治疗后各时点两组患者的CD8+T淋巴细胞计数均较基线时升高(均P<0.05),且持续处于相对稳定状态,并未观察到其呈先升高后下降并逐渐回落的变化趋势,这表明应用含替诺福韦的HAART方案后患者CD8+T淋巴细胞计数仍未能随病毒复制的抑制而相应下降。有学者指出,CD8+T淋巴细胞的恢复,可能与胸腺产生两类细胞的速率,两类细胞增殖和凋亡的速度,CD8+T淋巴细胞向记忆性细胞转化有关;同时发现随着治疗时间延长,人类白细胞抗原DR+CD8+T淋巴细胞计数的回落较CD38+CD8+T淋巴细胞更明显[17-18]。因此,笔者认为单纯比较外周血CD8+T淋巴细胞计数的变化不够准确,应结合人类白细胞抗原DR、CD38等相关活化分子的表达水平,需要更长的随访时间来评估替诺福韦与其他抗病毒药物对CD8+T淋巴细胞计数的影响。
综上所述,采用含替诺福韦的一线HAART方案可减少HAART治疗失败的发生,并可在较短时间内促进免疫重建,在治疗应答方面优于不含替诺福韦的一线HAART方案。本研究为回顾性研究,仅按临床治疗进行分组,因此在评估含替诺福韦方案对患者病毒学、免疫学应答方面可能产生偏倚,有待进一步优化研究设计来提高评估的准确性。
