甲烷二次燃烧自点火影响机理数值研究*
2019-07-30史增凯席文雄王伟东
史增凯,席文雄,金 星,王伟东
(航天工程大学激光推进及其应用国家重点实验室, 北京 101416)
0 引言
在高速推进领域,二次燃烧自点火现象广泛存在于燃气涡轮发动机、RQL燃烧室、航空发动机和分级燃烧系统中,是提高推力性能、控制燃烧进程的重要方式[1-2]。从几何结构来看,一次燃烧在燃烧系统上游进行,而二次燃烧在下游进行;从微观火焰结构及化学动力学过程来看,二次燃烧处于一次引导火焰尾流中,受尾流高温、非平衡组分的促进作用和贫氧对燃烧的抑制作用影响[3]。
与一次燃烧不同,二次燃烧自点火具有新的特征[4]。然而,目前研究对二次燃烧关注却较少,且多集中于实验现象的定性分析[5],未能深入理解二次燃烧自点火机制[6],因而文中忽略复杂流动的影响,借助CHEMKIN软件从化学动力学角度[7]模拟研究了不同当量比下甲烷贫燃燃烧产物再次与补充的甲烷气体掺混时发生的二次燃烧自点火现象,揭示当量比对二次燃烧自点火延迟时间的影响规律,并借助温度敏感性分析了自点火过程中所涉及基元反应的作用机制。
1 研究方案
零维、定压、均质点火系统具有以下特征:无对流扩散,状态量在空间中均匀分布,只随时间变化;封闭系统,质量固定;绝热,无热损失。对于热力学参数为P、V、ρ的N组分零维、定压、均质点火系统,组分i(摩尔数为ni)控制方程为:
(1)
(2)
式中:Yi、T表示组分i的质量分数和温度,MWi、Ri为组分i的摩尔质量和反应速率,h和CP分别表示比焓和定压热容。
甲烷/空气的第r个基元反应速率常数k(T)r可通过Arrhenius定律计算,其三参数函数形式为:
kr(T)=ArTbre(-Er/(RuT))
(3)
式中:Ar、br和Er分别为第r个基元反应的指前因子、温度因子和活化能。根据基元反应类别——单分子、双分子或三分子反应来选择反应速率与反应速率常数关系式,再联立式(1)~式(3)即可解出物质组分和温度随时间的变化情况。
数值模拟中采用甲烷燃烧的详细化学反应机理GRI-Mech3.0,文中所用各反应编号与GRI-Mech3.0编号一致;计算所涉及的空气组成为氮气∶氧气=79∶21,忽略空气中的二氧化碳、水等成分,压力值均为101 325 Pa;自点火延迟时间定义为点火开始到温度变化最快所需要的时间。
文中主要借助CHENKIN中相应模块,分为以下两个部分:1)采用平衡器计算不同当量比Φ1甲烷/空气贫燃燃烧产物的绝热火焰温度和各组分浓度,T0=300 K为平衡器初始温度;2)采用零维、均质、完全混合的闭式均相反应器参数化研究上述燃烧产物中添加不同量甲烷M1时的二次燃烧自点火延迟时间τ及组分摩尔分数的影响规律。局部当量比Φ2定义为反应器中添加甲烷量与贫燃燃烧产物中所余氧气的当量比。注意:接下来文中所述反应器起始温度T1指闭式均相反应器的初始温度,t、T分别代表反应时间和反应器温度,MOH表示反应器中OH的摩尔分数。
2 数值模拟结果及分析
甲烷添加量M1=0.05时计算所得不同当量比时绝热火焰温度、局部当量比及自点火延迟时间如表1所示。

表1 不同当量比时绝热火焰温度、局部当量比及自点火延迟时间(M1=0.05)
由表1分析知,随着当量比Φ1由0.3升高至0.7,自点火延迟时间降低了3个数量级;Φ1由0.7增加到0.8,自点火延迟时间又增加至6.90×10-1s,而Φ2由1.75增加至2.70;当Φ1=0.9时,自点火失败,此时Φ2=5.42。这说明在一定范围内,增加当量比有助于缩短延迟时间,使得自点火更容易发生,但当量比较大时,则会增加自点火延长时间,抑制自点火发生;而当量比过大时,由于燃烧产物中氧气组分过低,造成局部当量比过大,从而造成自点火失败。
不同当量比时绝热火焰温度不同,接下来探究T1对自点火延迟时间的影响规律,此时暂不考虑改变起始温度对各平衡组分摩尔组分的影响。选取Φ1=0.3与0.6时甲烷贫燃燃烧产物的摩尔分数作为反应器中初始值,并向其中添加甲烷摩尔分数M1=0.1。不同起始温度对自点火延迟时间的影响规律见图1。根据计算结果与图1:起始温度较低会造成自点火失败,在一定范围内,升高起始温度能够显著缩短自点火延迟时间,提高点火成功率,这是因为温度升高有助于自由基生成,加快反应速率,但当起始温度超过一定范围后,其对自点火延迟时间降低的贡献率减少,推测这是受组分浓度的限制,升高温度虽然会提高活性基团的碰撞概率,但反应空间有限也限制了活性基碰撞概率,这点在较高起始温度时比较显著。

图1 不同起始温度对自点火延迟时间的影响规律
自点火过程中,OH、温度作为点火进程重要指示剂能够有效反映出自点火进程。选取Φ1=0.6、T0=300 K时甲烷贫燃燃烧产物的摩尔分数作为反应器中初始值,并向其中添加甲烷摩尔分数M1=0.1。起始温度T1=1 666 K下OH和温度随时间的变化规律如图2,其中右图为左图中OH摩尔分数在0~2.0×10-6s时的局部放大图。由图2看出,随着时间的增加,温度先是逐渐上升后趋于不变,温度斜率最大时刻即自点火延迟时间约为1.71×10-3s;而OH摩尔分数初始时一直减少,然后又迅速增加。如图3为起始温度T1=3 000 K时OH摩尔分数和温度随时间的变化情况,其中右图为温度在0~2×10-5s时的局部放大图,由图像看出,随着时间的增加,温度先降低又迅速升高,继而持续下降并最终达到稳定,自点火延迟时间为2.71×10-6s;而OH摩尔分数则随着时间逐渐增加并最终趋于稳定。根据上述分析,本节观察到较低起始温度与较高起始温度下OH摩尔分数和温度随时间的变化存在显著区别,尤其是在反应起始时刻,推测原因可能是较低起始温度时,与OH消耗相关的基元反应速率加快并释放热量,使得温度上升,而在较高起始温度时,与OH生成相关的基元反应速率加快并吸收热量,与OH消耗相关的基元反应被抑制,从而使得温度降低。
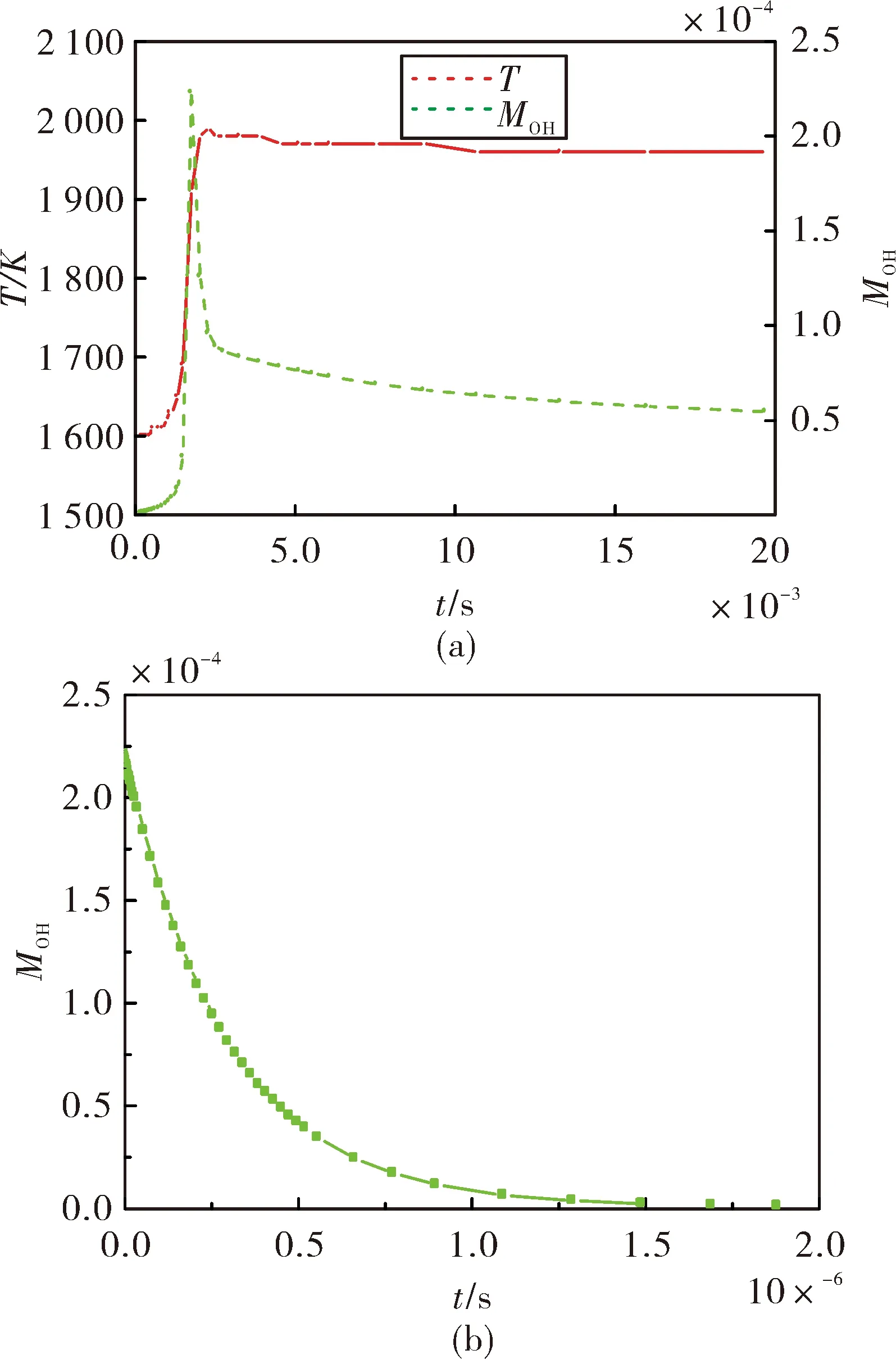
图2 起始温度T1=1 666 K下温度和OH摩尔分数随时间的变化规律(其中(b)图为(a)图中OH摩尔分数在0~2.0×10-6 s时的局部放大图)
为进一步探究当量比的作用规律,现对Φ1=0.6、T0=300 K、M1=0.1及T1=1 666 K工况下反应器自点火过程进行温度敏感性分析,由于本章自点火延迟时间定义为初始至温度变化最快所需要的时间,因而最大温度敏感度发生在自点火时间附近,且由上文知温度升高能够缩短自点火延迟时间。鉴于自点火延迟时间为1.71×10-3s,图4(a)为此时温度敏感性分析图。

图3 起始温度T1=3 000 K时OH摩尔分数和温度随时间的变化情况,(其中(b)图为温度在0~2×10-5 s时的局部放大图)
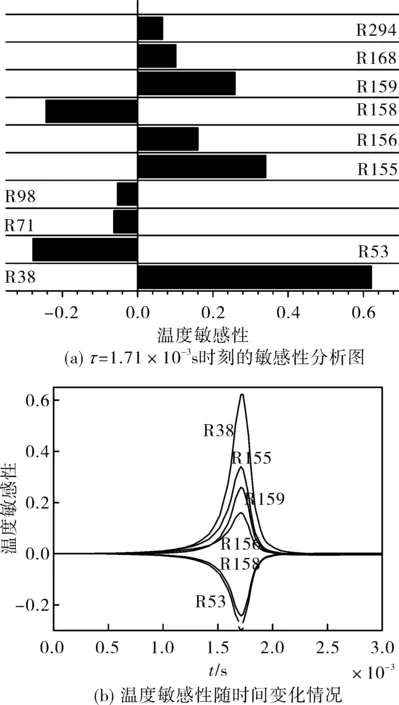
图4 温度敏感性分析
由图4(a)知对气体温度有重要影响的反应式如表2所示。由表2知,自点火发生时影响气体温度变化的重要反应式为R38、R53、R155、R156、R158和R159,此6个反应的温度敏感性随时间变化曲线见图4(b)。由两幅图像知,整个反应过程中影响最显著的是R38:H+O2<=>O+OH,其温度因子约为-0.67,加快此反应速度将生成更高的温度,故而能够缩短自点火延迟时间;R155、R156均为CH3的氧化反应,加剧氧化反应会放出大量热,并加快缩短自点火延迟时间;加快R53和R158的反应速率则会吸收更多热量,造成温度减少,进而会增加自点火延迟时间。
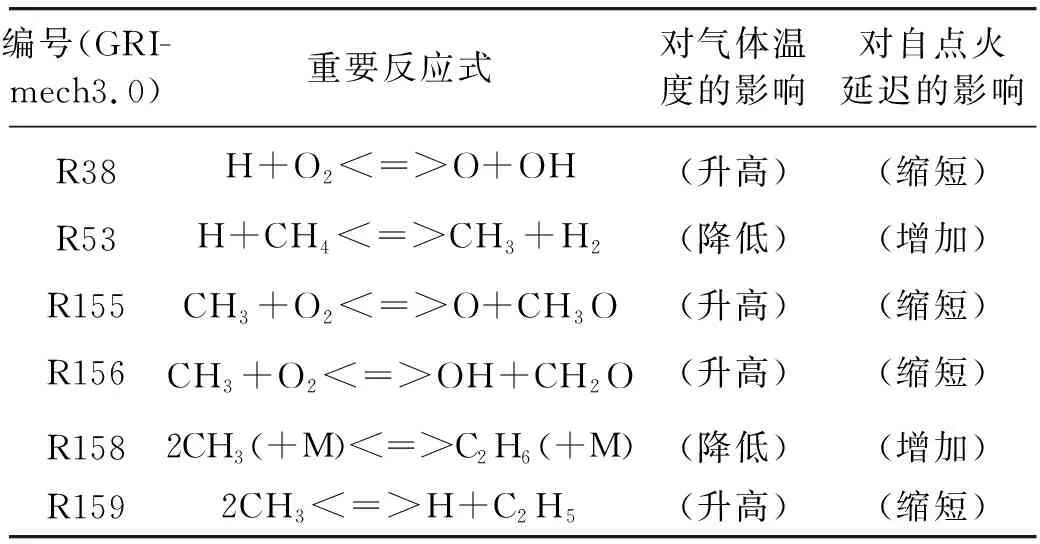
表2 自点火发生时影响气体温度的主要反应式(T1=1 666 K)
3 结论
文中借助CHEMKIN软件数值模拟了甲烷二次燃烧自点火过程,研究了当量比对自点火延迟时间的影响规律,并分析了点火过程中OH和温度变化情况,且对温度进行了敏感性分析,主要得出以下结论:
(1)在一定范围内,增加当量比有助于缩短延迟时间,使得自点火更容易发生,但当量比较大时,则会延长自点火延长时间,抑制自点火发生;而当量比过大时,由于燃烧产物中氧气组分过低,造成局部当量比过大,从而造成自点火失败。
(2)起始温度较低会造成自点火失败,在一定范围内,升高起始温度能够显著缩短自点火延迟时间,提高点火成功率,但当起始温度超过一定范围后,其对自点火延迟时间降低的影响程度减弱。
(3)较低起始温度与较高起始温度下OH摩尔分数和温度随时间的变化存在显著区别,且温度升高会缩短自点火延迟时间,而敏感性分析表明与CH3、OH物质变化相关的基元反应显著影响反应过程中温度变化,进而影响自点火进程。
