水解释放刺梨汁键合态香气化合物及糖基组成解析
2019-07-26彭邦远丁小娟赵泽伟丁筑红
彭邦远 丁小娟 赵泽伟 丁筑红
(1.兴义市农业农村局,贵州 兴义 562400;2.贵州大学酿酒与食品工程学院,贵州 贵阳 550025;3.贵州省农畜产品贮藏与加工重点实验室,贵州 贵阳 550025)
刺梨(RosaroxburghiiTratt)系蔷薇科蔷薇属落叶灌木,富含黄酮[1]、超氧化物歧化酶[2]、甾醇[3]等生物活性物质,刺梨香气成分是其品质的重要构成[4]。研究表明,水果中芳香物质主要以游离态和键合态形式存在[5],其中游离态挥发性物质主要用来呈现水果中的香气,糖苷键合态风味前体主要是通过糖苷利用其糖的端基碳原子将苷元或者相对应的配基相连形成[6],在水果中以非挥发性形式存在[5]。在果实成熟期,水解和高温等条件下,键合态挥发性物质的糖苷键断裂,游离态香气化合物被释放进而被感知[7-9]。刺梨汁主要是利用β-葡萄糖苷酶或相应的酸解处理,进而可以得到刺梨风味前体中独有的键合态物质,进而可强化和增强刺梨相关产品的风味品质,该方法已成为水果制品增香的重要途径。目前,研究者[10-12]已从刺梨中分离鉴定出130余种挥发性成分,主要以醇类、酯类和酸类物质为主。而对刺梨汁中挥发性物质和香气成分的来源及构成缺乏系统分析,特别是键合态香气成分信息不够清楚。相关研究表明,键合态风味物质的释放方法中,酶法条件较为温和且不会导致物质结构变化[13],所释放的香气更能够呈现水果的特征香气[14]。本研究利用AmberliteXAD-2树脂分离键合态香气物质,通过探究β-葡萄糖苷酶与酸解刺梨汁键合态风味前体的挥发性物质的组成差异,以及刺梨汁中糖苷键合态香气化合物的糖基组成,以期为刺梨汁及其加工制品的增香调控提供理论依据。
1 材料与试剂
1.1 材料与试剂
刺梨:采摘新鲜且充分成熟的贵农5号品种,产于贵州龙里刺梨种植基地。
C7~C30正构烷烃混合标样:色谱纯,美国Supelco公司;
Almondsβ-D-葡萄糖苷酶(微生物来源):100 U/g,美国Sigma公司;
鼠李糖、甘露糖、葡萄糖:生化试剂,中国Solarbio公司;
硅藻土:化学纯,天津市富宇精细化工有限公司;
正戊烷、乙醚、乙酸乙酯、甲醇、氯仿等:分析纯,天津市富宇精细化工有限公司。
1.2 仪器与设备
GC/MS联用仪:HP6890/5975C型,美国安捷伦公司;
弹性石英毛细管柱:ZB-5MSI 5%Phenyl-95%DiMethylpolysiloxane (30 m×0.25 mm×0.25 μm),美国安捷伦公司;
硅橡胶隔垫:PTFE型,美国安捷伦公司;
手动固相微萃取装置:2 cm-50/30 μm DVB/CAR/PDMS型 StableFlex纤维头,美国Supelco公司。
1.3 方法
1.3.1 刺梨汁的制备 刺梨果实经挑选、清洗、去蒂、切分、榨汁,4层纱布粗滤,在4 ℃,12 000 r/min冷冻离心15 min,留上清液备用。
1.3.2 Amberlite XAD-2树脂柱处理 参照文献[15]。
1.3.3 刺梨汁键合态香气前体物的提取 将刺梨汁(3 mL/min)上柱静置吸附10 h,用400 mL去离子水(3 mL/min)洗脱除去水溶性糖、酸等成分;用300 mL乙醚—戊烷(体积比1∶1)(3 mL/min)洗脱游离态组分;用300 mL甲醇(3 mL/min)洗脱键合态组分,得洗脱液。利用旋转蒸发仪在35 ℃将甲醇洗脱液浓缩至干,溶解于pH 5.0,20 mL 0.06 mol/L柠檬酸缓冲液,分3次用120 mL 乙醚—戊烷(体积比1∶1)萃取去除游离态组分,水相备用[16-18]。
1.3.4 刺梨汁键合态香气前体物的酶解 参照文献[19]。
1.3.5 刺梨汁键合态香气前体物的酸解 将刺梨汁水相中的萃取物用1.0 mol/L HCl调整pH为1.0,沸水浴60 min,在将溶液用1.0 mol/L NaOH调节至中性,分3次用120 mL乙醚—戊烷(1∶1)萃取酸解液,除去键合态挥发性物质,水相于旋转蒸发仪减压浓缩至干,备用[6,20]。
1.3.6 刺梨汁水解后香气物质分析 将1.3.4、1.3.5中乙醚—戊烷(体积比1∶1)萃取液,分别用Na2SO4干燥(4 ℃静置4 h)除水,过滤,浓缩至5 mL,用N2吹至0.5 mL,取20 μL浓缩液,用二氯甲烷定容至1 mL,取1 μL 进样,供GC-MS分析。
采用“气味活化值(odor activity value,OAV)”[21-23]明确刺梨汁中主要挥发性物质。气味活化值指气味的物质浓度与其阈值的比值,反映各香气组分对刺梨汁整体香气的贡献情况,按式(1)计算:
(1)
式中:
OAV——气味活化值;
C——化合物在果汁中的绝对浓度;
T——化合物在果汁中的感觉阈值。
OAV值越大,对香气的贡献越大。当OAV>1时,为果汁中典型挥发性物质(OAV>10时,为果汁中重要挥发性物质);当OAV<1时,该化合物对果汁整体香气无明显作用。由于本研究样品包含较多挥发性物质,精确定量非常繁琐且成本较高,且试验旨在筛出OAV最高的挥发性物质。因此,可用所测挥发性物质的相对百分含量分析。W按式(2)计算:
W=f×C×100%,
(2)
式中:
W——所测挥发性物质的相对百分含量,%;
f——相对质量矫正因子;
C——化合物在果汁中的绝对浓度。
相对气味活度值(relative odor activity value,ROAV)[21],样品中对总体风味贡献最高的组分ROAV值为100,其他组分(A)则有:
(3)
式中:
ROAVA——A组分的相对气味活化值;
OAVA——A组分的气味活化值;
OAVmax——A组分对总体风味贡献最高值。
由式(1)~(3)可得:
(4)
式中:
Wmax——对刺梨总体风味贡献最大的组分的相对百分含量,%;
WA——各挥发性物质的相对百分含量,%;
TA——各挥发性物质的相对感觉阈值;
Tmax——各挥发性物质对刺梨总体风味贡献最大的相应的感觉阈值。
ROAV≥1表示挥发性物质为刺梨关键风味物质,0.1≤ROAV≤1表示挥发性物质对刺梨总体风味存在重要修饰作用[24]。
1.3.7 样品衍生物的制备 参照文献[25]59-60。
1.3.8 糖标准品衍生物的制备 参照文献[26]87。
1.3.9 刺梨汁挥发性香气成分及GC-MS条件
(1)GC条件:色谱柱为ZB-5MSi 5% Phenyl-95% DiMethylpolysiloxane (30 m×0.25 mm×0.25 μm)石英毛细管柱,柱温45 ℃(保留2 min),4 ℃/min升温至220 ℃ (保留2 min);汽化室温度250 ℃;载气为高纯氦气(99.999%);柱前压52 538.071 2 Pa,载气流量1.0 mL/min;不分流进样;溶剂延迟时间:1.5 min。
(2)MS条件:EI源为离子源,温度230 ℃;四极杆温度150 ℃;电子能量70 eV;发射电流34.6 μA;倍增器电压1 615 V;接口温度280 ℃;质量范围20~450 amu。糖衍生物样品色谱条件:色谱柱为HP-5MS(5% Phenyl-95% DiMethylpolysiloxane)(30 m×0.25 mm×0.25 μm)弹性石英毛细管柱,FID检测器温度250 ℃,气化室温度280 ℃,进样量1 μL。程序升温,起始温度160 ℃,10 ℃/min 升至180 ℃,3 ℃/min升温至208 ℃(保留2 min),1 ℃/min升温至210 ℃(保留4 min)。
1.3.10 酶解酸解刺梨汁键合态化合物的定性定量分析
运用计算机谱库(Nist/Wiley)将检测结果进行初期检索,参照相关文献资料定性,确定其分子式。其相对含量采用峰面积归一法确定[27]。
1.3.11 数据统计分析 试验数据结果用Excel 2010软件统计,HPLC及GC-MS结果由SPSS 20.0进行相关统计分析。
2 结果与分析
2.1 酶法及酸法释放刺梨汁键合态挥发性物质结果分析
由图1~2和表1可知,刺梨汁键合态底物经酶解、酸解共检出49种挥发性物质,β-葡萄糖苷酶水解得到31种挥发性物质,酸类10种(25.78%)、醛类3种(19.96%)、醇类7种(16.79%)、酮类4种(13.38%)、酯类3种(11.03%)、酚类1种(7.14%)、烯烃类2种(3.46%)、呋喃1种(0.16%),含量较高的物质有乙醛(9.78%)、硬脂酸(9.68%)、4-羟基-2,5-二甲基-3(2H)呋喃酮(8.78%)、乙酸乙酯(8.37%)、愈创木酚(7.14%)等。酸解释放24种挥发性物质,呋喃1种(0.57%)、酸类3种(0.83%)、醇类2种(1.14%)、酯类2种(1.25%)、烯烃类7种(3.36%)、酮类2种(18.59%)、酚类7种(53.23%),含量较高的物质有2,6-二叔丁基对甲酚(49.55%)、胡薄荷酮(13.71%)、5-己烯-2-酮(4.88%)、5-甲基间苯二酚(2.03%)、α-无水葡萄糖酯(1.10%)。酸解和酶解对释放刺梨汁键合态风味前体物质有较大差异,共同的风味物质分别为肉桂酸、棕榈酸、油酸、胡薄荷酮、2,3-二氢-2-甲氧苯并呋喃。风味前体水解物的不同主要与糖苷类前体的断键方式存在相关性,酶解反应主要断糖苷键,而酸解反应断醚键[28]。酸解反应在高温条件下断键更彻底,酶解依赖于酶的种类及活性。酶解主要释放酸类、醛类、醇类物质,醇、醛类物质呈青草味,酸解主要释放烯烃类、酮类及酚类物质,酮、酚类物质呈果香味,烯烃类物质有花香味[26]5-7。酶解释放的香气物质更接近刺梨自身香气,起增香作用[26]93。酸解反应条件影响香气稳定性,且酸解无选择性,易产生刺激性甚至异味成分[29]。研究发现经酸水解,在刺梨汁中得到风味前体有二氢月桂烯醇、苄醇、4-甲基辛烷、5-己烯-2-酮、胡薄荷酮、1,3,5,5-四甲基-1,3-环己二烯、十六烷、二十二烷、二十五烷等。经酶解得到风味前体有丙酮醇、3-羟基丁醛、羟基香茅醛、丁酸、己酸等。本研究发现经水解后得到风味前体有叶醇、蘑菇醇、D-异薄荷醇、肉桂酸、对羟基肉桂酸、棕榈酸、2-更酮、乙酸乙酯、愈创木酚,本研究和周志[11]、彭邦远等[12]的研究结果一致。
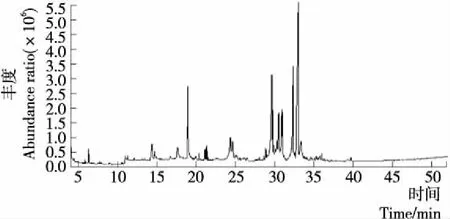
图1 刺梨汁键合态挥发性物质的酶解产物GC-MS总离子流图Figure 1 GC-MS total iol current chromatogram of the bond flavor components enzymolysis products in Rosa roxburghii juice
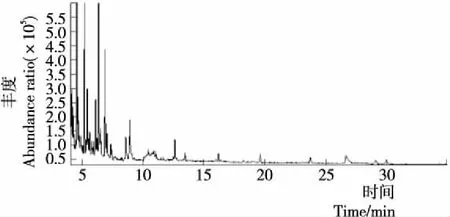
图2 刺梨汁键合态挥发性物质的酸解产物GC-MS总离子流图Figure 2 GC-MS total iol current chromatogram of the bond flavor components acidolysis products in Rosa roxburghii juice
表1酶解与酸解法刺梨汁键合态挥发性物质比较
Table 1The Comparison of Enzymatic Hydrolysis and Acidolysis of bond flavor components inRosaroxburghiijuice
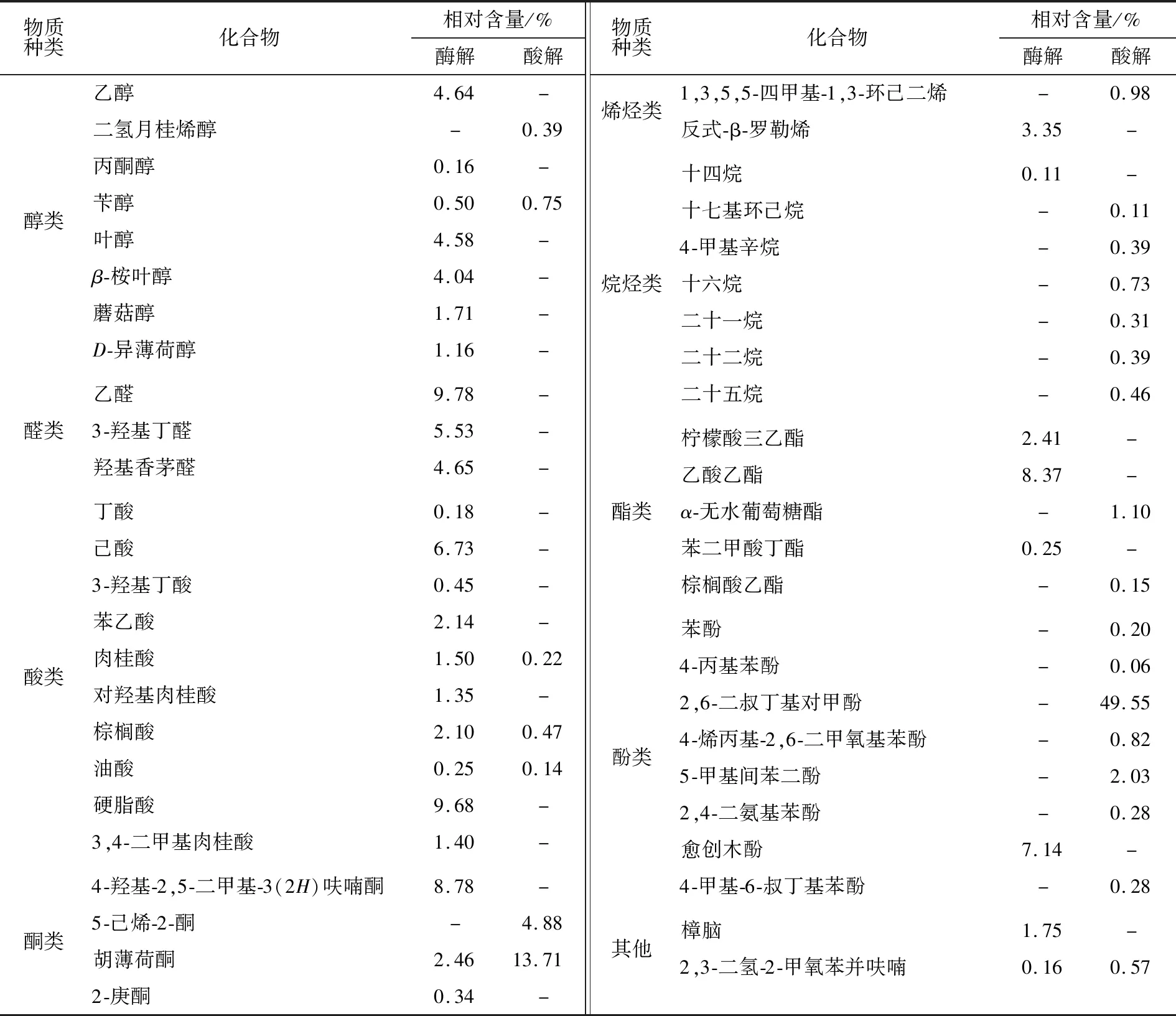
物质种类化合物相对含量/%酶解酸解物质种类化合物相对含量/%酶解酸解醇类乙醇4.64-二氢月桂烯醇-0.39丙酮醇0.16-苄醇0.500.75叶醇4.58-β-桉叶醇4.04-蘑菇醇1.71-D-异薄荷醇1.16-醛类乙醛9.78-3-羟基丁醛5.53-羟基香茅醛4.65-酸类丁酸0.18-己酸6.73-3-羟基丁酸0.45-苯乙酸2.14-肉桂酸1.500.22对羟基肉桂酸1.35-棕榈酸2.100.47油酸0.250.14硬脂酸9.68-3,4-二甲基肉桂酸1.40-酮类4-羟基-2,5-二甲基-3(2H)呋喃酮8.78-5-己烯-2-酮-4.88胡薄荷酮2.4613.712-庚酮0.34-烯烃类1,3,5,5-四甲基-1,3-环己二烯-0.98反式-β-罗勒烯3.35-烷烃类十四烷0.11-十七基环己烷-0.114-甲基辛烷-0.39十六烷-0.73二十一烷-0.31二十二烷-0.39二十五烷-0.46酯类柠檬酸三乙酯2.41-乙酸乙酯8.37-α-无水葡萄糖酯-1.10苯二甲酸丁酯0.25-棕榈酸乙酯-0.15酚类苯酚-0.204-丙基苯酚-0.062,6-二叔丁基对甲酚-49.554-烯丙基-2,6-二甲氧基苯酚-0.825-甲基间苯二酚-2.032,4-二氨基苯酚-0.28愈创木酚7.14-4-甲基-6-叔丁基苯酚-0.28其他樟脑1.75-2,3-二氢-2-甲氧苯并呋喃0.160.57
2.2 酶解与酸解法释放刺梨汁键合态典型风味化合物差异性分析
由表2可知,酸类、酚类物质阈值较高,饱和烷烃为挥发性非嗅感物质,不易引起嗅感[29]对特征风味贡献较小。经β-葡萄糖苷酶水解得到β-桉叶醇(ROAV=1.84)、3-羟基丁醛(ROAV=2.52)及愈创木酚(ROAV=1.84)3种物质ROAV>1,可能为酶解刺梨汁键合态风味物质的重要香气成分。乙醛(ROAV=0.30)对酶解液整体风味具有重要的修饰作用。酸解法主要释放的物质为酸类和酯类,棕榈酸阈值为10 000 μg/kg,棕榈酸乙酯阈值为2 000 μg/kg,苯酚、4-丙基苯酚阈值分别为5 900,55 μg/kg,均为非嗅感物质对风味贡献较小。4-丙基苯酚ROAV<0.1,对刺梨汁整体香气贡献较小。综上可知,酶解法释放挥发性风味物质多于酸解法,酶解后对刺梨汁风味影响较大的风味物质(ROAV≥1)有4种,其贡献顺序为:3-羟基丁醛>β-桉叶醇>愈创木酚>羟基香茅醛;酸解法释放的挥发性物质对风味贡献不明显。
酶具有专一性和高效性,能够催化葡萄糖的半缩醛羟基和其它物质羟基相连的糖苷键[30],通过移除香味前体的相应糖配体释放挥发性物质,而酸解法使糖苷键的成键原子质子化形成阳离子中间体,减少空间张力致糖苷键断裂释放配基[31],使其更易于被酸水解。酸解反应较剧烈,释放风味成分不足,刺激性气味较重[25]47。
† “ND”表示酶解未检测到而酸解检测到的化合物或酸解未检测到而酶解检测到的化合物。
2.3 刺梨汁键合态挥发性物质的糖基成分分析
利用三氟乙酰化法,对键合态糖苷糖基进行探究,能够较明确地得到糖苷和糖基的结构[29]。由图3~6可知,在相同GC-MS条件下混合糖标品中鼠李糖、甘露糖、葡萄糖保留时间为12.674,7.301,12.945 min,与单糖相比在相同检测条件下,各保留时间的标准差均小于±0.038,因此,峰的保留时间可用于刺梨汁糖基的鉴定。由图7~8可知,酶解法可释放的刺梨汁键合态香气组分含有两种糖基,保留时间分别为12.767,13.094 min,与鼠李糖(12.674 min)、葡萄糖(13.097 min)保留时间相符合,根据保留时间定性进行GC-MS分析及参考相关文献,可初步确认酶解法能够得到刺梨汁键合态风味物质中糖基由葡萄糖、鼠李糖组成。酸解法可释放的刺梨汁键合态风味物质的糖基有3种,保留时间分别为12.784,13.107,7.482 min,与鼠李糖(12.674 min)、葡萄糖(13.097 min)、甘露糖(7.346 min)保留时间相符合。初步判定,刺梨汁中键合态香气物质的糖基由葡萄糖、鼠李糖、甘露糖组成。酶解与酸解刺梨键合态风味前体糖基有差异,共同可释放的糖基为葡萄糖与鼠李糖。宛晓春等[32]采用HPLC检测到酸解后柠檬汁中糖苷键合态挥发性物质的糖基部分可能由葡萄糖和鼠李糖组成。奕志英等[19]采用HPLC检测到酶解后石榴汁中糖苷键合态香气前体物质的糖基主要以葡萄糖和果糖为主。目前鉴定出糖苷的糖基部分一般含有葡萄糖、鼠李糖、甘露糖等单糖[33-34],大多数键合态风味物质与葡萄糖键合[35]。
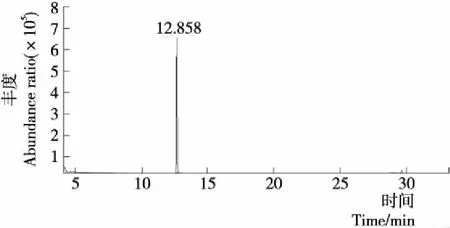
图3 鼠李糖的离子流图Figure 3 GC-MS chromatogram analysis of Rhamnose
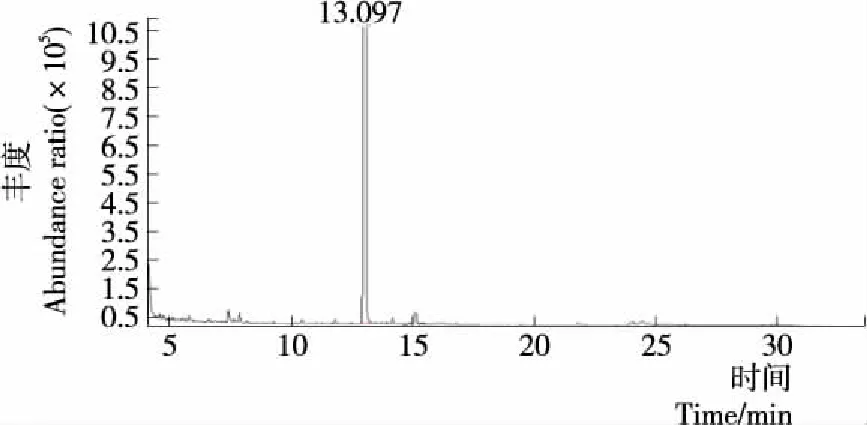
图4 葡萄糖的离子流图Figure 4 GC-MS chromatogram analysis of Glucose
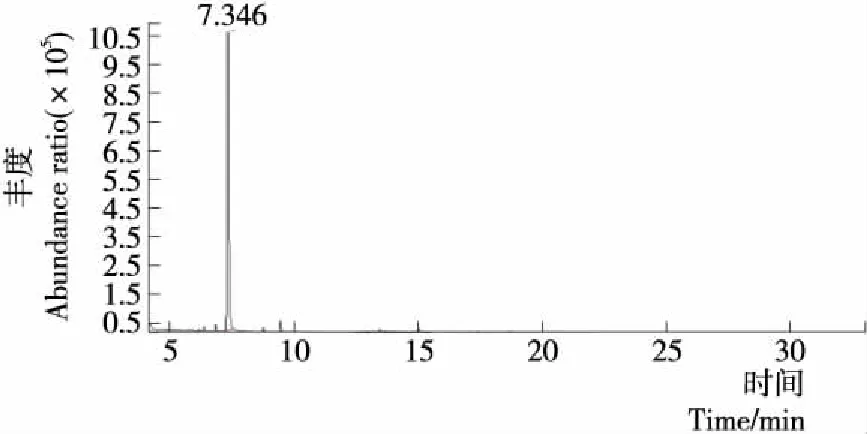
图5 甘露糖的离子流图Figure 5 GC-MS chromatogram analysis of Mannose
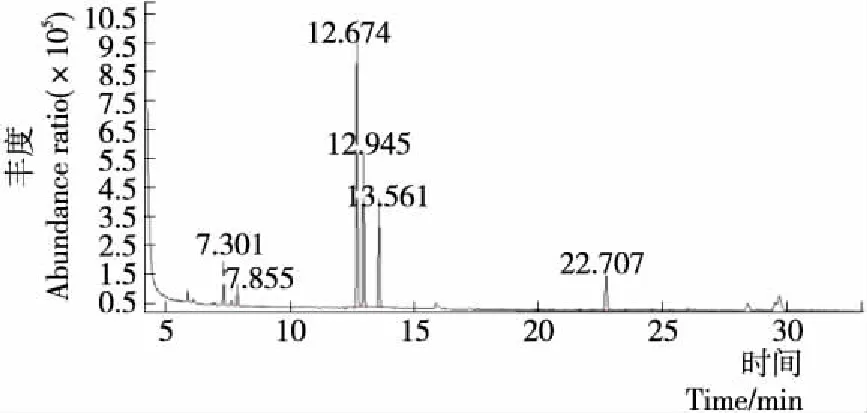
图6 葡萄糖、甘露糖、鼠李糖等混合标品的离子流图Figure 6 GC-MS chromatogram analysis of Galactose,Xylose,Glucose,Mannose,Fructose,Rhamnose
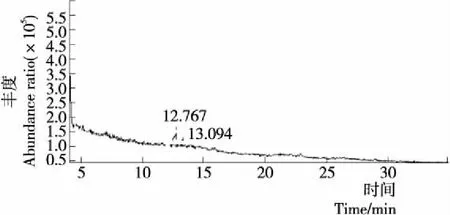
图7 刺梨汁酶解糖基衍生化离子流图Figure 7 GC-MS chromatogram of Rosa roxburghii juice enzymatic Glycosylation
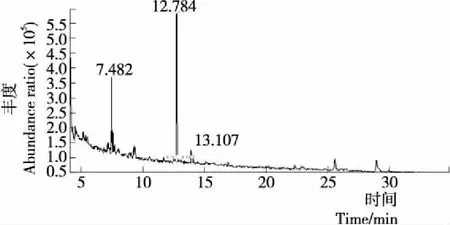
图8 刺梨汁酸解糖基衍生化离子流图Figure 8 GC-MS chromatogram of Rosa roxburghii juice acidolysis Glycosylation
3 结论
采用β-葡萄糖苷酶水解刺梨汁键合态香气前体物质,共得到49种挥发性物质,酶解释放31种挥发性物质,其中乙醛(9.78%)、硬脂酸(9.68%)、4-羟基-2,5-二甲基-3(2H)呋喃酮(8.78%)、乙酸乙酯(8.37%)、愈创木酚(7.14%)等含量较高。酸水解得到24种挥发性物质,其中2,6-二叔丁基对甲酚(49.55%)、胡薄荷酮(13.71%)、5-己烯-2-酮(4.88%)、5-甲基间苯二酚(2.03%)、α-无水葡萄糖酯(1.10%)含量较高。酸解与酶解释放的香气物质不同,可能与反应强度和水解机制有关。
经ROAV值分析,刺梨汁酶解液中典型挥发性物质多于酸解液,酶解后对风味影响较大的典型风味物质(ROAV≥1)有4种,贡献顺序为3-羟基丁醛>β-桉叶醇>愈创木酚>羟基香茅醛;酸解后对风味影响的重要风味物质少,可能与酸解条件及反应剧烈程度有关。通过衍生化法探究刺梨汁键合态香气前体酶解与酸解法可释放的糖基,得出不同水解法可释放的糖基不同,本研究初步确定刺梨汁键合态香气前体物质的糖基有葡萄糖、鼠李糖和甘露糖。
