不同营养素对活动期溃疡性结肠炎患者肠道生物屏障的影响
2019-07-25吴慧博赵海英朱圣韬吴咏冬张澍田
吴慧博 赵海英 朱圣韬吴咏冬张澍田*
(1.首都医科大学附属北京潞河医院消化内科, 北京 101100;2.首都医科大学附属北京友谊医院消化内科, 北京 100050)
溃疡性结肠炎(ulcerative colitis, UC)每年的发病率大约为10~20/105,有报道[1]称可达到100~200/105,患者多为青壮年,可能会影响其终生健康,对社会造成了极大的影响,既往对UC的治疗主要是5-氨基水杨酸、糖皮质激素,不良反应多,有研究[2-4]显示,肠内营养素能够通过免疫调节作用保护肠道生物屏障,谷氨酰胺作为一种肠道必需的氨基酸能够为肠上皮细胞提供能量[5],乳酸杆菌对肠道屏障的益处也有很多报道[6],为此,本研究拟采用细菌培养法探讨不同营养素配方对UC活动期肠道生物屏障的影响及不同配方用于UC活动期治疗的可行性。
1 对象与方法
1.1 研究对象
2008年11月至2010年3月于首都医科大学附属北京友谊医院、附属北京朝阳医院、北京大学第三医院、解放军总医院、北京大学第一医院、南方医科大学附属南方医院、武汉协和附属同济医院、黑龙江省人民医院住院治疗的79例活动期UC患者。按入院时间采用数字表法将研究对象随机分为5组,常规组(16例),肠内营养组(16例),微生态制剂组(15例),免疫增强剂组(15例),微生态免疫增强肠内营养组(17例)。
1)入选标准:①年龄18~70岁,符合轻中度溃疡性结肠炎临床表现者;②结肠镜检查为溃疡性结肠炎活动期表现者;③黏膜组织学检查为溃疡性结肠炎活动期表现者。
2)排除标准:①病情分度为重度者;②需要排除其他原因引起的结肠炎性反应:如克罗恩病、各种细菌感染引起的感染性肠炎及其他真菌性肠炎、肠结核、出血坏死性肠炎、抗生素相关性肠炎、阿米巴肠炎血吸虫病、结直肠癌、肠易激综合征、缺血性结肠炎、放射性肠炎、过敏性紫癜胶原性结肠炎等;③暴发型结肠炎:症状严重,每日血便10次以上,并伴有全身中毒症状,合并中毒性巨结肠、肠穿孔、脓毒血症;④患有恶性或严重的心、肺、肾、胰、肝脏疾病或其他疾病被研究者判断为影响研究的评估;⑤需要在研究期间继续合并服用以下对治疗有影响的药物:糖皮质激素,免疫抑制剂(硫唑嘌呤、环孢素等),生物制剂(英昔单抗等),非甾体抗炎类药物(包括小剂量阿司匹林),肠道菌群调节药物(整肠生、培菲康、金双歧等);⑥已知或怀疑对柳氮磺胺吡啶或5-氨基水杨酸类药物过敏者;⑦怀孕或哺乳;⑧乙醇、烟草和/或药物滥用(成瘾或依赖)或医生判断依从性差者;⑨曾入组本研究及本研究相关人员等。
1.2 药物、检查试剂
美沙拉秦缓释颗粒剂(500 mg/袋,爱的发制药公司,法国),短肽型肠内营养制剂(125 g/袋,Nutricia Export B.V,荷兰),谷氨酰胺颗粒制剂(2.5 g/袋,重庆药友制药有限责任公司),嗜酸乳杆菌颗粒制剂(800 mg/袋,乐托尔制药公司,法国),VITEK GNI鉴定卡片、VITEK GPI鉴定卡片、VITEK ANI鉴定卡片、厌氧菌鉴定卡片(生物梅里埃公司,美国)。
1.3 治疗方法
常规组给予美沙拉秦缓释颗粒剂1.0 g qid+少渣饮食;肠内营养组给予美沙拉秦缓释颗粒剂1.0 g qid+短肽型肠内营养制剂125 g,qid,该组患者除可饮用水外禁止其他食物或液体;微生态制剂组给予美沙拉秦缓释颗粒剂1.0 g qid+少渣饮食+乳酸杆菌800 mg,bid,首剂加倍;免疫增强剂组给予美沙拉秦缓释颗粒剂1.0 g qid+少渣饮食+谷氨酰胺颗粒制剂5 g,tid;微生态免疫增强肠内营养组给予美沙拉秦缓释颗粒剂1.0 g qid+短肽型肠内营养制剂125 g qid+谷氨酰胺颗粒制剂5 g tid+嗜酸乳杆菌颗粒制剂800 mg bid(首剂加倍),该组患者除可饮用水外禁止其他食物或液体。治疗时间为14 d,均经口服给药,于治疗前后应用细菌培养法测定各组调查对象粪便中的菌群,计数治疗前后乳酸杆菌、双歧杆菌、肠球菌、肠杆菌及酵母菌菌落数,比较各组的肠道菌群构成的差异, 观察患者病情缓解情况。
1.4 监测指标
选择肠道菌群中具有代表性的需氧菌、厌氧菌和酵母样真菌共5种:肠杆菌、肠球菌、酵母菌、双歧杆菌、乳杆菌。其中,肠杆菌、肠球菌及酵母菌为需氧菌;双歧杆菌及乳杆菌为厌氧菌。
1.5 菌落计数及鉴定
使用VITEK GNI鉴定卡片、VITEK GPI鉴定卡片、VITEK ANI鉴定卡片。需氧菌直接使用VITEK-AMS全自动微生物鉴定系统对细菌进行生化鉴定;放置35 ℃孵箱4~6 h后,将生化反应结果输入VITEK-AMS厌氧菌鉴定系统中鉴定。结果以每克粪便湿质量中菌落的个数表示,即每克粪便湿质量中菌落形成单位(CFU/g)。
1.6 治疗效果评价
完全缓解:临床症状消失,结肠镜检查黏膜大致正常;有效:临床症状基本消失,结肠镜复查黏膜轻度炎性反应或假息肉形成;无效:经治疗后临床症状、结肠镜及病理检查无改善。
1.7 统计学方法
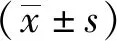
2 结果
2.1 基础数据分析
5组患者的性别、年龄、发病部位、病程等基线资料,差异均无统计学意义(P>0.05,表1、2)。其中常规组中2例患者、微生态制剂组及免疫增强剂组中各1例患者因发热应用抗生素类药物退出,肠内营养制剂组中2例患者因服用短肽型肠内营养制剂后腹泻而退出,微生态免疫增强肠内营养制剂组中2例患者对短肽型肠内营养制剂口味不耐受退出、1例患者因服用短肽型肠内营养制剂后腹泻而退出。
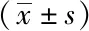

ItemT-groupE-groupME-groupIS-groupIEEN-groupFPNumberofcases1616151517Age/a38.6±10.6944.25±17.6942.25±15.6940.25±17.7849.25±13.661.610.18Diseaseduration/a4.40±3.654.62±3.484.36±3.242.71±2.403.24±2.781.110.36DAI5.00±1.415.28±1.564.32±0.584.67±0.584.82±0.361.900.12BMI/(kg·m-2)23.83±0.2424.34±0.6523.62±0.4822.00±1.5023.12±1.401.220.10
DAI:disease activity index;BMI:body mass index;T-group:traditionary group;E-group:enteral nutrition group;ME-group:microecologicalagent group;IS-group:immunostimulants group;IEEN-group:immune enhanced enteral nutrition group.

表2 入组病例计数基线资料Tab.2 Baseline data on admitted cases
T-group:traditionary group;E-group:enteral nutrition group;ME-group:microecological agent group;IS-group:immunostimulants group;IEEN-group:immune enhanced enteral nutrition group;RSC:Rectum Sigmoid colon;LC:left colon;EC:entire colon.
2.2 5组患者治疗前后效果比较
经列联表χ2检验,5组间的治疗效果差异有明显统计学意义,进一步进行行×列分割,采用Fisher精确单侧检验,肠内营养制剂组(P=0.000 9)、微生态免疫增强肠内营养组(P=0.003)疗效均优于常规组,其余各组之间治疗效果差异无统计学意义(表3)。

表3 5组患者治疗效果比较Tab.3 Different clinical effects between groups n (%)
**P<0.01vsT-group; χ2=15.83,P<0.01;T-group: Traditionary group;E-group:enteral nutrition group;ME-group:microecological agent group;IS-group: immunostimulants group;IEEN-group:immune enhanced enteral nutrition group.
2.3 5组患者治疗前后菌群分析
5组患者治疗前后菌群差异无统计学意义。治疗2周后,常规组、肠内营养制剂组、微生态制剂组、免疫增强剂组、微生态免疫增强剂组与治疗前相比,肠球菌、肠杆菌的数量明显减少(P<0.05),双歧杆菌和乳杆菌的数量显著增加(P<0.05),酵母菌变化不明显(P>0.05)。进一步比较治疗后5组间细菌的差值,微生态免疫增强剂组、微生态制剂组和免疫增强剂组的肠杆菌数量变化与肠内营养制剂组相比差异具有统计学意义(P<0.05),且肠内营养制剂组菌落群数下降较微生态制剂组及免疫增强剂组菌落群数显著,但低于微生态免疫增强肠内营养组。微生态制剂组的肠球菌菌落数变化与肠内营养制剂组相比差异具有统计学意义,免疫增强剂组的肠球菌菌落数变化与微生态制剂组相比差异具有统计学意义。
比较各组双歧杆菌菌落数在治疗前后的变化发现,微生态制剂组及免疫增强剂组与肠内营养制剂组相比差异具有统计学意义(P<0.05),且肠内营养制剂组菌落数的增多趋势较二组显著。
比较治疗前后乳酸杆菌菌落数变化,微生态制剂组及免疫增强剂组与常规组及肠内营养制剂组相比差异具有统计学意义(P<0.05),且二组治疗后乳酸杆菌菌落数增多高于常规组但低于肠内营养制剂组,详见表4。
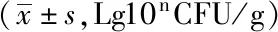
表4 针对5种治疗方案的菌群分析结果Tab.4 Results of flora analysis for five treatment options
▲The difference between the number of bacteria before treatment and the number after treatment was statistically significant;The difference between the two results was statistically significant(P<0.05),avsT-group,bvsE-group,cvsME-group,dvsIS-group;T-group:traditionary group;E-group:enteral nutrition group;ME-group:microecologicalagent group;IS-group:immunostimulants group;IEEN-group:immune enhanced enteral nutrition group.
3 讨论
溃疡性结肠炎(ulcerative colitis, UC)是原因不明的非特异性结肠炎性疾病,发病率不断增高,UC患者在疾病诊断时往往存在营养不良,并且贯穿疾病的不同阶段[7-8]。肠内营养(enteral nutrition, EN)已广泛应用于克罗恩病的治疗中,总缓解率可达60%[9-10],疗效仅稍逊于肾上腺皮质激素,但其应用于UC治疗的经验尚需进一步积累。谷氨酰胺作为肠道必需氨基酸能够为肠道黏膜提供能量,动物实验[11-12]表明,外源性给予谷氨酰胺能够减低肠道的损伤程度,改善氮平衡,改善疾病过程。有研究[13-15]表明,乳酸杆菌对炎性肠病的治疗有益,其作用的发挥主要是通过调节黏膜免疫的稳定性而实现的。
既然,各种营养素治疗能够改善患者的营养状态及改善肠道免疫屏障功能,影响疾病活动的作用,那么,不同营养素综合治疗能否改善活动期UC症状达到临床完全缓解,从而影响疾病的活动,改善患者症状,达到临床治愈?为此,本实验通过细菌培养法计数活动期UC患者治疗前后大便中乳酸杆菌、双歧杆菌、肠球菌、肠杆菌及酵母菌变化情况,比较各组的肠道菌群构成的差异, 观察患者病情缓解情况,以期为活动期UC患者的临床治疗提供一定的线索。
本研究中,活动期UC患者治疗前与治疗后粪便菌群相比,肠杆菌和肠球菌呈有意义降低,肠杆菌可释放内毒素,而肠球菌可释放外毒素,这些可能与UC的发生有密切关系,经治疗后益生菌数上升,在整个肠道表面形成生物学屏障阻止有害菌和外袭菌对人体的侵袭,有益菌群通过产生有机酸、细菌素或争夺营养物质抑制有害菌的繁殖,还可抑制有害菌产生内毒素和致癌物质,能够降低炎性反应因子水平从而实现免疫调节作用,维护人体正常生理功能。这与既往研究[16-17]相吻合。既往研究[18-19]表明炎性肠病(inflammatory bowel disease,IBD)患者的粪便菌中,肠球菌、肠杆菌、酵母菌是增高的,而双歧杆菌、乳酸杆菌的数量是减少的。
本研究中对活动期UC患者在基础性治疗上加用肠内营养制剂后,偶有口感不耐受、腹泻、腹胀等不良反应,但均未发生严重不良事件,应用肠内营养制剂是安全的。加用肠内营养制剂、谷氨酰胺、嗜酸乳杆菌颗粒制剂后能够更明显的抑制肠道菌群异位,改善肠道生物屏障,从而有效改善患者病情。本研究治疗前后患者大便中酵母菌的变化趋势无差异,可进一步扩大样本量进行研究。在临床疗效方面,微生态免疫增强肠内营养组及肠内营养组优于常规组,其他各组间差异无统计学意义,可能与样本量偏小有关,可进一步扩大样本量完成。可见肠道菌群的改善早于临床症状的改善出现,从而为活动期UC患者的发病机制及治疗配方提供了一定的线索。综上所述,在活动期UC患者中应用美沙拉秦缓释颗粒剂、嗜酸乳杆菌颗粒制剂、谷氨酰胺、肠内营养制剂能够增强对肠道菌群失调的改善作用,进而保护活动期UC患者肠道生物屏障,从而影响疾病的活动,改善患者症状,达到临床完全缓解。
