茶溴香酰胺脂质体对黑色素瘤细胞生长和迁移的抑制作用
2019-07-19张伟伟石晓玉孙紫薇张国营
张 欣,张伟伟,张 燕,石晓玉,孙紫薇,刘 昆,张国营
(烟台大学药学院分子药理学实验室,烟台大学新型制剂与生物技术药物研究山东省高校协同创新中心、分子药理和药物评价教育部重点实验室(烟台大学),山东 烟台 264005)
黑色素瘤是易转移、侵袭力强且恶性程度较高的一类肿瘤[1],发病率逐年上升,生存期短,使人类的生命健康受到极大地威胁.目前对黑色素瘤的医治以化疗和生物疗法为主,但化疗药物强烈的毒副作用使患者的依从性较差,生物疗法虽然在一定程度上优于化疗,却并不能延伸患者生命和提升生活质量[2].除此之外,靶向治疗、电化学疗法和免疫治疗药物的联合疗法等也正在研究之中,但还有很大的改进空间[3].因此亟需寻找一种治疗效果优、毒副作用低的药物用于抑制黑色素瘤的生长和迁移.
茶氨酸是从茶叶中提取的一种化合物,具有镇静、增强免疫、抑制肿瘤生长等药理活性,在抗肿瘤方面其单独用药也可对多种癌症细胞的生长发挥一定的抑制作用[4].本实验室在茶氨酸的基础上对其进行改造,制成了具有更强的药理活性的化合物茶溴香酰胺(TBrC),化学结构如图1所示.但是由于其口服生物利用度差,所以对其进行剂型改进,合成了茶溴香酰胺脂质体(TBrC-L),前期初步研究显示其对肺癌细胞的生长和迁移具有抑制作用[5].本研究重点聚焦TBrC-L体外对黑色素瘤细胞生长和迁移的影响与其作用的分子机制,为进一步进行体内动物实验和研发抗黑色素瘤新药提供科学依据.

图1 TBrC化学结构式
1 材料与方法
1.1 材料
1.1.1 药品与试剂 黑色素瘤B16细胞购自中科院上海细胞所;胎牛血清(FBS)、双抗溶液和DMEM细胞培养液购自美国Hyclone 公司;NF-κB抑制剂Bay11-7082(Bay)购自碧云天生物技术研究所;BCA工作液、台盼蓝染色液、四甲基偶氮唑盐(MTT)、Hoechst33258荧光染料、c-Met、HGF、Bcl-2、NF-κB、VEGFR2、Caspase-3、E-cadherin、Bax、p53和Cytochrome c抗体、HRP标记山羊抗小鼠和抗兔购自美国Cell Signaling Technology Inc. 公司.TBrC-L由本实验室依据之前已经发表的方法[5]制备.
1.1.2 仪器 3111型二氧化碳培养箱(Thermo公司);离心机(Eppendorf公司);TE2000-U型倒置荧光显微镜(Nikon公司);全自动酶标仪(Bio-tek公司);小型垂直电泳槽、电转移槽(BIO-RAD公司).
1.2 实验方法
1.2.1 细胞培养 将黑色素瘤B16细胞培养于DMEM高糖培养基(提前加入10%FBS、1%的双抗混合液),将其置于37 ℃恒温常规培养.待细胞贴壁后根据细胞密度及状态进行实验.
1.2.2 MTT法检测TBrC-L对黑色素瘤B16细胞生长的影响 参考之前已有的试验方法[6],在无菌环境下,胰酶消化细胞后收集,再将其制成细胞悬液,在96孔板中每孔接种2 000个细胞,24 h后分组加药,每组设3个平行复孔,分别加入2 μL浓度为16、64、125、250 μmol·L-1的TBrC-L、2 μmol·L-1的Bay以及空白对照.加药后置于培养箱内常规培养,至48 h和72 h时取出,每孔加入提前配置好的MTT溶液10 μL,作用4 h后弃上清液,加入150 μL的DMSO溶解甲瓒晶体,置于摇床震动15 min后用酶标仪检测(检测波长设为570 nm,参考波长为630 nm).根据吸光度计算细胞生长率.
1.2.3 细胞划痕术评估TBrC-L对黑色素瘤B16细胞迁移的影响 用已灭菌的记号笔和直尺在六孔板背面画5条平行直线,将细胞按常规方法收集,并按照每孔5×105个种于六孔板后置于培养箱.培养过夜后用移液枪枪头垂直于板背面的线进行划痕,PBS洗涤2次后拍照.加入2 mL DMEM(无FBS),依次加入16、64、125、250 μmol·L-1的TBrC-L、2 μmol·L-1的Bay以及空白对照,作用12 h后弃去培养液,PBS稍加清洗后拍照.对迁移到划痕处的细胞进行计数.相对细胞迁移率(%)=给药组划痕处细胞数量/空白对照组划痕处细胞数量×100%.
1.2.4 Hoechst 33258染色法观察药物作用下细胞凋亡形态的变化 参考已报道的方法稍加优化[7-8],培养黑色素瘤B16细胞至对数生长期,常规方法处理至浓度为5×105个/mL,并以1 mL/孔种于六孔板,24 h后取出,PBS冲洗2次后加入培养液并加入TBrC-L、Bay以及空白对照,作用48 h后,弃培养液,加入冷固定液(甲醇∶冰醋酸=3∶1),置冰上10 min后弃去上清液,用冷的PBS洗涤3次,加入Hoechst 33258染色液(10 μg/mL),随即放冰上15 min使其充分染色,染色完成后用PBS洗涤,荧光显微镜下观察细胞形态并拍照.
1.2.5 Western Blotting检测TBrC-L对B16细胞中与肿瘤细胞生长、迁移和凋亡相关蛋白表达的影响 基于报道的方法[9],对黑色素瘤B16细胞进行蛋白印迹实验.首先用之前所述的不同浓度的TBrC-L、Bay作用于B16细胞48 h,将细胞刮下收集至EP管中,3 000 r/min离心4 min,弃上清,视细胞数量加入RIPA裂解液(提前加入PMSF),低温裂解15 min,裂解后将细胞在低温下进行超声破碎,用12 000 r/min离心6 min,用BCA法检测并计算蛋白浓度,以50 μg的上样量求得上样体积.按顺序将预染好的Marker和分装好的蛋白加入样品槽,记录上样顺序,接通电源,用SDS-PAGE凝胶电泳将蛋白按照分子质量分离出来,然后将蛋白转至用甲醇活化好的PVDF膜上,转膜后TBST洗3次,每次5 min,用7%的脱脂奶粉封闭,置于摇床上晃动2 h,按说明书封一抗并放在4 ℃过夜,第二天洗涤后封二抗,孵育1 h后洗涤3次,然后进行ECL显色,按序进行显影、定影,然后根据条带面积及曝光度软件分析计算相对蛋白表达水平,以GAPDH作为内参分析所检测蛋白的相对表达水平.
本实验中均采用NF-κB抑制剂Bay为阳性对照,是由于NF-κB在大多数肿瘤都是高激活状态,参与调控与肿瘤细胞生长、迁移和侵袭等相关基因的转录,被认为是最重要的原癌基因之一[10],NF-κB的组成性活化是黑色素瘤的标志之一[11],因此,抑制NF-κB的活性是治疗黑色素瘤的关键位点之一.故本实验以NF-κB抑制剂Bay为阳性对照,评估TBrC-L对B16细胞生长、迁移的影响及其分子机制.
1.3 统计方法
2 结果与分析
2.1 TBrC-L对黑色素瘤B16细胞生长的影响
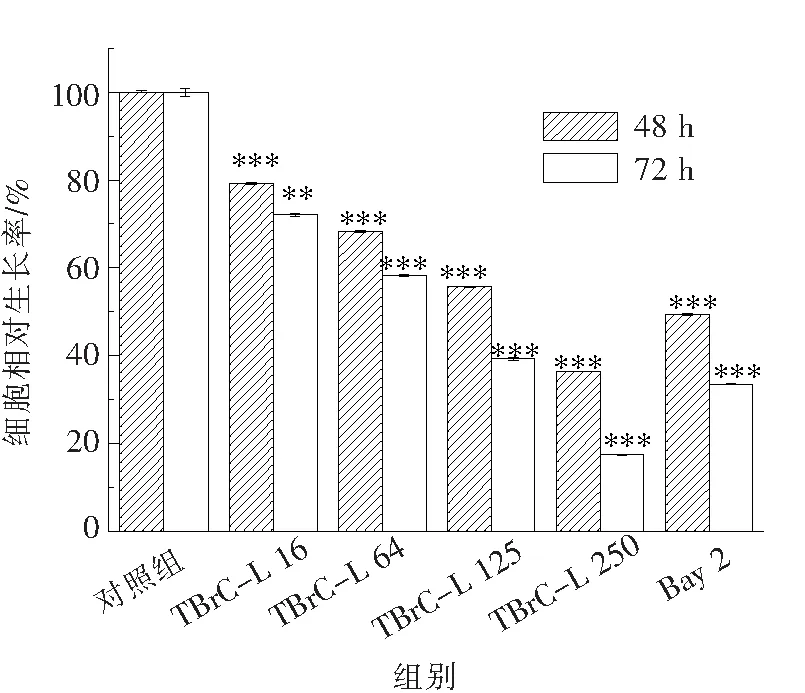
如图2所示,MTT实验结果中,16~250 μmol·L-1的TBrC-L均能对B16细胞的生长产生不同程度的抑制作用,在药物浓度递增过程中,其抑制作用也逐渐加强,药物作用72 h时产生的抑制作用显著优于48 h.数据显示,250 μmol·L-1的TBrC-L在48 h和72 h分别能产生63%及80%的抑制效果,高剂量的TBrC-L甚至可以产生比阳性对照NF-κB抑制剂Bay稍强的抑制作用.
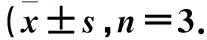
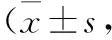
2.2 TBrC-L对黑色素瘤B16细胞迁移的影响
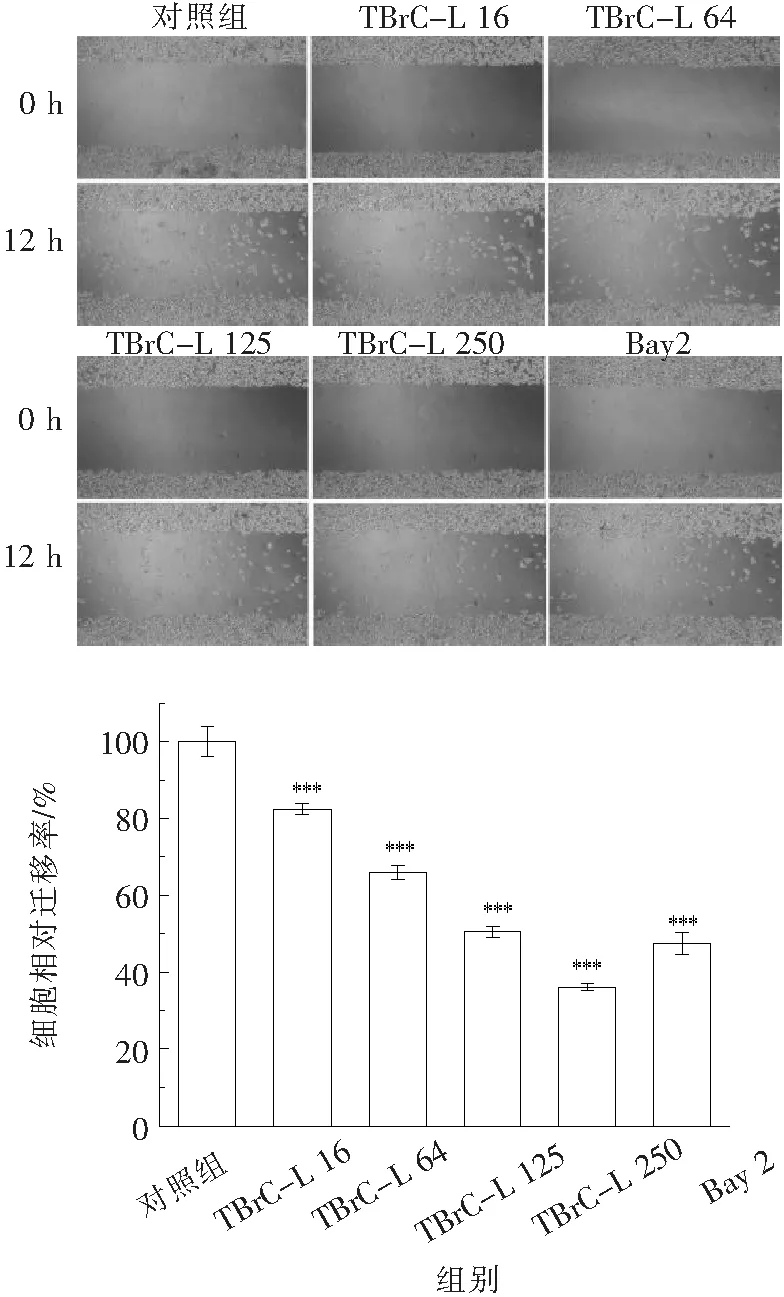
细胞划痕实验结果见图3,在划痕后12 h时,空白对照组细胞迁移数量较多,说明B16细胞具有很强的迁移能力,不同浓度给药组表现出了显著的抑制迁移的作用,高浓度的TBrC-L相对迁移率为36.17%,而阳性对照Bay组的相对迁移率为47.2%,表现出稍优于阳性对照组的抑制作用.实验结果表明,TBrC-L可对黑色素瘤B16细胞的迁移发挥显著的抑制作用.
2.3 TBrC-L对黑色素瘤B16细胞凋亡的影响
通过Hoechst 33258染色法评估TBrC-L对B16细胞产生的凋亡作用,结果如图4所示.荧光显微镜下,空白对照组细胞均匀分布,细胞形态完整,而药物作用下的细胞形态产生了变化,如细胞核浓缩,染色质聚集、边缘化,出现凋亡小体等.实验结果表明,TBrC-L可对B16细胞的凋亡产生诱导作用.高浓度的TBrC-L作用下,细胞的凋亡率为29%,阳性对照Bay组的细胞凋亡率为26%.
2.4 TBrC-L对黑色素瘤B16细胞相关蛋白表达的影响
2.4.1 TBrC-L对B16细胞中p53蛋白表达的影响 如图5所示,在TBrC-L的作用下B16细胞中p53蛋白表达水平显著升高,且药物浓度增加,p53蛋白表达也明显上调.高、低浓度药物作用下分别上调2.3和1.3倍.阳性对照NF-κB抑制剂Bay也增加了p53蛋白的表达,上调了2.5倍.
2.4.2 TBrC-L对B16细胞中Bcl-2和Bax蛋白表达的影响 由图6可知,高低浓度的TBrC-L 作用于B16 细胞后,Bcl-2蛋白表达量显著降低,而Bax表达量增多,所以Bcl-2/Bax值变小,16、250 μmol·L-1的TBrC-L分别使比值下调60%和78%,阳性对照Bay使其下降了81%.

图4 TBrC-L对B16细胞凋亡的影响与空白对照组相比,***P<0.001)
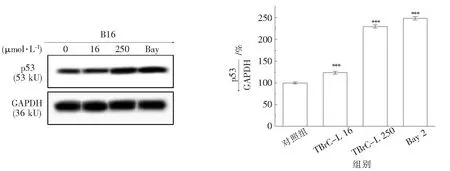
图5 TBrC-L对B16细胞中p53蛋白表达的影响与对照组相比,***P<0.001)


图6 TBrC-L对B16细胞Bcl-2和Bax蛋白表达的影响与对照组相比,***P<0.001)
2.4.3 TBrC-L对B16细胞中胞浆细胞色素C(cy c)蛋白水平的影响 TBrC-L作用于B16细胞48 h后,胞浆中细胞色素C水平显著提高,高低浓度药物处理后,其胞浆蛋白水平分别提高了2.6和1.6倍,阳性对照Bay组提高了2.5倍.结果见图7.
2.4.4 TBrC-L对B16细胞中Caspase-3蛋白表达的影响 如图8所示,B16细胞中Caspase-3蛋白在高低浓度的TBrC-L作用下其表达量均显著上调,与未用药组相比分别上调8倍和5倍,阳性对照Bay组也上调7.9倍.
2.4.5 TBrC-L对B16细胞中HGF蛋白表达的影响 结果如图9所示,在TBrC-L 48 h作用下,细胞中的肝细胞生长因子HGF蛋白表达水平显著降低, 与空白对照组相比, 高低浓度的TBrC-L分别使其下调了51%和26%,根据结果可知,随着药物浓度增高,HGF蛋白的表达量下调更显著.阳性对照Bay组,使其下调57%.
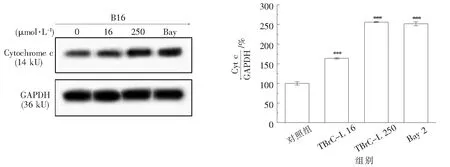
图7 TBrC-L对B16细胞中胞浆细胞色素C蛋白水平的影响与对照组相比,***P<0.001)
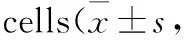
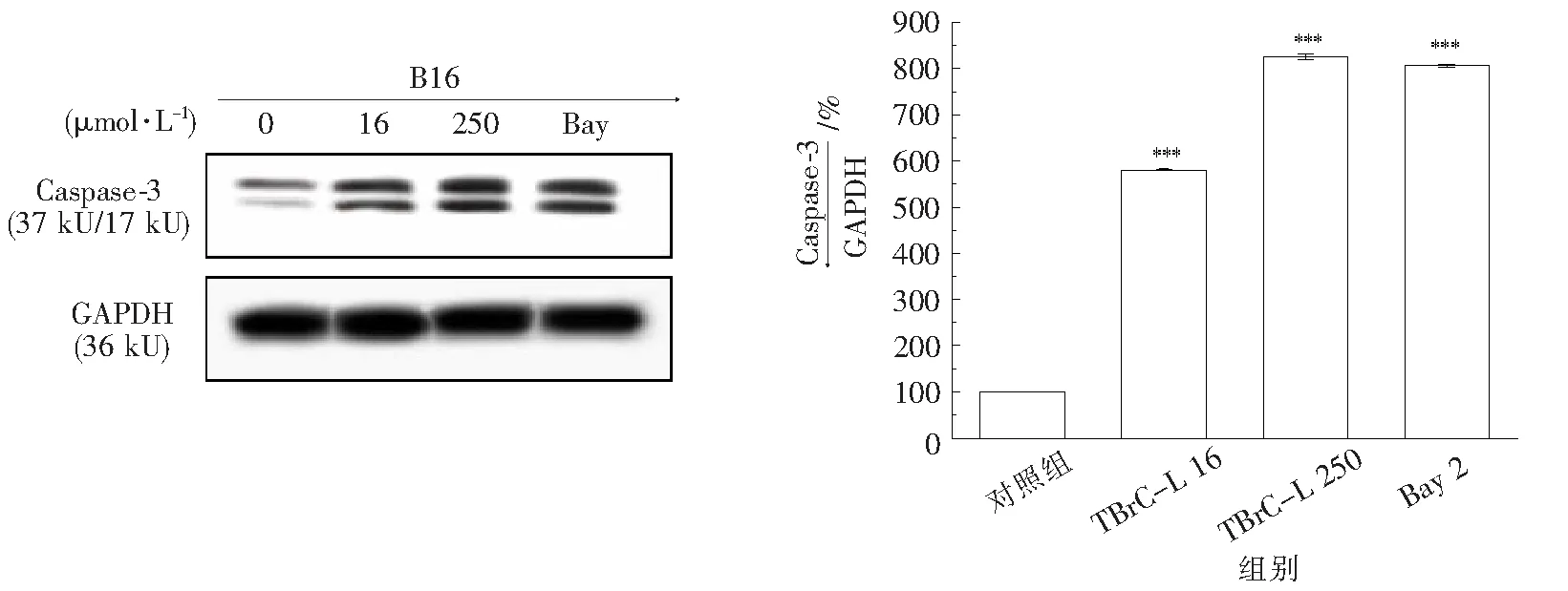
图8 TBrC-L对B16细胞Caspase-3蛋白表达的影响与对照组相比,***P<0.001)

图9 TBrC-L对B16细胞中HGF蛋白表达的影响与对照组相比,***P<0.001)
2.4.6 TBrC-L对B16细胞中c-Met蛋白表达的影响 结果如图10所示,16 μmol·L-1和250 μmol·L-1的TBrC-L均可下调B16细胞中c-Met受体蛋白的表达水平,与未给药组相比,高低浓度的TBrC-L分别使其下调了58%和37%,阳性对照组使其下调了56%,可见,高浓度的TBrC-L对c-Met蛋白表达的影响甚至稍优于阳性对照Bay组.
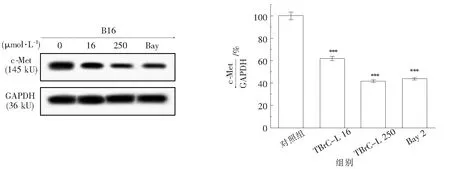
图10 TBrC-L对B16细胞中c-Met受体蛋白表达的影响与对照组相比,***P<0.001)
2.4.7 TBrC-L对B16细胞中NF-κB蛋白表达的影响 实验结果如图11所示,TBrC-L作用于B16细胞后可显著下调NF-κB蛋白的表达水平,由实验结果可见,16、250 μmol·L-1的TBrC-L分别使其表达量下调了29%和54%,阳性对照Bay组使其下调了56%.
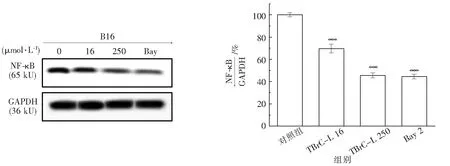
图11 TBrC-L对B16细胞中NF-κB蛋白表达的影响与对照组相比,***P<0.001)
2.4.8 TBrC-L对B16细胞中VEGFR2蛋白表达的影响 实验结果如图12所示,两浓度作用下,B16细胞内VEGFR2受体蛋白的表达水平显著降低,16、250 μmol·L-1的TBrC-L分别使其表达量下调了34%和51%,阳性对照Bay组使其下调了54%.
2.4.9 TBrC-L对B16细胞中E-cadherin蛋白表达的影响 实验结果如图13所示,不同浓度的TBrC-L作用于B16细胞后,E-cadherin蛋白表达量上调,与空白对照组相比,高低浓度药物作用下其表达量分别上调了1.4倍和2倍,阳性对照Bay组使其上调了1.9倍.
3 讨论与结论
TBrC是本实验室由茶氨酸修饰而得,并进一步合成TBrC-L,大大改善了生物利用度,使其抗癌作用效果显著提高.本研究结果提示,TBrC-L在黑色素瘤B16细胞的生长和迁移方面均可发挥较强的抑制作用,可促进B16细胞的凋亡,通过Western blotting实验进一步了解其抗黑色素瘤的分子机制,初步明确其对黑色素瘤B16细胞中与肿瘤生长、迁移和凋亡相关蛋白的影响.

图12 TBrC-L对B16细胞中VEGFR2受体蛋白表达的影响与对照组相比,***P<0.001)
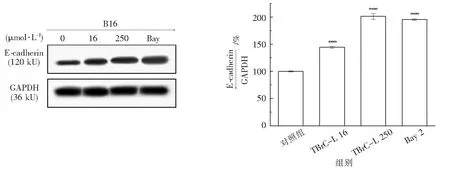
图13 TBrC-L对B16细胞中E-cadherin蛋白表达的影响与对照组相比,***P<0.001)
细胞的凋亡过程受到许多相关蛋白的严格控制. Bcl-2家族蛋白[12]在细胞凋亡过程中发挥着不容小觑的作用,其中Bcl-2可促进细胞增殖,减少凋亡的产生,Bax蛋白可与其结合,产生异构二聚体,影响Bcl-2蛋白的表达,使其抑制细胞凋亡的作用大大削减,Bax蛋白的作用却会加强,二者结合可加速细胞凋亡,二者比值的平衡性在细胞凋亡过程中也至关重要,它决定了细胞凋亡与否,并且影响细胞凋亡的阈值[13]. 抑癌因子p53蛋白在细胞周期中可发挥调控作用,当细胞内的DNA遭破损时,p53蛋白可根据其损伤程度给予修复或促进其凋亡[11-15]. p53的激活还可触发包括Bax在内的促凋亡基因的激活,进而促进肿瘤细胞凋亡[16].Bcl-2与Bax比值的变化还可引起线粒体膜通透性的增强,从而释出细胞色素C,胞浆中细胞色素C的增多可间接激活半胱天冬酶(Caspase-3)[17].Caspase-3活化后,便可发挥很强的促细胞凋亡的作用,它可以通过裂解DNA损伤相关修复因子、抑制细胞凋亡相关分子等发挥促进细胞凋亡的作用[18].本实验研究证实,TBrC-L可显著下调Bcl-2的表达,上调Bax的表达,使Bcl-2/Bax值降低,并且使细胞色素C表达水平上调,进而增加Caspase-3的表达,加速肿瘤细胞的凋亡.
肝细胞生长因子(HGF)及其受体Met可调节多种细胞功能,包括生长、增殖、迁移和形态等[19].HGF作为细胞中重要的活性因子拥有复杂的生物活性,在免疫调节、血管生成等方面都有着至关重要的作用,它可以参与细胞有丝分裂、促进细胞运动从而促进肿瘤细胞的生长和转移[20].原癌基因编码的c-Met蛋白是一种跨膜受体,可以通过自身反应完成磷酸化[21].当HGF与c-Met结合后,促进酪氨酸残基磷酸化,进而刺激细胞内其他信号通路产生活性,最终引起肿瘤细胞的增殖、迁移和侵袭.本实验研究中,TBrC-L可显著下调HGF和c-Met蛋白的表达,在B16细胞生长和迁移方面发挥了显著性抑制作用.
核转录因子NF-κB是REL蛋白家族的一员,存在形式通常是二聚体,未被激活时与其抑制底物 IκB存在于细胞质之中,一经激活,便迅速进入胞核,作用于凋亡基因调节细胞周期,遏抑细胞凋亡,促进肿瘤生长[22].其次NF-κB还能够诱导血管内皮生长因子(VEGF)的表达,研究表明,应激机制通过VEGF在肿瘤细胞中的分泌刺激肿瘤血管生成,血管新生在肿瘤的生长和转移中起着关键性的作用, 且与预后不良密切相关[23].VEGFR2是VEGF非常重要的受体之一[24],二者结合后,在促进血管生成方面的能力显著增强,可加速肿瘤细胞的增殖和转移.此外,有研究表明,NF-κB与上皮型钙粘蛋白(E-cadherin)也有着千丝万缕的关系,若将NF-κB信号通路阻断,E-cadherin的表达也会受到影响,而E-cadherin的缺失或低表达又可以刺激NF-κB通路产生活性[25].E-cadherin在正常细胞间的黏连和信号传导方面发挥着不可或缺的作用,若E-cadherin表达下降,那么细胞间粘附和细胞连接的丧失使细胞与原始肿瘤分离,侵袭周围组织,并迁移到远处[26]. 这类蛋白还可对细胞内多条信号通路的活性产生一定的影响,如MAPK、PI3K、NF-κB等信号通路[27].TBrC-L可显著下调NF-κB和VEGFR2的表达,并诱导E-cadherin蛋白的表达,从而达到抑制肿瘤细胞生长增殖和转移的效果.
综上所述,TBrC-L可有效地抑制黑色素瘤B16细胞的生长、迁移,促进肿瘤细胞的凋亡,其作用的分子机制可能与HGF/Met/VEGFR2-NF-κB信号通路有关.本研究在黑色素瘤的医治方面提供了新的线索,进一步确认了TBrC-L开发为抗癌新药的潜力.但是本实验中TBrC-L对黑色素瘤的作用仍处于体外研究阶段,由于体外和体内环境差异较大,后续研究将进一步进行体内动物实验,以证实体外实验和脂质体制剂的体内靶向性及其生物利用度,TBrC-L实现黑色素瘤的靶向治疗效果和作用机制值得进一步的深入研究.
