一例重症/难治性哮喘合并肺栓塞的机制探究和体会
2019-07-16卢朝晓苏楠崔晓阳王辰
卢朝晓 苏楠 崔晓阳 王辰
1中日友好医院呼吸与危重症医学科 中日友好医院呼吸中心 国家呼吸疾病临床研究中心,北京100029;2中国医学科学院 北京协和医学院100730
卢朝晓现在天水四零七医院呼吸感染内科741000
1 病例资料
患者男,55岁,主因 “发作性喘息15年,加重伴呼吸困难2个月”于2018年6月21日收入中日友好医院呼吸与危重症医学科。患者2003年接触刺激性气体后出现咳嗽、咳痰伴发作性喘息,当地诊断为支气管哮喘 (简称哮喘),经住院治疗后好转。此后症状反复发作,每年5月初和10月初前后明显。多次因 “哮喘急性发作”住院治疗,住院期间均给予地塞米松、抗生素及茶碱治疗。2005年开始使用舒利迭 (沙美特罗氟替卡松吸入剂,50μg/250μg,1吸/次,2次/d)联合醋酸泼尼松片 (30 mg/次,口服,2次/d)治疗。2010年开始改用信必可都保 (布地奈德福莫特罗吸入剂,160μg/4.5μg,1吸/次,2次/d)联合醋酸泼尼松片 (20 mg/次,口服,2次/d)治疗,其喘息症状时轻时重,醋酸泼尼松片减量至15 mg/次 (口服,2次/d)维持治疗。2018年4月受凉后喘息再次加重,口服泼尼松 (30 mg/次,2次/d)改善不明显。2018年6月呼吸困难进一步加重,就诊于当地医院呼吸科,行胸部CT平扫示双肺肺气肿。给予哌拉西林他唑巴坦、多索茶碱、氢化可的松、泮托拉唑静脉点滴治疗后症状仍不缓解,并出现少尿、端坐呼吸、全身水肿等症状。为进一步诊治,转入中日友好医院就诊,急诊以 “哮喘急性发作”收入呼吸与危重症医学科。患者既往糖尿病病史8年,右下肢深静脉血栓病史5年,右手食指、中指、无名指栓塞病史3年。否认食物药物过敏史。吸烟15年,20支/d,已戒烟15年。家族史无特殊。入院查体:体温36.8℃,脉搏108次/min,呼吸频率25次/min,血压130/80 mm Hg(1 mm Hg=0.133 kPa);库欣面容,意识清楚,精神弱,颜面及四肢凹陷性水肿,口唇发绀;双肺可闻及弥漫呼气相哮鸣音,心音正常,心率108次/min,心律整齐,各瓣膜听诊区未闻及病理性杂音;腹部膨隆,无腹壁静脉曲张,无压痛、反跳痛;肝脾未触及,Murphy氏征阴性,无移动性浊音。入院时血气分析 (吸入氧浓度为0.21):p H值7.47,PaCO2为 36.2 mm Hg,PaO2为 57 mm Hg,HCO3-为27.2 mmol/L,剩余碱3.4 mmol/L,血乳酸1.8 mmol/L。血常规示:白细胞12.16×109/L,中性粒细胞10.41×109/L,嗜酸粒细胞0.01×109/L,红细胞4.82×1012/L,血红蛋白152 g/L。凝血六项示:凝血酶原时间13.5 s,凝血酶原活动度92%,国际标准化比值1.05,纤维蛋白原定量测定2.72 g/L,活化部分凝血活酶时间32.3 s,凝血酶时间14.8 s,D-二聚体定量0.8 mg/L,纤维蛋白原降解产物4.11 mg/L。心梗四项示:肌酸激酶同工酶MB 3.9μg/L,肌红蛋白55.92μg/L,肌钙蛋白I 0.045μg/L,B-型利钠肽492.4 ng/L。C反应蛋白、降钙素原、ESR、抗核抗体谱、血管炎抗体谱、类风湿抗体谱及自身免疫性肝炎抗体谱均阴性;血清过敏原总IgE为67.6 IU/ml。吸入及食物 (19项)特异性IgE均阴性。蛋白C活性测定:137%(70%~130%);蛋白S活性测定:103%(55%~140%);抗凝血酶Ⅲ活性测定:102%(80%~120%);狼疮抗凝血因子试验初筛比值为0.29(<1.20)。副鼻窦CT平扫示双侧上颌窦、右侧筛窦炎,鼻中隔略偏曲。超声心动图示主动脉根部、肺主动脉内径正常范围,各房室内径正常范围,室间隔正常上限,主动脉瓣硬化。左心室射血分数为73%。初步诊断考虑哮喘急性发作,给予甲泼尼龙琥珀酸钠40 mg和多索茶碱300 mg静脉滴注以及支气管舒张剂雾化治疗,同时给予哌拉西林钠舒巴坦钠5 g(静脉滴注,每8小时1次)、托拉塞米10 mg(静脉注射,1次/d)。治疗3 d后,患者呼吸困难症状明显好转,查体双肺哮鸣音明显减少,监测峰流速占预计值百分比 (peak expiratory flow per prediction,PEF%pred)较入院时(34%)显著上升,但Ⅰ型呼吸衰竭仍未纠正,难以用哮喘急性发作解释,行CT肺血管造影示肺段及亚段动脉中除左上叶肺动脉、左上叶尖段肺动脉、左下叶肺动脉以外,余肺动脉均可见充盈缺损样血栓征象 (图1)。考虑急性肺栓塞。
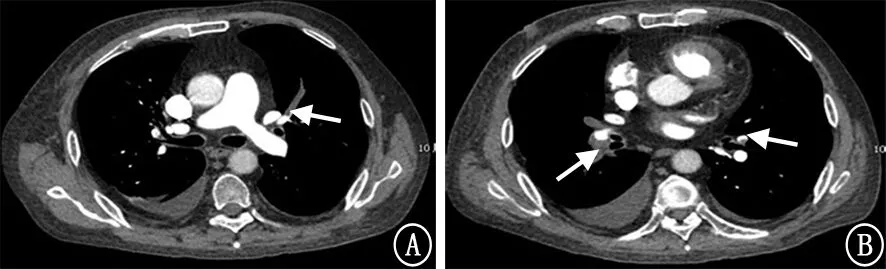
图1 CT肺血管造影 A:左肺舌段肺动脉内充盈缺损样血栓征象 (箭头示);B:双肺下叶基底段肺动脉内充盈缺损样血栓征象 (箭头示)
肺通气/灌注断层显像示双肺多发血流灌注受损,通气大致正常,考虑肺栓塞改变 (图2)。

图2 肺通气/灌注断层显像示双肺多发血流灌注受损,通气大致正常 A:肺灌注扫描;B:肺通气扫描
下肢血管超声检查示右侧股静脉管腔内可见实性低回声,长约15 cm,宽约0.6 cm,左侧腘静脉管腔内可见实性低回声,长约2.4 cm,宽约0.6 cm。
给予修正诊断:急性肺栓塞 (中低危);重症/难治性哮喘;Ⅰ型呼吸衰竭;下肢静脉血栓形成;糖尿病。给予依诺肝素 (100 U/kg,皮下注射,每12小时1次)抗凝和规范的第五级哮喘治疗 (信必可、缓释茶碱、孟鲁司特钠、噻托溴铵和口服泼尼松30 mg/d);因难治性哮喘患者长期激素依赖,目前并发腹型肥胖、高脂血症、糖尿病、深静脉血栓栓塞症等多种疾病,为减少全身激素的用量,根据其血总IgE水平 (67.6 IU/ml)和体质量 (60 kg)给予奥马珠单抗 (150 mg,皮下注射,每4周1次)抗IgE治疗,1周后PEF%pred上升至60%以上,遂将口服激素快速减量,4周后减至15 mg/d(低于患者既往最小维持剂量),无哮喘症状发作,PEF%pred可维持在60%左右,日变异率基本稳定在5%以内 (治疗前PEF变异率为30%左右)。治疗2周时 (7月6日)复查下肢血管超声显示左胫后静脉见条状实性低回声,长约1.1 cm,右股静脉内见1.7 cm×1.32 cm低回声,较前明显好转,提示抗凝治疗有效。治疗2个月后患者复诊,超声心动图示主动脉根部、肺主动脉内径正常范围,肺动脉高压 (估测肺动脉收缩压约65 mm Hg),右心房、右心室比例增大,右室/左室横径为1.09,右心室壁增厚约8 mm,三尖瓣反流 (少量),主动脉瓣硬化。左心室射血分数为76%。补充诊断:慢性血栓栓塞性肺动脉高压。随访至2019年4月患者口服皮质激素已减停,继续奥马珠单抗 (150 mg,皮下注射,每4周1次)抗IgE治疗,未因哮喘急性发作住院治疗。复查下肢以及肺动脉血栓无复发,慢性血栓栓塞性肺动脉高压择期给予球囊扩张术治疗后,病情基本稳定,患者生存质量较前明显升高。
2 讨论
该患者为IgE介导的重症/难治性哮喘,反复哮喘发作具有明显的季节性,长期口服醋酸泼尼松片30~50 mg仍反复出现喘息加重,合并腹型肥胖、高血糖、高血压、静脉血栓栓塞 (venous thromboembolism,VTE)等并发疾病,本次确诊了肺栓塞。对于第四级治疗不能控制的重症/难治性哮喘,国内外哮喘指南均建议给予奥马珠单抗治疗,此患者在充分给予第五级哮喘治疗药物的基础上给予奥马珠单抗治疗后也获得了较好的疗效。刘长智等[1]的一项meta分析显示,对于难治性哮喘,在常规方案的基础上加用奥马珠单抗治疗,可减低哮喘急性发作风险,减少激素用量,改善症状,减少缓解药物用量。麦林等[2]的一项系统评价亦显示,奥马珠单抗在重症/难治性哮喘患者的治疗中,可明显减少其急性加重的次数,改善肺功能,减少激素的用量,提高哮喘患者的生活质量,并对奥马珠单抗治疗过敏性哮喘的安全性亦有肯定的结论。
该患者在哮喘症状好转、监测PEF亦明显好转后,呼吸衰竭仍不能纠正,结合患者既往有长期口服糖皮质激素、下肢静脉血栓等病史,行CT肺血管造影以及肺通气/灌注断层显像示肺栓塞,最后确诊为重症/难治性哮喘合并肺栓塞。虽然该患者既往有长期口服糖皮质激素史,并且合并高脂血症、反复静脉血栓等病史,但是起因皆从哮喘开始。关于哮喘与肺栓塞之间的联系,Chung等[3]的一项队列研究跟踪调查了186 182人年的哮喘患者和743 374人年的非哮喘患者,经过性别、年龄、共病和雌激素补充调整后,结果显示哮喘队列的肺栓塞危险比为3.24,并且随着哮喘发作和住院次数的增加,肺栓塞发生的风险显著增加。Majoor等[4]认为糖皮质激素治疗是哮喘患者并发肺栓塞的因素之一。Zöller等[5]研究发现哮喘患者的肺栓塞风险增加,且重症哮喘患者的风险高于轻-中度哮喘患者;全身糖皮质激素治疗的哮喘患者风险更高。该研究者在大样本数据中分析了肺栓塞、VTE及肺栓塞+VTE患者,得出2个结论:一是发现了时间依赖效应,即在哮喘加重入院后3个月内发生VTE的风险最高;二是发现重症哮喘,尤其是长期应用糖皮质激素的重症/难治性哮喘患者中,并发肺栓塞的风险明显升高。Sneeboer等[6]的研究选取了648例哮喘患者,其中重症患者283例,总共有35个VTE事件,包括16个深静脉血栓和19个肺栓塞,得出结论为重症哮喘和口服皮质类固醇激素是肺栓塞的独立危险因素,哮喘与深静脉血栓形成无关。与普通人相比,重症哮喘患者患肺栓塞的风险几乎增加了9倍,轻度至中度哮喘患者的肺栓塞风险增加了3.5倍。因此,重症哮喘极大地增加了肺栓塞的风险,特别是使用皮质类固醇激素治疗的哮喘患者。
Majoor等[4]提出了哮喘并发肺栓塞的3个机制:(1)气道炎症通过多种途径影响凝血,其中嗜酸粒细胞、中性粒细胞以及支气管上皮细胞、肥大细胞都有可能导致凝血不平衡,增加静脉血栓风险,并且发现在气道炎症与哮喘的严重程度成正比时,其静脉血栓风险也在升高。(2)哮喘患者血栓形成前状态可能与缺氧有关,缺氧可引起全身炎症和凝血激活。(3)皮质类固醇激素的使用。这一点在同样需要长疗程糖皮质激素治疗的COPD、慢性肾病等被列入肺栓塞危险因素的疾病中已得到证实。Sneeboer等[6]提出慢性炎症性疾病与凝血激活相关,可致静脉血栓栓塞事件的风险增加,尤其是在疾病活动的期间,这在炎症性肠病、风湿性关节炎、糖尿病和COPD中已经得到证实。de Boer等[7]认为经典参与促凝血和抗凝血途径的介质和细胞在哮喘病理生理学中起作用。为此,哮喘患者表现出气道凝血活化增强、抗凝血蛋白C系统功能受损和纤维蛋白溶解减弱的迹象。
笔者在万方数据库中,以肺栓塞和哮喘为关键词搜索到84篇文献,国内只有2篇文献报道了3例哮喘合并肺栓塞[8-9]。据我国台湾以及国外的相关研究显示,哮喘合并肺栓塞的发病率并不低,且国外已有研究者开展了哮喘合并肺栓塞可能机制与发病情况的大样本研究。我国最新版肺栓塞指南[10]在内科患者VTE风险评估的危险因素中暂未提到重症/难治性哮喘,而重症哮喘专家共识[11]中也只是提出重症哮喘控制不佳时需鉴别肺栓塞,并未提出需考虑重症哮喘合并肺栓塞的可能。本文旨在表明,肺栓塞是一个潜在的威胁生命的疾病,近年来肺栓塞的发病率与日俱增,它可能发生在相对年轻的重症哮喘,而重症哮喘和激素依赖性哮喘患者具有较高的肺栓塞风险,其严重程度以及口服皮质激素的剂量可能与肺栓塞的风险成正比,临床医师应该提高这一意识。该病例的诊治体会是建议对重症哮喘和激素依赖性哮喘患者临床上应该进行血栓或肺栓塞的评估,并及时给予血栓预防策略,因为合并肺栓塞的哮喘更难以控制,合并哮喘的肺栓塞更易慢性化,进而增加并发肺动脉高压的风险。
利益冲突所有作者均声明不存在利益冲突
