外泌体检测及其临床应用研究进展*
2019-07-16林慧娴刘春辰
林慧娴 刘春辰 郑 磊*
外泌体作为细胞外囊泡(extracellular vesicles,EVs)的一种类型,以信号介质的形式参与了机体众多生理病理过程,例如细胞分化、细胞增殖、血管新生、炎症免疫反应以及肿瘤转移与耐药等,在揭示疾病机制的基础研究与疾病诊断、预后评估、靶向治疗等临床应用中极具发展前景。通过聚焦于分离富集、鉴定与内容物分析这三大视角,简要总结外泌体的检测技术,并对其原理和优缺点进行客观评价,这对外泌体检测新技术的开发与临床应用进程的推进具有深远意义。
1 外泌体的生物学特性
外泌体是细胞外环境中含脂质双分子层的一种膜性囊泡,呈杯状和(或)双凹碟状,直径为30~100 nm,密度为1.11~1.19 g/ml[1-2]。外泌体不仅可以被大多数细胞分泌,还可被细菌[3]和病毒[4]分泌,存在于血浆、血清、唾液、羊水、母乳和尿液中,具有特异性的蛋白质、活性的核酸和脂质,在细胞间的物质传递、信息交流、细胞增殖分化、血管生成、免疫调节等过程中发挥重要的生物学作用,并参与了肿瘤以及心血管、消化、免疫、神经等系统疾病的病理过程,有望成为一种新型的疾病诊断标志物。
2 外泌体的主要分离富集技术
外泌体以非均一膜性囊泡的结构散在存在于成分复杂的人体体液标本中,因此外泌体的分离富集是其检测技术的关键环节,所得外泌体的纯度与活性可直接影响后续的鉴定与功能分析。目前,常用的外泌体分离富集技术主要基于外泌体的物理特性(大小、密度等)与免疫学特征,具体原理与优缺点见表1。
3 外泌体的鉴定分析技术
外泌体是EVs的一种类型,为保证不同研究机构研究结果的可信度与重复性,国际细胞外囊泡协会(International Society for Extracellular Vesicles,ISEV)于官方会刊(Journal of Extracellular Vesicles,JEV)发布了EVs研究最低要求(minimal information for studies of EVs,MISEV)的国际研究指南。参考MISEV的建议,外泌体的鉴定主要包括形态学特征、浓度和(或)径粒、蛋白分子表征鉴定,可累加组分的拓扑鉴定[14-15]。
针对外泌体的形态学特征,扫描电子显微镜[16]、透射电子显微镜[17]、原子力显微镜[17]以及随机光学重构显微镜[18]等可直观地表征外泌体的形态学特征,如直径、形状等。其中透射电子显微镜可观察外泌体的内部结构,原子力显微镜可提供三维表面图,随机光学重构显微镜在提高成像分辨率的基础上还可进行目标分子的精确定位。但此类方法不适合大量样本与浓度鉴定。除原子力显微镜外其余方法均需复杂的预处理,脱水固定或是荧光染料染色等均可能影响其活性,不利于后续功能分析。
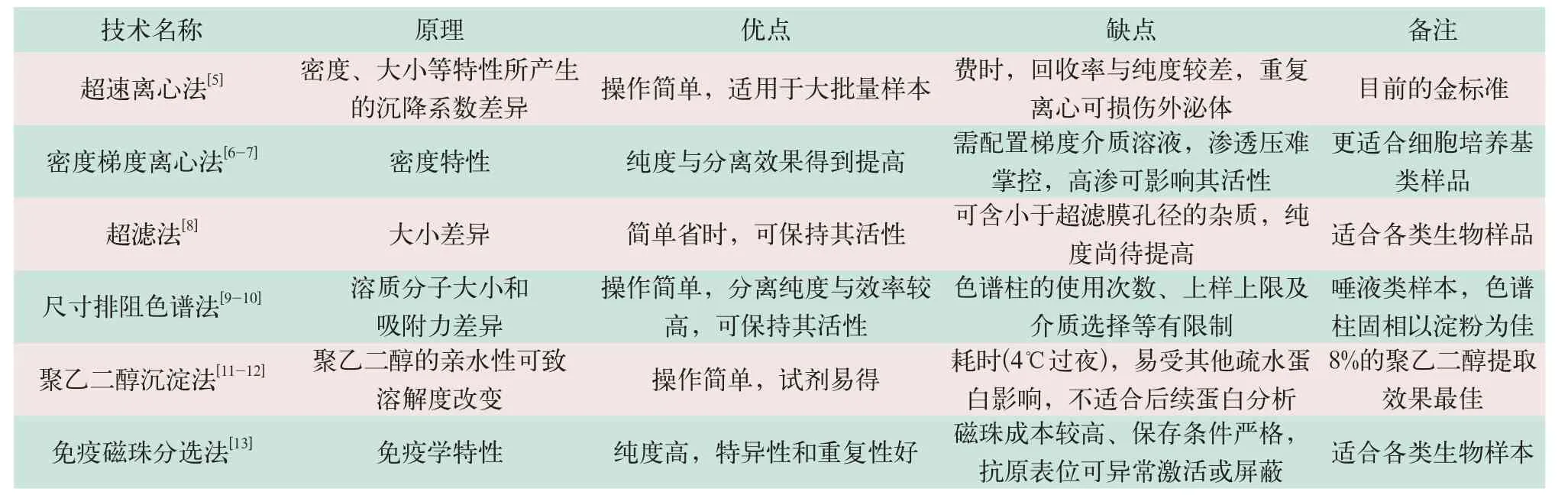
表1 常用外泌体分离技术比较
外泌体的量化,纳米粒子追踪分析(nanoparticle tracking analysis,NTA)[19]与动态光散射(dynamic light scattering,DLS)[20]则可对外泌体进行实时浓度与径粒可视化分析。前者适用于单和(或)多分散性样本,但无法区分样本表型;而后者对均质性样本分析灵敏度高,但不适于非均质样本,因为小颗粒光强波动信号极易被大颗粒所掩盖。可调谐电阻脉冲传感技术[21]通过对瞬时电流的检测亦可实现对外泌体浓度与尺寸等进行精确鉴定。常规和(或)高分辨率流式细胞术也适用于外泌体的粒子数分析。此外,通过十二烷基硫酸钠-聚丙烯酰胺凝胶电泳(sodium dodecyl sulphate-Polyacrylamide gel electrophoresis,SDS-PAGE)、比色法如二喹啉甲酸法(Bicinchoninic acid,BCA)[22]等测总蛋白;荧光测定法(如亲脂性荧光染料DiR)[23]、全反射傅里叶变换红外光谱[24]等测总脂质;毛细管电泳获得图谱测总RNA与酶联免疫吸附分析(enzyme-linked immunosorbent assay,ELISA)、流式细胞术等测特异性分子,亦可获得外泌体的浓度信息。
外泌体蛋白分子表征的方法主要包括ELISA、蛋白印迹法(Western blot)、质谱法及流式细胞术等。根据MISEV的规定,需要选择验证至少3种阳性蛋白标志物(包括跨膜、胞浆及脂质结合型蛋白)与至少1种阴性蛋白标志物的表达来进行外泌体的鉴定。
外泌体的拓扑鉴定主要是针对外泌体的膜蛋白与囊泡内蛋白而言,为其功能研究的进一步深入提供思路。具体可用蛋白酶K处理或胰蛋白酶和(或)胞内蛋白酶Lys-C处理并生物素化后经柱分离,液相色谱串联质谱或质谱进行蛋白组学分析,流式细胞术与荧光显微镜法进一步验证分析,并结合生物信息学完成鉴定[25]。在此过程中,亦可累加原子力显微镜、场发射扫描电子显微镜等手段进行辅助分析[26]。
4 外泌体的内容物分析技术
外泌体可选择性包裹核酸、蛋白质和脂质,真正具有诊断意义的是这些表达了疾病特异蛋白或核酸的外泌体亚群。因此,基于外泌体的临床诊断技术的开发大多聚焦于外泌体亚群内容物的检测。
在疾病特异外泌体核酸亚群的研究中,多采用与血清核酸类似的检测技术:利用二代测序技术或杂交芯片技术[27]对外泌体差异表达的核酸进行筛选,再用实时荧光定量PCR[28]或液滴数字PCR进行验证[29]。
疾病特异外泌体蛋白质标志物的检测是外泌体亚群分类分析的另一重要组成部分。蛋白标志物的筛选多采用标记、非标记蛋白质质谱[30]或蛋白芯片技术[31]对外泌体差异表达的蛋白进行筛选,再用Western blot[32]、纳米流式技术[33]、ELISA及平行反应监测等进行验证。
近年来,关于外泌体核酸和蛋白质综合检测技术的研究众多且日趋成熟,涌现出一批外泌体检测平台,并将其用于疾病的诊断与预后监测。常见外泌体检测平台有光学、电化学和小型微流控检测平台,在分析灵敏度、特异度、检测仪器的微型化、自动化与便捷化上均具有显著优势,有望在未来实现即时检测(point-of-care testing,POCT),见表2。
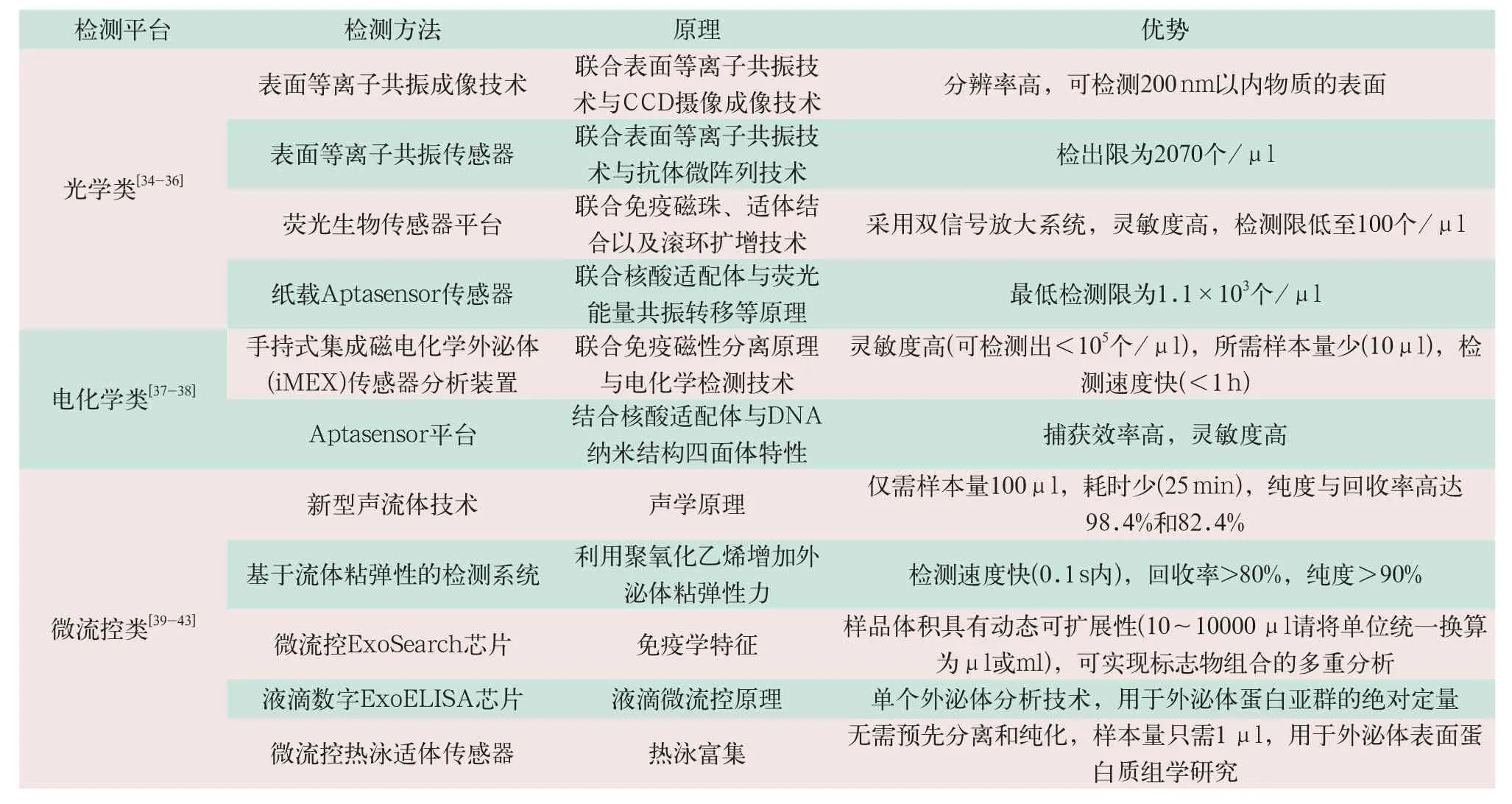
表2 新型检测平台列举
5 外泌体的临床应用
外泌体广泛散布于机体中且运载着多种分泌源细胞的信号分子,是颇具临床价值的循环疾病标志物。与组织病理检查相比,基于血液等体液外泌体的检测方法,患者接受程度更高,便于进行病情监测,更能反映疾病整体情况。与传统血清游离核酸及蛋白标志物相比,外泌体具有显著的靶向性、包含更大量信息、易于保存、检测基质的干扰小等优势。
在恶性肿瘤疾病中,对外泌体内核酸分子的检测展现出极高的诊断应用价值。例如胃癌患者的外泌体miR-423-5p[44]表达水平显著升高,提示其可成为胃癌诊断的标志物,临床试验亦进一步证实外泌体miR-423-5p的诊断灵敏度与特异度分别为81.0%和57.5%,高于传统的血清学标志物CA-199和CEA。在心血管疾病中,受损内皮细胞分泌异常外泌体,能够准确反映病变组织的病理情况,是心血管疾病诊断的良好标志物[45]。糖尿病患者血浆中外泌体水平显著高于健康人群,患不同并发症的糖尿病患者,相应外泌体的内容物表达谱与表达水平也会出现相应改变,如miR-320c[46]/miR-145[47]以及miR-126[48]分别与糖尿病患者的肾脏病变和心肌损伤有关,有望成为预测糖尿病患者并发症发生风险的诊断标志物。
除恶性肿瘤、心血管疾病以及糖尿病外,其他如神经系统退行性疾病、自身免疫性疾病和感染性疾病等均与外泌体的异常密切相关。在神经退行性疾病中,聚集的β淀粉样蛋白具有结合循环外泌体的特性,并且证实通过检测β淀粉样蛋白阳性的循环外泌体水平可以反映患者的神经病变进展[49]。外泌体还可通过产生免疫复合物、抗原提呈以及凝血等过程,参与自身免疫性疾病[50]。病毒感染的细胞释放的外泌体可将病毒RNA递送到树突细胞和巨噬细胞,从而激活受体细胞的模式识别受体,诱导I型干扰素和促炎细胞因子的表达,增强机体抗病毒能力[51]。
6 展望
外泌体作为疾病标志物,用于疾病“液体活检”具有巨大的前景。从以上研究可发现,外泌体检测技术的准确可靠性是外泌体全面发挥其应用潜力的必要条件。虽然随着对外泌体认识的不断加深,涌现出了许多新型检测技术,但到目前为止尚无任何方法可视为外泌体检测的金标准。如何在检测特异性、灵敏度以及回收率、分离纯度与成本上取得平衡仍是亟待解决的问题。再者,各检测技术缺乏统一标准的规范化操作指南,质量控制体系也处于起步阶段,这极大限制了外泌体的应用。未来将联合分子生物学、光学、声学、电磁学、机械自动化、计算机技术以及纳米材料和传感器等多学科优势开发新检测技术,提高检测准确性,促进其微型化与自动化发展。此外,进一步探究外泌体的生物学特性,有利于新检测技术开发,亦有利于其临床有效性与实用性证明,对推进外泌体的应用进程具有深远意义。
