山药水溶性蛋白质凝胶特性的研究
2019-07-10于昊蕊陈佳男王晓文张俊伟薛友林
高 琦,于昊蕊,陈佳男,王晓文,张俊伟,薛友林,*
(1.辽宁大学轻型产业学院,辽宁沈阳 110036; 2.辽宁行政学院,辽宁沈阳 110161)
山药是薯蓣科薯蓣属(Dioscoreaspp,Dioscoreaceae)的一种常见的块茎作物,具有药食兼用的特点,为一年或多年生蔓生草本植物[1]。我国拥有丰富的山药资源,种植面积广,具有较高的产量和悠久的药用历史,具有降血脂,降血糖,抗衰老,调理肠胃,增强免疫等功能[2]。通常山药(干重)中淀粉含量为75%~84%,粗蛋白含量为6%~8%,粗纤维含量为1.2%~1.8%[3]。另外,山药中含有多种生物活性物质,例如:酚类化合物、糖蛋白、多糖、甾体皂甙等,其还含有丰富的人体需要的必需氨基酸等17种氨基酸,其中谷氨酸和精氨酸含量较高[4],故拥有较高的营养价值。山药储藏蛋白Dioscorin占山药总可溶性蛋白(YSP)的80%,其分子量为31 kDa,且在体内和体外都能表现出较好的生物活性,包括碳酸酐酶活性、胰蛋白酶抑制剂活性、抗氧化活性、免疫调节活性、抗高血压活性、凝集素活性、呼吸道上皮细胞保护活性等[5],因此有作为保健品或食品功能性添加成分的潜力,需要对其加工特性进行深入研究[6]。实验室前期研究表明,YSP具有较好的溶解性、持油力及乳化活性,这些能力对其应用于食品体系来说十分重要[7]。
蛋白的胶凝作用是指变性蛋白分子聚集并形成有序的蛋白质网络结构的过程,是蛋白质的一种重要的功能性质,同时其凝胶的流变学特性也可以作为调整食品物理性质的重要依据[8]。此外,蛋白的凝胶行为及其流变学性质与某些食品中独特的质构、风味、感观品质、保水性和保留其他成分的能力有着密不可分的关系[9]。在食品中添加植物蛋白,例如大豆分离蛋白[10],可以增加其水分含量,由于其良好的凝胶组织性,使食品的质构和口感得到很好的改善,同时在一定程度上可以降低食品中脂肪含量,显著提高食品的营养价值和商品价值。
目前,国内外对YSP的研究一般集中在蛋白质的提取工艺的优化,还有物理性质和功能性质的研究,例如:溶解度、起泡性及泡沫稳定性、乳化性及稳定性等[11],但是对山药蛋白质凝胶特性的详细研究鲜有报道。有研究认为,蛋白质凝胶形成受加热温度、加热时间、pH、蛋白质浓度、离子强度等因素的影响[12]。因此,本文利用质构仪和流变仪对YSP的凝胶特性进行研究,可以为综合开发山药新产品提供数据支持。
1 材料与方法
1.1 材料与仪器
白玉山药 沈阳十二线果品蔬菜批发市场;氯化钠、亚硫酸氢钠 均为分析纯;甲基硅油 国药集团化学试剂有限公司。
PHS-3CB型pH计 上海越平科学仪器有限公司;TG16G台式高速离心机 长沙英泰仪器有限公司;FB124电子分析天平 上海舜宇恒平科学仪器有限公司;LGJ-10型冷冻干燥机 北京松源华兴科技发展有限公司;CT3质构仪 美国博勒飞Brookfield;TH-400 BQ型数控超声波清洗机 济宁天华超声电子仪器有限公司;磁力搅拌器 上海凌科实业发展有限公司;恒温水浴锅 上海启前电子科技有限公司;漩涡振荡器 广东安胜仪器有限公司;TA-DHR2型流变仪 美国TA仪器;Microza MF/UF小型膜试验设备 日本Asahi Kasei公司。
1.2 实验方法
1.2.1 YSP的提取 首先将山药洗净、去皮、切块,加入一定量的冰水抽提溶液进行打浆(料液比为1∶2),并加入1%的亚硫酸氢钠作为护色剂,用1 mol/L的NaOH调节pH至9,在4 ℃时磁力搅拌20 min,5000 r/min离心30 min,双层纱布过滤后取上清液,用2 mol/L的HCl调节pH至3.5(根据初步研究确定山药可溶性蛋白的等电点pI=3.5),4 ℃磁力搅拌1 h后,5000 r/min离心30 min,双层纱布过滤,得到的沉淀加水回溶,用1 mol/L的NaOH调节pH至7,最后经过超滤(截留物质的分子量为10 kDa)、冷冻干燥获得YSP[13]。
1.2.2 YSP最小凝胶浓度的测定 根据Aluko等的方法[14],测定YSP的最小凝胶浓度(LGC),将不同蛋白质浓度(2%~14%,w/v)(2%、4%、6%、8%、10%、12%、14%)的样品悬浮在水中,95 ℃水浴1 h,在自来水中冷却,然后放在冰箱(4 ℃)冷却2 h。取出烧杯并倒置,其最低样品浓度使凝胶不滑动即为最小凝胶浓度。
1.2.3 YSP凝胶的制备
1.2.3.1 不同YSP浓度的凝胶的制备 分别取YSP 0.40、0.50、0.60、0.70 g于烧杯中,并加入蒸馏水,分别配制成质量浓度为8%、10%、12%、14%的YSP溶液,调节pH=7,漩涡振荡器搅拌10 min,95 ℃水浴1 h,然后4 ℃冷却24 h,即得到不同蛋白质浓度的凝胶。
1.2.3.2 不同pH的YSP凝胶的制备 固定YSP浓度为8%,分别调节pH为8、9、10、11,后续处理同1.2.3.1,即得到不同pH下的凝胶。
1.2.3.3 不同NaCl浓度的YSP凝胶的制备 固定YSP浓度为8%,体系的pH为7,将YSP分别溶于不同浓度的NaCl(0.05、0.10、0.15、0.20 mol/L)溶液中,后续处理同1.2.3.1,即得到不同NaCl浓度的凝胶。
1.2.4 YSP凝胶流变性质的测定 将制备好的凝胶置于流变仪平行板之间,间隙设为1 mm,抹去过多的样品,并在样品裸露的边缘处涂上一层薄薄的甲基硅油,避免水分蒸发[15]。随着时间的变化,测定不同温度下G′(储能模量,Storage modulus)、G″(损耗模量,Loss modulus)、剪切速率的变化。在振荡(oscillation)和温度梯度(temperature ramp)模式下设置升温程序(起始温度25 ℃,终止温度95 ℃)和降温程序(起始温度95 ℃,终止温度25 ℃),升温和降温速率均为5.0 ℃/min,角频率(angular frequency)为1.0 rad/s[16]。最后在25 ℃下进行频率扫描(frequencysweep),频率扫描范围为0.1~10 Hz。
1.2.5 YSP凝胶持水性的测定 利用离心法测量凝胶持水性(water holding capacity,WHC),将浓度分别为8%、10%、12%、14%的YSP溶液1 mL放置在1.5 mL的离心管中,至于恒温水浴锅中,保持水浴温度为95 ℃,在此条件下加热1 h蛋白形成凝胶,烧杯从水浴中取出置于常温流水中冷却,冷却至室温,放于4 ℃冰箱冷却24 h待测。将离心管从冰箱取出,放置在室温下,当温度达到室温时,以6000 r/min的速度离心15 min,用滤纸条吸取离心出来的水,记录离心管、离心前离心管与凝胶的重量和离心后离心管与凝胶的重量,凝胶持水性计算如下:
式中:WHC为凝胶持水性;W1为离心管重(g);W2为离心前离心管与凝胶的重量(g);W3为离心后离心管与凝胶的重量(g)[17]。
1.2.6 YSP凝胶质构的测定 凝胶特性利用质构仪进行测定,采用texture profile analysis(TPA)运行模式。测试前速度为2.00 mm/s,测试速度为2.00 mm/s,测试后速度2.00 mm/s,穿刺距离为2.0 mm,间隔时间为5 s,数据频率200 pps[18],探头为TA11/1000圆柱型。
1.3 数据处理
利用OriginPro8、IBM SPSS Statistics 19等软件进行作图和数据分析。
2 结果与分析
2.1 YSP的最小凝胶浓度
植物蛋白在加热时形成凝胶的能力在食品加工和食品功能特性配方中有很大作用。蛋白质凝胶形成能力和粘弹性与内部结构、共价键和氢键、静电和疏水相互作用有密切关系。Sathe等研究发现蛋白的溶解性和非蛋白成分可以影响凝胶形成[19]。根据表1结果显示,山药蛋白的最小凝胶质量分数为8%,表明山药水溶性蛋白质具有较好的凝胶能力。

表1 YSP最小凝胶浓度的测定结果Table 1 Determination result of the minimum gel concentration of YSP
2.2 YSP的凝胶特性
蛋白质凝胶实际上是蛋白质-蛋白质、蛋白质-溶剂及相邻肽链间吸引力、排斥力相互平衡的结果。形成蛋白质凝胶的作用力与稳定蛋白质三维结构的作用力大致相同。除在蛋白凝胶结构中占主导地位的共价键外,一般认为,一些物理作用力如疏水相互作用、静电相互作用等也参与蛋白凝胶网络结构的形成。其中一些观点认为,凝胶的流变特性与凝胶聚集的颗粒大小、颗粒的体积分数以及凝胶的分形维数密切相关[20]。
2.2.1 YSP浓度对山药蛋白质凝胶特性的影响 储能模量G′代表能量储存后可恢复的弹性性质,损耗模量G″代表能量消散的粘性性质[21]。根据图1(a、b)的动态流变结果和表2的质构结果显示,所测样品的G′均大于G″,随着蛋白质浓度增大,G′与G″均显著增大(p<0.05),山药蛋白质凝胶的硬度也随着YSP浓度的增大而增大。根据频率扫描的测定显示,由图1c可知,损耗角正切值tanδ在测试的频率范围内,随着蛋白质浓度的升高而降低,表明在不同频率下,蛋白质浓度越小的凝胶,流动性越好,tanδ为G″与G′比值,tanδ越大,表明体系的粘性比例越大,流动性强,反之则弹性比例较大[22]。相同蛋白质浓度的G′曲线和G″曲线变化趋势基本相同,且G′>G″,tanδ<1,说明YSP凝胶以弹性为主体系,随着蛋白质浓度增大,弹性增强,具有较强的结构性[23]。这表明增大蛋白质浓度有助于凝胶具有更好的粘弹性和硬度。由于蛋白质浓度增大,单位体积内蛋白质分子的碰撞与缠结几率增大,氢键相互作用增强[24],同时,蛋白质分子间热运动随温度升高而加剧,导致流动阻力减小。
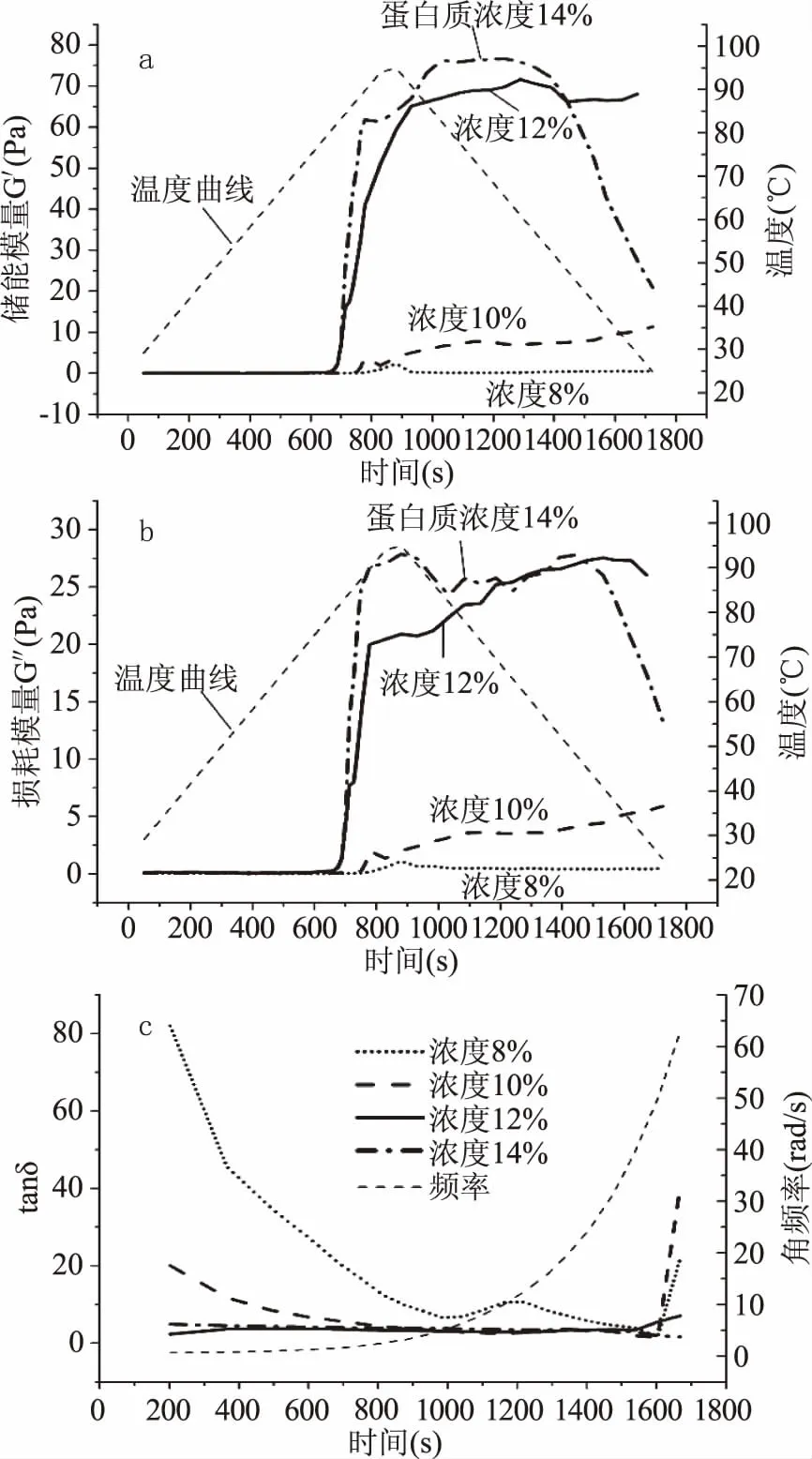
图1 YSP浓度对山药蛋白质凝胶G′(a)、G″(b)、和tanδ(c)的影响Fig.1 Effects of YSP concentration on the G′(a),G″(b)and tanδ(c)of YSP gel
蛋白质之间交联聚集形成的凝胶网络结构可以锁住并保持水分,网络结构锁住水分能力的大小,是在食品应用中衡量凝胶优劣的一个重要指标[25]。如表2所示,山药蛋白质凝胶具有良好的持水性,这种良好的持水性和凝胶的蛋白质浓度呈正相关,也和其蛋白质良好的溶解性有关[26]。凝胶的硬度的增大也有利于水的保持。所以随着蛋白质浓度的增加,凝胶的持水性也有所增大,当蛋白质浓度大于12%时,持水性达到70%以上。这种良好的持水性,可以使山药蛋白凝胶广泛应用于食品工业中,如肉类替代品,烘焙食品等。可以根据凝胶的持水性,在生产中调节水的用量来处理新产品的感官性状。
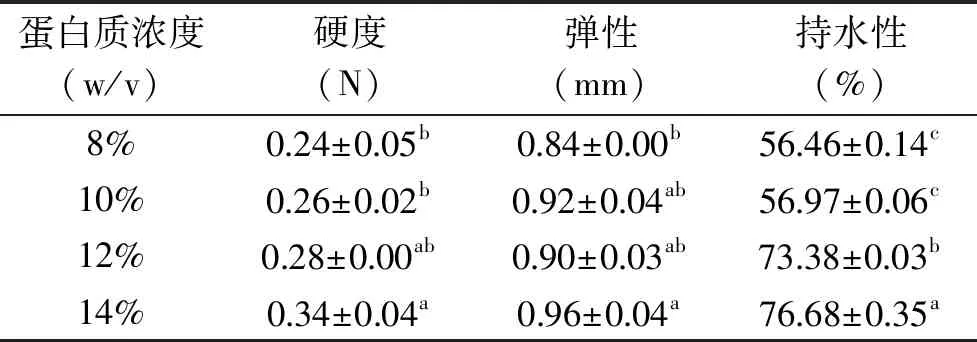
蛋白质浓度(w/v)硬度(N)弹性(mm)持水性(%)8%0.24±0.05b0.84±0.00b56.46±0.14c10%0.26±0.02b0.92±0.04ab56.97±0.06c12%0.28±0.00ab0.90±0.03ab73.38±0.03b14%0.34±0.04a0.96±0.04a76.68±0.35a
2.2.2 pH对YSP凝胶特性的影响 由图2可以看出,在所测范围内,pH=9时,储能模量G′、损耗模量G″和tanδ达到最大。在90 ℃左右时,凝胶的粘弹性最好,随着温度的降低,G′也明显下降。在碱性的条件下,由表3可以看出,随着pH的增大,凝胶的硬度、弹性和持水性呈现先增加后降低的趋势。蛋白质分子中包含羧基与氨基,能够呈现典型的两性特征。pH对凝胶的粘弹性有较大的影响,山药蛋白的等电点在3.5左右,当pH>pI时,凝胶中多数蛋白质通过解离氢离子而带负电荷,蛋白质分子之间的相互排斥,蛋白质分子与水分子之间的相互作用能有利于蛋白质凝胶网络的形成[27]。随着pH提高,凝胶中不溶物也有所减少,持水性较好[28]。pH>9时,蛋白质分子中的净负电荷密度过大,分子间的静电斥力就会大于分子间作用,使蛋白质凝胶形成和维持的作用力减弱[29],分子链变得比较舒展[30],不利于蛋白质分子的聚集,粘弹性减弱。
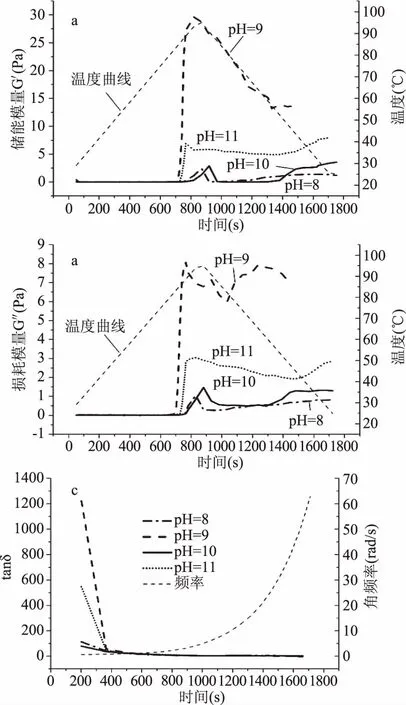
图2 pH对山药蛋白质凝胶G′(a)、G″(b)、和tanδ(c)的影响Fig.2 Effects of pH on the G′(a), G″(b)and tanδ(c)of YSP gel
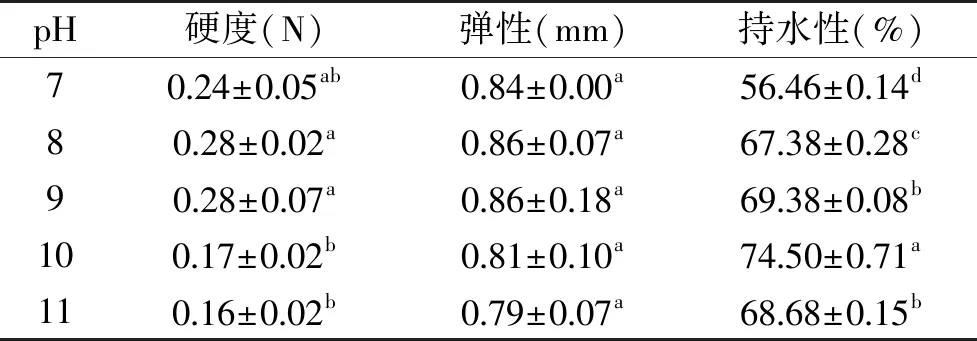
表3 pH对山药蛋白凝胶硬度、弹性和持水性的影响Table 3 Effects of pH on gel hardness,resilience and water holding capacity of YSP
2.2.3 NaCl浓度对YSP凝胶特性的影响 由图3可以看出,当NaCl浓度为0.1 mol/L时,山药蛋白凝胶的G′和G″较大;同时,由表4可以看出,当NaCl浓度超过0.05 mol/L时,将使凝胶的硬度降低,这与YSP凝胶形成时的动态过程一致[31]。在不同频率下,NaCl浓度对tanδ的影响较小。加入少量NaCl有助于凝胶持水性增强。蛋白质凝胶形成首先经历变性展开,使疏水基团暴露出来,蛋白质分子间作用使之发生交联形成集聚体,继而形成稳定的网络结构。由于中性电解质NaCl溶液影响电荷和极性基团之间的静电相互作用力,通过对水分子结构的修饰而影响疏水相互作用,加热蛋白质溶液时,包埋的非极性侧链暴露出来,从而增强了邻近多肽间非极性片段的疏水相互作用。适量NaCl的添加能够减弱分子间斥力作用,可以促进蛋白质交联聚合[32],形成的凝胶随机聚集较为粗糙[33]。而高浓度的NaCl会减小蛋白质之间的静电斥力,屏蔽电荷效应,增大分子间的吸引力,使蛋白质的构象趋于稳定,凝胶的粘弹性硬度减弱[34]。另一方面,高浓度的NaCl还会破坏凝胶中的次级键,水合键和氢键,改变凝胶形成区域周围水的形态从而破坏凝胶网络结构的稳定性,使凝胶G′和G″降低。
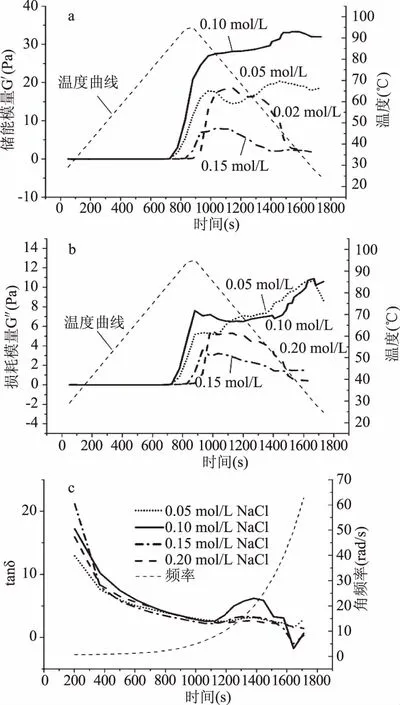
图3 NaCl浓度对山药蛋白质凝胶G′(a)、G″(b)、和tanδ(c)的影响Fig.3 Effects of NaCl concentrationon the G′(a),G″(b)and tanδ(c)of YSP gel
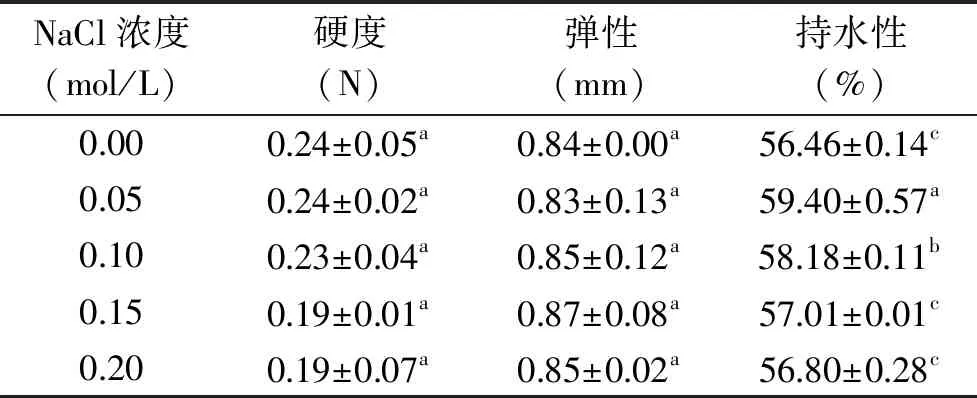
表4 NaCl浓度对山药蛋白质 凝胶硬度、弹性和持水性的影响Table 4 Effects of NaCl concentration on gel hardness and resilience and water holding capacity of YSP
3 结论
山药水溶性蛋白质凝胶的粘弹性随着蛋白质浓度的增大而增大,pH为9时,储能模量G′、损耗模量G″和tanδ达到最大,NaCl浓度超过0.05 mol/L时,凝胶的硬度较低。在蛋白质浓度为14%,pH为9,NaCl浓度为0.05 mol/L时具有最好的持水性。对其流变性和质构的研究,可以为山药类食品的创新提供依据。
