BiVO4/SBA-15光催化氧化苯乙烯制苯甲醛
2019-07-08陈政利
韩 娜,苏 炜,陈政利,沈 健,王 雷
(辽宁石油化工大学石化学院,辽宁 抚顺 113001)
苯甲醛作为一种重要的工业原料,在各类医药产品或食品添加剂生产中应用广泛[1-5]。工业上的苯甲醛制备工艺存在腐蚀严重、收率偏低等问题,且因在生产过程中大量使用氯气造成产品苯甲醛存在部分有毒成分,不符合绿色化学及清洁生产的要求,也令苯甲醛的使用范围受到限制[6-9]。因此,生产苯甲醛的重点问题在于寻找高效廉价的催化剂,并开发一种环境友好且工艺简单的苯甲醛生产技术来合成绿色苯甲醛产物[10-12]。
近些年,通过苯乙烯催化氧化制备苯甲醛的方法吸引了大量研究者的注意,其中光催化氧化反应兼具反应条件温和及操作简单两大优势,可作为一种苯甲醛的生产途径。催化剂作为光催化氧化反应的重要环节一直是众多研究者的研究重点,而在催化剂的制备中,活性组分和载体的选择也至关重要。半导体材料TiO2作为典型的光催化剂广泛应用于光催化领域,王瑞璞等[13]以TS-TiO2为催化剂,通过光催化氧化苯乙烯制备苯甲醛。然而,TiO2因带隙能高达3.2 eV仅对高能量的紫外光响应,而紫外光在太阳光谱中仅占8%左右,这使得其在实际应用中有所局限[14-15]。有研究者认为负载型TiO2催化剂可提高TiO2对太阳光的利用效率,赵地顺等[16]通过溶胶-凝胶法将TiO2负载于活性炭上,范立等[17]通过浸渍法将TiO2负载于USY微孔分子筛上,二者在光催化反应中均表现出较好的催化活性。与此同时,有更多的研究者将研究重点放在寻找新型高效光催化剂上。BiVO4凭借其高活性和稳定性成为备受关注的光催化剂,其相较于TiO2的突出优势在于禁带宽度较窄、可吸收可见光、高效利用太阳能等[18-19]。与其他光催化剂一样,体相BiVO4光生电子空穴对复合率高的问题限制了其在催化反应中的性能[20-21],张妍等[22]将BiVO4负载到MCM-41介孔分子筛上并在研究中发现负载后的BiVO4具有更好的吸附性能,有助于促进光生电子空穴对的分离,提高光催化活性。张璐璐等[23]选用SBA-15介孔分子筛为载体,合成了TiO2SBA-15光催化剂,通过表征发现其具有较大的比表面积和孔径,利于大分子颗粒快速扩散,进一步增强光催化效果。本研究结合BiVO4的高催化活性与SBA-15分子筛大比表面积和孔径,通过浸渍法将BiVO4负载于SBA-15介孔分子筛上合成BiVO4SBA-15光催化剂,采用X射线衍射(XRD)、N2吸附-脱附等手段对合成催化剂结构进行表征;在光照射下,以BiVO4SBA-15为催化剂进行苯乙烯氧化反应,考察反应条件对氧化性能的影响。
1 实 验
1.1 试验试剂
P123(EO20PO70EO20)模板剂,三嵌段共聚物,美国Mobil公司产品;浓HCl,浓度为6 molL;TEOS(正硅酸四乙酯)、Bi(NO3)3·5H2O、苯乙烯、NH4VO3、SDBS(十二烷基苯磺酸钠)、30%过氧化氢,均为分析纯,国药集团生产;硝酸、氨水,分析纯,沈阳市天罡化学试剂厂生产;无水乙醇,天津富宇化工有限公司生产;丙酮,分析纯,辽宁新兴试剂有限公司生产。
1.2 催化剂的制备
1.2.1 SBA-15分子筛的制备参考文献[24]方法制备SBA-15分子筛。称取P123模板剂加入晶化瓶中,于恒温水浴中采用去离子水搅拌溶解,然后加入50.2 g浓HCl,搅拌30 min后加入16.96 g TEOS,继续搅拌24 h后将晶化瓶放入100 ℃烘箱中晶化24 h。晶化结束后冷却至室温,洗涤,过滤,干燥,于500 ℃下焙烧4 h,得到SBA-15分子筛。
1.2.2 BiVO4催化剂的制备将相同物质的量的Bi(NO3)3·5H2O和NH4VO3分别溶解于硝酸溶液中,充分搅拌后混合均匀,将SDBS溶液加入至上述混合溶液中,磁力搅拌0.5 h。使用氨水调节溶液pH至6,继续搅拌2 h。陈化1 h,吸走上层清液后将前躯物移至带有聚四氟乙烯内衬的反应釜中,置于180 ℃烘箱中水热处理18 h,待冷却至室温后使用无水乙醇和去离子水洗涤过滤,将产品干燥后于马弗炉中530 ℃焙烧2 h,得到BiVO4催化剂。
1.2.3 BiVO4SBA-15催化剂的制备通过过饱和浸渍法合成BiVO4/SBA-15催化剂。将0.15 g BiVO4溶解于硝酸溶液中,搅拌溶解后加入1 g SBA-15分子筛,在40 ℃下搅拌3 h后升温蒸干成粉末,干燥后在马弗炉中530 ℃焙烧3 h,得到15%BiVO4/SBA-15催化剂。
1.3 苯乙烯光催化氧化制苯甲醛
将苯乙烯、丙酮、过氧化氢混合均匀后加入BiVO4/SBA-15催化剂,采用400 W金卤灯照射,在一定温度下进行光催化氧化反应,反应结束后对产物进行离心处理,苯乙烯光催化氧化反应的转化率(X)和选择性(S)用下式计算:
式中:wt为原料中苯乙烯的质量;w′t为产物中苯乙烯的质量;w0为产物中苯甲醛的质量。
2 结果与讨论
2.1 XRD表征
SBA-15和BiVO4/SBA-15的XRD图谱见图1。由图1可见:①纯SBA-15在2θ为0.9°处出现了与(100)晶面对应的特征峰,反映了介孔结构的存在,在2θ为1.6°和1.8°处出现了与(110)和(200)晶面对应的特征峰,反映了其六方晶型的特征[25];②改性后的BiVO4/SBA-15样品仍存在上述3处的衍射峰,但峰强度有一定程度的下降,且出现了向小角度方向的偏移,说明改性后的样品依旧具有SBA-15的六方晶型介孔结构,但BiVO4的引入降低了SBA-15分子筛孔道的规整性。

图1 SBA-15和BiVO4/SBA-15的XRD图谱a—SBA-15; b—BiVO4/SBA-15
2.2 N2吸附-脱附表征
SBA-15和BiVO4/SBA-15的N2吸附-脱附曲线见图2。由图2可见:当相对压力为0.6~0.8时SBA-15出现了带有因毛细凝聚现象产生的H1型滞后环的第Ⅳ类吸附曲线,且出现了N2吸附量明显突跃,表明该样品为具有规则孔道的介孔分子筛;BiVO4/SBA-15的等温曲线类型和滞后环形状未出现明显变化,但相对压力突跃点位置略微变化,且N2饱和吸附量稍有降低,表明BiVO4的引入对介孔分子筛结构造成了一定的影响。

图2 SBA-15和BiVO4/SBA-15的N2吸附-脱附曲线a—SBA-15; b—BiVO4/SBA-15
SBA-15和BiVO4/SBA-15的结构参数见表1。从表1可以看出,纯SBA-15样品的比表面积和孔体积分别为620.24 m2/g和1.20 cm3/g,介孔孔径为7.73 nm,而经BiVO4改性后的BiVO4/SBA-15样品的比表面积和孔体积分别为381.99 m2/g和0.84 cm3/g,介孔孔径为8.79 nm,孔径变大的可能原因是催化剂在焙烧处理过程中部分孔壁坍塌,从而导致孔体积和比表面积的减小。
表1 SBA-15和BiVO4SBA-15的结构参数

表1 SBA-15和BiVO4SBA-15的结构参数
SBA-15BiVO4∕SBA-15∕(m2·g-1)620.24381.99∕(cm3·g-1)1.200.84∕nm7.738.79
2.3 FT-TR表征
SBA-15和BiVO4/SBA-15的红外光谱见图3。从图3可以看出:①2个催化剂样品均在波数为3 442 cm-1处出现水合羟基Si—OH的较宽振动吸收峰;②SBA-15样品分别在波数为471,808,1 085 cm-1处出现Si—O键的弯曲振动、Si—O四面体对称伸缩振动及Si—O—Si键的反对称伸缩振动峰,BiVO4/SBA-15样品除以上吸收峰外,在波数为771,1 092,3 458 cm-1处出现Bi—V键振动、V=O双键及O—H的伸缩振动吸收峰;③SBA-15样品在波数为961 cm-1处的Si—OH的振动吸收峰有所减弱,这是因为除进入到介孔孔道内的BiVO4外,部分BiVO4负载于分子筛表面,消耗了分子筛表面非缩聚Si—OH,对其结构造成了一定影响[26]。
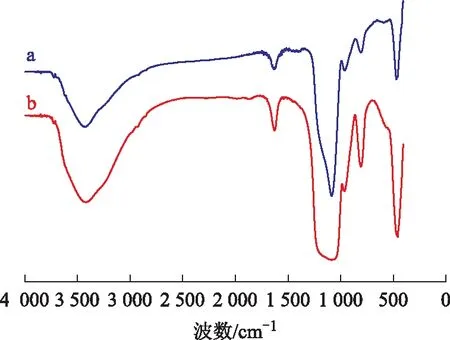
图3 SBA-15和BiVO4/SBA-15的红外光谱a—SBA-15; b—BiVO4/SBA-15
2.4 BiVO4/SBA-15光催化性能评价
在反应温度为70 ℃、反应时间为2 h、n(苯乙烯)∶n(丙酮)∶n(过氧化氢)= 1∶2∶3、m(BiVO4/SBA-15)∶m(苯乙烯)=10%的条件下,在不同反应体系中进行苯乙烯氧化反应,苯乙烯转化率见图4。从图4可以看出:①在仅采用400 W金卤灯照射时,苯乙烯转化率仅为8.62%,氧化效果可忽略;②400 W金卤灯照射条件下加入过氧化氢后,苯乙烯转化率出现小幅度提高,这是因为过氧化氢通过金卤灯照射产生了氧化物质,有助于促进苯乙烯的氧化;③加入BiVO4后,苯乙烯转化率有明显的提升,这要归因于BiVO4在可见光激发下产生的光生电子空穴对与过氧化氢分解产生的H2O和O2反应生成了具有强氧化性的超氧自由基·O2-和·OH,促进了氧化剂的氧化作用,推动苯乙烯催化氧化反应;④相比于BiVO4+H2O2+400 W金卤灯体系,BiVO4/SBA-15+H2O2+400 W金卤灯体系具有更高的苯乙烯转化率。这是因为SBA-15介孔分子筛具有较大比表面积,BiVO4均匀分散在其表面不仅增强对可见光的吸收也提高了催化剂的吸附性能,有利于苯乙烯的氧化。因此BiVO4/SBA-15+H2O2+400 W金卤灯为最理想的反应体系。

图4 不同反应体系的苯乙烯转化率a—400 W金卤灯; b—400 W金卤灯+H2O2; c—BiVO4/SBA-15+H2O2; d—BiVO4/SBA-15+400 W金卤灯; e—BiVO4/SBA-15+H2O2+400 W金卤灯; f—BiVO4+H2O2+400 W金卤灯
2.5 BiVO4/SBA-15用量的考察
在反应温度为70 ℃、反应时间为2 h、n(苯乙烯)∶n(丙酮)∶n(过氧化氢)= 1∶2∶3、400 W金卤灯光照的条件下,BiVO4/SBA-15的加入量对苯乙烯转化率和苯甲醛选择性的影响见图5。由图5可见,随着BiVO4/SBA-15催化剂用量的增加,苯乙烯转化率苯甲醛选择性逐渐升高,当m(BiVO4/SBA-15)∶m(苯乙烯)为10%时苯乙烯转化率达到最大值,苯甲醛选择性则持续上升。这是因为当催化剂用量较少时,只有少量的活性组分参与反应,光子利用率低,光催化效果差;增加催化剂用量,活性组分通过光照产生更多光生电子空穴对,将过氧化氢氧化成为氧化自由基,从而促进氧化剂的氧化作用,苯乙烯转化率及苯甲醛选择性有所提升;但加入过多催化剂时,从宏观动力学角度考虑,加重了溶液的搅拌阻力,造成催化剂分散度下降,减少了与反应物的接触几率,影响传质扩散效果。催化剂分散不均匀也导致溶液透光性变差,降低可见光利用率,阻碍生成光生电子空穴对,光催化效果减弱[27]。因此,最佳催化剂用量为:m(BiVO4/SBA-15)∶m(苯乙烯)=10%。

图5 BiVO4/SBA-15的加入量对苯乙烯转化率和苯甲醛选择性的影响■—转化率; ●—选择性。图6~图9同
2.6 反应温度的考察
在反应时间为2 h、n(苯乙烯)∶n(丙酮)∶n(过氧化氢)= 1∶2∶3、m(BiVO4/SBA-15)∶m(苯乙烯)=10%、400 W金卤灯光照的条件下,反应温度对苯乙烯转化率和苯甲醛选择性的影响见图6。由图6可见,随着反应温度的升高,苯乙烯转化率逐渐上升,苯甲醛选择性呈先上升后下降的趋势。这是因为低温条件下过氧化氢的分解受到限制,BiVO4/SBA-15催化剂表面的光生电子空穴对无法充分捕捉H2O和O2,导致生成的·O2-与·OH少,氧化反应不彻底;温度升高,有利于过氧化氢的分解促进氧化作用,且分子受热运动速率增加,促进了苯乙烯与催化剂表面光生电子空穴对的接触,利于苯甲醛的生成,故苯乙烯转化率和苯甲醛选择性逐渐上升;当反应温度过高时,加大了氧化深度,消耗苯乙烯生成其他副产物,导致苯甲醛选择性逐渐降低。另外,高温条件下的苯乙烯聚合与过氧化氢的分解也是苯甲醛选择性下降的原因。因此,最佳反应温度为70 ℃。

图6 反应温度对苯乙烯转化率和苯甲醛选择性的影响
2.7 反应时间的考察
在反应温度为70 ℃、n(苯乙烯)∶n(丙酮)∶n(过氧化氢)= 1∶2∶3、m(BiVO4/SBA-15)∶m(苯乙烯)=10%、400 W金卤灯光照的条件下,反应时间对苯乙烯转化率和苯甲醛选择性的影响见图7。由图7可见,随着反应时间的延长,苯乙烯转化率逐渐增加,苯甲醛选择性呈先上升后下降的趋势。这是因为BiVO4/SBA-15催化剂在光照时间较短时生成的氧化物质·O2-和·OH少,氧化反应无法进行完全。另外,苯乙烯制备苯甲醛的过程涉及到苯乙烯C=C双键断裂生成环氧苯乙烷,环氧苯乙烷水解生成苯基乙二醇,再进一步氧化生成苯甲醛[28]。在反应时间较短时,反应以生成环氧苯乙烷和苯基乙二醇为主,延长反应时间,二者含量减少,氧化物质·O2-和·OH生成量增多,苯甲醛含量逐渐上升;反应时间达到2.5 h后,继续延长反应时间,目的产物苯甲醛得到深度氧化,生成苯甲酸等副产物,导致苯甲醛选择性急剧下降。因此,最佳反应时间为2.5 h。
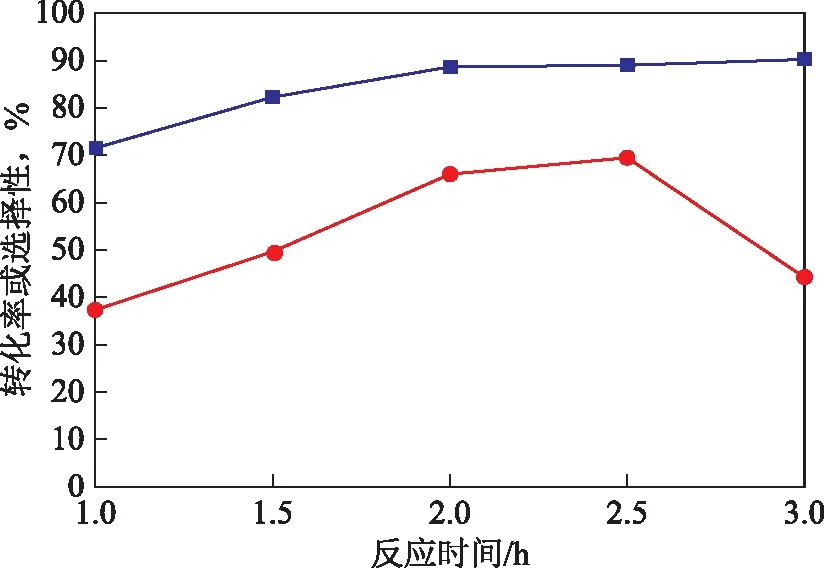
图7 反应时间对苯乙烯转化率和苯甲醛选择性的影响
2.8 过氧化氢用量的考察
在反应温度为70 ℃、反应时间为2.5 h、n(苯乙烯)∶n(丙酮)=1∶2、m(BiVO4/SBA-15)∶m(苯乙烯)=10%、 400 W金卤灯光照的条件下,过氧化氢用量对苯乙烯转化率和苯甲醛选择性的影响见图8。由图8可见,随着过氧化氢用量的增加,苯乙烯转化率逐渐上升,苯甲醛选择性呈先上升后下降的趋势,当n(苯乙烯)∶n(过氧化氢)=1∶3.5时苯甲醛选择性达到最大。BiVO4/SBA-15催化剂在可见光下产生光生电子空穴对,过氧化氢分解产生的H2O和O2在光生电子与光生空穴的作用下生成具有强氧化性的超氧自由基·O2-与·OH,可推动氧化反应的进行,因此增加过氧化氢用量可促进氧化反应的进行,使苯乙烯转化率与苯甲醛转化率上升;加入过多过氧化氢时,产生更多的氧化自由基,作为中间产物的苯甲醛深度氧化生成其他产物,故苯甲醛选择性下降,因此,过氧化氢的最佳用量为n(苯乙烯)∶n(过氧化氢)= 1∶3.5。

图8 过氧化氢用量对苯乙烯转化率和苯甲醛选择性的影响
2.9 丙酮用量的考察
在反应温度为70℃、反应时间为2.5 h、n(苯乙烯)∶n(过氧化氢)=1∶3.5、m(BiVO4/SBA-15)∶m(苯乙烯)=10%、 400 W金卤灯光照的条件下,丙酮用量对苯乙烯转化率和苯甲醛选择性的影响见图9。由图9可见,增加丙酮用量,苯乙烯转化率和苯甲醛选择性均呈先上升后下降的趋势,当n(苯乙烯)∶n(丙酮)=1∶2时苯乙烯转化率和苯甲醛选择性达到最大,分别为90.31%和70.65%。这是因为丙酮的加入可促进苯乙烯与过氧化氢两相混合,过氧化氢在光生电子空穴对作用下产生氧化物质,促进苯乙烯氧化;且丙酮中所含羰基可发生n-π*跃迁进而扩宽可吸收光范围[13],提高光子利用率。另外,丙酮可通过与过氧化氢结合生成过氧丙酮[3],有助于传递氧化物质,氧化反应效果增强;当加入过多丙酮时,反而降低反应物浓度,也减少了苯乙烯与催化剂和氧化剂的接触几率,阻碍氧化反应的进行,导致催化性能下降。因此,丙酮的最佳用量为n(苯乙烯)∶n(丙酮)= 1∶2。

图9 丙酮用量对苯乙烯转化率和苯甲醛选择性的影响
3 结 论
(1)采用浸渍法合成了BiVO4/SBA-15催化剂,不仅保持了分子筛的介孔结构,且有效提高了催化剂的活性。
(2)在反应温度为70 ℃、反应时间为2.5 h、n(苯乙烯)∶n(丙酮)∶n(过氧化氢)=1∶2∶3.5、m(BiVO4/SBA-15)∶m(苯乙烯)=10%的光催化条件下,苯乙烯转化率达到90.31%,苯甲醛选择性达到70.65%。
