原发性巨大肝血管肉瘤一例并文献复习
2019-07-04阿不都热依木吐尔洪韩铠泽艾达尔艾力斯拉依丁王琨刘松阳刘亚辉
阿不都热依木·吐尔洪,韩铠泽,艾达尔艾力·斯拉依丁,王琨,刘松阳,刘亚辉
(吉林大学白求恩第一医院,吉林 长春 130021,1.肝胆胰外二科,2.病理科)
原发性肝血管肉瘤是一种起源于肝窦血管内皮细胞的肝脏原发性间质性恶性肿瘤,罕见且恶性程度很高。因其临床表现以及相关辅助检查不具特征性,发现较晚,诊断较困难,易误诊,主要治疗方式为手术切除。吉林大学白求恩第一医院收治肝血管肉瘤患者一例,术前误诊为原发性肝癌,术后经病理确诊,随访7个月,未见肿瘤复发。
病例
患者,女,63岁,因“间断性右上腹部胀痛不适1个月”于2017年12月30日入院。病程中无发热,但伴夜间出汗、乏力等不适。既往:自述“银屑病”40余年,多次就诊中医以及诊所,具体口服以及涂抹药物不详。查体:无明显阳性体征。实验室检查:血常规提示轻度贫血(血红蛋白95 g/L),乙肝表面抗原、丙肝抗体未见异常,肝功能、生化、肿瘤标志物如甲胎蛋白(AFP)、癌胚抗原(CEA)、糖类抗原199(CA19-9)未见明显异常。影像学检查:肝胆脾胰多排CT平扫+三期增强(图1),提示:(1)肝脏形态所见,考虑肝硬化,脾大,门脉高压伴侧支循环开放,与左肾静脉沟通;(2)肝右叶占位性病变(黄色箭头所示),肝右后叶见一团块状稍低密度影,大小约12.7 cm×9.2 cm,部分突出于肝脏轮廓,增强扫描动脉期斑片状明显强化,静脉期及平衡期强化程度减低,考虑原发性肝癌;(3)胆囊结石。于2018年1月3日行肝部分切除、胆囊切除术,术后病理报告提示:肝血管肉瘤,分化较差(图2),伴大面积出血坏死,体积12.0 cm×10.0 cm×7.5 cm,切缘未见肿瘤。免疫组化提示:CD31(+),CD34(+),Vimentin(+)。患者术后恢复良好,无明显不适,复查各项指标未见明显异常,于术后第6天顺利恢复出院,随访7个月,未见肿瘤复发。
讨论
(1)肝血管肉瘤发病机制
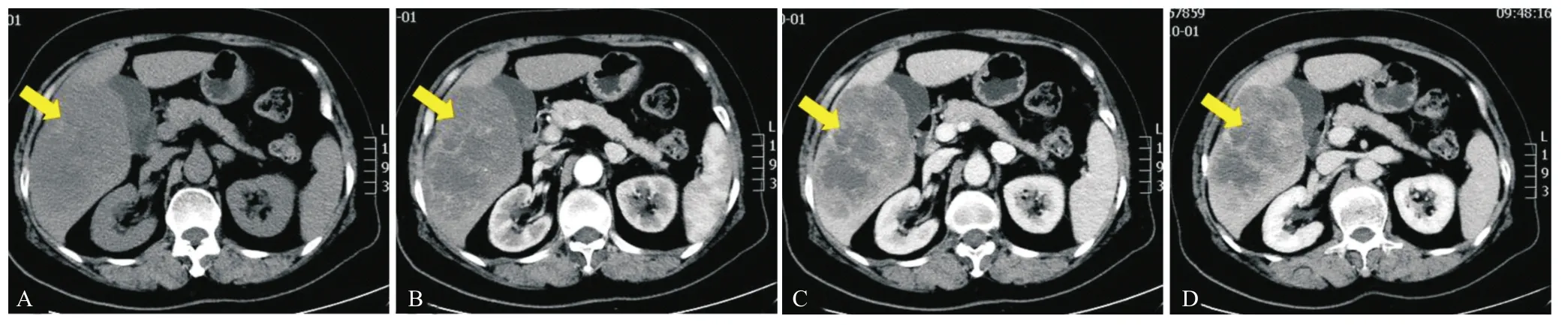
图1 腹部CT平扫+三期增强结果

图2 术后病理结果(HE,×200)
肝血管肉瘤是一种由肝窦血管内皮细胞异形增生所造成的肝脏原发性间质性恶性肿瘤,罕见且恶性程度很高。据文献报道,其在所有不同器官起源的血管肉瘤中不足5%[1-2],约占肝原发性恶性肿瘤的0.1%~2.0%[3],该病好发于60岁以上男性,男女比例为(1.9~4):1[4-5]。该病发病原因尚不明确,少数病例报道提示可能与接触二氧化钍、砷剂、氯乙烯、辐射、服用合成类固醇有关[6-7]。也有学者发现己烯雌酚、氨基甲酸乙酯、环磷酰胺、避孕药及肝吸虫感染可能与本病相关[6,8-9]。据日本学者报道,长期脂肪肝所致肝纤维化可能导致肝血管肉瘤,但肝纤维化与此病是否相关,目前仍存在争议[10-12]。本例患者患有“银屑病”病史,口服以及涂抹药物成分不详,术前查乙肝表面抗原、丙肝抗体未见异常,肝硬化具体原因尚不明确,不除外与本病发病相关。
(2)临床表现
肝血管肉瘤发病隐匿、进展较快,通常因腹部胀痛不适、劳累、体重减轻及发热等非典型症状就诊,使早期诊断困难。然而晚期患者常病情紧急,危及生命,表现为腹水、弥漫性血管内凝血(DIC)、肝功能衰竭或肿瘤破裂出血[13]。祖存等[14]报道肝血管肉瘤因血小板减少、脾大就诊,而误切脾,但其实凝血障碍主要系因血小板过多滞留于生长分化不良的血管腔及血窦有关,临床表现不典型是本病易误诊原因之一。
(3)实验室及影像学检查
实验室指标如肝功能、生化、血常规等无特异性,肿瘤标志物如AFP、CEA、CA19-9通常不升高[15]。影像学检查包括腹部增强CT、肝胆胰脾增强MRI、超声造影、PET/CT等,选择性肝动脉造影结合腹部增强CT,对本病诊断作用较大[16]。大部分肝血管肉瘤的CT征象较具特征性:较大肿块,边界不清,增强动脉期呈边缘轻度强化或无明显强化,门静脉期和延迟期呈向心性不均匀填充,伴或不伴离心性强化[17]。肝血管肉瘤的MRI表现为块状及结节状T1WI低信号,T2WI高信号影,增强后病灶呈渐进性充填,与周围肝实质分界清楚,较大病灶内伴出血及坏死[18]。超声造影应用于肝血管肉瘤的诊断逐渐增多,在超声造影动脉期可表现为周边增强,门静脉期及延迟期无增强,亦可表现为三期持续无增强[19-20]。PET/CT对明确肝外是否转移有帮助;本例患者术前行腹部增强CT,增强扫描动脉期可见肿物斑片状明显强化,静脉期及平衡期强化程度减低,误诊为原发性肝癌,因此确诊肝血管肉瘤仍需病理学诊断。
(4)病理学检查
穿刺活检常应用于术前诊断,而针对肝血管肉瘤的活检,目前尚无统一说法。部分学者不主张常规行活检,因考虑到肝血管肉瘤组织内富含血供,穿刺活检更易出现出血等风险,甚至可能危及生命[21]。此外,肿瘤组织内常伴有坏死及出血等,活检易出现假阴性[22]。而支持者认为活检可明确术前诊断,利于制定下一步治疗方案。笔者认为,是否穿刺活检应结合术前各项指标综合考虑。如病变在术前检查暂不能定性,患者无穿刺活检禁忌时,可行穿刺活检明确病变性质。如病变在术前检查已提示恶性,即便未明确具体恶变性质,无手术禁忌时应行肿瘤切除术。肝血管肉瘤的组织主要由梭形、多角形的瘤细胞组成,其细胞核有明显异型,染色质粗浓,核分裂相易见,瘤细胞可形成不规则形的血管腔。肝血管肉瘤通常对Ⅷ因子相关抗原及CD34、CD31免疫组化染色阳性。近年来,Wang等[23]的研究表明转录因子ERG亦可用于对肝血管肉瘤的免疫组化分析,且相对以上三项更准确,但尚未广泛应用。
(5)鉴别诊断
本病主要与肝血管瘤、肝细胞癌、肝转移癌鉴别。肝血管肉瘤肿瘤生长较快,且增强CT早期,区别于肝血管瘤的主要表现为非周边强化[24]。肝细胞癌通常AFP升高,伴肝炎、肝硬化,结合增强CT扫描呈“快进快出”,动脉期即可见显著的强化,可与肝血管肉瘤鉴别。肝转移癌与肝血管肉瘤的鉴别,需结合影像学检查发现原发病灶,且肝转移癌常伴肿瘤标志物升高。本例患者增强CT表现与原发性肝癌难以鉴别,影像学表现无特异性,术前误诊为原发性肝癌。
(6)治疗及预后
目前文献记载的主要治疗方式包括手术切除、化疗、肝动脉介入栓塞以及肝移植等,其中手术切除是肝血管肉瘤最佳的治疗方案[25]。Li等[26]回顾性分析了186例肝血管肉瘤行不同治疗方案的疗效,其中86例行肝部分切除术的患者,术后1、3、5年生存率分别为53.2%、30.8%、19.5%,中位生存期为15个月。相对行化疗、肝移植以及保守治疗预后好。36例行化疗的患者,中位生存期为10个月,大于行保守治疗的1.3个月。虽然针对肝血管肉瘤并无标准的化疗方案,但对于无手术指征的患者,如病情允许,行化疗可能改善预后。此外,术后辅助靶向药物治疗亦可能对改善预后有意义[19],但仍需更多的研究以及数据支持。肝动脉介入栓塞常用于肿瘤破裂出血的急诊治疗[16]。另有研究表明,肝移植术后中位生存期为5~6个月[26-27]。因术后复发率高达77%,且生存期短,故肝移植不再推荐[27-28]。本例患者术后因医师对本病认识不足,未推荐进一步行化疗。虽然本病尚无指南指导,化疗方案尚处于探索阶段,但如果患者条件允许,仍应在目前文献已记载的化疗方案中学习,吸取经验,可尝试行化疗,因此患者可能受益。
肝血管肉瘤因发病率低,临床表现以及辅助检查无特异性,早期难发现,易误诊。对于无肝炎、肿瘤标志物正常的患者,注意详细询问病史,与富血供肿瘤鉴别,必要时术前行穿刺活检明确,以免延误病情。结合本例以及相关文献可见,如病情允许应首选手术切除,术后可辅助化疗,以期提高术后存活时间。
