SD/HS-SPME-GC-MS分析海艾挥发性成分研究
2019-07-01周意卢金清龚敏
周意 卢金清 龚敏
摘要:分别采用水蒸气蒸馏法(SD)和顶空固相微萃取法(HS-SPME)提取海艾(Artemsia argyi)挥发性成分,并运用气相色谱-质谱联用技术(GC-MS)分析其成分类别及相对含量。结果表明,采用SD-GC-MS分离出42个组分,鉴定出22个组分,占挥发油总量的75.95%;采用HS-SPME-GC-MS分离出53个组分,鉴定出28个组分,占总挥发性成分的74.11%。SD与HS-SPME两种不同的前处理方法提取的挥发性成分有一定差异,二者联合分析海艾挥发性成分更全面。
关键词:海艾(Artemsia argyi);水蒸气蒸馏法(SD);顶空固相微萃取(HS-SPME);气相色谱-质谱(GC-MS);挥发性成分
中图分类号:S567.23+9;O657.7 文献标识码:A
文章编号:0439-8114(2019)07-0096-03
Abstract: The volatile components of Artemsia argyi were extracted by steam distillation(SD) and head space solid phase micro-extraction(HS-SPME),respectively,and their composition and relative content were analyzed by gas chromatography-mass spectrometry (GC-MS). The results showed that 42 components were separated by SD-GC-MS and 22 components were identified,accounting for 75.95% of the total volatile oil;53 components were separated by HS-SPME-GC-MS and 28 components were identified,accounting for 74.11% of the total volatile components. There are some differences in the volatile components extracted from the two different pretreatment methods of SD and HS-SPME. The combined analysis of the volatile components of folium artemisiae argy can provide more comprehensive information.
Key words: Artemsia argyi; SD; HS-SPME; GC-MS; volatile components
艾叶为菊科植物艾(Artemisia argyi)的干燥叶,具有温经止血,散寒止痛,祛湿止痒功效[1]。艾叶在全国各地均有分布,资源丰富,中国艾叶主产地为湖北蕲春(蕲艾)、河南汤阴(北艾)、浙江宁波(海艾)、四川资阳(川艾)、河北安国(祁艾)以及安徽霍山与江西樟树等,在中国本草古籍记载中曾作为道地艾叶的有北艾、海艾、蕲艾、祁艾[2]。《本草纲目》记载:“艾叶本草不著土产,但云生田野。宋时以汤阴复道者为佳,四明者图形。近代惟汤阴者谓之北艾,四明者谓之海艾。”四明在宋代是以四明山为中心的一块行政区域,现主要是指浙江省宁波市西南方向的四明山。海艾汤出自《外科正宗》:“油风乃血虚……外以海艾汤熏洗。”是中国古代医学常见的外洗方法之一,外洗治疗头部银屑病、头部脂溢性皮炎,疗效显著[3-5]。目前对海艾的研究报道较少,海艾富含挥发油,具有良好的抗菌消炎、抗病毒等作用[6,7]。本研究采用SD/HS-SPME-GC-MS分析海艾挥发性成分,为海艾的开发与应用提供科学依据。
1 材料与方法
1.1 材料
海艾药材由卢金清教授采于浙江宁波,经湖北中医药大学张秀桥教授鉴定为菊科植物艾的干燥叶。
1.2 仪器
Agilent6890/5973气相色谱-质谱联用仪(美国Hewlett-Packard公司);挥发油提取器;圆底烧瓶(3 000 mL);电子调温电热套(天津市泰斯特仪器有限公司);C-MAG HS-4磁力加热搅拌器(德国IKA公司);手动固相微萃取进样器(美国Supelco公司);顶空瓶(15 mL);65 μm PDMS/DVB萃取头(美国Supelco公司);JY1002电子天平(上海浦春计量仪器有限公司)。
1.3 方法
1.3.1 样品处理
1)水蒸氣蒸馏法。取海艾药材100 g,剪碎,置于3 000 mL圆底烧瓶中,加12倍水,浸泡3 h,提取至挥发油不再增加为止,即得海艾挥发油。精密量取海艾挥发油0.1 mL,乙醚稀释定容至1 mL,作为供试品溶液,进样量2 μL,进行GC-MS分析。
2)顶空固相微萃取。取海艾药材0.3 g,剪碎,置于15 mL顶空瓶中,插入经老化的装有65 μm PDMS/DVB萃取头的手动进样器,在85 ℃下平衡10 min后,压缩手柄伸出萃取头萃取10 min,取出,立即插入色谱仪进样口(温度230 ℃)解吸附3 min,不分流进样。
1.3.2 GC-MS色谱与质谱条件
1)水蒸气蒸馏法。色谱柱:HP-5MS石英毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度230 ℃;载气为高纯氦气(99.999%);流速0.8 mL/min;分流比10∶1,溶剂延迟3 min。程序升温:初始温度50 ℃,以2 ℃/min升温至80 ℃,以8 ℃/min升温至180 ℃,保留3 min;离子源为EI源;离子源温度230 ℃;四级杆温度150 ℃;接口温度280 ℃;电子能量70 eV;倍增管电压1.2 kV;质量范围35~550 m/z。
2)顶空固相微萃取。色谱柱:HP-5MS石英毛细管柱(30 m×0.25 mm×0.25 μm);进样口温度230 ℃;载气为高纯氦气(99.999%);流速0.8 mL/min;程序升温同水蒸气蒸馏法;离子源为EI源;离子源温度230 ℃;四级杆温度150 ℃;接口温度280 ℃;电子能量70 eV;倍增管电压1.2 kV;质量范围35~550 m/z。
2 结果与分析
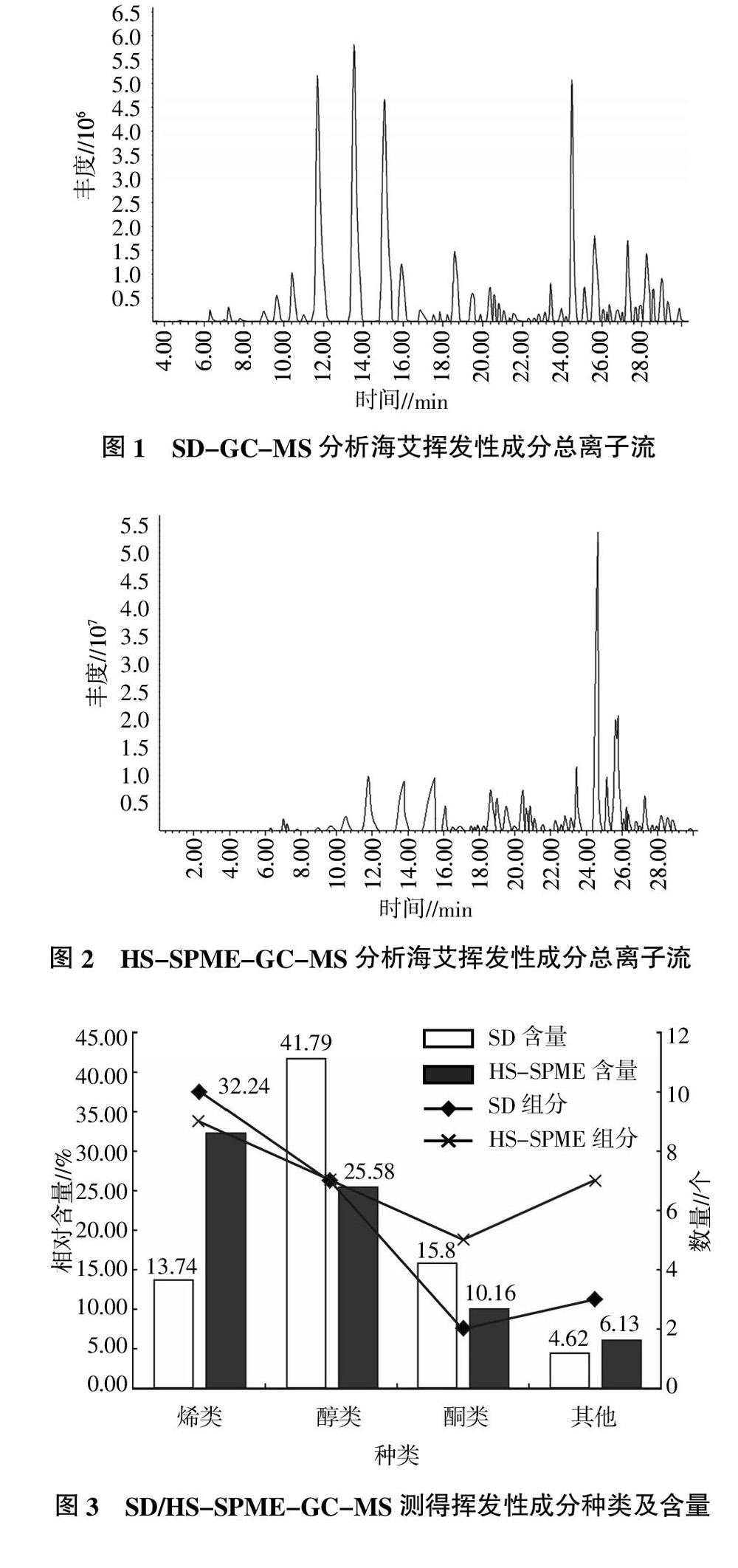
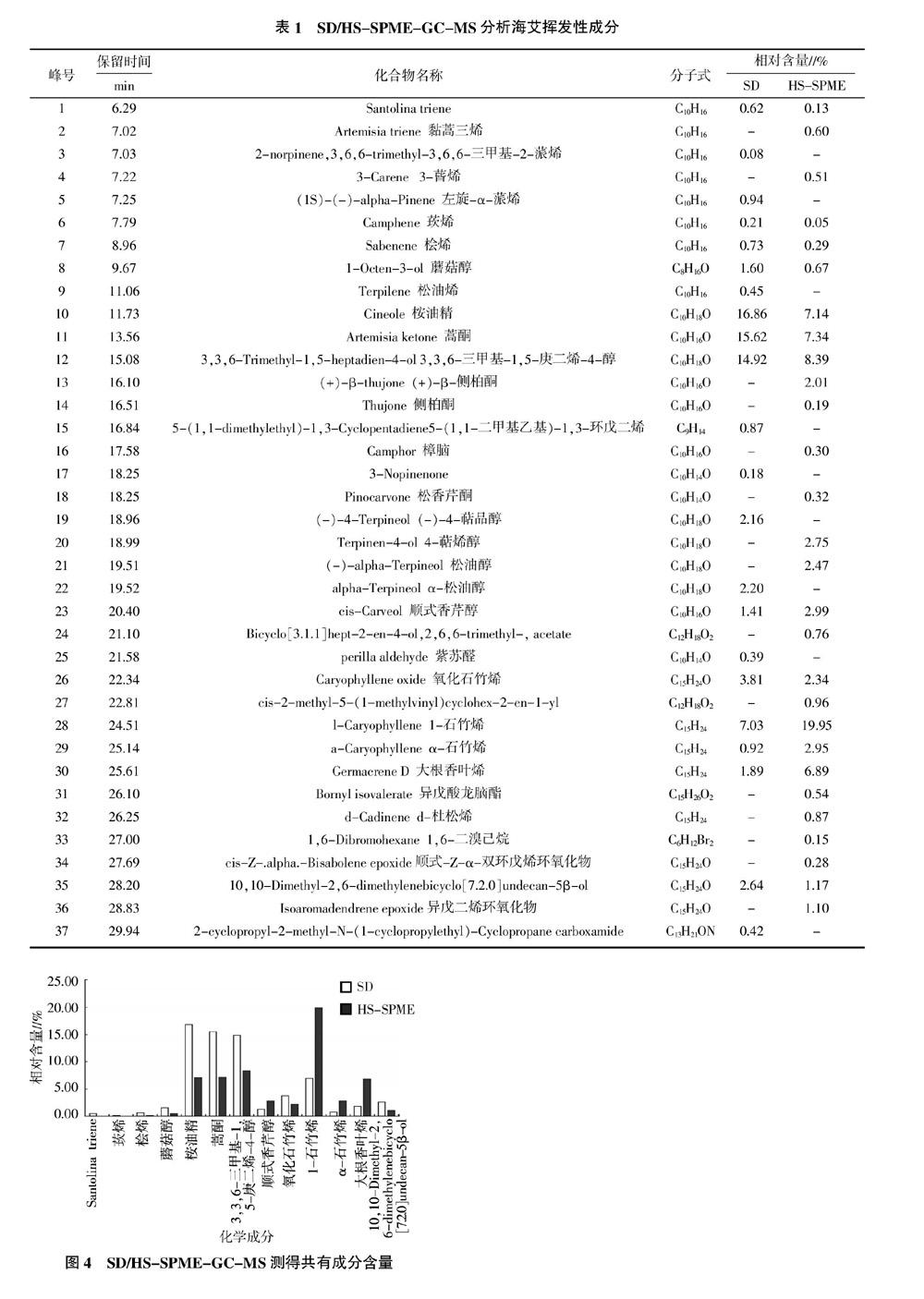
经化学工作站数据处理,采用峰面积归一化法计算总离子流中各组分的相对含量,根据各色谱峰的质谱图经NIST质谱数据库检索,结合质谱碎片的人工解析与文献资料核对,确定各个组分。采用SD-GC-MS分离出42个组分,鉴定出22个组分,占挥发油总量的75.95%。主要为烯类(13.74%)、醇类(41.79%)和酮类(15.8%)成分,其中,桉油精含量最高,约占16.86%,含量较高的还有蒿酮(15.62%)、3,3,6-三甲基-1,5-庚二烯-4-醇(14.92%)、1-石竹烯(7.03%);采用HS-SPME-GC-MS分离出53个组分,鉴定出28个组分,占总挥发性成分的74.11%,主要为烯类(32.24%)、醇类(25.58%)和酮类(10.16%)成分,其中,1-石竹烯含量最高,约占19.95%,含量较高的还有3,3,6-三甲基-1,5-庚二烯-4-醇(8.39%)、蒿酮(7.34%)、桉油精(7.14%)。两种方法鉴定出相同成分13种,含量各不相同。具体结果见图1、图2、图3、图4、表1。
3 讨论
研究结果显示,水蒸气蒸馏与顶空固相微萃取两种前处理方法都适于中草药中挥发性成分的提取,但水蒸气蒸馏法提取时间长,高温可能会导致一些低沸点、热敏性成分损失,所以它更适于高沸点易挥发成分的提取,而固相微萃取法无需溶剂,集采样、萃取、浓缩、进样于一体,适于挥发性、半挥发性成分的分离富集。桉油精为2015年版《中国药典》规定的艾叶指标性成分,具有解热、抗炎、抗菌、平喘和镇痛作用[8],对艾叶质量评价具有一定指导意义。本试验测得海艾中桉油精含量与道地药材蕲艾相比差别不大[9],表明海艾质量较佳,可为海艾的进一步开发和综合利用提供科学依据。
参考文献:
[1] 国家药典委员会.中华人民共和国药典 一部[M].北京:中国医药科技出版社,2015.
[2] 張 元,康利平,郭兰萍,等.艾叶的本草考证和应用研究进展[J].上海针灸杂志,2017,36(3):245-255.
[3] 李银玲.海艾汤加减方外泡联合中药内服治疗寻常型银屑病(血瘀证)疗效观察[D].南京:南京中医药大学,2016.
[4] 刘 岩,闵仲生,单敏洁,等.海艾汤外洗治疗头部银屑病35例[J].现代中医药,2011,31(6):24-25.
[5] 单敏洁.海艾汤外洗治疗头部脂溢性皮炎38例[J].江西中医药,2006(4):31.
[6] 符吴萸,阮碧波,张 莉,等.中药艾的抗炎免疫研究进展及临床应用[J].亚太传统医药,2016,12(10):76-79.
[7] 赵志鸿,王丽阳,郑立运,等.艾叶挥发油对HBV的抑制作用[J].郑州大学学报(医学版),2015,50(2):301-304.
[8] 曹 利,卢金清,叶 欣,等.降香及其伪品挥发性成分对比研究[J].国际药学研究杂志,2017,44(3):282-287.
[9] 许俊洁,卢金清,郭胜男,等.不同部位与不同采收期蕲艾精油化学成分的GC-MS分析[J].中国实验方剂学杂志,2015,21(21):51-57.
