重复经颅磁刺激联合加巴喷丁治疗脊髓损伤后神经病理性疼痛的临床观察
2019-06-30郭艳萍黄犇周学梅
郭艳萍 黄犇 周学梅
脊髓损伤(spinal cord injury,SCI)是指由外界直接或间接因素导致的相应脊髓节段出现各种运动、感觉、括约肌功能障碍,肌张力异常及病理反射等相应改变。神经病理性疼痛(neuropathic pain,NP)是由躯体感觉系统的损伤或疾病所引起的疼痛,是SCI 最常见的并发症之一[1-2]。据不完全统计,SCI 后NP 的发生率为70%~79%,常表现为剧烈的烧灼样疼痛、针刺痛、电击样疼痛、撕裂样疼痛、冷痛、紧束感等,有的表现为痛觉超敏和感觉异常,并持续存在[3]。超过2/3 的患者经过多种治疗仍不能有效地缓解疼痛,严重影响患者的日常生活及工作,增加抑郁、焦虑等情感障碍的发病率,增加社会负担[4-5]。目前NP的发生机制还不十分清楚,治疗困难,主要治疗方法有药物治疗、中医治疗、外科治疗、心理治疗等[6-9]。加巴喷丁可通过中枢神经系统和外周神经系统的多种机制,在神经性疼痛的治疗中发挥着重要作用。吴勤峰等[10]报道重复经颅磁刺激(repetitive transcranial magnetic stimulation,rTMS)治疗SCI 后NP 有一定的效果。然而相关临床研究较少,缺乏有力的证据支持。本研究旨在观察加巴喷丁联合rTMS 治疗SCI后NP 的治疗效果,现报道如下。
资料与方法
一、一般资料
选取苏州瑞盛康复医院神经康复科自2017 年1 月至2018 年12 月收治的SCI 患者60 例,男性43例,女性17 例,发病年龄范围22~60 岁,病程最短为1.5 个月~3 年,平均6 个月。损伤平面根据美国脊髓损伤协会(American Spinal Injury Association,ASIA)脊髓损伤评定量表评定:颈髓损伤21 例(A 级6 例、B 级10 例、C 级5 例),胸髓损伤20 例(A 级5例、B 级9 例、C 级6 例),腰髓损伤19 例 (A 级6例、B 级10 例、C 级3 例);致伤原因:车祸伤21 例,坠落伤14 例,重物砸伤16 例,挤压伤9 例;单侧肢体疼痛38 例,双侧肢体疼痛22 例。采用随机数字表法将患者分为观察组与对照组,每组30 例。2 组患者均口服加巴喷丁,观察组给予M1 区10 Hz 的rTMS 治疗(武汉依瑞德公司生产,型号:CCY-Ⅰ),对照组给予M1 区相同模式、相同音量的声音假刺激。2 组患者性别、年龄、病程等基线资料比较,差异均无统计学意义(P<0.05),具有可比性(表1)。

表1 2 组患者一般资料比较(Mean±SD)
二、纳入与排除标准
1.纳入标准:(1)有SCI 病史,并经MRI 证实诊断明确;(2)符合ASIA 诊断标准[11];(3)NP 符合国际疼痛研究协会(International Association for the Study of Pain,IASP)诊断或排除标准,且VAS 评分≥6 分[12];(4) 所有患者均根据IASP NP 治疗指南接受镇痛、抗焦虑及抑郁个体化治疗3 个月以上,疼痛症状无继续减轻[13];(5)无严重认知障碍(简易智力状态检查量表>24 分);(6) 年龄>18 岁;(7) 自愿签署rTMS治疗知情同意书。
2.排除标准:(1)有癫痫发作史或脑电图检查显示有痫样改变者;(2)有颅内无介入性金属植入物者;(3)有心脏支架或起搏器、恶性肿瘤等TMS 治疗的禁忌证者;(4)有糖尿病周围神经病变,颈、腰椎病,神经根炎等引起疼痛者;(5)有下肢骨折或下肢周围神经损伤者;(6)存在严重心、肺、肾功能不全等严重并发症者。
三、治疗方法
1.口服加吧喷丁治疗:2 组均口服加巴喷丁,第1 天300 mg、1 次/d,第2 天300 mg、2 次/d,第3 天300 mg、3 次/d,直至疼痛缓解或出现难以耐受的不良反应,最高剂量为3600 mg/d。
2.rTMS 治疗:首先在患者安静状态下测定静息运动阈值(rest motor threshold,RMT)。使用单个TMS脉冲刺激一侧初级运动皮层 (primary motor cortex,M1 区),表面电极在刺激对侧手第一骨间背侧肌处记录运动诱发电位;连续刺激10 次,其中有5 次诱发出至少50 mV 运动诱发电位的最低刺激强度即为RMT。观察组在口服加巴喷丁治疗的基础上,加rTMS 治疗,采用选用“8”字线圈治疗,刺激靶点为M1 区,刺激频率为10 Hz;刺激10 s,间隔50 s,10串,刺激强度80%RMT;5 d 为1 个疗程,疗程间隔2 d,连续治疗6 周[14-16]。对照组同样在口服加巴喷丁治疗的基础上,给予假刺激,将治疗线圈同样置于M1区,只给予相同模式,相同音量的声音提示。治疗时及治疗后观察患者有无不良反应。疗程结束后3 个月再次对疼痛程度、口服加巴喷丁剂量等进行电话随访。
四、疼痛评定
治疗前及6 周治疗结束后,采用视觉模拟评分(visual analogue scale,VAS)对患者进行评定,令患者使用游标卡尺对其自身的NP 进行主观评估,卡尺一端为0,表示无痛;另一端为10,表示剧痛;中间部分表示不同程度的疼痛。让患者根据自我感觉在卡尺上划一记号,表示疼痛的程度。VAS 评分标准:0 分,无痛,无任何疼痛感觉;1~3 分,轻度疼痛,不影响工作,生活;4~6 分,中度疼痛,影响工作,不影响生活;7~10 分,重度疼痛,疼痛剧烈,影响工作及生活。分值越大代表疼痛越重[17]。
五、情绪评定
1.抑郁程度评定: 采用汉密顿抑郁量表(Hamilton depression scale,HAMD),包括24 项评定内容。<8 分,无抑郁;8~20 分,可能抑郁;21~23 分,中等抑郁;>24 分,重度抑郁。
2.焦虑程度评定: 采用汉密尔顿焦虑量表(Hamilton anxiety scale,HAMA),包括14 项评定内容。<7 分,无焦虑;7~14 分,可能焦虑;15~20 分,有焦虑;21~28 分,明显焦虑;>29 分,重度焦虑[18]。
六、统计学分析
采用SPSS18.0 统计学软件进行数据处理,计量资料采用均数±标准差(Mean±SD)表示,组内比较采用配对样本t 检验,组间比较采用独立样本t 检验,计数资料采用χ2检验,以P<0.05 为差异有统计学意义。
结果
一、2 组患者治疗前后VAS 评分比较
2 组患者治疗前VAS 评分均衡,差异无统计学意义(P>0.05),具有可比性。观察组和对照组第1、第6 周的VAS 评分明显与同组治疗前比较,评分均降低,且第6 周评分低于第1 周,差异均具有统计学意义(P<0.05)。2 组治疗第1 周评分比较差异无统计学意义(P>0.05),第2、4、6 周观察组评分均低于对照组,差异具有统计学意义(P<0.05)。具体信息见表2。
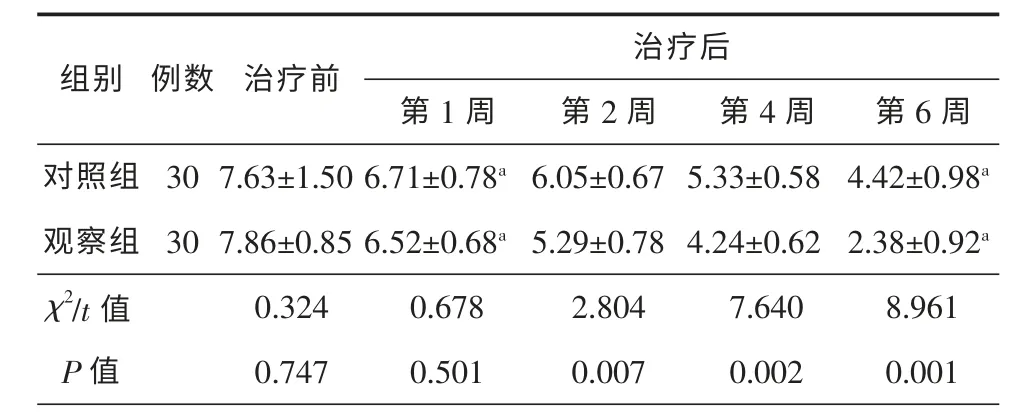
表2 2 组患者治疗前后VAS 评分比较(Mean±SD)
二、2 组患者治疗前后抑郁和焦虑程度比较
治疗前,2 组患者均存在不同程度的焦虑或抑郁状态,2 组患者治疗前HAMD 和HAMA 评分比较差异无统计学意义(P>0.05);治疗6 周后,2 组患者HAMD 和HAMA 评分较治疗前显著改善,观察组HAMD 和HAMA 评分显著优于对照组,差异均具有统计学意义(P<0.05),具体信息见表3。
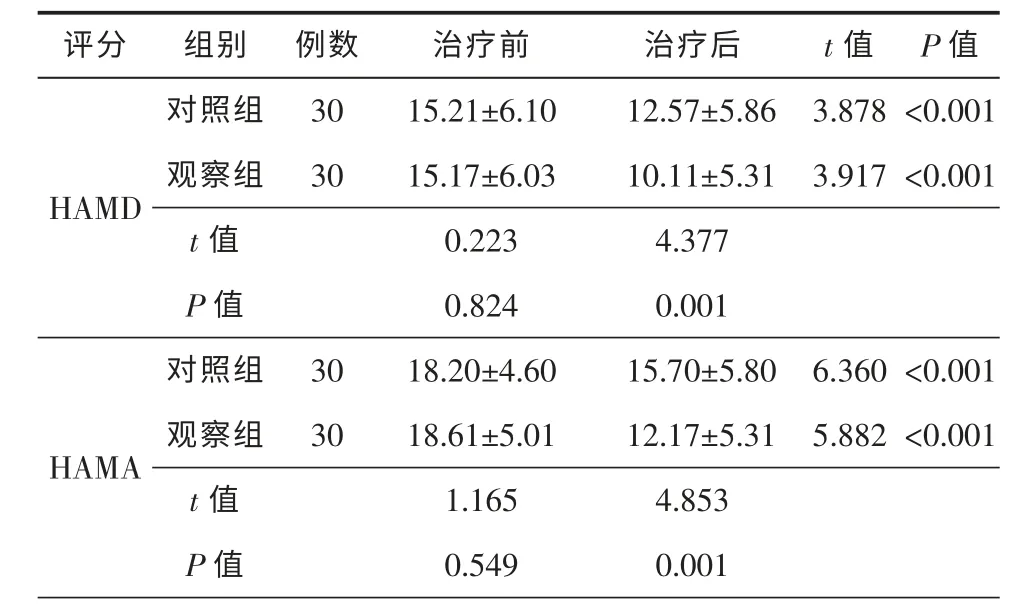
表3 2 组患者治疗前后HAMD、HAMA 评分比较(Mean±SD)
三、2 组患者治疗后睡眠改善情况比较
与同组治疗前比较,2 组患者睡眠时间差异均有统计学意义(P<0.05);治疗第4、6 周后,2 组患者睡眠时间比较差异有统计学意义(P<0.05)(表4)。
四、2 组患者治疗后的不良反应比较
1.加巴喷丁用量及不良反应比较:观察组口服加巴喷丁最大剂量为1800 mg,不良反应仅出现乏力、恶心,且各1 例;对照组口服加巴喷丁最大剂量为3600 mg,不良反应中眩晕、嗜睡各4 例,共济失调1 例,乏力、恶心各2 例;余病例无特殊不适。2 组治疗后不良反应数量比较差异有统计学意义(χ2=10.756,P=0.001)。

表4 2 组患者治疗后睡眠改善情况比较
2.rTMS 治疗安全性: 患者在rTMS 治疗过程中未出现严重的不良事件,仅1 例出现一过性头痛,发生在刺激强度较高时,调整刺激强度后,症状自然缓解。
讨论
NP 主要由一系列不同疾病或损伤所引起,临床表现各不相同,其特点是伤害性刺激消失后仍出现疼痛,且具有高发病率和低治愈率,受到国内外学者的密切关注,是医学界研究的热门课题。SCI 后,由于神经损伤、末梢神经兴奋性异常、神经源性炎症、交感神经系统异常及神经可塑性变化等原因,可并发NP。NP 的发病机制复杂,常由多种机制引起,包括解剖结构改变和功能受损[19]。有研究证实外周和中枢机制共同参与了NP 的发生发展过程[2]。外周机制主要包括受损神经产生的异位放电、炎性细胞与细胞因子的作用、交感神经的参与,其中异电活动中,Na+、K+、Ga2+离子通道参与形成NP;中枢机制主要是脊髓结构重塑、中枢敏化作用、胶质细胞的激活。由于NP 的病因、发病机制以及症状之间关系复杂,其治疗效果不尽人意。目前临床上仍以药物治疗为主,据报道只有30%~40%的患者对药物治疗的效果满意,疼痛程度缓解>50%,所以神经调控技术成为“神经病理性疼痛诊疗专家共识”推荐的治疗技术[20-21]。
TMS 技术是神经调控技术的一种,由Barker 首创于1985 年;rTMS 于2004 年开始应用于对药物治疗不敏感的顽固性NP[22]。rTMS 是利用时变磁场作用于大脑皮质产生感应电流,通过改变大脑皮质的兴奋性、改善脑血流和代谢、调节神经递质、改变神经系统可塑性、降低背根神经节内过度表达的神经元型一氧化氮合酶、抑制星形胶质细胞活性来发挥镇痛作用的[23-24]。
第二代抗癫痫药加巴喷丁是 “神经病理性疼痛诊疗专家共识”推荐的一线钙通道调节剂[21]。加巴喷丁的结构与γ-氨基丁酸(γ-aminobutyric acid,GABA)类似,能调节GABA 受体的活性及GABA 的释放,并具有抑制电压依赖型Ga2+通道、抑制兴奋性氨基酸释放、减少大脑去甲肾上腺素的释放等作用,从而抑制NP[25]。加巴喷丁在体内不代谢,以原形随尿液排出而消除,与其他抗癫痫药不同,对肝脏微粒体酶没有诱导或抑制作用,并且与血浆蛋白结合率很低,因此耐受性好,严重不良反应少。
本研究结果显示:在治疗的第1 周,2 组的VAS评分比较无显著差异;第6 周后观察组评分明显低于对照组,提示rTMS 治疗存在累积效应,联合治疗优于单纯的药物治疗;治疗前所有患者均存在不同程度的焦虑或抑郁状态,治疗6 周后,观察组HAMD 和HAMA 评分显著优于对照组,说明rTMS可以改善SCI 患者的抑郁、焦虑情绪状态,作用机制可能是高频rTMS 刺激后GABA 介导的皮层内抑制减弱,从而引起大脑皮质的兴奋性增强[2]。在睡眠改善方面,观察组明显优于对照组,说明rTMS 能改善因疼痛导致的睡眠障碍。在药物剂量及不良反应方面,观察组加巴喷丁最大剂量是1800 mg,而对照组加巴喷丁最大剂量是3600 mg;观察组不良反应也明显少于对照组。笔者曾经观察过加巴喷丁联合阿米替林治疗SCI 后中枢性疼痛,加巴喷丁最大剂量用到2400 mg,较单纯使用加巴喷丁治疗剂量小,但患者有嗜睡、眩晕、共济失调、乏力恶心、口干的不良反应[26]。而在本研究中,加巴喷丁联合sTMS 治疗,加巴喷丁的最大剂量只用到1800 mg,仅有1 例出现乏力恶心不良反应。在rTMS 整个治疗过程中患者未出现严重的不良事件,仅1 例出现一过性头痛,发生在刺激强度较高时,调整刺激强度后症状自然缓解,说明rTMS 治疗安全可靠。随访3 个月后,观察组疗效稳定,VAS 评分为3~5 分,加巴喷丁用药剂量基本不变;而对照组疼痛时有反复,VAS 评分为4~7 分,部分患者加巴喷丁用量需要加量,或加用rTMS 治疗后NP 有所缓解。说明rTMS 治疗需要有足够的刺激量才能起到较持久而确切的治疗效果。本研究对象没有区分完全性与不完全性损伤,这是本研究的缺陷。
综上所述,加巴喷丁联合rTMS 治疗SCI 后NP具有较好的临床疗效,能够明显减轻疼痛、缓解抑郁和焦虑症状,改善患者生活质量,并具有无创、无痛、无不良反应、价格低廉的特点,更容易被患者接受。
