黔产青钱柳化学成分及α-葡萄糖苷酶抑制活性研究
2019-06-25段玉书杨万霞杜彩霞苑春茂郝小江
段玉书 ,胡 永,杨万霞,熊 燕,杜彩霞,苑春茂,郝小江*,顾 玮*
1贵州大学药学院,贵阳 550025;2贵州医科大学药用植物资源功效利用与开发国家重点实验室;3贵州省中国科学院天然产物化学重点实验室,贵阳 550014
继心脑血管、癌症、肿瘤之后,糖尿病现已成为当今又一个疾病杀手。随着社会的进步与发展,生活水平的提高,因进食过多,体力活动减少而导致的肥胖糖尿病发病率逐年升高,且我国糖尿病患者呈年轻化,截止2018年其患病人数超过9 000万,占据全球患病率第1位[1]。青钱柳为我国珍贵药用植物,在降血糖、降血脂方面有良好的疗效且药用历史悠久,阐明青钱柳中的降血糖功效成分,具有重要的科研价值。
青钱柳青钱柳(Cyclocaryapaliurus)系胡桃科青钱柳属落叶乔木,又称为青钱李、摇钱树或金钱柳,属于国家二级保护树种,该属现仅存一种,且仅存于中国,因而被誉为植物界的大熊猫,医学界的第三棵树[2]。广泛分布于江西、江苏、贵州、四川、云南、湖北、湖南、广西、广东等地[3]。《中国中药资源志要》记载:其树叶,树皮具有清热,消肿的功能,可用于治疗顽癣。青钱柳的根、枝、叶均可入药,具有降血糖和血压、减肥、抗肿瘤、抗衰老、抗过敏、清热解暑、提高人体免疫力、促进新陈代谢等多种功效。民间常用青钱柳叶当茶叶泡茶饮用,因其味甘甜,有“甜茶、神茶”之称[2]。
青钱柳的研究始于上世纪70年代,但对其理化成分及保健药用研究始于上世纪80年代中期,青钱柳中主要含有三萜类、黄酮、甾体、萜类、有机酸、多糖等类型成分[4]。动物及临床试验研究表明,青钱柳具有多种对人体有益的生理和药理功能,尤其在降血糖、降血脂方面有独特的疗效。目前,对青钱柳不同部位的降血糖研究已经取得了一定的成果,但是对其降血糖作用的研究尚缺乏系统性,其降糖物质基础和作用机制仍不明确[5]。
用植物化学方法对黔产青钱柳叶进行了系统的提取分离,得到化合物13个,包括黄酮类化合物3个,萜类及甾体6个,其他类4个。其中,化合物9为新天然产物,化合物2~4、7、8、11、13为首次从该植物中分离得到。用PNPG法对化合物1~10进行了体外α-葡萄糖苷酶抑制活性筛选。结果显示,化合物1和2有较强的α-葡萄糖苷酶抑制活性,表明黄酮类成分是青钱柳降血糖功效的物质基础之一。
1 材料与方法
1.1 实验材料
干燥的青钱柳叶(20 kg)2015年由黔东南雷山县百佳尚品有限公司提供,经贵州省中国科学院天然产物化学重点实验室顾玮副研究员鉴定其为胡桃科青钱柳属植物青钱柳(Cyclocaryapaliurus)。
1.2 实验仪器
半制备型高效液相色谱仪:Waters 600(美国),日立Primaide(日本),一维核磁共振仪:INOVA-400和500型(Bruker公司,瑞士,TMS为内标),EI-MS质谱仪:安捷伦-5973型,ESI-MS质谱仪:惠普LC-MSD型高效液相色谱-质谱联用仪,循环水式多用真空泵:SHE-DⅢ型(巩义市予华仪器有限责任公司),低温冷却液循环泵:DLSB-D/20型(郑州长城科工贸有限公司),电热鼓风干燥箱:WGLL-230BE型(天津泰斯特仪器有限公司),三用紫外分析仪:ZF-6型(上海嘉鹏科技有限公司),电热恒温水浴锅:HWS24型(上海一恒仪器有限公司),BioTek Epoch全波长酶标仪(美国伯腾仪器有限公司)。
1.3 实验试剂
有机试剂:石油醚、乙酸乙酯、氯仿、甲醇、丙酮、乙醇、正丁醇、吡啶。除色谱甲醇、色谱乙腈为分析纯,其余均为工业纯。α-葡萄糖苷酶抑制活性试剂: Na2CO3、Na2HPO4、NaH2PO4、DMSO、PNPG均为分析纯,阿卡波糖(上海源叶生物科技有限公司,日本),α-葡萄糖苷酶(Sigma公司,美国)。
1.4 提取与分离
青钱柳干燥叶(20 kg)经粉碎后80%的甲醇加热回流提取三次(4 h/次),得到青钱柳浸膏。加水溶解成混悬液后依次用石油醚,乙酸乙酯,正丁醇分别萃取4次,合并浓缩每部分萃取液。将乙酸乙酯部分浸膏(770 g)用正相硅胶(40~80目)色谱柱梯度洗脱,洗脱体系依次为石油醚/乙酸乙酯(20∶1,10∶1,5∶1),氯仿/甲醇(1∶0,20∶1,10∶1,5∶1,1∶1,0∶1),将得到的样品组分分为得到6个组分(标记为A-F)。A(50 g)组分使用正相硅胶(300~400目)色谱柱,经石油醚/乙酸乙酯体系洗脱得到化合物8(15 mg)、化合物12(50 mg)和化合物13(30 mg)。经正相柱洗脱其他成分经MCI柱除去大部分叶绿素,再经C-18反相色谱柱(MeOH/H2O 50∶50~100∶0),得到五个组分(标记为A1-A5)。A2经石油醚/乙酸乙酯洗脱体系(PE/EtOAc 20∶1~10∶1;),石油醚/丙酮体系(PE/DMK 15∶1~5∶1,v/v)分离得到化合物10(20 mg)、化合物9和化合物7(26 mg)。D组(37 g)使用反相MCI柱进行分离(MeOH/H2O 30∶70~90∶10),得到7个组分(标记为D1~D7)。D1部分正相硅胶柱洗脱(CHCl3/MeOH 20∶1~10∶1),经葡聚糖凝胶柱分离得到化合物4,剩余部分进一步正相硅胶柱洗脱得到化合物1(15 mg),化合物2(21 mg)经HPLC纯化分离得到(MeOH/H2O 53:47,流速为2 mL/min,tR=39 min)。D2部分经正相硅胶柱洗脱(CHCl3/MeOH 20∶1~10∶1)得到化合物(50 mg),经葡聚糖凝胶柱分离得到化合物5(100 mg)。 E组(340 g)经梯度洗脱(CHCl3/MeOH 20∶1~1∶1)得到5个组分(标记为E1-5),E2部分使用C18反相色谱柱进行分离(CH3OH/H2O 50∶50~100∶0)得到5个组分(标记为E2-1~E2-5),E2-2部分经正相硅胶柱洗脱(CHCl3/MeOH 20∶1~1∶1)得到化合物6(100 mg)和化合物11,剩余部分经Sephadex LH-20、HPLC纯化得到化合物3(19 mg),(MeOH/H2O 40∶60,流速为2 mL/min,tR=126 min)。
1.5 α-葡萄糖苷酶抑制活性测定
α-葡萄糖苷酶抑制活性筛选使用PNPG法,参考Chen Z等[6]方法略加修改。向96孔板中加入70 μL的0.1 mol/L磷酸盐缓冲液(pH6.8)稀释的样品和20 μL的0.5 U/mLα-葡萄糖苷酶混溶后置于37 ℃温浴30 min。之后加入20 μL的10 mmol/L的PNPG,37 ℃孵育45 min。结束后加入80 μL的0.2 mol/L Na2CO3溶液终止反应,置酶标仪405 nm下检测吸光值。同时设定相同体系下的样品背景对照组、空白对照组,A为实验组吸光度;A0为背景组吸光度;B为阴性对照吸光度;B0为空白对照组吸光度。酶活抑制率计算公式如下:
抑制率(%)=[(B-B0)-(A-A0)]/(B-B0)× 100%
2 结果与分析
2.1 结构鉴定
化合物1黄色粉末(CH3OH);ESI-MS:m/z455 [M+Na]+;分子式:C21H20O10;1H NMR (CD3OD,400 MHz)δH:7.76 (2H,d,J=8.0 Hz,H-2′,6′),6.93 (2H,d,J=8.0 Hz,H-3′,5′),6.34 (1H,d,J=1.2 Hz,H-8),6.17 (1H,d,J=1.2 Hz,H-6),5.37 (1H,d,J=1.2 Hz,H-1′′),4.22 (1H,dd,J=2.8,1.2 Hz,H-2′′),3.71 (1H,dd,J=9.2,2.8 Hz,H-5′′),3.32 (1H,d,J=9.2 Hz,H-3″),3.32 (1H,m H-5′′),0.92 (3H,d,J=5.2 Hz,H-6′′);13C NMR (CD3OD,100 MHz)δC:179.4 (C-4),167.6 (C-7),163.1(C-5),161.6 (C-4′),159.1(C-2),158.7 (C-9),136.1 (C-3),131.9 (C-2′,6′),122.7 (C-1′),116.5 (C-3′,C-5′),105.5 (C-10),103.5 (C-1′′),100.4 (C-6),95.1 (C-8),73.2 (C-4′′),72.1 (C-5′′),72.0 (C-3′′),71.9 (C-2′′),17.7 (C-6′′)。以上数据和文献[7]对照一致,因此确定化合物1为阿福豆苷。
化合物2黄色粉末(CHCl3);ESI-MS:m/z473 [M-H]-;分子式:C23H22O11;1H NMR (CDCl3,400 MHz)δH:7.67 (2H,d,J=8.0 Hz,H-2′,6′),6.89 (2H,d,J=8.0 Hz,H-3′,5′),6.32 (1H,s,H-8),6.15 (1H,s,H-6),5.44 (1H,s,H-1′′),4.76 (1H,s,H-4′′),4.16 (1H,dd,J=4.0,4.0 Hz H-2′′),3.80 (1H,dd,J=4.0,4.0 Hz,H-3′′),3.15 (1H,m,H-5′′),1.98 (3H,s,OAc),0.71 (3H,d,J=8.0 Hz H-6′′);13C NMR (CDCl3,100 MHz)δC:178.1 (C-4),171.2 (Ac),164.6 (C-7),161.8 (C-4),160.3 (C-5),157.4 (C-9),157.2 (C-2),134.1 (C-3),130.5 (C-2′ C-6′),121.1 (C-1′),115.1 (C-3′ C-5′),104.5 (C-9),101.1 (C-1′′),98.6 (C-6),93.5 (C-8),73.5 (C-4′′),70.3 (C-3′′),68.6 (C-2′′),68.2 (C-5′′),19.6 (Ac-4′′),16.2 (C-6′′)。以上数据和文献[8]对照一致,因此确定化合物2为山柰酚3-O-(4′′-O-乙酰基)-α-L-吡喃鼠李糖苷。
化合物 3黄色粉末(CH3OH);ESI-MS:m/z485 [M-H]-;分子式:C25H26O10;1H NMR (CD3OD,400 MHz)δH:7.59 (1H,d,J=8.0 Hz H-7′′),7.43 (2H,d,J=8.0 Hz,H-3′′,5′′),7.42 (1H,d,J=8.0 Hz,H-8),6.80 (2H,d,J=8.0 Hz H-2′′,6′′),6.78 (1H,d,J=8.0 Hz,H-6),6.31 (1H,d,J=16.0 Hz H-8′′),5.35 (1H,m H-4),4.81 (1H,d,J=8.0 Hz H-1′),4.51 (1H,dd,J=1.8,1.9 Hz H-6′),4.36 (1H,dd,J=8.5,8.5Hz,H-6′),3.51 (2H,m,H-3′,4′),3.43 (1H,m,H-2′),2.49 (1H,dt,J=3.4,3.1 Hz,H-2),2.20 (1H,m,H-2);13C NMR (CD3OD,100 MHz)δC:206.5 (C-1),168.9 (C-9′′),161.4 (C-4′′),159.3 (C-5),148.4 (C-7′′),146.9 (C-7),135.3 (C-8a),131.3 (C-3′′),131.3 (C-5′′),128.9 (C-4a),127.0 (C-1′′),119.0 (C-8),116.9 (C-6),116.2 (C-2′′,C-6′′),114.9 (C-8′′),104.4 (C-1′),77.8 (C-3′),75.7 (C-5′),75.2 (C-2′),71.7 (C-4′),64.5 (C-4),61.3 (C-6′),33.5 (C-2),30.3 (C-3)。以上数据和文献[9]对照一致,故确定化合物3为juglanoside J。
化合物 4白色粉末(CH3OH);ESI-MS:m/z203 [M+Na]+;分子式:C10H12O3;1H NMR (CD3OD,400 MHz)δH:7.53 (H,d,J=8.0 Hz,H-8),7.38 (H,d,J=8.0 Hz,H-5),7.28 (2H,m,H-6,7),4.38 (1H,d,J=8.0 Hz,H-4),4.06 (1H,m,H-1),3.30 (1H,m,H-2),2.16 (2H,m,H-3),2.00 (1H,m H-2);13C NMR (CD3OD,100 MHz)δC:137.7 (C-4a),137.6 (C-8a),128.2 (C-8),127.6 (C-6),127.4 (C-7),73.6 (C-2),68.9 (C-2),66.7 (C-4),37.1 (C-3)。以上数据和文献[10],因此确定化合物4为1α,2α,4β-3羟基-1,2,3,4-四氢萘酮。
化合物 5白色粉末(CHCl3);ESI-MS:m/z659 [M+Na]+;分子式:C36H60O9;1H NMR (CDCl3,400 MHz)δH:0.91 (3H,s,H-19),1.09 (3H,s,H -29),1.20 (3H,s,H-21),1.36 (3H,s,H-18),1.38 (3H,s,H-27),1.42 (3H,s,H-26),1.87 (3H,s,H-30),4.39 (1H,dt,J=4.8,10.7 Hz,H-12),4.95,4.97 (each 1H,s,H-28),4.99 (1H,d,J=7.3 Hz,H-1′),3.94 (1H,t,J=7.5 Hz,H-2′),4.10 (1H,t,J=9.0 Hz,H-3′),3.63 (1H,t,J=8.8 Hz,H-4′),3.80 (1H,m,H-5′),1.56 (3H,d,J=6.1 Hz,H-6′);13C NMR (CDCl3,100 MHz)δC:179.8 (C-3),148.0 (C-4),113.5 (C-28),97.8 (C-1′),86.9 (C-20),83.6 (C-24),77.4 (C-3′),76.3 (C-4′),75.3 (C-2′),75.1 (C-12),72.8 (C-5′),71.4 (C-25),52.1 (C-5),50.4 (C-14),48.6 (C-17),44.1 (C-9),40.7 (C-13),40.7 (C-10),39.8 (C-8),37.1 (C-7),34.7 (C-11),33.9 (C-22),33.9 (C-15),31.5(C-1),29.9 (C-2),27.4 (C-27),26.7 (C-17),26.3 (C-23),26.2 (C-26),25.9 (C-6),25.0 (C-21),24.6 (C-30),19.9 (C-18),17.6 (C-6′),16.7 (C-29),16.5 (C-19)。以上数据和文献[11]对照一致,因此确定化合物5为青钱柳苷III。
化合物6黄色粉末(CHCl3);ESI-MS:m/z777 [M+Na]+;分子式:C41H70O12;1H NMR (CDCl3,400 MHz)δH:5.0 (2H,d,J=6.4 Hz,H-1′,H-1′′),4.33 (1H,dd,J=9.6,2.8 Hz,H-5′a),3.77 (1H,br d,J=9.6 Hz,H-5′b),1.62 (3H,d,J=5.2 Hz,H-6′′),1.49 (3H,s,H-26),1.42(3H,s,H-19),1.41 (3H,s,H-27),1.27 (3H,s,H-29),1.17 (3H,s,H-21),1.09 (3H,s,H-18),1.01 (3H,s,H-28),0.63 (3H,s,H-30);13C NMR (CDCl3,100 MHz)δC:102.4 (C-1′′),102.3 (C-1′),86.9 (C-20),84.7 (C-24),81.9 (C-3),78.8 (C-3′′),77.8 (C-12),77.3(C-4′′),76.0 (C-2′′),75.1 (C-3′),73.3 (C-5′′),72.9 (C-2′),71.6 (C-25),69.6 (C-4′),66.8 (C-5′),54.4 (C-9),51.5 (C-5),50.5 (C-14),49.6 (C-17),42.0 (C-8),41.6 (C-13),40.4 (C-10),38.6(C-4),36.9 (C-7),36.0 (C-1),35.0 (C-11),34.5 (C-22),32.0 (C-15),30.7 (C-29),28.2 (C-27),27.2 (C-2),26.8 (C-23),26.5 (C-26),25.0 (C-21),23.6 (C-28),22.3 (C-16),19.1(C-6),18.8(C-6′′),17.6 (C-18),17.2 (C-19),17.2 (C-30)。以上数据和文献[12]对照一致,因此确定化合物6为青钱柳苷J。
化合物7黄色粉末(CH3OH);ESI-MS:m/z325 [M+Na]+;分子式:C20H30O2;1H NMR (CD3OD,400MHz)δH:5.71 (1H,s,H-4),2.10 (3H,s,H-21),1.16 (3H,s,H-19),0.64 (3H,s,H-18);13C NMR (CD3OD,100 MHz)δC:209.4 (C-20),199.6 (C-3),171.0 (C-5),124.0 (C-4),63.6 (C-17),56.0 (C-14),53.7 (C-9),44.0 (C-13),38.7 (C-12),38.7(C-10),35.8(C-1),35.6 (C-8),34.0 (C-2),32.9 (C-6),32.0 (C-7),31.6 (C-21),24.4 (C-15),22.9 (C-16),21.1 (C-11),17.5 (C-19),13.4 (C-18)。以上数据和文献[13]对照一致,因此确定化合物7为黄体酮。
化合物8黄色粉末(CHCl3);ESI-MS:m/z403 [M+Na]+;分子式:C21H32O6;1H NMR (CDCl3,400 MHz)δH:5.53 (1H,s,H-6),2.07,2.03 (each,1H,m,H-12,H-3),1.11 (each,1H,m,H-21,18),0.93 (3H,s,H-19);13C NMR (CDCl3,100 MHz)δC:209.6 (C-20),140.6(C-5),118.7 (C-6),92.6 (C-17),89.2 (C-14),74.5 (C-8),72.0 (C-3),69.4 (C-12),60.5 (C-12),44.8 (C-9),43.1 (C-4),39.4 (C-1),37.5 (C-10),35.1 (C-15),34.3 (C-7),32.5 (C-16),31.9 (C-2),29.0 (C-11),27.6 (C-21),18.6 (C-19),8.7 (C-18)。 以上数据和文献[14]对照一致,因此确定化合物8为去酰基萝藦苷。
化合物9白色粉末(CHCl3);ESI-MS:m/z381 [M+Na]+;分子式:C23H34O3;1H NMR (CDCl3,400 MHz);δH:5.73 (1H,s,H-4),5.06 (1H,q,H-20β),1.27 (3H,d,J=4.0 Hz,H-21),1.18 (3H,s,H-19),0.74 (3H,s,H-18);13C NMR (CDCl3,100 MHz)δC:199.6 (C-3),171.3 (Ac-CO),160.8 (C-5),123.9 (C-4),73.1 (C-20),55.6 (C-17),55.2 (C-14),53.7 (C-9),41.7 (C-13),38.6 (C-10,12),35.7 (C-8),35.2 (C-1),33.9 (C-2),32.8 (C-6),31.9 (C-7),29.7 (C-16),25.7 (C-15),23.9 (Ac-CH3),20.7 (C-11),20.6 (C-21),17.3 (C-19),12.5 (C-18)。以上数据和文献[15]对照一致,因此确定化合物9为20-乙酰氧基-4-烯-3-酮。
化合物10白色粉末(CHCl3);ESI-MS:m/z479 [M+Na]+;分子式:C30H48O3;1H NMR (CDCl3,400 MHz)δH:5.20 (1H,m,H-12),3.20 (1H,m,H-3),2.80 (1H,m,H-18),1.90(1H,m,H-11b),1.86 (1H,m,H-11a),1.72 (1H,m,H-22b),1.68 (1H,m,H-19b),1.68 (1H,m,H-22a),1.67 (1H,m,H-15b),1.64 (1H,m,H-7b),1.63 (1H,m,H-1b),1.63 (1H,m,H-16b),1.61 (1H,m,H-2b),1.59 (1H,m,H-21b),1.58 (1H,m,H-2a),1.58(1H,m,H-7a),1.58 (1H,m,H-16a),1.58 (1H,m,H-19a),1.57 (1H,m,H-1a),1.54 (1H,m,H-21a),1.53 (1H,m,H-9),1.12 (1H,m,H-27),0.97 (1H,s,H-23),0.97 (1H,m,H-6b),0.92 (1H,m,H-16a),0.91 (1H,s,H-30),0.90 (1H,s,H-29),0.89 (1H,s,H-25),0.75 (1H,s,H-24),0.72 (1H,s,H-26),0.72 (1H,m,H-5);13C NMR (CDCl3,100MHz)δC:180.3(C-28),143.6 (C-13),122.7 (C-12),79.1 (C-3),55.2 (C-5),47.6 (C-9),46.5 (C-17),45.9 (C-9a,9b),41.6 (C-14),41.0 (C-18),39.4 (C-4),38.8 (C-16a,16b),37.4 (C-8),33.8 (C-21a,21b),33.1 (C-29),32.7 (C-22a,22b),32.5 (C-7a,7b),30.7 (C-20),28.0 (C-23),27.7 (C-15a,15b),27.2 (C-1a,1b),25.9 (C-27),23.6 (C-11a,11b),23.4 (C-2a,2b),18.3 (C-6a,6b),17.1 (C-26),15.5 (C-24),15.3 (C-25)。以上数据和文献[16]对照一致,因此确定化合物10为齐墩果酸。
化合物11白色粉末(CH3OH);ESI-MS:m/z375 [M+Na]+;分子式:C17H20O8;1H NMR (CD3OD,400 MHz)δH:7.65 (1H,d,J=8.0 Hz H-7′),7.46 (2H,d,J=8.0 Hz,H-2′,6′),6.81 (2H,d,J=8.0 Hz,H-3′,5′),6.28 (1H,d,J=8.0 Hz H-8′),5.28 (1H,m,HO-4),4.13 (1H,m,HO-1),3.31 (1H,dd,J=4.0,8.0 Hz,HO-3),3.69 (3H,s,MeO-7),3.31 (1H,m,H-4),2.21 (1H,dd,J=4.0,8.0 Hz,H-5),2.10 (2H,d,J=8.0 Hz,H-2),2.01 (2H,d,J=8.0 Hz,H-6);13C NMR (CD3OD,100 MHz)δC:175.7 (CO-7),168.5 (C-9′),161.7 (C-4′),147.1 (C-7′),134.0 (C-6′),131.4 (C-2′),127.3 (C-1′),116.7(C-5′),116.1 (C-3′),115.3 (C-8′),76.1 (C-1),72.8 (C-5),72.4 (C-4),70.6 (C-3),53.2 (OMe),38.3 (C-2),30.9 (C-6)。以上数据和文献[17]对照一致,因此确定化合物11为5-O-P香豆酰奎宁酸甲酯。
化合物12白色粉末(CHCl3);ESI-MS:m/z315 [M+Na]+;分子式:C19H32O2;1H NMR (CDCl3,400 MHz)δH:5.20-5.40 (6H,m),3.64 (3H,s),2.28 (2H,t,J=7.4 Hz),2.78 (4H,m),1.59 (2H,m),1.23-1.30 (CH2),0.95 (3H,t,J=7.4 Hz);13C NMR (CDCl3,100 MHz)δC:174.3 (s),131.9 (d),130.3 (d),128.2 (d),128.2 (d),127.7 (d),127.1 (d),51.4 (q),34.1 (t),29.7 (t),29.6 (t),29.1 (t),29.0 (t),27.2 (t),25.6 (t),25.5 (t),24.9 (t),20.5 (t),14.2 (q)。以上数据和文献[18]对照一致,因此确定化合物12为亚麻酸甲酯。
化合物13白色粉末(CHCl3);ESI-MS:m/z289 [M+Na]+;分子式:C19H32O2;1H NMR(CDCl3,400 MHz)δH:2.58 (2H,t,J=4.0,4.0 Hz,H-2),1.65 (2H,m,H-3),1.28 (24H,m,H-4~15),0.96 (3H,t,J=8.0,4.0 Hz,H-16);13C NMR(CDCl3,100 MHz)δC:180.1 (C-1),34.0 (C-2),24.7 (C-3),29 (C-4),29.2 (C-5),29.4(C-6),29.7 (C-7~12),29.3 (C-13),31.9 (C-14),22.7 (C-15),14.1 (C-16)。以上数据和文献[19],因此确定化合物13为软脂酸。
2.2 活性评价
对分离得到的化合物进行体外α-葡萄糖苷酶抑制活性筛选,结果显示化合物1和2有较强的α-葡萄糖苷酶抑制活性,其IC50分别为18.5 μmol/L和175 μmol/L,均高于阳性对照阿卡波糖(IC50=405 μmol/L),其余化合物均没有表现出明显活性。
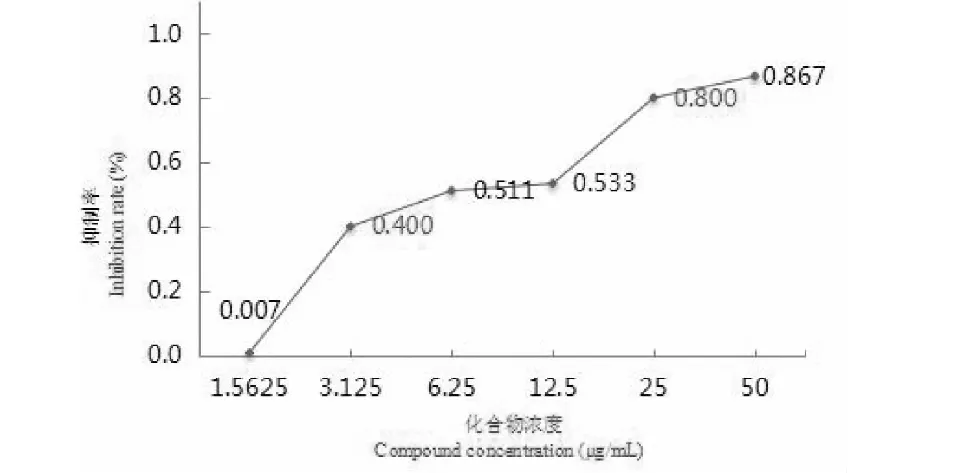
图1 化合物1抑制率曲线Fig.1 Compound 1 inhibition rate curve

图2 化合物2抑制率曲线Fig.2 Compound 2 inhibition rate curve
3 结论
青钱柳中主要含有三萜类、黄酮、甾体、萜类、有机酸、多糖等类型成分,青钱柳具有多方面的药理活性,尤其在降血糖方面有独特的疗效。目前研究的药理功效多集中在提取部位,并未确定其真正的活性成分,而且对其降血糖作用的研究尚缺乏系统性,其降糖物质基础和作用机制仍不明确。本次实验从黔产青钱柳叶中分离得到化合物13个,其中,化合物9为新天然产物,化合物2~4、7、8、11、13为首次从该植物中分离得到。对分离得到的化合物1~10进行了体外α-葡萄糖苷酶活性测定,结果显示黄酮类化合物1和2显示了较强的抑制活性,其余的萜类、甾体类和脂肪酸均没有活性。由此可以推测黄酮类化合物是青钱柳降血糖有效成分之一。从上述实验分析青钱柳中有降糖作用的物质不只是多糖类,还有可能为黄酮类成分。为进一步研究降血糖机制提供一定的思路和方向。
