HPLC-MS/MS法检测血浆伏立康唑、泊沙康唑和伊曲康唑浓度的方法建立及在白血病患者用药监测中的应用*
2019-06-21孙文利王红春刘红星
王 磊,孙文利,刘 瑞,王红春,刘红星,2
(1.河北燕达陆道培医院,河北三河 065201,2.北京陆道培血液病研究院,北京 100176)
关键字:伏立康唑;泊沙康唑;伊曲康唑;高效液相色谱-串联质谱法;治疗药物监测
白血病是一类造血干细胞的克隆性恶性疾病,免疫功能低下的患者容易受到真菌感染的侵袭[1-3],而唑类抗真菌化合物[1-13](如伏立康唑、泊沙康唑和伊曲康唑)在预防和治疗这些真菌感染方面占有坚实的地位。伏立康唑主要用于治疗侵袭性曲霉菌病或抗氟康唑念珠菌感染。泊沙康唑亦用于治疗真菌感染或侵袭性曲霉菌病的抢救治疗[6]。伊曲康唑对曲霉菌和念珠菌均具有活性,在预防真菌感染方面具有一定的地位。唑类抗真菌药[4-11]的药代动力学表现出较大的个体间和个体内变异,部分原因可由非线性药动学、生物利用度差异、药物相互作用和细胞色素P450多态性所致。多年来,这种变异一直困惑着临床。近期,有研究显示患者血浆中唑类药物浓度与疗效和毒性之间有一定相关性[5-13]。为了常规监测血浆中唑类抗真菌药物的含量,需要一种通用的高通量样品分析方法。目前尚无关于伏立康唑、泊沙康唑和伊曲康唑商品化的血药浓度检测试剂盒。因此,我们建立了一种简便、快速、灵活的高效液相色谱-串联质谱法(HPLC-MS/MS)分析患者血浆中此三种药物的浓度,通过血药浓度检测以解决临床在使用这三种药物时所面临的困境,让临床能更直观的调整患者给药剂量,达到更好地治疗效果。
1材料与方法
1.1 研究对象 由于笔者所在医院为血液病医院,移植患者口服伏立康唑和泊沙康唑较多,故收集近期服用伏立康唑和泊沙康唑患者血浆样本各1 000份,伊曲康唑患者血浆样本3例;标本采集时间均为下次服药前,采集静脉血2 ml,混匀,EDTA抗凝。室温(20~25℃)下标本存放时间不超过4 h,当日进行HPLC-MS/MS法检测。
1.2 试剂和仪器 色谱甲醇(fisher),水(广州屈臣氏);甲酸(HPLC Grade,MREDA TECHNOLOGY INC);乙酸铵(HPLC Grade,MREDA TECHNOLOGY INC);伏立康唑(中国食品药品检定研究院);伏立康唑-d3,泊沙康唑,泊沙康唑-d4,伊曲康唑和伊曲康唑-d9均来自TORONTO RESEARCH CHEMICALS INC(HPLC Grade)。高效液相色谱系统(SHIMADZU,含二元LC-AD XR高压输液泵,DGU-20A3在线脱气机,CTO-20A柱温箱,SIL-20ACXR自动进样器);质谱(AB Sciex 4000Qtrap);数据分析处理软件:Analyst V1.5.2工作站(AB公司)。
1.3 方法
1.3.1 液相色谱及质谱条件:见表1。
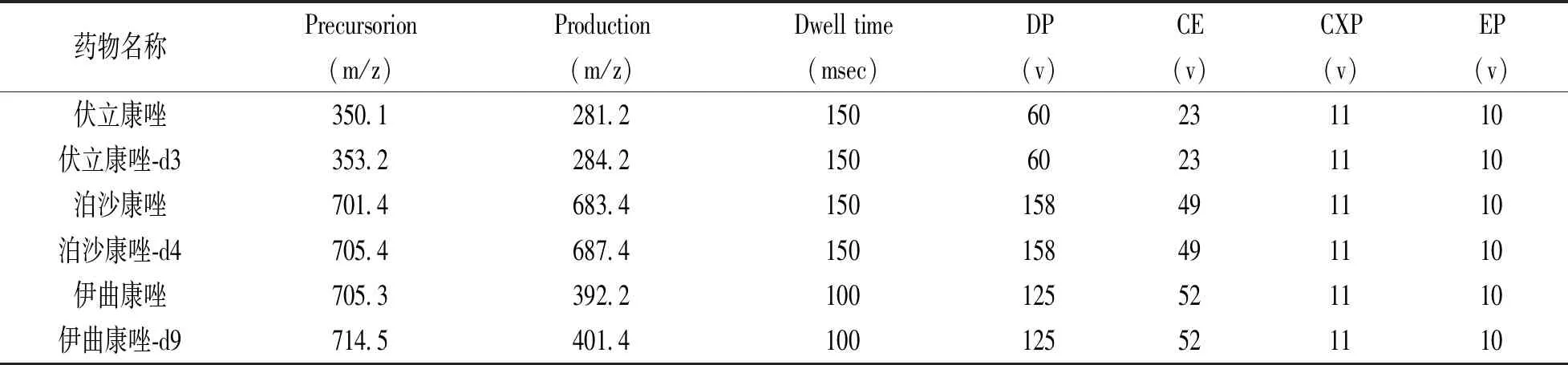
表1 质谱条件
注:DP:declustering potential;CE:collision energy;CXP:collision cell exit potential;EP:entrance potential。
色谱条件:采用Ultimate XB-C18色谱柱(4.6×50 mm,5 μm),柱温60℃;流速:0.8 ml/min;流动相:0.1 ml/dl甲酸甲醇溶液(A)- 0.1 ml/dl甲酸-2 mmol/L乙酸铵水溶液(B),进样量1 μl,洗脱方式:梯度洗脱,其中0.3~1.3 min,A相浓度为12%~82.5%,保持1.2~2.6min A相浓度从82.5%~100%,保持0.9~3.6min A相浓度从100%~12%,保持1.4 min停止。
质谱条件:电喷雾电离源(ESI);离子极性:正离子模式;监测模式为MRM;离子喷射电压:4 500 V;温度:500℃;GS1:55;GS2:55;Curtain gas:30;碰撞气压力:Medium。
1.3.2 标准品贮备液与内标贮备液的配制:精密称取标准品伏立康唑、泊沙康唑和伊曲康唑各10 000 0 mg,分别置于小烧杯中,用适量甲醇溶解,转移至10.00 ml容量瓶中,用甲醇定容,得1.0 mg/ml伏立康唑、泊沙康唑和伊曲康唑标准品母液,作为贮备液。分别移取各标准品贮备液适量,混合,再用甲醇-超纯水(1/1)依次稀释,分别得混合标准品浓度为1,5,10,25,50,75和100 μg/ml,作为1~7号系列混合标准工作液。精密称取标准品伏立康唑-d3 0.5000 mg,泊沙康唑-d4 0.5000 mg和伊曲康唑-d9 1.000 0 mg分别置于三个小烧杯中,用适量甲醇溶解,分别转移至三个10.00 ml容量瓶中,用甲醇定容,得50 μg/ml 伏立康唑-d3母液,50 μg/ml 泊沙康唑-d4和100 μg/ml 伊曲康唑-d9母液作为内标贮备液,分别移取各内标贮备液适量,配成浓度为伏立康唑-d3 5 ng/ml,泊沙康唑-d4 100 ng/ml和伊曲康唑-d9 200 ng/ml的混合内标液,备用。
1.3.3 样品处理方法:移取患者样本血浆100 μl置于1.5 ml EP管中,然后加入0.1 ml/dl甲酸-2 mmol/L乙酸铵水溶液100 μl,涡旋振荡0.5 min,再加入混合内标液800 μl,涡旋振荡0.5 min,13 000 r/min,离心10 min,取上清液150 μl置于自动进样器。
1.3.4 标准曲线的制备:分别在7个1.5 ml EP管中加入空白血浆90 μl,并加入含有伏立康唑、泊沙康唑和伊曲康唑各系列混合标准工作液10 μl,得各标准品浓度分别为0.1,0.5,1,2.5,5,7.5和10μg/ml,按“1.3.3”项下样品处理方法处理后进样测定,分别以伏立康唑峰面积/伏立康唑-d3峰面积为(Y)对伏立康唑浓度(X),泊沙康唑峰面积/泊沙康唑-d4峰面积为(Y)对泊沙康唑浓度(X)和伊曲康唑峰面积/伊曲康唑-d9峰面积为(Y)对伊曲康唑浓度(X)进行线性回归,分别得伏立康唑、泊沙康唑和伊曲康唑标准曲线。
1.3.5 回收率、精密度试验:分别在3个1.5 ml EP管中加入空白血浆90 μl,并加入含有伏立康唑、泊沙康唑和伊曲康唑2,3,5号混合标准工作液各10 μl,得各标准品浓度分别为0.5,1和5 μg/ml,按“1.3.3”项下样品处理方法处理后进样测定,各浓度日内重复测定5次,计算相对回收率及日内精密度,并连续测定5天,计算日间精密度。
1.3.6 稳定性试验:分别在3个1.5 ml EP管中加入空白血浆90 μl,并加入含有伏立康唑、泊沙康唑和伊曲康唑2,3,5号标准工作液各10 μl,得各标准品浓度分别为0.5,1和5 μg/ml。取一份样品按“1.3.3”项下血样处理方法处理后置于4℃自动进样器中,于放置时间72 h分别测定各样品的浓度;其余样品于4℃冰箱中放置72 h后取出放至室温,按“1.3.3”项下样品处理方法处理后进样测定,考察其稳定性。
1.4 统计学分析 对伏立康唑和泊沙康唑血药浓度检测结果作四分位法分析。
2结果
2.1 色谱质谱行为 在“1.3.1”项下的色谱质谱条件下,测得伏立康唑、泊沙康唑和伊曲康唑二级碎片离子质谱图,见图1;其质谱色谱图见图2。由图2可见,血中没有物质干扰伏立康唑、泊沙康唑和伊曲康唑的测定,出峰时间分别是2.61,2.87和3.35 min;各物质能实现较好分析,各峰型良好,无杂质峰干扰。
2.2 标准曲线回归方程 在“1.3.4”条件下,伏立康唑回归方程为:Y=1.58X+0.011 6 (r=0.998 7),泊沙康唑回归方程为:Y=1.38X+0.021 7(r=0.998 2)和伊曲康唑回归方程:Y=1.42X+0.032 5(r=0.999 1),表明此三种物质在浓度0.1~10.0 μg/ml 范围内线性关系均较好,可用于血浆中此三种药物的含量测定,最低定量限分别为0.009,0.021和0.085 μg/ml。
2.3 方法学评价结果 伏立康唑、泊沙康唑和伊曲康唑的相对回收率和日内、日间精密度测定结果,见表2。由表2可知,伏立康唑、泊沙康唑和伊曲康唑相对回收率均在±5%之间,日内及日间精密度RSD均小于5%。说明此方法检测血中伏立康唑、泊沙康唑和伊曲康唑浓度精密度和准确度较好。
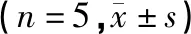
表2 回收率和精密度试验结果
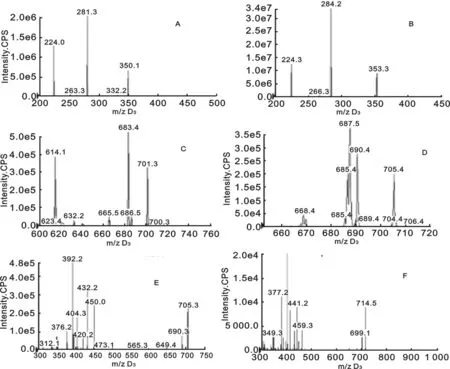
伏立康唑(A),伏立康唑-d3(B),泊沙康唑(C),泊沙康唑-d4(D),伊曲康唑(E)和伊曲康唑-d9(F)。
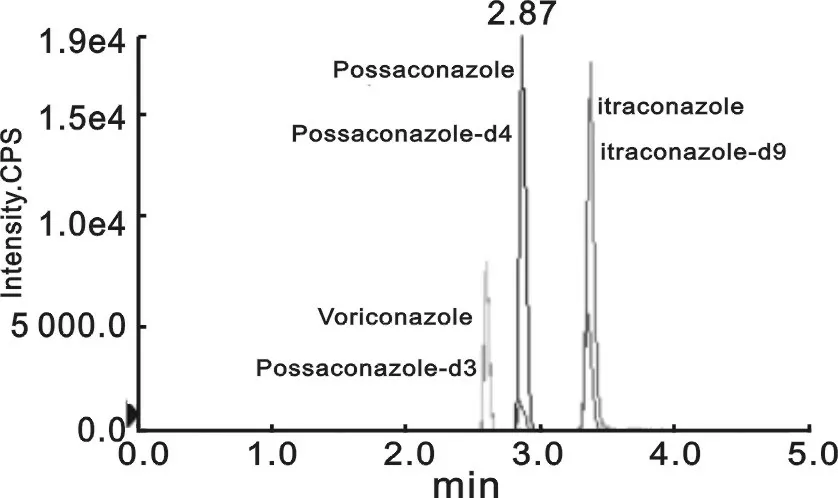
图2 伏立康唑、泊沙康唑和伊曲康唑质谱色谱图
2.4 稳定性考察结果 见表3。在4℃条件下,血中伏立康唑、泊沙康唑和伊曲康唑放置72 h浓度无变化;血样经过处理后,在4℃条件下,放置72 h,伏立康唑、泊沙康唑和伊曲康唑浓度亦无变化。说明伏立康唑、泊沙康唑和伊曲康唑在血中较稳定,同时血浆样本经前处理后不会影响其稳定性,可长时间放置,待检。由此可知,在此条件下测定血中伏立康唑、泊沙康唑和伊曲康唑浓度,稳定性较好。
表3 稳定性考察结果
2.5 临床应用结果 白血病患者伏立康唑和泊沙康唑血药浓度检测结果做成箱式图,可以得知1 000例伏立康唑样本浓度检测结果中位数是0.8 μg/ml,上四分位数是0.3 μg/ml,下四分位数是1.7 μg/ml,伏立康唑 0.1~10 μg/ml的检测范围符合临床需求。1 000例泊沙康唑样本浓度检测结果的中位数是0.8 μg/ml,上四分位数是0.4 μg/ml,下四分位数是1.4 μg/ml,与泊沙康唑 0.1~10 μg/ml的检测范围相符合。
3讨论本实验采用混合内标法,通过蛋白沉淀法进行甲醇沉淀蛋白和释放伏立康唑、泊沙康唑和伊曲康唑,使其充分溶解于甲醇。通过质谱对其进行快速检测,进而实时定量,能节约各药物的定标时间和检测各样本平衡时间,能快速报告各药物血药浓度,辅助临床尽早调整用药,使患者得到适宜的个体化治疗。
此1 000例伏立康唑血药浓度检测结果表明目前使用伏立康唑剂量偏小,浓度偏低,明显低于伏立康唑有效谷浓度范围0.5~5μg/ml[1-13],说明白血病患者服用伏立康唑尚有一部分患者不能达到有效的预防和治疗浓度,对其进行血药浓度监测具有重要的临床意义。而1 000例泊沙康唑血药浓度检测结果表明目前使用泊沙康唑的剂量也较低,血药浓度结果偏低,亦小于相关文献报道[1-13]的有效谷浓度(>0.7 μg/ml),其检测结果中位数明显低于理想靶值(1.25 μg/ml),说明白血病患者在目前临床给药情况下,有相当一部分患者未能达到有效的治疗浓度,足见对其进行血药浓度监测能更好地使患者得到治疗,有效控制感染和避免感染的发生。而伊曲康唑目前临床应用较少,3例检测数据表明,伊曲康唑在目前临床给药情况下,其血药浓度尚可,其主要代谢产物羟基伊曲康唑[3-9]与原药伊曲康唑的浓度比例为2∶1,且羟基伊曲康唑体外研究表明还有活性,体内研究尚无完整数据可查。
目前国内[3-7]对于抗真菌药物的治疗药物监测已经有一些共识和具体建议,越来越多的国外[11-13]研究结果认为血浆药物浓度监测在抗真菌药物的安全性和有效性优化方面起到重要的作用;美国感染病学会(IDSA)关于曲霉菌病治疗的临床实践指南中,建议结合血浆抗真菌药物浓度和其他临床评价指标来评估药物暴露不足导致的治疗失败以及药物毒性。
