胰十二指肠切除术后胰瘘危险因素及风险预测
2019-06-20吴耐任泽强张蓬波张秀忠张冲龚帅张易
吴耐,任泽强,张蓬波,张秀忠,张冲,龚帅,张易
作者单位:徐州医科大学附属医院胰腺外科,江苏 徐州 221003
胰十二指肠切除术(Pancreaticoduodenectomy,PD)是治疗胰头及壶腹周围良恶性病变的标准术式,因手术涉及脏器广、切除范围大、消化道重建多,故其操作难度大、风险高、术后并发症多、病死率高。据报道,其术后并发症发生率高达30%~60%[1-3],而胰瘘(pancreatic fistula,PF)是PD术后最常见而且最严重的并发症,发生率为3%~45%[4],且其发生与术后病死率较高有显著的相关性[5]。临床上已采取诸多措施以降低围手术期并发症的发生,目前,胰十二指肠切除术后病死率已降到5%以下[2,6]。
本研究回顾性分析161例行胰十二指肠切除术病人的临床资料,探讨胰十二指肠切除术后胰瘘发生的独立危险因素,并尝试建立胰瘘风险预测模型,以期对PD术后胰瘘(POPF)的预防拥有更深入的认识。
1 资料与方法
1.1 一般资料徐州医科大学附属医院胰腺外科2014年1月至2017年3月收治的161例行PD病人,男性100例,女性61例;年龄范围为25~83岁,平均年龄60岁;术前合并高血压38例;合并糖尿病56例;术后病理类型:胰腺癌30例,胆管癌51例,壶腹癌26例,十二指肠癌22例,其他32例(主要包括胰腺导管内乳头状瘤、胆管上皮增生、十二指肠乳头炎症、胰头囊肿以及胰腺、十二指肠神经内分泌肿瘤等)。病人及近亲属知情同意并签署同意书。本研究符合《世界医学协会赫尔辛基宣言》相关要求。
1.2 手术方式本组161例病人中,行胰十二指肠切除术(PD)151例,保留幽门胰十二指肠切除术(PPPD)10例;开放手术96例,腔镜手术65例;消化道重建方式均采用Child术式,即按胰肠、胆肠、胃肠顺序进行消化道吻合重建;胰肠吻合方式:胰管-空肠黏膜吻合130例,胰腺-空肠端侧吻合31例;所有病人均放置胰管支撑管内引流(放置方法:探及主胰管,将胰管支撑管插入主胰管约2~3 cm,并缝线固定于胰管周围胰腺组织,支撑管横跨胰肠吻合口并延肠道走行引流)。
1.3 胰瘘定义、诊断标准、分级参照2016年国际胰瘘研究小组更新的胰瘘定义与分级[4]以及2017年中华医学会外科学分会胰腺外科学组关于胰腺术后并发症诊治的专家共识[7]。
(1)胰瘘定义:胰瘘是胰腺导管上皮与其他上皮表面的异常通道,内有源自胰腺富含酶类的液体[4]。
(2)胰瘘诊断标准:术后≥3 d任意量的引流液中淀粉酶浓度高于正常血清淀粉酶浓度上限3倍以上,同时强调必须具有相应临床表现(如发热、腹痛等)。
(3)胰瘘分级:在2016年国际胰瘘研究小组更新的胰瘘定义与分级中,既往认为的A级胰瘘被定义为生化瘘(非胰瘘),B级胰瘘指需要术后治疗策略变动(如持续胰周引流>3周、需要通过内窥镜或经皮穿刺引流),C级胰瘘则明确指那些需要重新手术、导致器官功能衰竭(尤其是呼吸、肾脏、心脏功能不全)和(或)由此引发死亡的胰瘘。
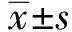
2 结果
2.1 概况本组161例病人中,A级胰瘘(非胰瘘组)133例,B、C级胰瘘(胰瘘组)28例,其中B级26例(26/161,16.15%),C级2例(2/161,1.24%)。B级胰瘘病人经引流管充分引流、经引流管腹腔冲洗、彩超引导下经皮穿刺引流等痊愈。2例C级胰瘘病人,均为术后引流管短时间内引流出大量血性液体,分别于术后9、31 d行再手术治疗,术中证实为胰瘘导致的腹腔内出血。本组病人无围手术期死亡病例。
2.2 单因素分析结果单因素分析表明,与非胰瘘组病人相比,胰瘘组病人BMI大、胰腺质地软、胰管直径小,差异有统计学意义(P<0.05);其余因素两组间比较均差异无统计学意义(P>0.05)。见表1。
2.3 多因素分析结果将发生胰瘘状态作为因变量(赋值1=发生,0=无),胰腺质地、胰管直径作为自变量进行logistic回归分析,发现BMI较大、胰腺质地软、胰管直径小为胰瘘发生的独立危险因素(P<0.05)。见表2。
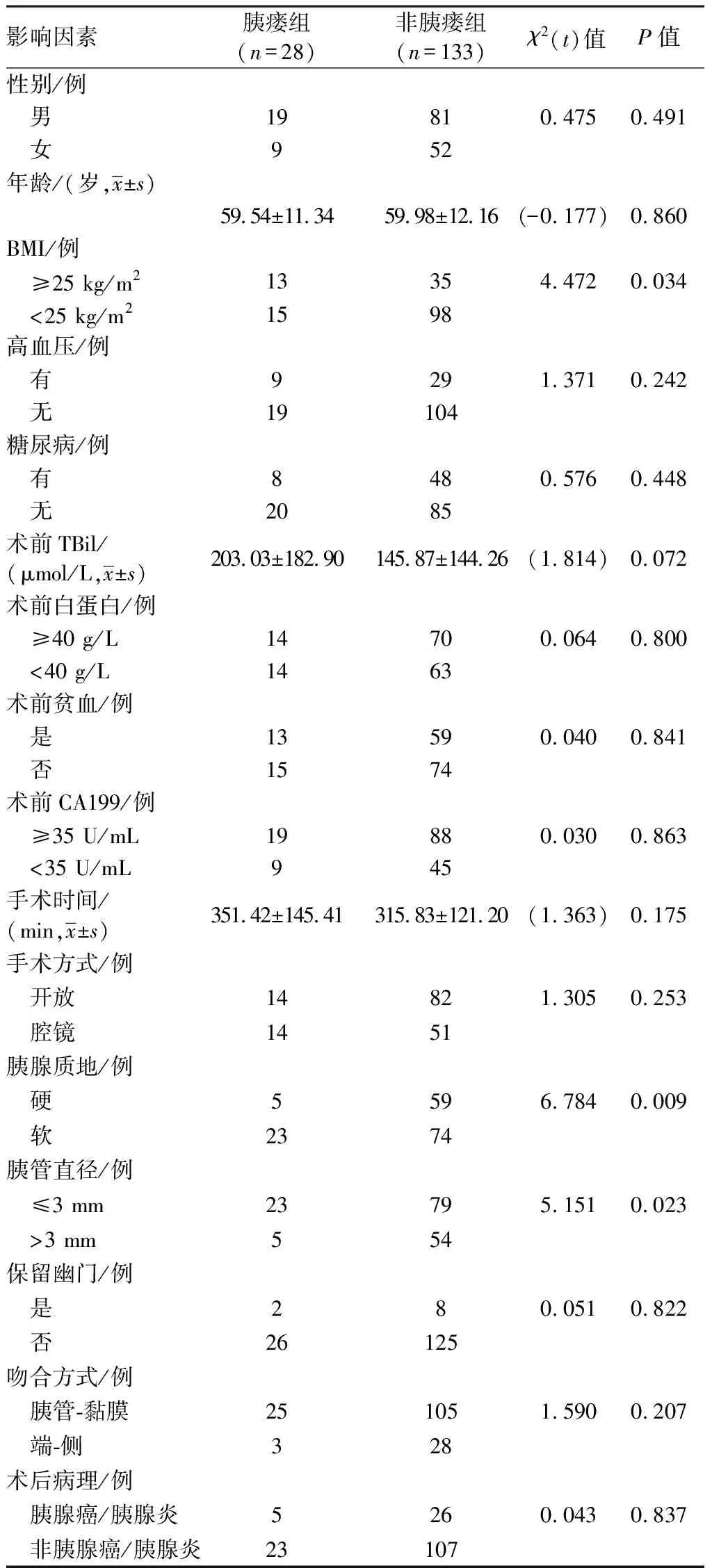
表1 161例行胰十二指肠切除术后胰瘘相关因素单因素分析

表2 161例行胰十二指肠切除术后胰瘘相关因素多因素logistic分析
2.4 胰瘘风险预测模型根据logistic多因素回归分析结果(表2),建立胰十二指肠切除术后胰瘘发生风险的预测模型,该模型受试者工作特征曲线(ROC曲线)下面积0.750(95%CI:0.658~0.841)(图1),阈值点的灵敏度为0.786,特异度为0.639。

图1 胰十二指肠切除术后胰瘘发生风险的预测模型--ROC曲线
3 讨论
胰瘘作为PD术后最常见且最严重的并发症,一直是临床研究的热点和难点,本组病人胰瘘发生率17.39%,与文献报道相当。而关于POPF的发生机制尚不明确,一方面可能因吻合不确切,加之肠管内消化液的侵蚀,造成吻合薄弱处消化液及胰液漏入腹腔;另一方面可能为缝针穿透细小胰管而引起的单纯性胰液外漏。目前,临床上已经采取多种预防措施以降低POPF的发生率,如胰肠吻合方式的改进、生长抑素的应用等。
既往研究认为,POPF发生的危险因素有病人自身因素(性别、年龄、基础疾病等),疾病相关因素(胰腺质地、胰管直径、病理类型等),手术相关因素(手术时间、术中失血量、吻合方式、胰管引流等)。虽然POPF危险因素的研究结果众多,但目前尚无定论。本组研究结果显示POPF的发生与体质指数(BMI)、胰腺质地及胰管直径有关。
BMI反映身体肥胖程度,有研究显示[8],肥胖(POPF率:36.8%)与非肥胖(POPF率:15.1%)病人之间胰瘘发生率差异有统计学意义。更有研究结果[9-10]直接指出BMI>25 kg/m2是PD术后胰瘘的危险因素。随着BMI的增加,内脏脂肪含量往往也升高,胰腺组织的脂肪含量亦如此。胰腺脂肪含量的增加一方面会导致胰腺质地较软,增加术中胰肠吻合口缝合的难度,另一方面可能有导致术后吻合口延迟愈合的风险。胰腺质地及胰管直径是目前较为公认的POPF的危险因素。软胰腺质地容易被缝线切割,不利于保持吻合口的完整性,Belyaev等[11]研究发现也证实,缝线保持能力与组织硬度呈正相关,而且他还认为缝合胰管可以增加吻合的机械强度。胰腺质地由胰腺组织脂肪含量及纤维化程度决定,临床上关于胰腺质地的评定尚无定量测量方法,通常由主刀医生用手的触感判断,描述中不乏模棱两可的词语,如尚软、稍硬、韧等,主观性强。目前已有学者[12]提出胰体部CT值作为胰腺纤维化程度的量化指标,并且其发现胰瘘的严重程度与胰体部CT值呈负相关。胰管直径小作为POPF的危险因素,其原因可能在于,较细的胰管直径一方面增加术中吻合难度,另一方面不利于残端胰液的排出。目前,胰管直径≤3 mm被认为是POPF的独立危险因素。
胰瘘的危害在于,被激活的胰酶侵蚀临近的组织器官,引起出血、吻合口瘘等,加之消化道细菌移位,造成严重的腹腔内感染。因此,胰瘘的预防至关重要,已有多位学者尝试建立胰瘘风险预测评分系统,以期对POPF的预防提供帮助。Callery等[13]以术中和术后指标为判断依据,采用胰腺质地、胰管直径、术中出血量和术后病理四项指标建立评分模型。该评分模型包括术后病理,试想,如果胰瘘先于病理结果发生,则该评分模型就失去了胰瘘预测的意义。Yamamoto等[14]提出的 NCCH(日本国立癌症中心医院)术前预测评分系统,采用性别、是否诊断为胰腺癌、主胰管指数(主胰管直径与胰体最短直径比值)、CT判断门静脉是否受侵、腹腔内脂肪厚度(脐水平腹直肌腹腔内侧面至腹主动脉后壁间的距离)五项指标建立预测模型,所有评价指标术前均可获得,但该模型取值较为复杂,很大程度上限制了其临床应用。Wellner等[15]以年龄、术前诊断、吸烟史、有无体重减轻、有无急性胰腺炎病史建立术后胰瘘评分系统,该评分系统中指标的界定较为模糊,对评定结果的影响较大。
本研究结果显示BMI、胰腺质地、胰管直径为POPF的独立危险因素,因此以其作为指标建立预测模型,量化分析POPF的发生风险,数据简单易得,可为预测POPF的发生提供参考。但本研究仍存在诸多不足,模型中胰腺质地分为软、硬,由术者判断,主观性过强;胰管直径由术中测量胰腺残端得出,有被切割器影响测量结果的可能。今后的研究中,关于胰管直径的测量,可由术前彩超、CT得出,胰腺质地的判断亦可由CT值的高低判断。此外,本研究纳入的样本量尚且不足。在今后的工作中,我们将以当前的模型作为基础进行前瞻性验证,以期进行完善。
