肝脏原发性未分化多形性肉瘤的MSCT 表现及临床病理分析
2019-06-15吴彩云严静东李文菲
吴彩云,陈 涛,严静东,李文菲,陈 伟
(1.湖北文理学院附属医院 襄阳市中心医院综合内科,PET-CT 中心,湖北 襄阳 441000;2.南方医科大学南方医院信息科,广东 广州 510515;3.秦皇岛市第一医院放射科,河北 秦皇岛 066000)
未分化多形性肉瘤(Undifferentiated pleomorphic sarcoma,UPS)以往称之为恶性纤维组织细胞瘤,是一种较为常见的软组织肉瘤,起源于间叶组织,可发生于全身各部位,多见于四肢及腹膜后,发生于肝脏者极为罕见,误诊率高[1]。本文回顾性分析6 例经病理证实的肝脏原发UPS,探讨其MSCT影像学表现及临床病理特点,以提高对本病的诊断水平。
1 资料与方法
搜集2011 年8 月—2018 年8 月经我院病理证实的6 例肝脏UPS 患者,男5 例,女1 例,年龄41~59 岁,中位年龄50岁。6 例患者均有不同程度腹痛,2 例伴发热,1 例伴体质量减轻。2 例有乙型肝炎病史,且合并肝硬化。实验室检查:AST 及ALT 升高者2 例,6 例AFP、CAl99、CAl25 及CEA 均呈阴性。
采用Siemens 公司Sensation 16 CT 及Philips 公司Brilliance 64 CT,6 例均行平扫后动态增强扫描。扫描参数:管电压120 kV,管电流260 mAs,层厚5 mm,层距5 mm,增强扫描采用高压注射器经肘静脉注射对比剂碘佛醇 (320 mgI/mL),注射速度为3 mL/s,剂量为1~1.5 mL/kg。所有扫描数据均传到PACS 工作站进行多平面重组后处理,再由两名影像医师共同阅片。
5 例行手术后病理检查,1 例于CT 引导下行经皮肝细针穿刺活检检查,标本取材后用10%福尔马林固定,行常规HE及免疫组织化学染色。
2 结果
6 例肿瘤大小约6.6 cm×4.5 cm~9.7 cm×6.8 cm;位于肝右叶及肝左叶各3 例;除1 例外余5 例形态呈类圆形,边界清晰(图1a,2a),周围见假包膜(图2b);6 例平扫均呈不均匀低密度,内见囊变坏死区。增强后动脉期5 例呈不均匀轻中度强化,1 例呈不均匀明显强化,周围均可见供血血管(图1b),静脉期及延迟期5 例强化程度减低,1 例强化程度增高,囊变坏死区无强化 (图1c);1 例伴肝内胆管内多发条片状高密度,提示癌栓形成可能;1 例双肺见多发结节,提示肺转移可能。
镜下肿瘤细胞异型性明显,呈梭形或类圆形,胞浆丰富红染,核为卵圆形及不规则形,核仁明显,核分裂象易见;免疫组化分析示6 例Vim 呈阳性,5 例CD68 及Mac387 呈阳性(图2c),2 例CD31、CK7 及CK19 呈阳性,1 例AAT、S-100及Ki-67 呈阳性。
3 讨论
3.1 肝脏原发性UPS 的组织学来源、临床表现及病理特征
UPS 以往也被称为恶性纤维组织细胞瘤,肝脏UPS 是成人肝脏罕见的软组织肉瘤,其组织起源多数学者认为是原始间叶细胞向组织样细胞和成纤维细胞双向分化的结果[2-3]。Weiss 等[4]根据肿瘤细胞的组成成分和形态特点曾将其分为五类,即席纹状多形性型、黏液样型、巨细胞型、炎症型和血管瘤样型。2002 年WHO 对恶性纤维组织细胞瘤的术语及分类方法进行了重新评估及修订,大部分学者认为恶性纤维组织细胞瘤的本质是UPS,其组织学来源及分化方向仍不明确,故去除了黏液样型及血管瘤样型;而2013 年WHO 最新软组织分类以UPS 取代了恶性纤维组织细胞瘤[5]。
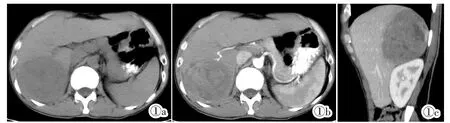
图1 男,46 岁,间断右上腹疼痛两月余。图1a:横断位平扫示肝右叶类圆形低密度肿块,边界尚清,其内密度不均匀,见片状囊变坏死。图1b:横断位增强示不均匀轻中度强化,周围见供血血管。图1c:矢状位增强示囊变坏死区无强化。Figure 1.A 46 years old man with intermittent right-upper abdominal pain for more than two months.Figure 1a:Axial unenhanced CT image showed a round mass of uneven low density with cyst degeneration and necrosis and clear border in the right liver.Figure 1b:Axial contrast-enhanced CT showed non-uniform mild-to-moderate enhancement with supplying vessels around.Figure 1c:Sagittal contrast-enhanced CT showed unenhanced cyst degeneation and necrosis.
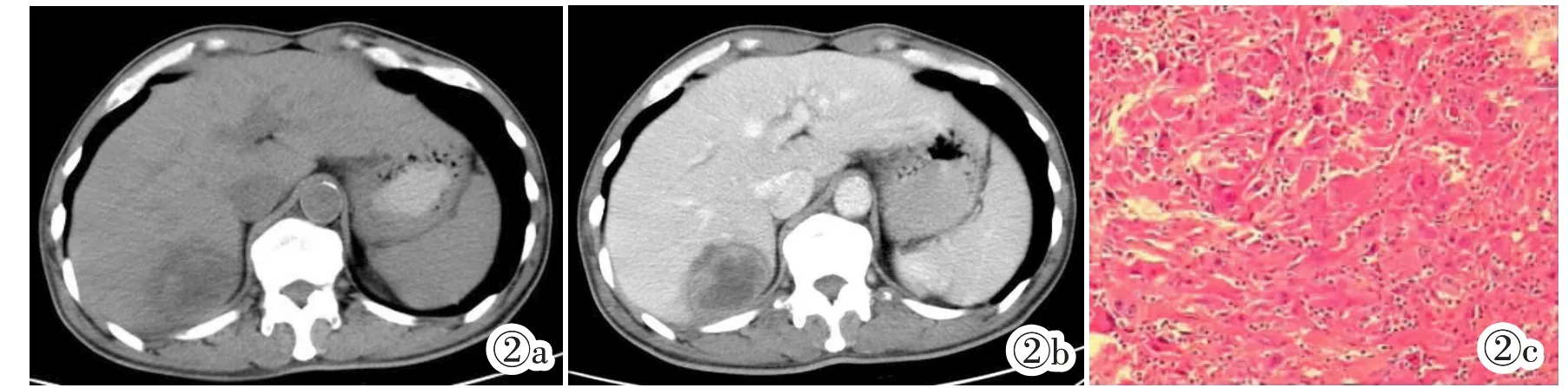
图2 男,59 岁,右上腹疼痛伴体质量减轻3 月。图2a:横断位平扫示肝右叶类圆形低密度肿块,边界清晰,其内密度不均匀,见囊变坏死区。图2b:横断位增强示轻度不均匀强化,周围见无强化假包膜。图2c:镜下示(HE 染色)癌细胞异型性明显,呈梭形或类圆形,胞浆丰富红染,核分裂象易见;免疫组化分析示Vim、CD68、Mac387 及Ki-67 呈阳性。Figure 2.A 59 years old man with right-upper abdominal pain and weight loss for three months.Figure 2a:Axial unenhanced CT image showed a round mass with clear border and uneven low density in the right liver which contained cyst degeneration and necrosis.Figure 2b:Axial contrast-enhanced CT showed non-uniform mild enhancement with unenhanced pseudocapsule.Figure 2c:Under the microscope (HE staining),the cancer cells were fusiform or round with marked pleomorphism,abundant red plasma and obvious mitotic figures.Immunohistochemical analysis showed that Vim,CD68,Mac387 and Ki-67 were positive.
UPS 是一种常见的软组织肉瘤,可发生于任何年龄,但常见于中老年人,男性多于女性[6-7]。本组研究患者年龄在41~59 岁之间,且6 例患者中有5 例为男性,与文献报道相符。该病可发生于全身任何部位,据Dong 等[3]及Chow 等[8]报道其好发于四肢、腹膜后及躯干,也可见于上颌窦、甲状腺、肺及胸腺等部位,但罕见于肝脏等内脏实质器官。该病病因及发病机制尚不明确,可能与创伤、烧伤、放射/手术损伤等有关[9]。然而,鉴于我国为肝炎大国,本研究有2 例伴乙型肝炎病史,故肝炎是否与肝UPS 的发生有关仍待进一步研究。肝脏UPS患者早期多无明显临床症状,常因腹痛、腹部肿块或体质量减轻而就诊。血清学检查无特异性,AFP、CAl99 及CEA 等肿瘤标记物常呈阴性。治疗上因肝脏UPS 对放化疗不敏感,且肿瘤多呈浸润性生长,术后易复发,因此早期外科扩大切除手术是其治疗较为有效的方式[10]。
病理学上该类肿瘤细胞成分较为复杂,可由组织细胞、成纤维细胞、泡沫细胞、多核瘤巨细胞、炎性细胞或黄色瘤细胞等构成,肿瘤细胞异型性明显,核分裂象易见。免疫组化染色法对该类肿瘤诊断具有很大作用,肿瘤细胞能够表达多种标志物,但不同肿瘤表达标记物的类型不同,大部分肿瘤对Vim、CD68、Actin、AAT、AACT 呈阳性,少部分对Keratin、S-100、Ki-67、CK、CD31 等呈灶性阳性,其中Vim、CD68 是诊断UPS 极为重要的标志物[7,11],以上这些标记物的同时表达则更有利于该病的诊断。本组病例6 例表达Vim,5 例表达CD68,2 例表达CD31、CK7 及CK19,1 例表达AAT、S-100 及Ki-67,与文献报道相仿。但本研究有5 例表达Mac387,而以往文献对此并无阐述,因此笔者认为该标记物是否与肝脏UPS 有关需进一步研究证实。
3.2 肝脏原发性UPS 的MSCT 影像学表现
肝脏原发性UPS 是一种临床较为罕见高度恶性肿瘤,以往文献对该病影像学表现报道较少,术前误诊率较高。据赵才勇等[6]及Karki 等[12]报道,该病好发于肝右叶,体积较大,形态多呈类圆形,边界不清,密度不均匀,增强后呈轻中度强化,易侵犯邻近组织结构及远处转移。笔者结合相关文献[2-3,6,12-13]及本组病例分析,认为其影像学表现如下:①肿块发生部位:据报道该类肿瘤常发生于肝右叶,肝左叶或左右叶同时受累较为少见,且多为单发。本组病例位于肝右叶及肝左叶各有3 例,病灶均为单发,与上述文献报道不完全相符。②肿块大小及形态:肿瘤因恶性程度高细胞生长迅速常形成较大肿块,因此在CT 上病灶体积一般较大,约有80%以上病灶的长径大于5 cm;病变形态常为类圆形或不规则形。本研究肿块长径范围为6.6~9.7 cm,5 例形态呈类圆形,1 例呈不规则形,与文献报道大致相符。③肿块边界:侵袭性生长是肝脏原发性UPS 的特征之一。多数学者认为该类肿瘤因常突破肝包膜而侵犯邻近结构,如腹膜、膈肌、大网膜等,与周围组织分界不清;但少部位学者认为肝脏UPS 肿块因易形成假包膜而边界清晰。本组有5 例肿块边界清晰,并周围可见假包膜;1 例边界不清,肿块向外生长突破肝包膜而侵犯邻近腹膜组织,向内侵犯周围肝内胆管结构。④肿块密度及强化特点: 据报道肝脏UPS 肿块CT 平扫多呈不均匀低密度,少数呈等或高密度,病灶内部常可见更低密度的囊变坏死区域,部分合并有出血或见网格状/轮辐状纤维分隔,钙化较为少见;若肿块体积较小,则常表现为均匀的实性软组织密度。增强扫描后病灶强化形式多样,它取决于肿瘤的血管分布和肿瘤坏死的程度。肝脏UPS 恶性程度高,肿块的供血血管呈多样性,但多数肿瘤内部血管供血适当,其供血主要来自其周围血管。因此增强后多数病灶实性部分呈轻度至中度强化,坏死区域无强化,其内纤维分隔可见不同程度强化,周围假包膜不强化或呈显著强化。本研究病灶平扫均呈不均匀低密度,内见囊变坏死区,未见钙化。增强后动脉期有5 例呈不均匀轻中度强化,1 例呈不均匀明显强化,6 例周围均可见供血血管,呈“抱球样”改变,该征象在以往的文献中很少报道过,笔者认为其可能是该肿瘤的一个重要的MSCT 征象。静脉期及延迟期5 例强化程度减低,1 例呈渐进性强化,笔者认为可能与肿瘤内纤维成分的多少有关。⑤伴随症状及远处转移:肝脏UPS 恶性程度高,侵袭性强,肿块易侵犯邻近组织结构及远处转移,且有较高的局部复发率和转移率,其复发及转移的风险与原发肿瘤的浸润程度有关。远处转移可能通过血液循环和(或)淋巴系统传播,而血行转移多见,最常见的是肺部转移。但多数学者认为其区域淋巴结转移较少见,亦较少侵犯周围大血管及胆道系统。本组有1 例伴双肺多发结节,提示肺转移;1 例伴肝内胆管内多发条片状高密度,提示癌栓形成;6 例均未见肝门区、腹膜后淋巴结转移及门静脉癌栓形成。
3.3 鉴别诊断
肝脏原发性UPS 临床上较为罕见,术前误诊率较高,需与以下疾病鉴别:①原发性肝细胞癌:常合并有肝炎、肝硬化病史,实验室检查AFP 升高,增强扫描表现为“快进快出”强化模式,常伴有肝内多发转移,且易侵犯门静脉及局部淋巴结转移。②肝内胆管细胞癌:常有肝内胆管结石病史,实验室检查CAl9-9 常升高,肿瘤内可见结石或钙化,周围可见扩张胆管或肿瘤包埋胆管表现,增强扫描表现为不均匀性渐进性强化,局部淋巴结转移较常见。本组1 例病例肝内胆管内见高密度影,增强后呈渐进性强化,术前被误诊为胆管细胞癌。③肝内其他肉瘤如血管肉瘤、平滑肌肉瘤:前者增强扫描类似肝血管瘤样强化,动脉期肿块周边呈明显花环状强化,但门脉期、延迟期强化填充速度较慢[14];后者增强扫描病灶实性部分呈明显强化,内可见条状及团块状肿瘤供血动脉,呈类分隔状[15];可与UPS 鉴别。
综上所述,肝脏原发性UPS 为一种罕见的软组织肉瘤,其MSCT 影像表现具有一定的特征性,多表现为类圆形肿块,边界清晰,内见囊变坏死,增强后呈轻中度不均匀强化,周围见供血血管呈“抱球样”改变。同时,MSCT 可清楚的显示肿瘤的内部结构及与周围组织器官的关系,便于术前充分评估,指导临床诊疗及评估预后。
