搅拌棒萃取-气相色谱-质谱法分析地表水中合成麝香及紫外线吸收剂
2019-06-10杨志鹏宋淑玲
佟 玲,潘 萌,杨志鹏,田 芹,宋淑玲
(国家地质实验测试中心,北京 100037)
合成麝香和紫外线吸收剂是一类新兴污染物,常作为个人护理品中的添加物质,广泛用于日用化工产品中。这些化合物存在潜在的致癌性、雌激素作用,会抑制生物生长发育[1],同时具有生物累积性和内分泌干扰效应[2],对人体健康具有一定的威胁。这类物质可通过污水处理厂、娱乐活动场所排污,以及垃圾渗滤液渗透等多种途径持续不断地进入环境,也被称作“伪持续性”化合物[3]。其中,硝基麝香具有生物蓄积作用和潜在的致癌性,欧盟一些国家已对其中的一些产品做出了禁止和限制使用的规定[1],我国2007年修订的《化妆品卫生规范》中也明确将硝基麝香列入禁限用物质表中[4]。据调查,我国约82%的日化产品中含有合成麝香,其中多环麝香中的佳乐麝香和吐纳麝香检出率最高,分别达78%和65%[5]。随着化学合成技术的不断发展,一些易降解的新型合成麝香(如大环麝香)不断涌现。紫外线吸收剂产量较高的两类是苯并三唑类和二苯酮类,在化妆品、清洗剂、防冻剂、食品包装材料中都有应用,而我国紫外线吸收剂的年产量从2010年开始已经达到了万吨以上[6],但对这些物质在环境排放的限制以及环境中污染水平的监测还处于起步阶段。
目前,多采用固相萃取技术对水样中合成麝香和紫外线吸收剂进行分离富集[7-10],浓缩富集大多选用HLB小柱。固相萃取技术的富集倍数较大,能够得到更低的方法检出限,但存在样品用量大、耗时较长、操作繁琐等问题。近年来,一些简便、绿色的富集手段,如固相微萃取[11-12]、搅拌棒吸附萃取(SBSE)[13-14]被广泛应用。SBSE结合热解吸[15-16]进样技术能够减少有机溶剂的使用量。Zhang等[17]采用分散液液微萃取(DLLME)技术分析紫外吸收剂时富集因子为64~110;Homem等[18]采用三氯甲烷作为DLLME的提取溶剂分析了12种麝香类化合物。该技术的有机溶剂用量少、萃取时间短、具有较高的萃取效率和富集倍数,但不适用于批量分析。合成麝香和紫外线吸收剂的测定方法主要有气相色谱法[19]、气相色谱-质谱法[20-23]、气相色谱-串联质谱法[8,24],以及液相色谱-质谱法[25-26],其中气相色谱-质谱法应用较为广泛。
目前,我国缺少包括大环麝香在内的多种合成麝香的分析方法,且未见同时测定合成麝香和紫外线吸收剂的报道。这两类化合物极性不同,同时萃取存在一定的难点。因此,本工作拟采用SBSE技术对水样中这两类目标物进行富集,少量有机溶剂解吸搅拌棒后结合气相色谱-质谱法分析其中16种合成麝香及2种紫外线吸收剂,希望能为我国地表水中合成麝香及紫外线吸收剂的监测提供方法参考。
1 实验部分
1.1 仪器与试剂
TRACE DSQ-Ⅱ气相色谱-质谱联用仪:美国Thermo公司产品;磁力搅拌器:美国Thermo Scientific公司产品;超声波清洗器:中国昆山市超声仪器有限公司产品; 12位恒温水浴氮吹仪:北京康林科技股份有限公司产品;旋转蒸发仪:瑞士BUCHI公司产品;聚二甲基硅氧烷(PDMS)涂层的磁力搅拌子(20 mm×1.0 mm):德国GERSTEL公司产品。
硝基麝香、多环麝香、大环麝香和替代物标准品:德国Dr. Ehrenstorfer公司产品;紫外线吸收剂和内标物:百灵威公司产品;丙酮、乙腈、正己烷:均为色谱纯,百灵威公司产品;氯化钠(NaCl)、盐酸、氢氧化钠(NaOH):均为分析纯,北京化工厂产品。
空白水样为Milli-Q超纯水:由美国Millipore Simplicety 185制备;待测试样为北京市内公园、河流地表水、实验室自来水。
具体标准物质信息列于表1。
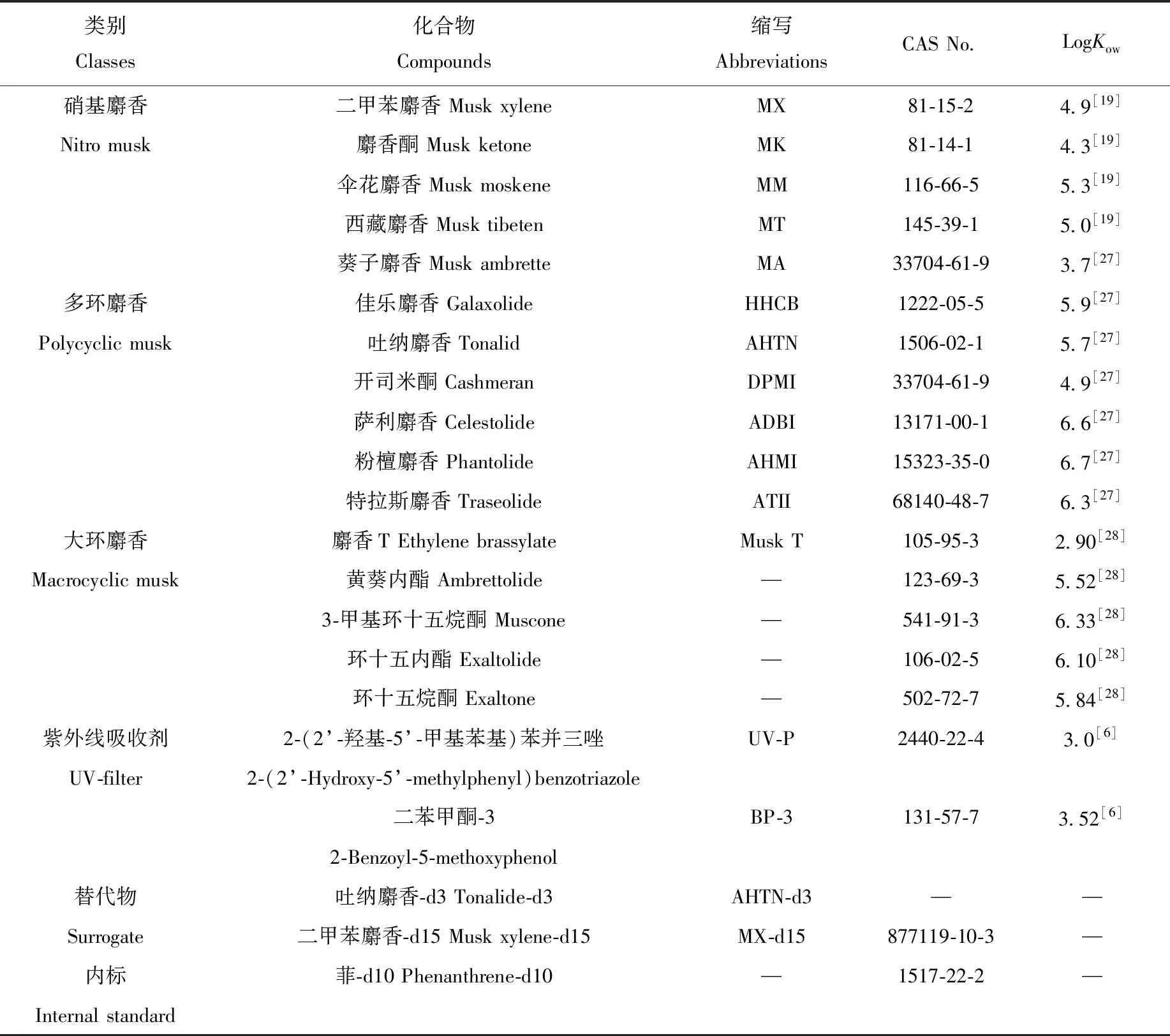
表1 标准物质信息Table 1 Information of reference compounds
1.2 标准溶液的配制
将5种硝基麝香配制成浓度为2.0 mg/L的混合标准储备液;将6种多环麝香配制成浓度为1.6 mg/L的混合标准储备液;将5种大环麝香配制成浓度为5.0 mg/L的混合标准储备液;将紫外线吸收剂配制成浓度为10.0 mg/L的混合标准储备液,均置于4 ℃冰箱中保存。使用时,将待测物配制成500 μg/L的混合标准工作溶液(用甲醇定容并加入适量的丙酮混匀)。采用正己烷将内标菲-d10稀释成1.0 mg/L的标准工作液,备用。替代物为吐纳麝香-d3和二甲苯麝香-d15,用甲醇稀释并加入适量的丙酮混匀,配制成1.0 mg/L的混合工作溶液。
1.3 样品分析
用棕色玻璃瓶采集地表水样品后冷藏保存。分析时,水样经滤纸过滤去除大颗粒杂质,准确量取50 mL水样于三角瓶中,加入50 μL 1.0 mg/L的替代物,混合均匀,待分析。
样品提取:用镊子将PDMS磁力搅拌棒加入50 mL水样中,40 ℃下以950 r/min搅拌萃取4 h。取出搅拌棒,用无尘纸吸水,待下一步解吸。将搅拌棒放入带刻度的锥形试管中,加入0.6 mL乙腈-丙酮萃取液(1∶1,V/V),超声提取20 min,再次加入0.6 mL萃取液,重复解吸10 min,合并提取液,氮气浓缩至约0.2 mL,加入一定浓度的内标物(绝对质量为25 ng)后,用丙酮定容至0.5 mL,进行气相色谱-质谱分析。
1.4 实验条件
1.4.1色谱条件 DB-5MS Ultra Inert毛细管色谱柱(30 m×0.25 mm×0.25 μm);进样口温度250 ℃;载气为氦气,流速1.2 mL/min;不分流进样,进样量1.0 μL;程序升温:初始温度70 ℃,保持1 min,以40 ℃/min升至150 ℃,保持3 min,再以5 ℃/min升至200 ℃,最后以20 ℃/min升至300 ℃,保持5 min。
1.4.2质谱条件 接口温度280 ℃;离子源温度240 ℃;电离方式为电子轰击电离,电离能量70 eV;溶剂延迟5 min。为了提高分析灵敏度,选择化合物的基峰作为定量离子,但大环麝香高丰度的特征离子质量数较小,为了降低背景干扰,选择较高质量数的特征离子作为定量离子,各目标化合物的保留时间及质谱参数列于表2。
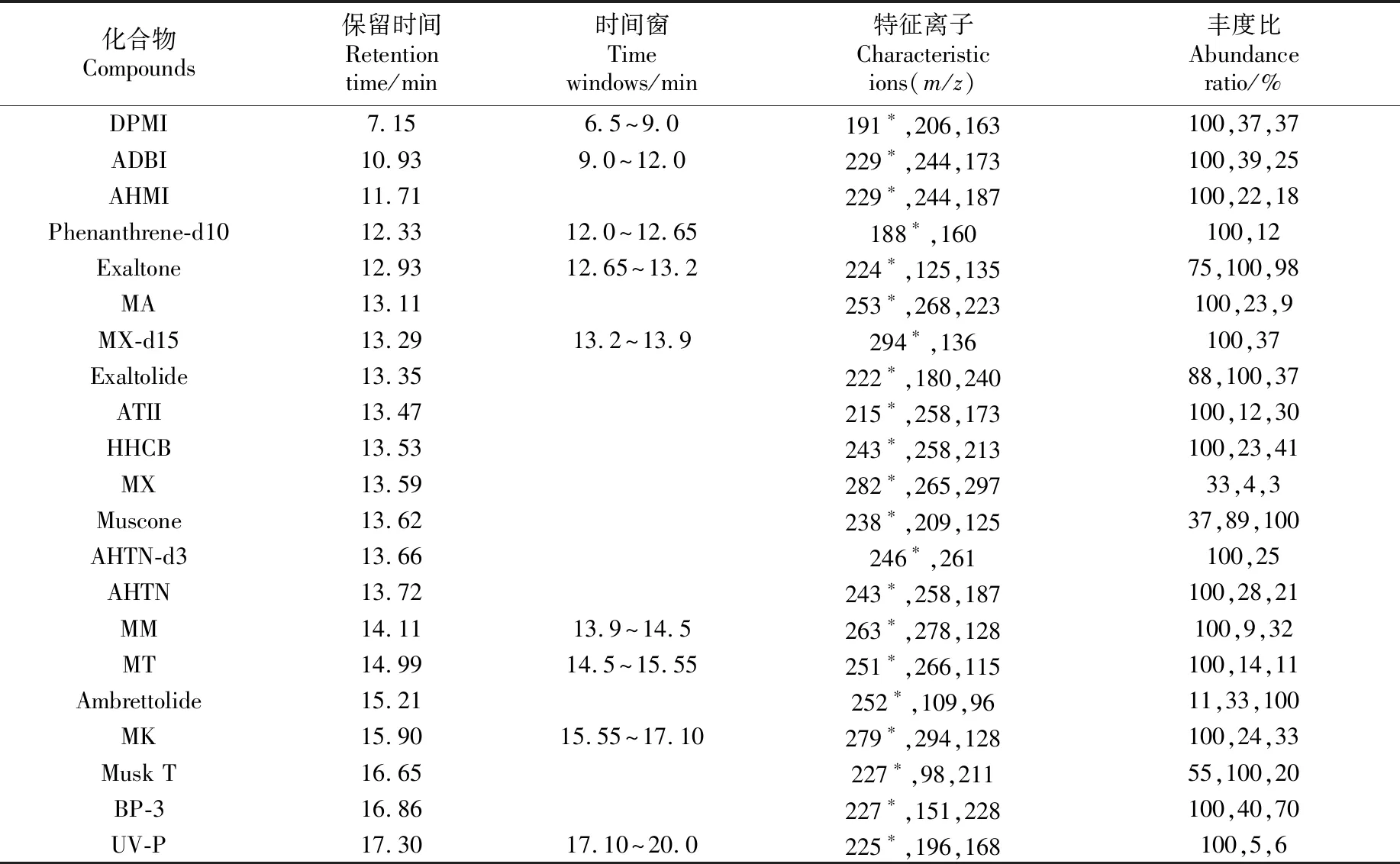
表2 保留时间及质谱参数Table 2 Retention time and parameters of mass spectrometry
注:*为定量离子
2 结果与讨论
2.1 空白实验及质量控制
由于合成麝香和紫外线吸收剂容易受到环境干扰,因此实验前应确保玻璃器皿清洁,避免使用洗涤精等进行清洗,清洗后用溶剂润洗。实验人员应佩戴手套。
PDMS磁力搅拌棒预处理:用乙腈浸泡过夜,再用超纯水清洗3次,确保无目标物残留及其他杂质。样品分析前,采用空白水样进行全流程空白实验,监控测定的质量过程。吐纳麝香-d3和二甲苯麝香-d15的理化性质与待测物相近,在样品提取前加入已知浓度的两种化合物作为替代物用于监控样品的测试过程,2种替代物的回收率应控制在70%~120%之间。菲-d10化合物的性质稳定,保留时间处于20种待测化合物中间,将其选为内标物,可以避免仪器的波动带来测试结果的偏差。
2.2 萃取条件的优化
PDMS作为商业化的搅拌棒涂层,应用范围较广,适用于水中非极性化合物的富集[29]。本实验选用PDMS搅拌棒作为富集材料,并优化了影响富集效率的主要参数。
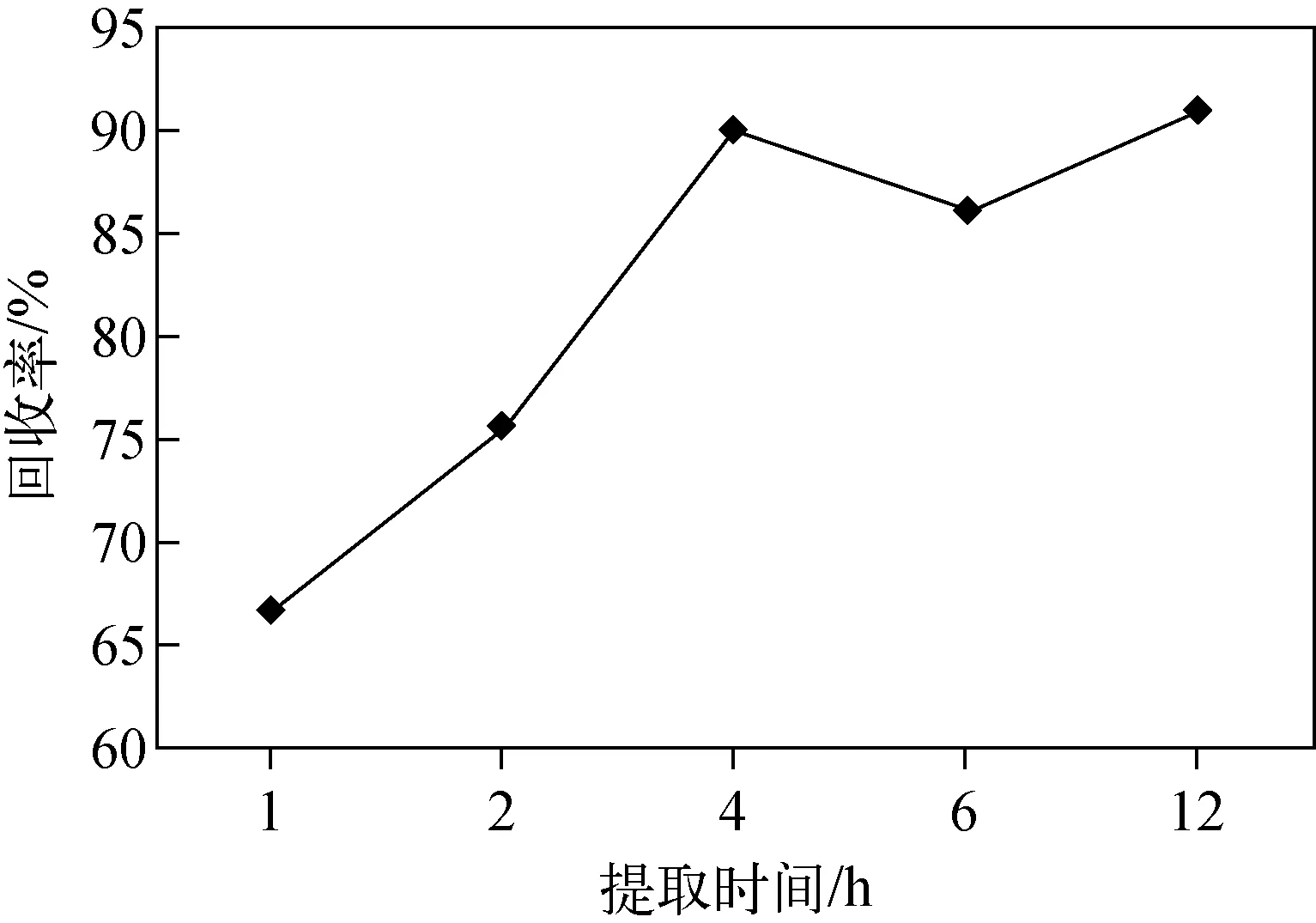
图1 提取时间对目标化合物平均回收率的影响Fig.1 Effect of extraction time on average recovery of target compounds
2.2.1萃取时间、温度及搅拌速度 将搅拌速度设为500 r/min,在室温下,比较了添加样品在1、2、4、6、12 h不同提取时间的提取效果,示于图1。可以看出,提取4 h和12 h时,20种化合物的平均提取回收率较高,因此选择4 h作为提取时间。实验进一步比较了25、40、60 ℃的提取效果,结果表明,提高提取温度有助于目标物的富集,但温度过高会影响PDMS的使用寿命,并降低Kow分配系数[30],因此选择40 ℃作为提取温度。
在40 ℃下,实验比较了500、750、950、1 200 r/min不同搅拌速度提取4 h对添加样品中目标物的富集情况,结果示于图2。由图可见,当搅拌速度为950 r/min时,所有目标分析物的平均回收率最高。

图2 不同转速下,目标化合物的平均提取回收率Fig.2 Average recoveries of target compounds at different rotational speeds
2.2.2离子强度 向水溶液中加入适量的NaCl能够提高溶液的离子强度,并促进目标分析物从水相转移到有机相,可以提高提取效率,但对于logKow<3.5的极性化合物,则会减小提取效率[16]。本实验比较了NaCl含量为0%、5%、10%、20%时目标物的提取回收率,结果示于图3。可以看出,除了BP-3和UV-P,其余大部分化合物在NaCl含量为0%时的提取效果最好。
2.2.3pH值 用2 mol/L盐酸或NaOH调节空白添加水样的pH值,比较pH值为2、7和12时的提取效果,结果示于图4。当pH 12时,musk T、UV-P和BP-3的回收率明显降低,仅为5.2%~11.3%。这是由于大环内脂类化合物musk T在碱性条件易降解,而UV-P和BP-3具有酚羟基基团,碱性条件增大其在水中的溶解度。大部分化合物在pH 2和pH 7时的回收率差别不大,因此选择pH 7作为萃取条件。
2.2.4有机改性剂 加入有机改性剂(甲醇)能够减少目标化合物对玻璃瓶的吸附作用,并提高疏水性化合物的提取回收率[13]。本实验比较了0%、10%、20%、30%不同甲醇含量时添加样品的提取效果,示于图5。可以看出,当甲醇含量为10%时,BP-3、UV-P的提取回收率最高,表明玻璃瓶对含有酚羟基化合物的吸附作用减弱,甲醇含量过高会影响PDMS对目标化合物的吸附作用。对于大部分化合物,不加甲醇时的提取效率最高。因此,选择不添加甲醇进行提取。

图3 不同离子强度对提取效率的影响Fig.3 Effect of ionic strength on extraction efficiency
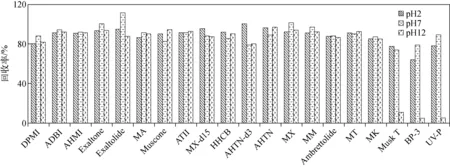
图4 不同pH值条件下的提取效率Fig.4 Extraction efficiency at different pH value
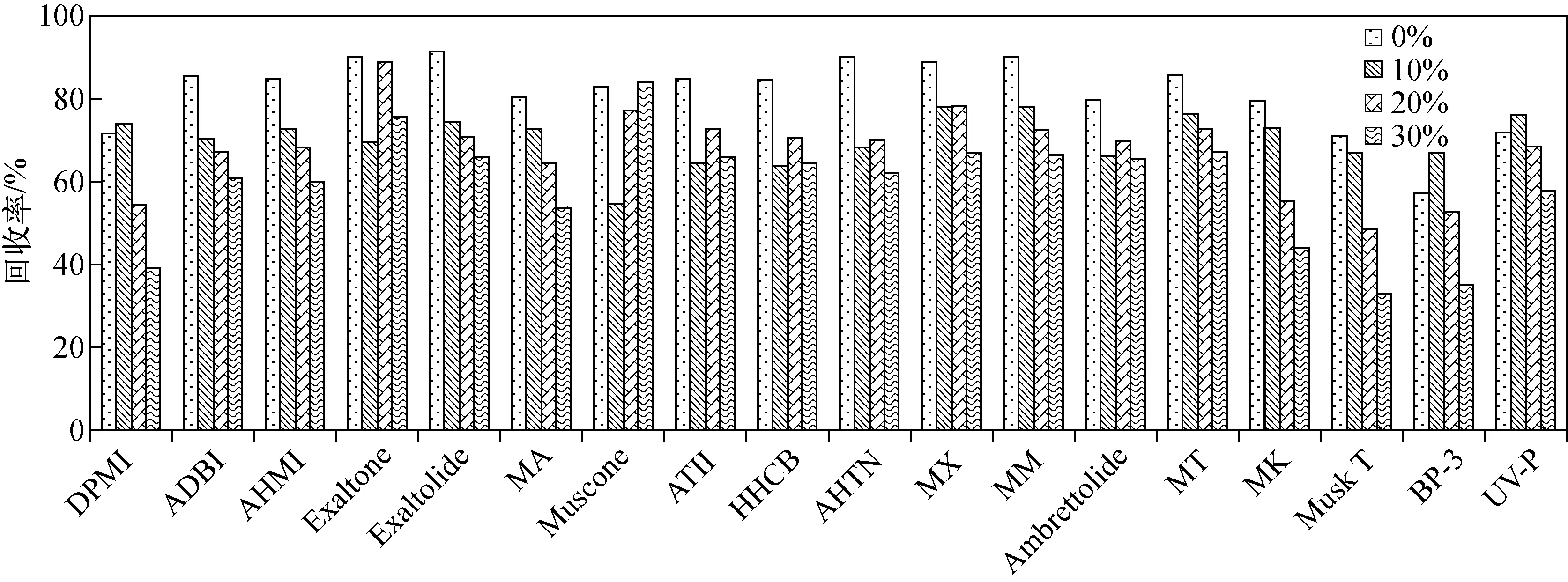
图5 甲醇含量对提取效率的影响Fig.5 Effect of methanol content on extraction efficiency
2.2.5萃取体积 增大样品体积能够降低方法检出限,但同时会延长萃取平衡时间,降低分析效率。在其他条件不变的情况下,本实验比较了样品不同体积对提取回收率的影响。当样品体积为100 mL时,目标化合物的平均回收率为60.9%;样品体积为30 mL和50 mL时,平均回收率在77.6%~81.7%之间,综合考虑,选择样品体积为50 mL进行分析。
2.2.6解吸条件的优化 搅拌棒采用有机溶剂进行解吸,无需热解吸进样装置就能与GC/MS结合进行分析,同时解吸过程有机溶剂用量很少,明显减少了对环境的二次污染。一般选择甲醇、乙腈等[31-32]作为解吸溶剂。由于采用气相色谱进行分离,本实验比较了正己烷、乙腈、乙腈-丙酮(1∶1,V/V)作为解吸溶剂超声萃取2次,每次20 min的萃取效果。当解吸溶剂为正己烷时,平均回收率为73.7%;当解吸溶剂为乙腈-丙酮时,平均回收率为100.2%,且该混合溶剂比乙腈更易浓缩。因此,选择乙腈-丙酮混合体系作为解吸溶剂。当溶剂解吸1次时,搅拌棒上残留的目标物含量在7.6%~19.5%之间,说明解吸不完全,因此选择解吸2次对搅拌棒进行反萃取。解吸时间是影响提取回收率的一个重要参数,本实验比较了不同超声解吸时间对目标化合物回收率的影响,结果示于图6。可以看出,超声时间为(20+10) min时的解吸效果最好,分析搅拌棒溶剂浸泡过夜后的浓缩提取液,未发现残留情况。

图6 溶剂解吸时间对目标化合物回收率的影响Fig.6 Effect of different liquid desorption time on the recovery of target compounds
2.3 方法性能确证
将混合标准工作液用正己烷稀释成不同浓度的溶液,考察方法的线性范围及相关系数。采用空白水样添加的方法考察本方法对待测物的分析精密度,3个添加水平分别为0.05(其中Exaltolide、Muscone和Ambrettolide的最低添加水平为0.1 μg/L)、0.5、1.0 μg/L。添加样品的制备:向50 mL水样中加入一定体积500 μg/L的混合标准工作液和1.0 mg/L的替代物标准工作溶液,混合均匀后待测定。按照1.3节方法进行富集,并重复测定7次,采用内标标准曲线法对目标化合物进行定量分析。根据低浓度添加测定数据,按照EPA推荐方法计算方法检出限(MDL=S×t,S为重复测定的标准偏差,t为T分布检验,查表可得),具体结果列于表3。可见,各化合物的回收率在68.5%~126%之间,相对标准偏差为2.3%~14.9%,方法检出限在0.003~0.038 μg/L之间。
2.4 实际样品分析
为考察方法的适用性,选取自来水样和护城河水样进行基质加标实验,添加水平为1.0 μg/L,按照1.3节步骤操作,分别重复测定2次。18种待测物和2种替代物的回收率范围为:自来水69.8%~96.3%,河水样80.2%~117.8%,表明该方法能够应用于实际样品的分析。应用本方法分析2017年9月北京市内采集的7个地表水样品(编号1~7)和1个自来水样品(编号8),采样点示于图7。检出化合物的结果列于表4。样品的替代物回收率在70.8%~88.6%之间,能够满足分析要求。样品中佳乐麝香的浓度范围在0.003~0.337 μg/L之间,其他可检出的化合物有环十五烷酮和麝香酮,2种紫外线吸收剂均未检出。可以看出,佳乐麝香的检出率最高,而我国已经限用的麝香酮也有检出,表明地表水中该类物质的监控应引起人们的进一步重视。

表3 线性范围、相关系数、相对标准偏差、回收率及检出限Table 3 Linear ranges, correlation coefficients, relative standard deviations (RSDs), spiked recoveries and LODs
注:*添加水平为0.1 μg/L
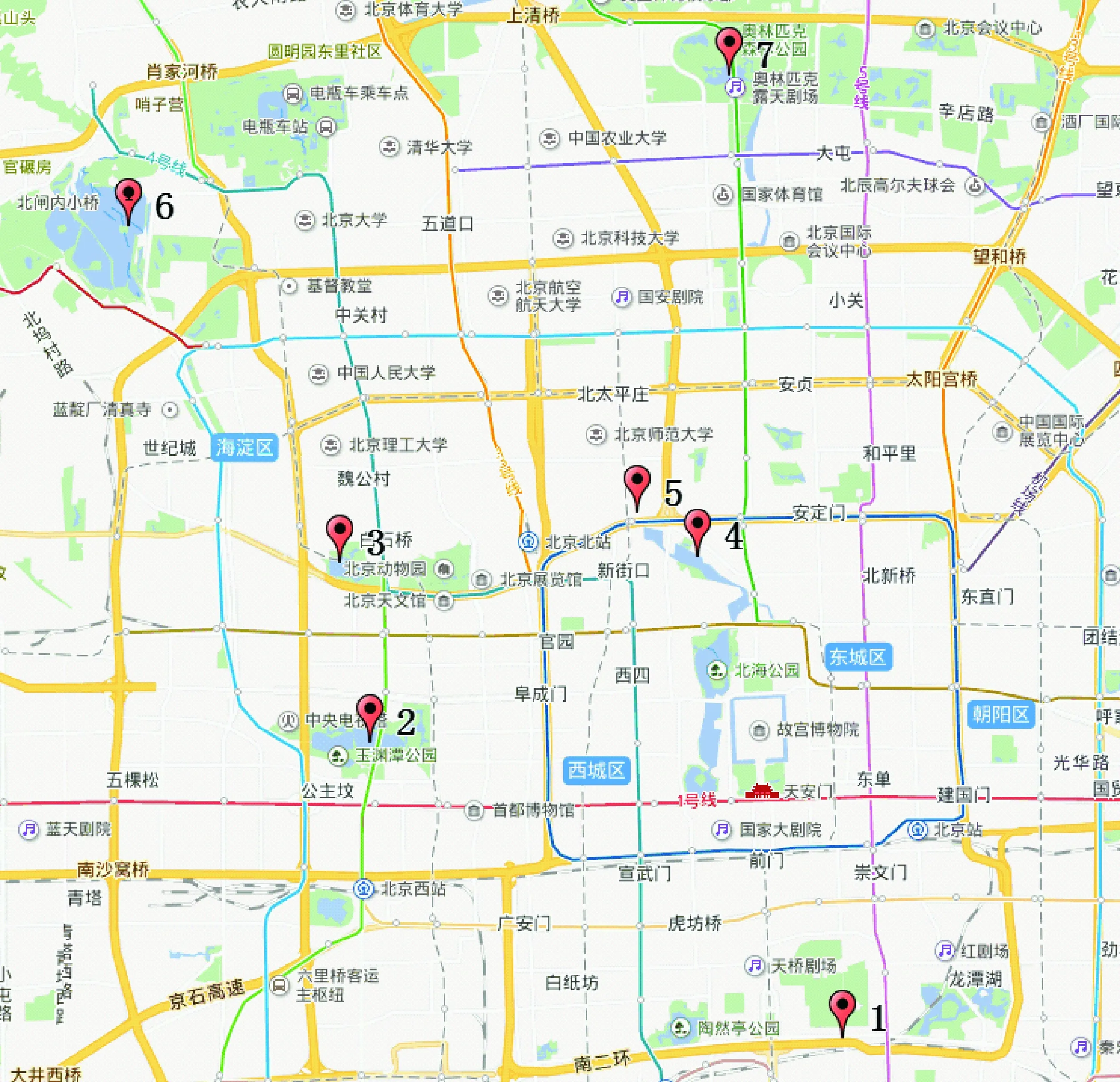
图7 地表水采样分布图Fig.7 Distribution of sampling sites of surface water
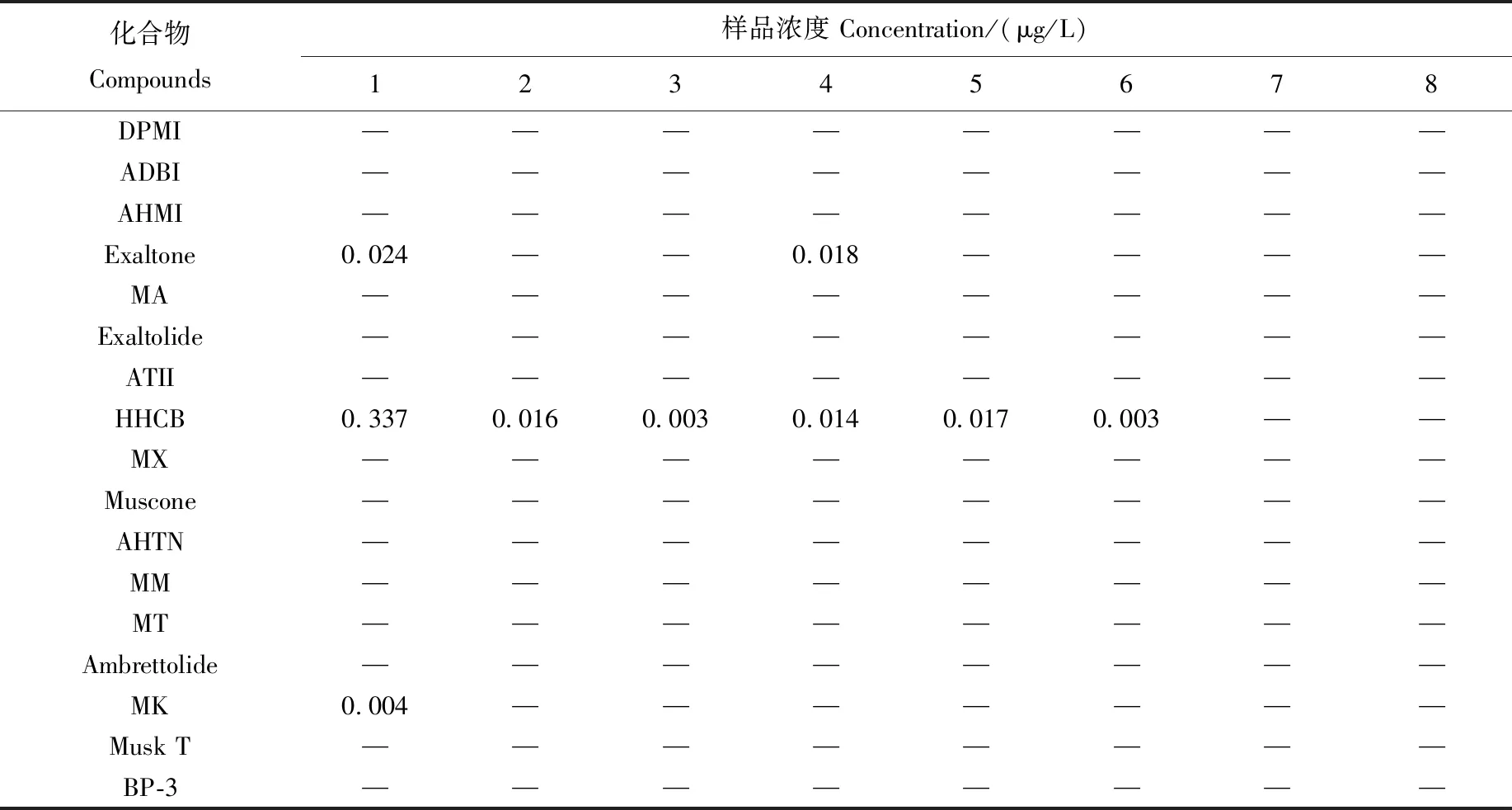
化合物Compounds样品浓度 Concentration/(μg/L)12345678DPMI————————ADBI————————AHMI————————Exaltone0.024——0.018————MA————————Exaltolide————————ATII————————HHCB0.3370.0160.0030.0140.0170.003——MX————————Muscone————————AHTN————————MM————————MT————————Ambrettolide————————MK0.004———————Musk T————————BP-3————————
注:—表示未检出
3 结论
本研究建立了测定地表水中多种合成麝香及2种紫外线吸收剂的快速分析方法。该方法采用PDMS搅拌棒富集地表水中的目标化合物,结合有机溶剂解吸-气相色谱-质谱检测,简化了操作流程,减少了样品用量,提高了分析效率,同时减小了有机溶剂的使用量,达到了绿色环保的目的。该方法适用于地表水中16种合成麝香及2种紫外线吸收剂的同时定量分析。
