弥散加权成像上颅内动脉粥样硬化狭窄致首发缺血性脑卒中不同发病机制的危险因素
2019-06-10郭婷王炎强陆正齐肖成华耿德勤
郭婷 王炎强 陆正齐 肖成华 耿德勤
(1徐州医科大学研究生学院,江苏 徐州 221002;2徐州医科大学附属医院神经内科;3潍坊医学院附属医院神经内科;4中山大学附属第三医院神经内科)
颅内动脉粥样硬化性狭窄(ICAS) 是缺血性脑卒中的最常见病因之一,是世界范围内患病及死亡主要原因之一,尤其在我国,30%~50%脑梗死与超过50%短暂性脑缺血发作与ICAS密切相关〔1,2〕。我们研究证实ICAS致首发缺血性脑卒中发病机制主要包括动脉到动脉栓塞(A-A)、穿支动脉闭塞(LBO)、低灌注(HI)、原位血栓形成(STO)、多发机制〔3~5〕。本研究探讨弥散加权成像上分析ICAS致首发缺血性脑卒中不同发病机制的危险因素。
1 对象与方法
1.1研究对象 2012年9月至2015年9月就诊于涂州医科大学附属医院神经内科ICAS致首发缺血性脑卒中患者283例,年龄33~94岁,平均年龄(65.72±12.41)岁,其中男161例,女122例;≥64岁178例。并符合以下条件:①年龄≥18岁,②病程<7 d,③符合中国急性缺血性脑卒中(ACI)诊治指南诊断标准,经颅脑弥散加权成像(DWI)和磁共振血管成像(MRA)和(或)CT血管造影(CTA)证实ACI诊断明确〔6〕;④据TOAST分型,脑梗死病因考虑为大动脉粥样硬化〔7〕。排除标准〔6~10〕:①DWI显示与临床表现不相符的急性梗死灶及DWI显示的梗死病灶不在同侧颅内动脉供血区患者;②无脑血管狭窄的缺血性脑卒中及有颅内、外动脉狭窄的缺血性脑卒中、静脉梗死患者;③应用降脂药物超过1个月及溶栓或血管内介入治疗患者;④心源性相关的脑卒中包括近期心肌梗死(<4 w)、心房颤动、人工瓣膜、扩张型心肌病、心脏瓣膜病变、左心耳血栓形成、左心室附壁血栓及室壁瘤、心房黏液瘤、感染性心内膜炎、升主动脉或主动脉弓近端动脉粥样硬化患者;⑤ 动脉夹层、烟雾病、风湿免疫病、恶性肿瘤、外伤、凝血功能障碍或血液系统疾病患者,⑥其他原因导致的脑卒中样发作及无法明确病因患者;⑦皮质下病灶DWI上直径是小于15 mm患者,⑧各种腔隙综合征患者,⑨双侧前循环或前后循环均有梗死病变患者;⑩检查及资料记录不全患者。
1.2方法
1.2.1ICAS的判定 依据头颅MRA检查,采用华法林阿司匹林治疗症状性颅内疾病(WASID) 研究中标准计算,狭窄率=(1-狭窄直径/正常直径)×100%,只有狭窄≥50%或闭塞者纳入研究。颅内动脉包括大脑前动脉(ACA),大脑中动脉(MCA),大脑后动脉(PCA),基底动脉(BA),椎动脉远端(distal VA),包括硬膜内V4段,颈内动脉远端(distal ICA),包括海绵状与岩段。前循环(ACV),包括ACA、MCA、脉络膜前动脉等;后循环(PCV),包括PCA、BA的旋支、椎动脉、小脑动脉等〔3~5〕。
1.2.2脑卒中机制 根据DWI 、MRA或CTA血管造影分为A-A组、LBO组、HI组、STO组、多发机制组包括A-A+LBO,A-A+HI,A-A+LBO+HI〔3~5〕。
1.2.3危险因素收集 包括人口学(年龄、性别);生活习惯(吸烟、饮酒);既往病史〔糖尿病、高脂血症、高血压、代谢综合征、高同型半胱氨酸血症(HHcy)、周围动脉病〕;血清学指标,包括血脂、糖化血红蛋白、血尿酸、血Hcy、C反应蛋白(CRP)等;磁共振成像(MRI)、MRA、DWI、CTA、颈部血管超声、心脏超声等〔8~12〕。
1.3统计分析方法 采用SPSS17.0软件进行方差分析及χ2检验。
2 结 果
2.1发病机制及其危险因素 机制:LBO 67例(23.67%),多发机制93例(32.86%),A-A 116例(40.99%)。多发机制包括A-A+LBO 57例(61.29%),A-A+HI 26例(27.30%),A-A+LBO+HI 10例(11.41%),STO组和HI组分别只有3及4例(1.06%、1.41%)。三组发病机制中高血压病史,差异有统计学意义(P<0.01);AA组与LBO组比较差异有统计学意义(P<0.01),AA组与多发机制组比较差异有统计学意义(P<0.01)。见表1,图1。

表1 缺血性脑卒中不同发病机制危险因素的比较〔n(%)〕
1):3组比较;2):A-A组与LBO组比较,3):A-A组与多发机制组比较;4):LBO组与多发机制组比较,下表同

图1 ICAS致首发缺血性脑卒中不同发病机制颅脑DWI影像学表现
2.2血清学指标比较 LBO、多发机制、A-A三组中总胆固醇(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)、载脂蛋白(Apo)A-1、脂蛋白(LP)(a)、尿酸(UA)、TRIG/HDL-C、TC/ HDL-C、LDL-C/HDL-C、CRP、Hcy、糖化血红蛋白比较,差异无统计学意义;ApoB与ApoB/ApoA-1相比,差异有统计学意义(P<0.05)。LBO、A-A两组机制ApoB与ApoB/ApoA-1均明显低于多发机制组(P<0.05),见表2。
2.3受累血管部位比较 LBO、多发机制、A-A三组中受累血管部位distal ICA、MCA、ACA、PCA、BA、distal VA、ACV、PCV、前后循环(APCV)、单血管受累组间比较,差异无统计学意义(P>0.05);而2支及以上血管受累,差异有统计学意义(P<0.05)。LBO、A-A两组机制2支及以上血管受累均明显低于多发机制组(P<0.05),见表3。

表2 缺血性脑卒中不同发病机制血清学检测指标的比较
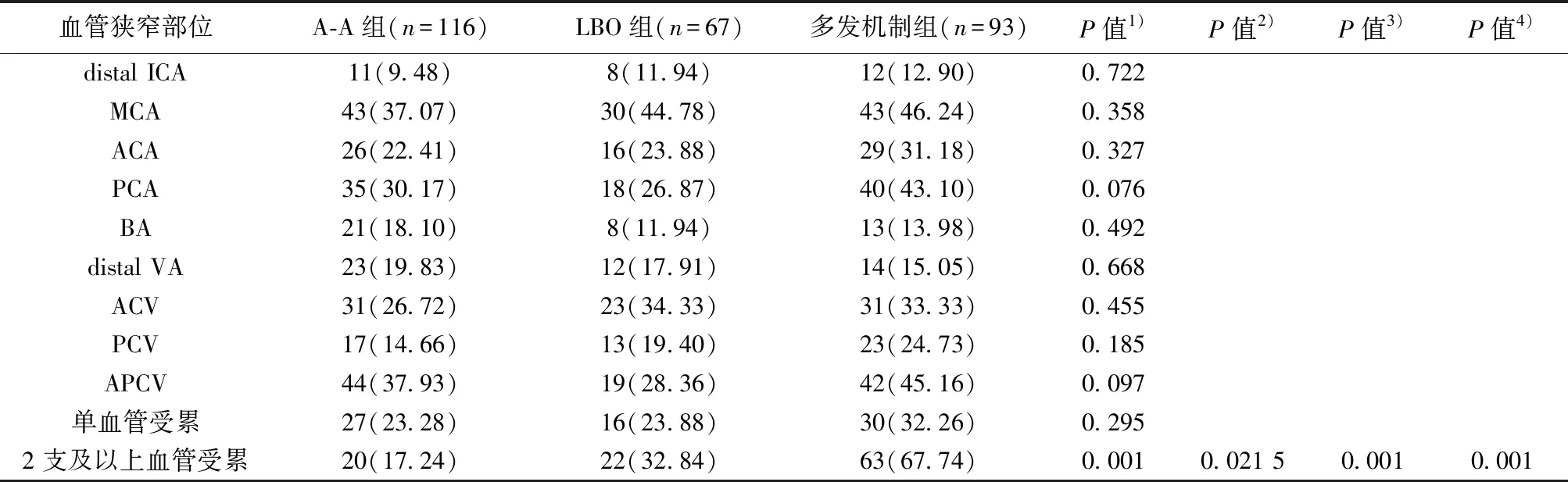
表3 缺血性脑卒中不同发病机制受累血管部位的比较〔n(%)〕
3 讨 论
ICAS致首发缺血性脑卒中不同发病机制的确定,有利于缺血性脑卒中诊治策略的选择,而其危险因素的明确有利于不同卒中机制的防控及干预。本研剔除常见如心源性因素、动脉夹层、烟雾病、血管畸形、血管炎等非动脉粥样硬化性疾病,以DWI、MRA或CTA血管造影评判脑卒中机制及ICAS病变,探讨不同机制的危险因素。
本研究结果提示对常见危险因素进行分层分析干预仍是不同脑卒中机制的主要防控基础。这与既往研究报道吸烟、高血压、糖尿病、代谢综合征与ICAS密切相关基本一致〔13,14〕。此外MCA、前后循环、PCA、多血管床是常见受累部位血管,这与Kim等〔5〕报道ICAS致A-A主要与远端ICA、前循环、远端BA、MCA及ICAS致LBO与基底动脉、PCA、后循环;ICAS致多发机制与远端ICA、前循环、后循环不一致,考虑与纳入患者年龄、病例选择纳入、排除标准等因素相关。
本研究证实ApoB/ApoA-I是ICAS的标志物,反应了胆固醇转运平衡动态变化,本研究也支持这一观点,随着ApoB与ApoB/ApoA-I升高,加重了动脉硬化及脂质沉积,诱发炎性因子聚集及炎症反应,促进ICAS进展,进而导致血流动力的改变;与多血管床狭窄互为因果,互相促进,导致ICAS致缺血性脑卒中单一机制向多发机制的演变〔8,15~17〕。
综上所述,ICAS致首发缺血性脑卒中患者中高血压病史、吸烟、糖尿病史、代谢综合征病史是不同脑卒中机制常见主要危险因素,代谢性因素促进不同脑卒中机制的发展,MCA、多血管床、前后循环、PCA是主要受累血管。ApoB、ApoB/ApoA-I与多血管床受累是促进单一向多发机制演变主要危险因素,动态监测其变化有助于预测ICAS致首发缺血性脑卒中的发病机制。由于本研究存在的某些局限性,如回顾性研究、样本量偏小、单中心、男性患者偏多、DSA检查群体不普遍、未采用高分辨磁共振观察动脉斑块状况,可能引起研究结果的偏倚,因此基于DWI对ICAS致首发缺血性脑卒中不同发病机制的危险因素分析仍期待更全面的研究。
