基于PRIME HLB快速前处理技术的鸡蛋中38种药物残留快速检测方法研究及其在风险监测中的应用
2019-06-06尹伶灵杨修镇李有志牛华星刘少宁陈玲
尹伶灵,杨修镇,李有志,牛华星,刘少宁,陈玲
(山东省兽药质量检验所,山东省畜产品质量安全监测与风险评估重点实验室,济南 250022)
鸡蛋富含优质蛋白以及丰富的维生素和矿物质,是日常生活不可或缺的一种健康食品。由于不合理使用和滥用兽药以及不遵守休药期等原因,致使鸡蛋中的各种药物残留(母体化合物和代谢物)频频检出,其产生的危害不可忽视[1]。因此,鸡蛋中的兽药残留越来越引起人们的广泛关注。目前国内外现有的鸡蛋中多残留检测方法主要采用液相色谱串联质谱法[2-10],存在检测药物的种类单一,前处理方法复杂,灵敏度低等缺点。本文选取了日常检测中风险比较高的β-内酰胺类、抗病毒类、大环内酯类、喹诺酮类、四环素类、林可胺类、磺胺类、氯霉素类和氟虫腈及其代谢物共 9大类38种药物,结合PRIME HLB快速通过式前处理技术,研究建立了超高效液相色谱串联质谱同时测定方法。该方法简单快速、灵敏度高、准确性好,适用于大批量鸡蛋样品的高通量快速定性定量检测,为鸡蛋样品的风险监测提供了有力的技术手段。将该方法应用于200批鸡蛋风险监测样品的检测,共检出阳性样品10批,阳性药物有磺胺间甲氧嘧啶、磺胺甲噁唑、多西环素、替米考星、氧氟沙星、诺氟沙星、氟苯尼考,并将阳性样品通过国标方法进行复检,结果吻合,进一步证明了该方法的准确性。
1 材料与方法
1.1 仪器与试剂 Waters Xevo TQ-S高效液相-串联质谱仪(美国Waters公司),配有电喷雾电离接口(ESI)及Masslynx数据处理系统; BT125D电子天平(感量0.01 g、 0.00001 g, 德国赛多利斯公司); Allegra64R台式高速冷冻离心机(美国贝克曼公司); XW-80A涡旋混合器(上海精科实业有限公司); HY-4调速多用振荡器(北京踏锦科技有限公司); MilliPAK纯水器(Millpore公司); Oasis PRiME HLB固相萃取柱(美国Waters公司)。
对照品:阿莫西林(德国Dr. Ehrenstorfer公司,批号:00907),氨苄西林(德国Dr. Ehrenstorfer公司,批号:21108),头孢氨苄(中国食品药品检定研究院,批号:130408-201411),头孢喹肟(中国兽医药品监察所,批号:K0320906),头孢噻呋(中国兽医药品监察所,批号:K0331408),金刚烷胺(上海安普科学仪器有限公司,批号:A0309578),泰乐菌素(中国兽医药品监察所,批号:K0161305),替米考星(中国兽医药品监察所,批号:K0311407),红霉素(中国兽医药品监察所,批号:K40528),恩诺沙星(中国兽医药品监察所,批号:H0081206),环丙沙星(中国食品药品检定研究院,批号:130451-201203),沙拉沙星(中国兽医药品监察所,批号:H0181108),达氟沙星(中国兽医药品监察所,批号:H0201210),氧氟沙星(中国食品药品检定研究院,批号:130454-201206),培氟沙星(中国食品药品检定研究院,批号:130459-201402),诺氟沙星(中国兽医药品监察所,批号:H0071305),洛美沙星(中国兽医药品监察所,批号:H0121505),噁喹酸(德国Dr. Ehrenstorfer公司,批号:G142374),土霉素(中国兽医药品监察所,批号:K0031208),金霉素(中国兽医药品监察所,批号:0041110),四环素(中国兽医药品监察所,批号:0011209),多西环素(中国兽医药品监察所,批号:0131209),林可霉素(中国兽医药品监察所,批号:0101503),磺胺间甲氧嘧啶(中国兽医药品监察所,批号:C0031610),磺胺二甲嘧啶(中国兽医药品监察所,批号:C0061007),磺胺甲噁唑(中国兽医药品监察所,批号:H0261106),磺胺二甲氧嘧啶(中国兽医药品监察所,批号:H0371406),磺胺喹噁啉(中国兽医药品监察所,批号:H0251407),磺胺氯吡嗪钠(农业部环境保护科研检测所,批号:SB06-087-2008),磺胺氯达嗪钠(农业部环境保护科研检测所,批号:SB05-083-2008),氯霉素(中国兽医药品监察所,批号:K0320906),氟苯尼考(中国兽医药品监察所,批号:K0320906),氟苯尼考胺(中国兽医药品监察所,批号:K0320906),甲砜霉素(中国兽医药品监察所,批号:K0320906),氟虫腈(美国A Chemtek. Inc.公司,批号:S880057),氟甲腈(美国A Chemtek. Inc.公司,批号:S008833),氟虫腈砜(美国A Chemtek. Inc.公司,批号:S011903),氟虫腈硫醚(美国A Chemtek. Inc.公司,批号:S008647)。
乙腈(色谱纯, 德国Merck公司),甲醇 (色谱纯, 德国Merck公司);甲酸(色谱纯,美国Sigma-Aldrich公司);水为超纯水(自制);乙二胺四乙酸钠(EDTA)(分析纯, 上海国药集团化学试剂有限公司)。
1.2 标准溶液配制
1.2.1 标准储备液 分别精密量取浓度为1000 μg/mL的氟虫腈和氟虫腈砜各1.00 mL,置于10 mL棕色容量瓶中,用甲醇溶解并定容至刻度,标准储备液浓度为100 μg/mL;分别精密称取0.01 g(精确至0.1 mg)标准品置于10 mL棕色容量瓶中,用甲醇溶解并定容至刻度,标准储备液浓度为1 mg/mL,-20 ℃冰箱保存。
1.2.2 混合标准工作溶液 将各标准储备溶液稀释,配成混合标准工作液,各组分浓度为10 mg/L。
1.3 实验方法 取5枚鸡蛋混合均匀,称取(2.00±0.02) g混匀的蛋液置于50 mL离心管内,加入2 mL 0.02 mol/L EDTA溶液,涡旋1 min。再加入乙腈8 mL,漩涡震荡提取1 min,超声波萃取10 min,5000 r/min高速离心5 min,取5 ml上清液直接加载到6cc规格PRiME HLB固相萃取柱,无需活化和平衡,保持一秒一滴的流速,收集全部流出液,在40 ℃下氮气吹至近干,残留液体用20%甲醇水溶液定容至1.00 mL,过0.2 μm微孔滤膜,上LC-MS/MS测试。
1.4 液相色谱条件 色谱柱为BEH C18(100 mm×2.1 mm,1.7 μm), 流动相:正离子模式下,流动相A:甲醇;流动相B:0.1%甲酸水;负离子模式下:流动相A:甲醇;流动相B:水。流速:0.2 mL/min;进样量:1 μL;柱温: 35 ℃。液相色谱梯度洗脱程序见表1。
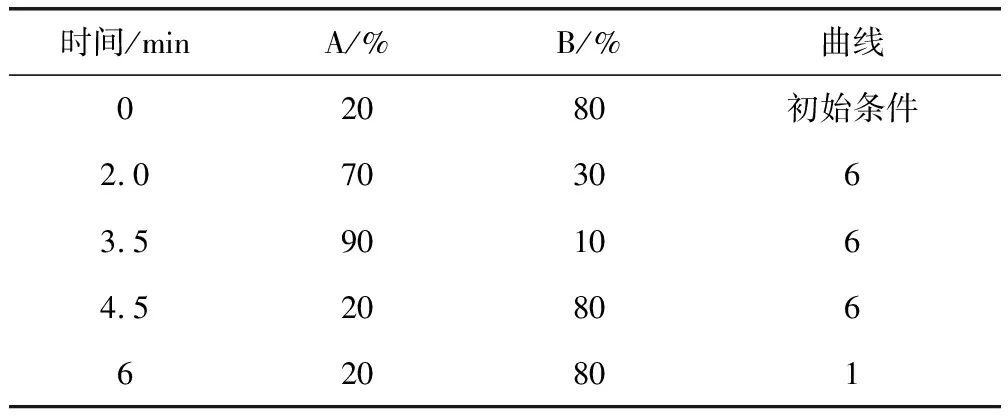
表1 液相色谱梯度洗脱程序Tab 1 HPLC gradient elution program
1.5 质谱条件 电喷雾离子源;多反应监测(MRM);离子源温度:150 ℃;脱溶剂温度:400 ℃;脱溶剂氮气流速:900 L/h;毛细管电压:3 kV。所选择的母离子、子离子、锥空电压和碰撞能量等参数见表2。

表2 38种兽药的MRM离子测定参数表Tab 2 Table of MRM ion monitor parameters of the 38 veterinary drugs
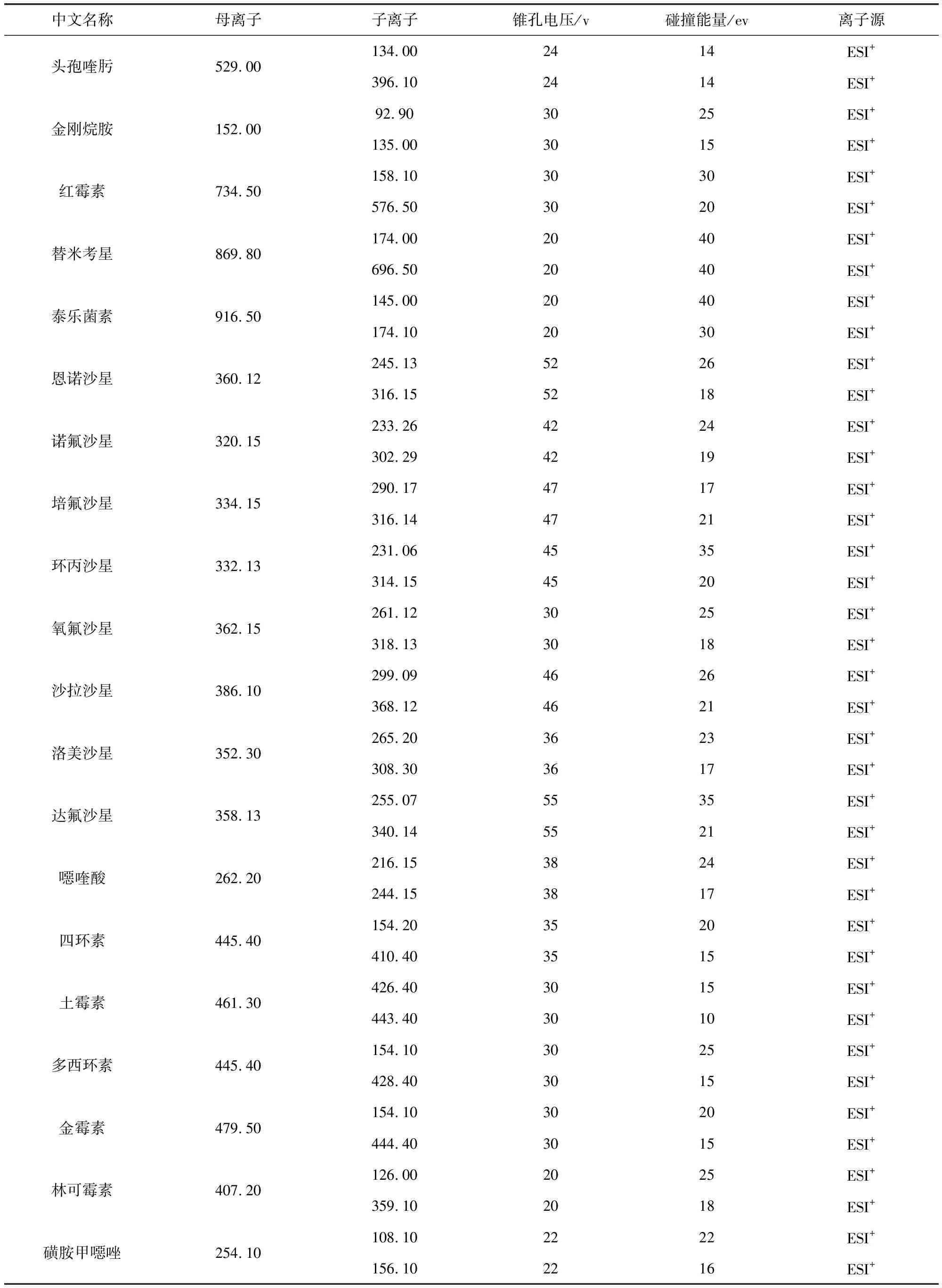
续表
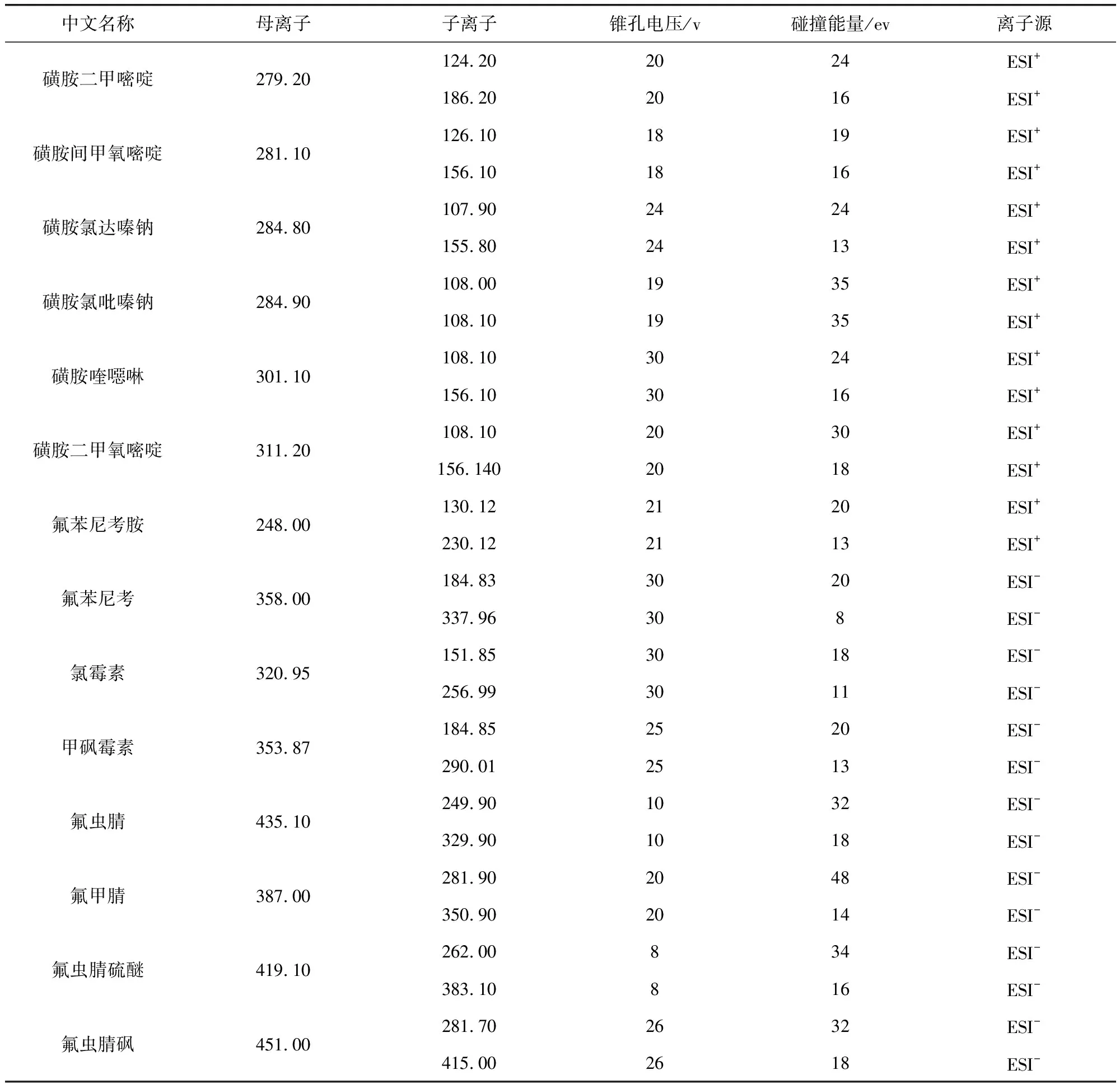
续表
2 结果与分析
2.1 方法的回收率、精密度、检出限和定量限 为降低基质效应, 采用空白基质匹配标准溶液进行定量,将鸡蛋的提取液作为基质本底液。在上述确定的优化条件下,在鸡蛋空白样品中准确加入混合标准溶液,采用基质匹配标样进行定量,考察方法回收率、相对标准偏差、检出限(信噪比S/N=3)和定量限(信噪比S/N=10)。在鸡蛋样品中加入浓度为定量限、2倍定量限、5倍定量限的3个浓度的标准品,按上述方法对样品进行检测,每个浓度做6个平行样品,38种目标分析物的各效能指标验证结果如表3所示。从表3可以看出,38种待测物的加标回收率为71.4%~108.2%,方法的相对标准偏差(RSD)为0.7%~8.1%。可见,该方法精密度良好,检出限和回收率均能够满足多残留样品检测的相关要求。

表3 鸡蛋中38种药物残留的检出限、定量限、平均加标回收率及RSD(n=6)Tab 3 LODs, LOQs, average recoveries, and RSDs of the 38 veterinary drugs in eggs ( n=6)
2.2 实际样品的测定 该方法用于检测200批鸡蛋样品(采集自山东省各地市超市和农贸市场),共检出阳性样品10批,其中磺胺间甲氧嘧啶(0.57 μg/kg)、磺胺甲噁唑(1.20 μg/kg)、多西环素(两批分别为4.33、22.31 μg/kg)、替米考星(两批分别为8.93、6.46 μg/kg)、氧氟沙星(1.84 μg/kg)、诺氟沙星(7.53 μg/kg)、氟苯尼考(两批分别为1.0、11.2 μg/kg),并将阳性样品通过国标方法进行复检,结果吻合,进一步证明了该方法的准确性(典型阳性样品的多反应监测色谱图见图1)。

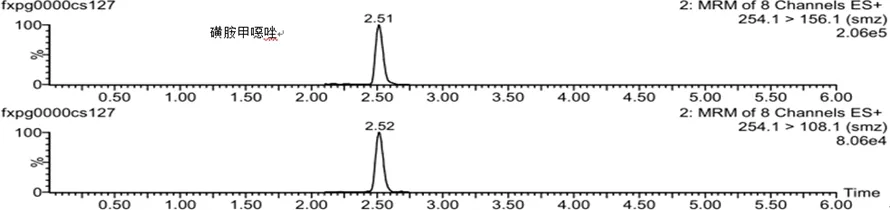
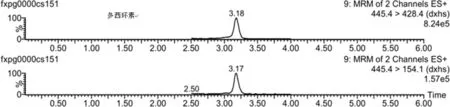

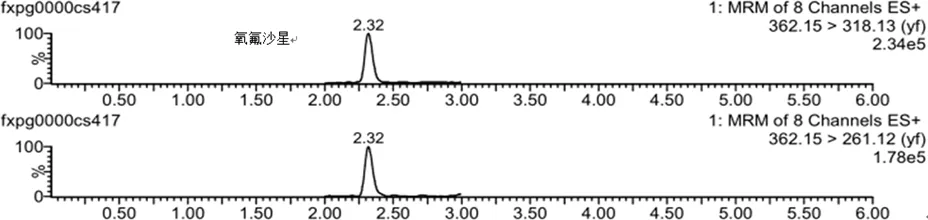

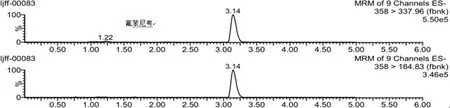
图1 典型阳性样品的多反应监测色谱图Fig 1 MRM chromatogram of typical positive sample
3 讨论与结论
3.1 色谱条件的优化 本试验选用 Waters Acquity UPLC BEH C18(2.1 mm × 100 mm ×1.7 μm)色谱柱分离9类兽药,此色谱柱对各化合物具有较强的保留,各色谱峰峰形较好,并可以得到有效的分离,减少了杂质的干扰。本试验用甲醇作为强洗脱流动相,在流动相中加入甲酸能增加各种化合物在 ESI+模式下的离子化效率,改善各化合物的峰形。本试验分别配制0.05%、0.1%和0.2%甲酸水溶液作为流动相,结果表明,0.1%甲酸水溶液体系能提供最佳的离子化条件,峰面积信号最强,灵敏度最高。在 ESI-模式下,用纯甲醇和纯水作为流动相。
3.2 质谱条件的优化 在电喷雾质谱模式下,分别对毛细管电压、锥孔电压、碰撞能量和选择离子等进行了充分的优化,选取经碰撞后所得丰度较高的2个子离子作为定量和定性离子,并确定其最佳碰撞能量的电压值。依据子离子相对丰度比(定性离子/定量离子)和化合物保留时间进行定性。理论上,MRM 采集模式可以同时对数十种化合物进行定量分析。然而,同时测定的化合物数目越多,MRM 离子对通道也越多,分配给每个 MRM 离子对通道的驻留时间越短,而离子驻留时间对检测的灵敏度和准确定量有较大影响。为了提供较高的检测灵敏度和确保定量的准确性,本文采用动态多反应监测模式进行数据的采集,在该采集方式下,MRM 离子对通道根据设定好的目标物保留时间及相应的时间窗口进行有针对性的采集,而不在此保留时间段内的药物离子对不予采集,使采集效率得到极大提高。
3.3 样品前处理方法的优化 分别提取这9类化合物的方法已有许多报道[2-10],但都不完全适用于这9类化合物的同时提取和净化。由于这9类药物多易溶于甲醇、乙腈等极性溶剂,本研究分别考察了90%甲醇水溶液,80%甲醇水溶液,90%乙腈水溶液,80%乙腈水溶液。实验证明, 乙腈的提取回收率和沉淀蛋白的效果好, 且重复性较好, 因而选用乙腈作为提取溶剂。通过考察90%乙腈水溶液,80%乙腈水溶液,发现除四环素类药物和氟喹诺酮类药物外,其他大部分药物采用80%乙腈水溶液提取净化后的回收率最高,稳定性最好。根据文献[9-10],把提取液中所含的20%的水,用0.02 mol/L EDTA溶液来替代,发现大大提高了四环素和氟喹诺酮类药物的回收率,其他7类药物的提取回收率不受影响。
样品净化,本文采用的是Waters公司的Oasis PRiME HLB固相萃取小柱,与目前常用的净化方法C18固相萃取小柱相比,它是简单的通过式净化处理,无需任何活化和平衡,直接上样, 简化了实验步骤, 减少了有机溶剂的使用量,使得样品净化过程简单、快速、有效[11-13]。PRiME HLB 固相萃取柱是基于 HLB 填料进行的升级产品,属于反相保留机理,对于脂肪、磷脂、色素具有很好的吸附作用,可以有效去除蛋白、盐、磷脂等 95%以上的基质干扰物。本研究采用超高效液相色谱-串联质谱法(UPLC-MS/MS),结合PRIME HLB快速通过式净化方法,建立了同时提取、动态多反应监测(DMRM)同时测定β-内酰胺类、抗病毒类、大环内酯类、喹诺酮类、四环素类、林可胺类、磺胺类、氯霉素类和氟虫腈及其代谢物共 9 类 38种药物残留的新方法。该方法大大简化了前处理步骤、缩短了前处理时间、减少了溶剂用量, 同时质控样品回收率达到分析要求,结果准确可靠,适用于大批量鸡蛋样品的快速定性定量检测。
