顶空气相色谱法测定15 种中药材、 中药饮片中磷化铝残留量
2019-06-01曹依敏
周 恒, 苗 水, 陈 铭, 兰 岚, 曹依敏, 季 申
(上海市食品药品检验所, 上海 201203)
磷化铝是国内外粮食贮藏中普遍使用的高效杀虫剂,近年来也广泛应用于部分中药材仓库贮存[1-3], 它遇水或酸可产生磷化氢, 是杀虫有效成分, 对霉菌也有抑制作用,但其属于剧毒易燃气体, 穿透性强, 易挥散, 在磷化铝熏蒸过程中如处理不当会造成严重后果, 如引起人体中枢神经损害, 心、 肝、 肾等重要器官衰竭等[4-5]。 磷化铝用于中药材熏蒸防虫防霉时, 其残留安全性缺乏系统研究, 检测手段也较匮乏, 可能会对中药材安全造成较大影响。
目前, 磷化铝尚无直接检测的方法, 通常是将其转化成磷化氢后再进行测定, 主要有钼蓝比色法、 滴定法、 离子色谱法等[6-8], 但这些方法的前处理操作均较复杂, 灵敏度相对较低, 并且需要较大取样量。 近几年来, 有文献报道顶空气相色谱法应用于烟草、 水果等基质中磷化氢的检测, 但由于前处理方法为固态测定法, 仅适合磷化氢, 不能完整体现磷化铝残留水平[9-12], 同时中药材中磷化铝残留分析的研究仍十分有限[13]。 因此, 本实验拟建立顶空气相色谱法测定15 种中药材、 中药饮片中磷化铝残留量, 并通过残留数据积累科学评价该成分熏蒸对中药安全性的影响。
1 材料
1.1 仪器 Agilent 7890A 气相色谱仪 (美国Agilent 公司), 配置火焰光度检测器; CTC 进样系统(瑞士CTC 公司); Milli-Q 超 纯 水 仪 (美 国 Millipore 公 司); Mini Vortexer 涡旋仪(美国Thermo Fisher Scientific 公司); 10、25、 50、 100、 250、 500 μL 气密针(瑞士Hamilton 公司);Tedlar 气体采样袋(美国SKC 公司)。
1.2 试药 硫酸(纯度98%)、 盐酸(含氯化氢36% ~38%) 为分析纯(国药集团化学试剂有限公司); 磷酸(纯度85%) 为分析纯(上海凌峰化学试剂有限公司); 去离子水(美国Millipore 公司); 标准磷化氢气体由德国Linde 公司提供(75 mL/m3磷化氢/氮气混合气, 磷化氢含有量108.126 μg/L)。 15 种中药材、 中药饮片为上海市场抽检样品, 经上海市食品药品检验所杨新华主管药师鉴定为正品, 具体见表1。

表1 中药材、 中药饮片基本信息
2 方法与结果
2.1 对照品溶液制备 精密吸取5% 硫酸10 mL, 置于20 mL顶空进样瓶中, 迅速密封。 将标准磷化氢气体填充至Tedlar 气体采样袋, 气密针精密吸取5、 10、 20、 50、 100、200 μL (分别约相当于0.5、 1、 2、 5、 10、 20 ng), 注入顶空进样瓶中, 涡旋10 s, 即得。
2.2 供试品溶液制备 精密称取样品细粉(过3 号筛) 约0.5 g, 置于20 mL 顶空进样瓶中, 精密加入5% 硫酸10 mL, 迅速密封, 涡旋10 s, 即得。
2.3 色谱条件 Agilent PoraPLOT/Q 色谱柱 (25 m×0.53 mm×20 μm), 配置火焰光度检测器、 磷滤光片; 检测器温度250 ℃; 升温程序为初始50 ℃保持12.5 min,30 ℃/min 升至200 ℃保持2 min; 进样口温度220 ℃, 不分流进样; 载气氦气, 体积流量5.0 mL/min; 顶空进样,采用气密针模式(温度70 ℃); 进样体积500 μL; 顶空瓶平衡温度65 ℃, 平衡时间20 min。 色谱图见图1。
2.4 方法学考察
2.4.1 线性关系考察 精密吸取“2.1” 项下对照品溶液各500 μL, 注入气相色谱仪, 在“2.3” 项色谱条件下进样测定。 以进样量为横坐标(X), 峰面积为纵坐标(Y)进行回归, 得方程为Y= 348.157 75X-145.287 41 (r =0.999 74), 在0.5~20 ng 范围内呈良好的线性关系。
2.4.2 精密度试验 精密量取5%硫酸10 mL, 置于20 mL顶空进样瓶中, 迅速密封, 气密针精密吸取标准磷化氢气体100 μL (约相当于10 ng), 注入顶空进样瓶中, 涡旋10 s, 平行6 份, 在“2.3” 项色谱条件下进样测定, 测得磷化氢峰面积RSD 为1.4%, 表明仪器精密度良好。
2.4.3 稳定性试验 按“2.4.2” 项下方法制备20 份对照品溶液, 于0、 1、 2、 3、 4、 5、 6、 7、 8、 9、 10、 11、 12、13、 14、 15、 16、 17、 18、 24 h 在“2.3” 项色谱条件下进样测定, 测得溶液在10 h 内基本稳定(磷化氢峰面积RSD为1.3%), 10 h 后有逐渐减小的趋势, 可能是由于磷化氢被顶空瓶内空气缓慢氧化所致。
2.4.4 重复性试验 取5 号样品, 按“2.2” 项下方法制备供试品溶液6 份, 在“2.3” 项色谱条件下进样测定, 测得磷化铝残留量(以磷化氢计) RSD 为4.6%, 表明该方法重复性较好。
2.4.5 加样回收率试验 取1、 7、 10 号样品细粉(金银花、 三七、 黄芪), 按“2.2” 项下方法操作, 以4、 10、20 μg/kg 水平添加标准磷化氢气体, 每个质量浓度平行7份, 涡旋10 s, 在“2.3” 项色谱条件下进样测定, 计算回收率。 结果, 金银花中平均加样回收率分别为61.2%
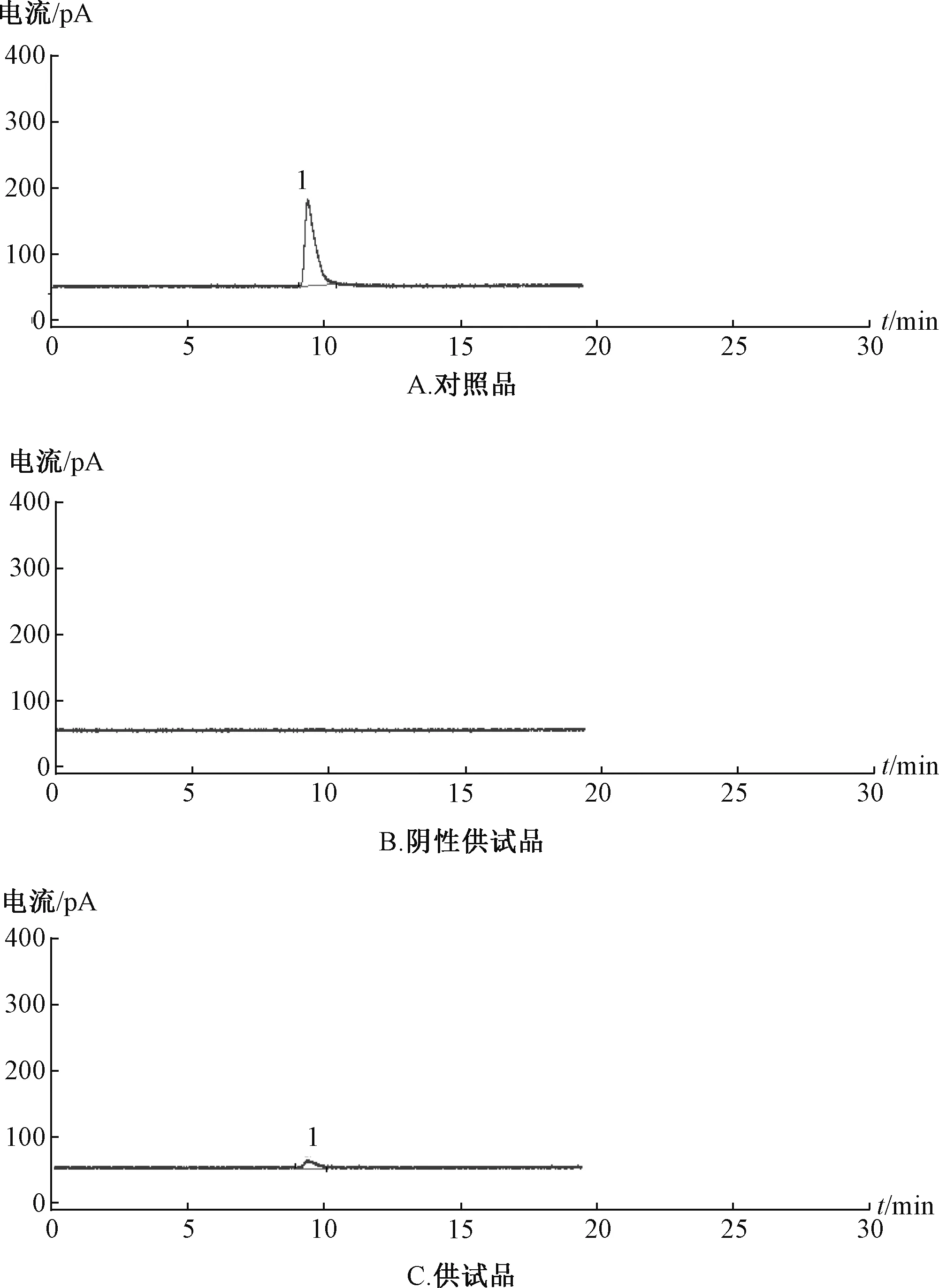
图1 磷化氢气相色谱图
(RSD=2.5%)、 59.8% (RSD=0.75%)、 62.2% (RSD=2.1%), 三七 中分别为58.6% (RSD = 4.6%)、 54.5%(RSD= 1.7%)、 59.9% (RSD = 3.5%), 黄芪中分别为73.6% (RSD = 3.6%)、 78.5% (RSD = 4.0%)、 80.0%(RSD=3.5%)。
2.5 磷化铝残留量测定 取上海市场抽检的15 种中药材、中药饮片, 共48 批, 按“2.2” 项下方法制备供试品溶液,平行2 份, 在“2.3” 项色谱条件下进样测定, 标准曲线法计算磷化铝残留量(以磷化氢计), 结果见表2。
3 讨论
3.1 溶剂酸考察 磷化铝在酸性条件下的水解反应较中性条件下更剧烈迅速, 为了使样品中该成分能迅速转换成磷化氢, 需要使用酸作为溶剂。 本实验考察了5%硫酸、 4%磷酸、 6%盐酸(3 种溶剂的氢离子摩尔浓度近似), 按“2.4.2” 项下制备, 平行3 份, 发现以盐酸为溶剂时磷化氢峰面积相对较小, 其原因可能是盐酸易挥发, 其挥发出的氯化氢与磷化氢可能发生反应, 从而降低了磷化氢的浓度; 以硫酸或磷酸为溶剂时, 其峰面积基本一致, 均明显高于以盐酸为溶剂。 同时, 考虑到GB/T 25222—2010 钼蓝比色法及其他文献中普遍选择的溶剂是硫酸, 最终确定溶剂酸为5%硫酸。
3.2 溶剂体积考察 以5%硫酸为溶剂, 考察溶剂体积0、2.5、 5、 7.5、 10、 12.5、 15 mL 对磷化氢峰面积的影响,发现随着溶剂体积增大, 磷化氢峰面积显著升高, 这可能是由于磷化氢在水中的溶解度较差, 对于密封的20 mL 顶空进样瓶而言, 溶剂体积越大, 气体所占体积越小, 磷化氢在顶空瓶内气相中的浓度越高, 故溶剂体积与磷化氢峰面积呈正相关。 考虑到实际进样情况, 溶剂体积过大时会影响到样品称量, 最终确定溶剂体积为10 mL。
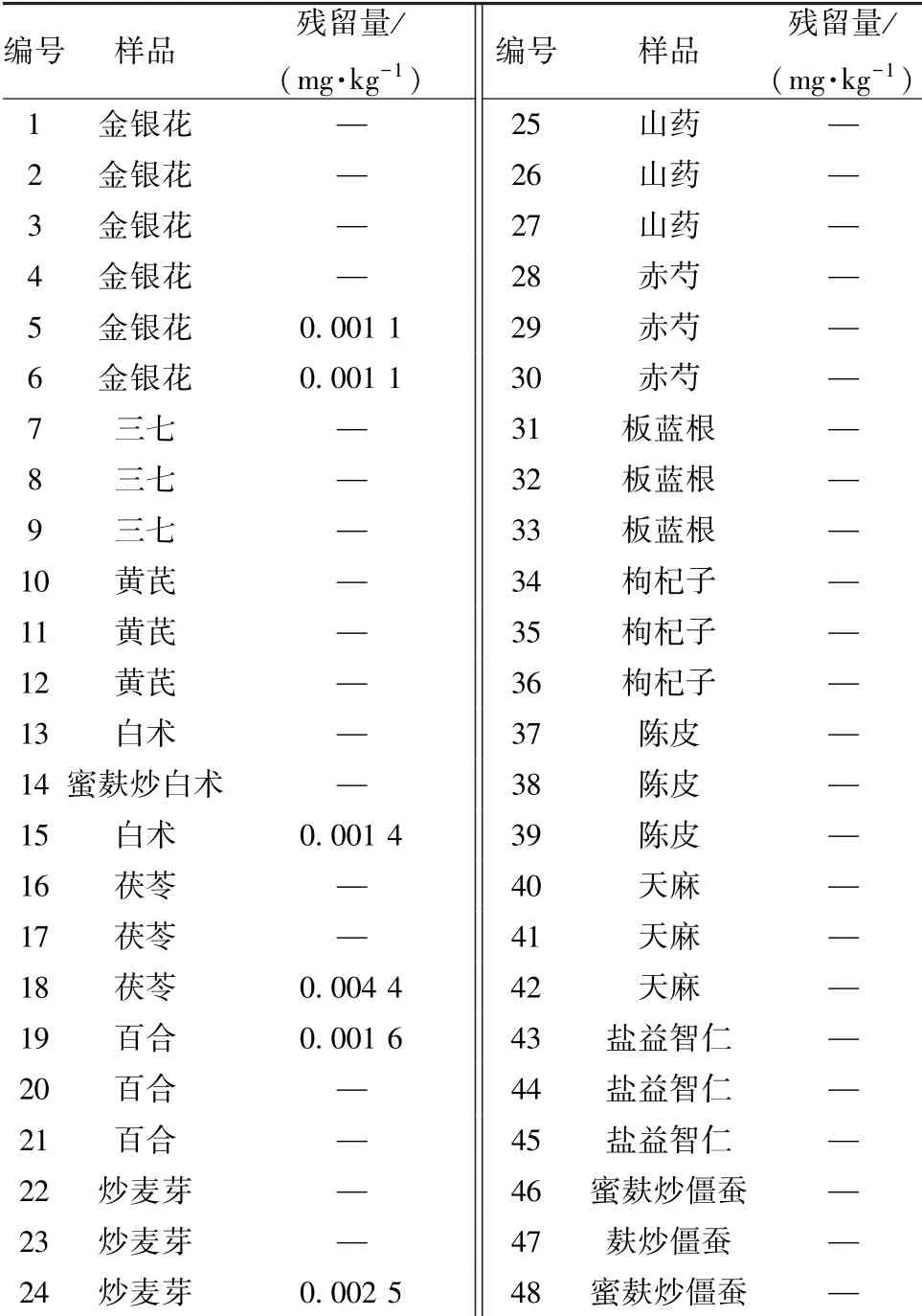
表2 磷化铝残留量测定结果(以磷化氢计)
3.3 顶空平衡温度考察 在顶空进样系统中, 最关键的影响因素是顶空瓶平衡温度。 本实验考察50、 55、 60、 65、70、 75、 80 ℃对磷化氢峰面积的影响, 发现平衡温度从50 ℃增至65 ℃时, 其峰面积逐渐上升, 在65 ℃时达到最大, 这可能是由于温度升高增大了磷化氢在顶空瓶内的气液分配比例; 平衡温度继续上升时, 其峰面积反而开始减小, 这可能是由于磷化氢发生氧化反应或其他副反应的概率提高, 导致其响应强度变弱。
3.4 影响加样回收率因素考察 金银花、 三七、 黄芪加样回收率为55% ~80%, 基本满足残留实验要求, 但相对偏低, 这可能是由于中药材基质较复杂, 对磷化氢存在吸附作用; 同时磷化氢化学性质活泼, 具有强还原性, 可与药材基质发生氧化反应或其他副反应。 若样品检出阳性, 可考虑采用标准加入法或基质对照品溶液, 以进一步提升定量结果的准确性。
3.5 磷化铝残留情况 表2 显示, 15 种中药材、 中药饮片中磷化铝检出率较低, 残留量也低于中国食品安全国家标准GB 2763—2016 及国际食品法典委员会针对干制蔬菜、 干制水果、 香料等中磷化氢残留量的限量规定0.01 mg/kg[14-15]。
4 结论
本实验建立顶空气相色谱法测定15 种中药材、 中药饮片中磷化铝的残留量, 该方法操作简便, 耗时短, 样品取样量少, 重复性好, 灵敏度高, 适用于其他活泼金属磷化物及磷化氢检测, 也可以考虑作为中药中磷化铝残留的快速筛选方法。
