海藻酸盐共混泊洛沙姆的可注射水凝胶的制备及表征
2019-05-31许宁侠曹蓉马政生
许宁侠,曹蓉,马政生
(1.西安外事学院 医学院,陕西 西安 710077;2.西北大学 化工学院,陕西 西安 710069;4.国药控股陕西分公司,陕西 西安 710077)
可注射水凝胶作为智能凝胶的一种,除对环境产生敏感性响应外,可在局部产生响应,且形成凝胶态,与注射部位解剖特点形成契合度较高的形态,广泛应用于组织工程、创伤辅料、药物缓释等领域[1-2]。目前,可注射水凝胶的制备材料主要有壳聚糖[3]、胶原[4]等生物高分子、聚乙烯[5]和聚乙烯醇[6]等聚合物材料。但大部分可注射水凝胶是通过物理交联,其凝胶机械强度较低[7],缺乏足够的力学强度、抗压和抗剪切性能来承受一定的负载环境;而化学交联法过程较复杂,且不具备可注射条件。所以,如何提高可注射凝胶的可注射性和机械强度目前是研究的热点。
泊洛沙姆是由聚氧乙烯(EO)和聚丙乙烯(PO)组成的三嵌段共聚物,通常用来制备可注射凝胶。P407与P188混合制备的混合凝胶可以很好地增加凝胶的强度与黏膜黏附力[8-9]。但泊洛沙姆凝胶机械强度较小,不适合机械强度要求较高的部位[10]。海藻酸钠(SA)可与二价金属离子(Ca2+、Mg2+、Zn2+等)结合成蛋壳状结构而形成凝胶,机械强度较高,可用于组织修复、药物控制释放或细胞免疫隔离等技术[11]。Baysal等研究发现[12],环境溶液中Ca-Alg的稳定性较弱。Loebasack等[13]证明离子交联的藻酸盐水凝胶机械性质变化范围窄,不能控制降解时间。通常形成Ca-SA凝胶的金属离子源由CaCl2溶液提供,但利用CaCl2作为交联剂,凝胶形成的速度过快,对于可注射凝胶来说,缺乏时间允许性。可作为Ca2+源的物质还有Ca(OH)2、CaCO3等。目前还没有直接以CaCO3作为Ca2+源,形成Ca-SA凝胶的研究。
本文以SA为基材,共混泊洛沙姆,制备可注射原位混合凝胶,以CaCO3作为Ca2+源,利用CaCO3为弱电解质,存在解离平衡,缓慢释放Ca2+的特点,同时调整泊洛沙姆的浓度,使泊洛沙姆凝胶的胶凝速度与Ca-SA交联速度相适应,以期通过化学与物理双重交联,形成一种互穿网络结构,具有内部孔径较均匀的微观结构,进而改善混合凝胶的机械强度及抗压能力,提高临床应用范围。
1 实验部分
1.1 试剂与仪器
海藻酸钠(SA),化学纯;泊洛沙姆188(P188)、泊洛沙姆407(P407)购自德国BASF公司;碳酸钙、二甲亚砜(DMSO)、3-(4,5-二甲基噻唑-2)-2,5-二苯基四氮唑溴盐(MTT)等均为分析纯。
IKA-EW120电动搅拌机;DF-101S集热式恒温水浴锅;Hitachi S-4800扫描电子显微镜;D/Max-3c X射线衍射仪;XMN-GB1040电子万能拉力机;TA.XTPlus质构仪;CVO型流变仪。
1.2 可注射水凝胶的制备
将SA加入去离子水中,搅拌均匀。将P407和P188分别加入去离子水中,在4 ℃条件下完全溶解成均匀溶液。将P188和SA溶液按1∶1混合均匀,形成A液。将P407液和碳酸钙溶液混合,使碳酸钙的最终浓度为2 g/mL,形成B液。将A液和B液按1∶1混合,充分搅拌,即得可注射原位凝胶。
1.3 性能检测
1.3.1 样品的形态学检测 将混合凝胶样品在37 ℃胶凝24 h,冷冻24 h,真空冷冻干燥,在20 kV的加速电压下,利用扫描电镜(SEM)观察表面喷金的冻干凝胶的微观形貌。
1.3.2 凝胶的机械性能检测 凝胶样品的机械强度用质构仪进行检测。样品厚度为20 mm,测试条件为:探头为P/0.5R型,探头测试速度为3.0 mm/s,压缩变形为样品原高度的90%,测定温度为室温,每个样品测定3次,取平均值。在万能电子拉力机上进行试样压缩模量测试,其中横梁速度10 mm/min,室温保持在25 ℃。每种样品测试5个,取平均值。在材料的线性弹性范围内,对凝胶样品采用不同频率进行应变扫描,其中频率的范围为0~10 Hz,平板半径40 mm,板间距5 mm,样品平衡5 min后在37 ℃条件下进行振荡频率扫描,可得G′和G″与频率的变化曲线。
1.3.3 凝胶性能表征及生物学检测 将干燥后的凝胶样品 50 mg 进行 X-ray 粉末衍射测定。Cu 靶,2θ角20~80°。利用MTT法测定凝胶对成纤维细胞(L-929)生长增殖过程的影响。按文献[14]法进行检测。酶标仪于 490 nm 处测定吸光度,计算细胞的相对存活率(CV)。
其中,A1是培养液的吸光值,A0为空白培养基的吸光值,A2为含样品凝胶的吸光值。
2 结果与讨论
2.1 泊洛沙姆性能
泊洛沙姆具有独特的疏水内核-亲水外壳结构,在温度升高时,表现出凝胶性质:疏水性的PO被包裹在内部,形成内核;相对亲水的EO则与水结合后缠绕包围在疏水结构的外部,从而形成形态大小不等但组成相似的胶束结构(图1a)。本实验以泊洛沙姆共混SA后,再与Ca2+进行交联,以期形成相互物理-化学双重交联的微观状态(图1b),即可增加机械强度,还可增加混合凝胶的稳定性。

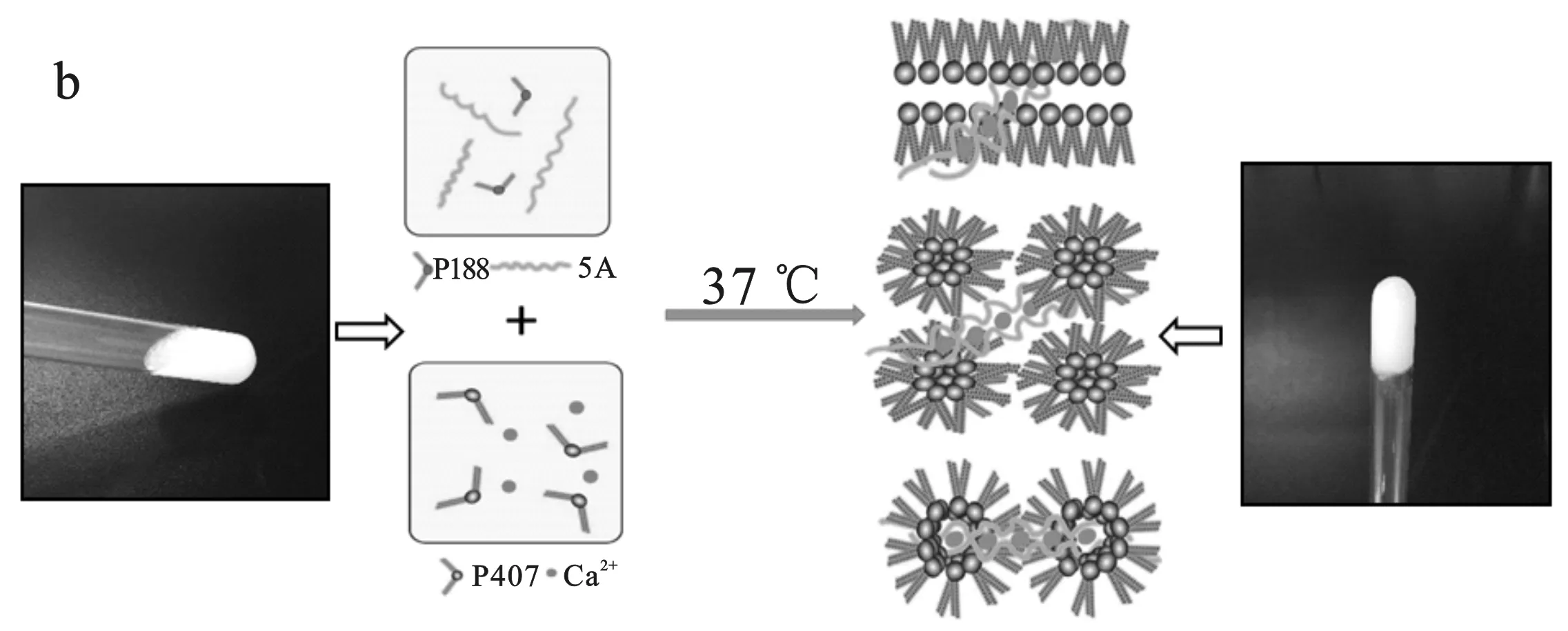
图1 反应模拟图
泊洛沙姆在温度升高时形成胶凝,由液态转变成不流动的固态(图1a中小图)。共混SA后,混合凝胶样品在37 ℃条件下,也可产生温度响应形成胶凝态(图1b中小图)。对于可注射凝胶,以凝胶不流动为止,所用时间为凝胶的相转变时间。根据前期实验结果,采用3 g/mL的SA溶液,P188选择浓度为5 g/mL。当P407浓度<10 g/mL时,凝胶不具备温度响应性,而当浓度>30 g/mL,在4 ℃下都可形成凝胶,与胡洁等的实验结果一致[15]。所以本实验利用10,15,20,25 g/mL的P407溶液制备混合凝胶(CH),分别为CH1、CH2、CH3和CH4。
2.2 混合凝胶的SEM表征
将4种混合凝胶冷冻干燥后进行SEM图谱扫描,结果见图2。

图2 混合凝胶样品截面的SEM图谱
由图2可知,所有混合凝胶材料混合均匀,孔隙结构明显,材料之间并无明显的分层,说明原料之间相容性较好。CH1样品具有大小不同的孔径,类似蜂窝或陷窝结构的多孔网状结构,凝胶中的三维多孔网络结构有相互交叉连通的孔隙,这些孔隙可作为药物、生物活性分子及其它小分子扩散的通道。CH2、CH3和CH4都具有大小不同孔径的孔洞样结构,不同孔隙之间形成连通结构,但b图中形成的孔径相差较大,孔隙结构不均匀;c和d图中有孔道形成,伴随有不同直径的孔洞结构,孔隙结构也不规则,且表现出局部较为致密的结构。CH1可能是Ca-SA网络形成化学交联时,与P407和P188的胶束结构形成物理交联作用互穿,使凝胶内部形成化学-物理多重作用,分子间或分子内的缠结作用加强,形成了密集的网络结构;因CaCO3是弱电解质,在溶液中Ca2+是缓慢释放的,而这种缓慢释放使得Ca-SA的网络结构形成较慢,可与P407和P188形成互穿网络结构,且可看出交联点多于其它3种情况。CH2、CH3和CH4由于P407的浓度增加,对微观网络结构的形成可能存在一定空间位阻作用,形成了具有多孔道的结构,P407的作用较明显,所以形成了类似于胶束的微观结构。
2.3 凝胶样品的机械特性
2.3.1 凝胶样品的抗外压作用和压缩模量 图3显示了样品凝胶在受力下的压缩状态及压缩模量大小。

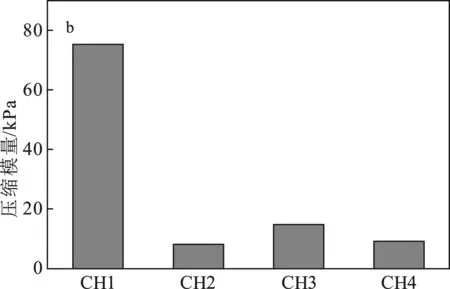
图3 样品的机械强度随时间的变化趋势和压缩模量
由图3a可知,所有样品的机械强度在凝胶形成初期较高,但随着时间延长,整体强度有所下降。CaCO3与SA不能有效地形成胶凝作用,当SA加入CaCO3溶液中时,SA发生了溶解。混合凝胶的强度明显增强,说明样品中除了有效地形成了Ca-SA凝胶化学交联体系的同时,还通过P407与P188的物理微观交联作用,形成了两种凝胶互穿交联体系,在CH1中,由于Ca2+缓慢释放,与SA的交联即可能穿插在其内,也有可能环绕在其周围,才形成这种分子链内或链间的相互作用,从而增强了其抗压性和弹性,明显强于其它样品。
由图3b可知,CH2、CH3和CH4样品的压缩模量相似,分别为8.25,14.73,8.92 kPa,而CH1的压缩模量为75.32 kPa,远大于后三种凝胶样品。弹性压缩模量是指材料在外力作用下产生单位弹性变形所需要的应力,是反映材料抵抗弹性变形能力的指标,所以弹性模量可视为衡量材料产生弹性变形难易程度的指标。从微观角度来说,则是原子、离子或分子之间键合强度的反映。所以可知,CH1凝胶具有较好的抵抗外力作用,可能是Ca-SA凝胶的形成与泊洛沙姆凝胶作用形成过程中,不但有互穿结构的存在,同时不同分子也会形成键合作用,如泊洛沙姆是非离子型表面活性剂,其分子中含有 —OH,而SA分子中也含有大量 —OH,在交联过程中两者之间也可能形成氢键,从而增加其抗压缩性能。这个结果与前述抗外力作用相符合。
2.3.2 凝胶的流变学特点 4种凝胶的流变学特性见图4,采用动态振荡扫描模式研究复合凝胶的储能模量G′和损耗模量G″,其中,G′表征的是材料变形后回弹的指标,可反应样品的弹性性能;G″表征材料耗散变形能量的能力,体现材料的粘性本质,可反应样品的流动性能;用tanδ=G′/G″为损耗因子,其值越大,说明体系黏性比例越大,反之,则弹性比例越大[16]。
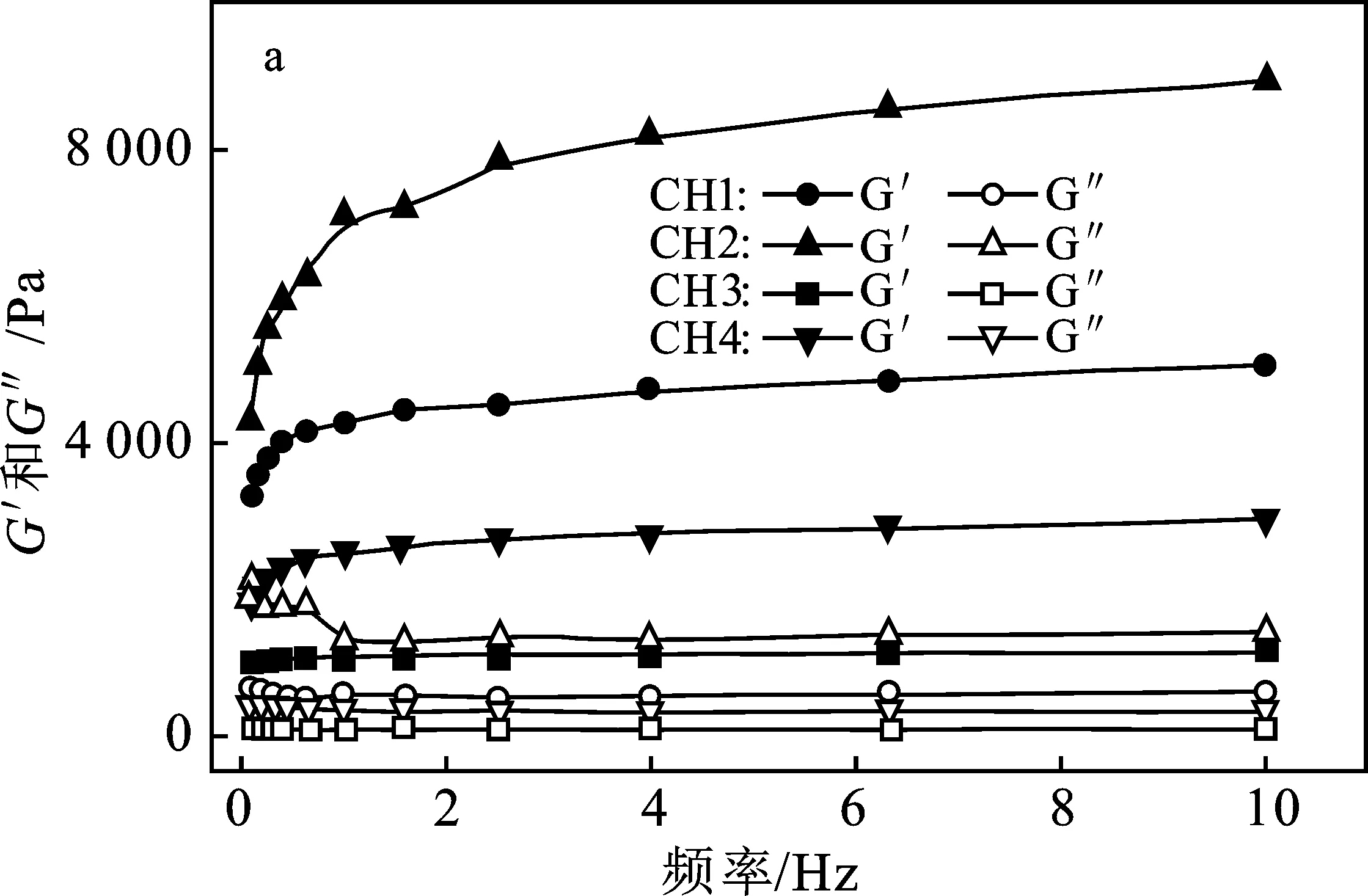

图4 4种凝胶的贮能模量、损耗模量及损耗因子与频率的关系
由图4a可知,在振荡频率0~10 Hz范围内,4种凝胶样品的储能模量G′均远大于损耗模量G″,尤其是CH1和CH2,表明这两种凝胶的弹性性能优于流动性能,两者的G′分别为5.047,8.945 kPa,表明凝胶弹性优良,机械强度较好,可以承受较强外力的作用。由图4b可知,4种凝胶样品的G′/G″值减小,且tanδ值都>1,说明4种样品中弹性成分大于黏性成分,表明凝胶样品中的分子间或分子内的交联程度增加。CH4的tanδ最大,说明P407的浓度增加,混合凝胶的黏性也相应增加。说明P407在高浓度时,单位体积中P407分子数量较多,不同分子链之间形成了分子内或分子间的缔合作用。
2.4 凝胶的性能表征及细胞毒性实验
虽然CH1和CH2流变学特性及稳定性相似,但CH1样品表现出较好的抗外压作用和较高的压缩模量,后期的研究以CH1为目标进行。利用X射线衍射仪对CH1样品进行XRD分析,结果见图5。

图5 混合凝胶的FTIR图谱
由图5可知,样品则在2θ=19.23,23.34,29.47,36.52,39.51,43.25,47.58°处有晶体衍射峰,其中19.23,23.34°处的衍射峰与P407和P188基本在相同位置,但强度减弱,说明样品在形成凝胶时,由于链间分子间作用增强,相应基团的晶体衍射峰吸收减弱。
原料及样品CH1的MTT实验结果见图6。

图6 混合凝胶的MTT实验结果
由图6可知,3种原料细胞增殖率分别为97%,98%和97%,细胞生长良好。对于CH1来说,其细胞增殖率为95%,略低于原料,但同样细胞生长良好,所以制备的混合凝胶对机体无毒性作用,具有较好的生物相容性。
3 结论
以SA为基本原料,CaCO3为交联剂,通过共混P407和P188,制备了可注射原位凝胶,利用CaCO3为弱电解质,缓慢释放Ca2+,在与SA形成化学交联的同时,伴随泊洛沙姆的物理交联过程,形成分子间或分子内氢键、离子键,还可能存在泊洛沙姆分子间的范德华力作用,构成多位点的缔合结构,混合凝胶机械抗外压能力提高,压缩模量为75.32 kPa,同时其弹性和稳定性也有所提高,且对机体无毒性作用,可满足可注射条件,制备过程简单,材料易得,可作为一种潜在临床医用凝胶。作为可注射凝胶,如果应用于人体关节部位,其抗剪切性还需要提高,所以后期的研究应在如何更好提高压缩性的同时,还应关注抗剪切性能的提高途径。
