葡萄糖在咪唑类离子液体中的溶解研究
2019-05-31郑永军张艳维
郑 勇,郑永军,王 振,张艳维
(安阳工学院 化学与环境工程学院,河南 安阳 455000)
在当今的社会和经济发展中,化石能源的过度消耗带来了较为严重的环境问题,不利于可持续发展。从长远的角度出发,利用自然界中广泛存在的生物质资源是解决能源问题的重要途径。其中,以葡萄糖为代表的糖类化合物是生物质资源的主要成分之一,也是纤维素等高分子碳水化合物水解后的重要产物。葡萄糖通过化学反应可以进一步转化为呋喃、糠醛、乙醇等精细化学品和清洁燃料,是一种具有广泛应用前景的可再生物质[1]。为了实现这一目标,首先需要解决葡萄糖的溶解问题。在传统的化学反应中,人们一般使用水、有机溶剂或酸碱溶液进行葡萄糖的溶解和转化。然而,这些体系往往存在着易挥发、易燃烧和污染重的问题。因此,开发更为绿色环保的新型溶剂是解决问题的关键。
离子液体是一种新型的低温熔盐,具有不易挥发、不易燃、熔点低和稳定性高等优点,是葡萄糖等糖类化合物的理想绿色溶剂。目前,国内外在离子液体溶解葡萄糖方面做出了不少的研究工作,取得了一定的进展[2-4]。然而,已有工作对葡萄糖溶解过程的认识仍然较为有限,缺乏系统的溶解热力学数据,不利于相关工作的进一步开展。
针对上述研究现状,选择了两种典型的离子液体1-丁基-3-甲基咪唑四氟硼酸盐([Bmim][BF4])和1-丁基-3-甲基咪唑六氟磷酸盐([Bmim][PF6])作为溶剂,系统研究了不同温度下葡萄糖的溶解情况。根据溶解度数据,计算了溶解过程的热力学函数值,并对反应过程进行了分析和讨论。
1 实验部分
1.1 实验原料
离子液体[Bmim][BF4]和[Bmim][PF6]购于河南利华制药有限公司,纯度高于99%。葡萄糖由上海阿拉丁生化科技股份有限公司提供,纯度大于99.5%。使用前,将离子液体和葡萄糖在真空干燥箱中干燥24 h。
1.2 实验仪器
电子分析天平(瑞士METTLER TOLEDO,ME 104);加热磁力搅拌器(德国IKA,RCT);真空干燥箱(上海精宏,DZF-6020)。
1.3 实验方法
标准大气压下,用电子天平精确称量5 g的离子液体并置于氮气保护的烧瓶中。然后,将约等于离子液体质量0.1%的葡萄糖加入到体系中,在313~353 K下搅拌到完全溶解。在相同温度下,继续加入同量的葡萄糖,直至溶液达到饱和。最后,根据添加的葡萄糖的总量和分子量计算得到该温度下的溶解度S以及摩尔分数x。其中,溶解度代表100 g离子液体所溶解的葡萄糖的质量。
2 结果与讨论
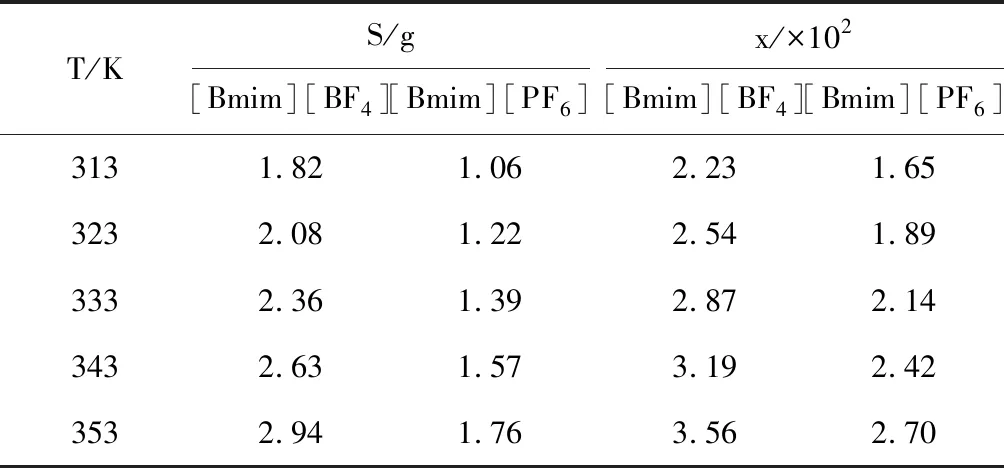
表1 不同温度T下,葡萄糖在离子液体中的溶解度S和摩尔分数x
在313~353 K下,实验测得的葡萄糖溶解度以及摩尔分数见表1。根据实验结果,葡萄糖在离子液体中的溶解度和摩尔分数随温度的升高而显著增大。温度相同时,离子液体[Bmim][BF4]对葡萄糖的溶解能力更强,[Bmim][PF6]则相对较弱。这说明,离子液体的阴离子结构对溶解过程具有重要影响。根据实践经验和文献调研,[BF4]-阴离子的亲水性较强,有助于溶解一些极性物质,包括含有羟基的糖类化合物。相比之下,含有[PF6]-阴离子的离子液体大多呈现疏水性质,这对其溶解糖类化合物产生了一定的不利影响。因此,葡萄糖在这两种离子液体中的溶解度存在明显不同。
为了进一步研究葡萄糖溶解过程的热力学特征,根据理论公式计算得到了相关热力学函数值。其中,标准压力下,葡萄糖的溶解自由能可由下列公式1进行计算[5]。该公式中,R和T分别为气体常数和绝对温度。
(1)
(2)
根据上述方法计算得到的溶解热力学函数值列于表2。可以看出,葡萄糖在两种离子液体中的所有溶解热力学函数均为正值,证明溶解过程需要吸收热量并且受到溶解焓的控制。当温度较高时,反应的熵值增大,自由能降低,表明温度的升高可以使体系获得更多的能量,有利于促进葡萄糖的溶解。同时,该反应是典型的熵增过程,葡萄糖的溶解使离子液体体系的混乱程度增大。自由能大于零反映出溶解过程是难以自发进行的,葡萄糖和离子液体间的相互作用是决定反应程度的重要因素之一。与[Bmim][PF6]相比,[Bmim][BF4]中的溶解自由能较低,进一步证明葡萄糖更容易溶解于[Bmim][BF4]。[BF4]-阴离子与葡萄糖分子之间具有较强的相互作用,使其产生了更为显著的溶剂化效应。
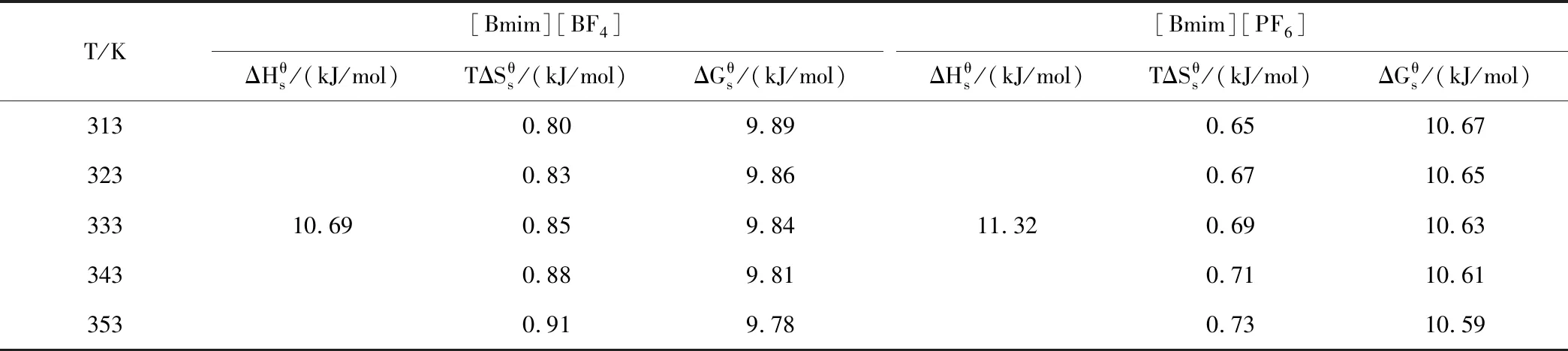
表2 不同温度T下,葡萄糖在离子液体中的溶解热力学函数值
3 结论
离子液体作为一种绿色溶剂,为葡萄糖等糖类化合物的溶解提供了新的途径。从这一背景出发,通过溶解度的测定和数值分析,系统研究了葡萄糖在[Bmim][BF4]和[Bmim][PF6]中的溶解热力学规律。研究发现,[Bmim][BF4]对葡萄糖的溶解能力较强,阴离子的结构是影响溶解度的重要因素之一。根据热力学函数的数值结果,葡萄糖在离子液体中的溶解受到焓控制,是典型的吸热过程。温度的升高有利于葡萄糖的溶解,使体系的熵值增大。上述工作进一步加深了对溶解反应的认识,完善了相应的热力学数据体系,对葡萄糖等糖类化合物的溶解和转化研究将起到一定的推动作用。
