Cu2O纳米粒子的可控制备及可见光催化性能研究
2019-05-24胡亚微温永超
高 慧, 胡亚微, 杜 鑫, 温永超
(陕西科技大学 陕西省轻化工助剂重点实验室, 陕西 西安 710021)
0 引言
21世纪,“绿色”是发展的必要前提,然而水体和空气质量已经受到极大破坏,二者严重影响到整个生物界的生存与发展[1,2].对于水体净化,虽然膜技术可以处理这一问题[3],但是由于该技术耗电量高并需要较大的空间使得成本较高而受到限制.现在随着半导体技术的发展使得可以成为代替这一技术[4],实现水体中有机污染物的有效去除.
自从1972年,Fujishima等[5]采用TiO2半导体作为电极通过电化学方法电解水得到了H2,使得越来越多的学者开始致力于这一发展[6,7].然而除了产氢技术的革命,光催化剂也可以通过吸收可再生的太阳光能转化为化学能然后使得有机分子被破坏成为可降解的小分子来达到净化水[8-10].
目前,在众多半导体材料中,由于Cu2O具有较窄的带隙(2.2 eV),可以很好的吸收可见光,因此成为研究热点[11].但是由于Cu2O在可见光下存在光腐蚀的缺点而导致对太阳光的利用率极大下降,所以为了克服这一缺点众多研究者制备出不同形貌的Cu2O,如:纳米或者微米球[12]、薄膜[13]、立方体[14]、六面体和八面体[15]等;或是通过与其他材料(金属:Ag、Cu等;金属氧化物:TiO2、ZnO等;有机物:石墨烯、g-C3N4等)[16-21]复合使得光生电子发生转移来降低光生电子与空穴的复合,从而提高对太阳光的利用并提高其光催化活性.目前,对于Cu2O及其复合物可通过湿化学法(如:化学沉淀、水热法、溶剂热法和微乳法)、电化学法和新型的气相沉积技术、辐照法、声化学法等来合成.然而,水热法、溶剂热法和电化学法耗能增加了生产成本,新型的技术对设备要求严格,而微乳法生成的产物均匀性较差[22].
因此,本文采用简单的化学还原法,通过控制合成条件来调控粒子尺寸,从而得到可见光光催化活性优异的Cu2O.
1 实验部分
1.1 Cu2O纳米粒子的制备
本文根据Chen等[23]的合成方法并进行一定的优化来制备Cu2O纳米粒子.具体实施步骤如下:首先,分别配制0.5 mol/L的聚乙二醇600(PEG)溶液、0.01 mol/L的硝酸铜溶液、0.5 mol/L的NaOH溶液和0.1 mol/L的抗坏血酸(Vc)溶液;其次取6 mL PEG溶液稀释到48 mL,同时加入12 mL的Cu(NO3)2溶液形成A液,取3 mL的Vc溶液加入到30 mL H2O中形成B液,取9 mL的NaOH溶液加入到30 mL的H2O中形成C液.然后将B液与C液混合后搅拌均匀加入到在恒温水浴锅加热条件下的三口烧瓶中,并迅速将A液转移至混合液中,在氮气条件下搅拌反应30 min,得到悬浮液;最后离心、用去离子水和乙醇分别洗涤3次和2次后,在真空干燥箱60℃下干燥24 h,即可得到氧化亚铜纳米粒子.
1.2 表征和测试
采用日本Rigaku D/Max-3c型X射线粉末衍射仪(XRD,Cu-Kα为入射源,扫描速率和范围分别为8 °/min和20 °~70 °)分析样品物相;采用美国FEI Verios 460型(FE-SEM)和美国FEI Tecnai G2 F20 S-TWIN型透射电子显微镜(TEM)对样品的微观形貌进行分析;采用紫外-可见漫反射光谱仪(Lambda 950,PerkinElmer)测定样品的紫外-可见漫反射光谱图(UV-Vis DRS).
使用上海佳鹏科技有限公司生产的CHX系列光化学反应仪对样品的光催化性能进行测定,采用500 W的氙灯作为光源,并安装滤光片以获得λ>420 nm范围的光.光照前,将10 mg制得的样品浸入到5 mL、20 mg/L或者50 mL、20 mg/L的甲基橙(MO)溶液中,在黑暗下搅拌30 min使其达到吸附/脱附平衡,随后采用紫外可见分光光度计(723N型),每隔30 min光照后取其上清液测其吸收强度,记录其在462 nm处的吸光度.通过Ct/C0研究样品对MO的光降解程度,从而评价其光催化活性.Ct代表时间t时MO的浓度,C0代表MO的初始浓度.
2 结果与讨论
2.1 NaOH浓度对Cu2O的影响
本文通过控制氢氧化钠的浓度(0.062 5 mol/L~2.0 mol/L)制备Cu2O,但是由于氢氧化钠的浓度低于0.125 mol/L时,无固体产物产生,所以对低于0.125 mol/L的研究未进行说明,后续将不再赘述.
2.1.1 X射线衍射(XRD)分析
图1为在25 ℃下,不同NaOH浓度条件下的Cu2O的XRD谱图.从图1可看出,在不同NaOH浓度下制备的样品均在2θ约为29.6 °、36.4 °、42.3 °和61.3 °处出现强而尖的衍射峰,对应于Cu2O的(110)、(111)、(200)和(220)晶面,这与赤铜矿Cu2O标准卡片(PDF Card No.05-0677)的衍射峰相一致,而且除此之外没有其它衍射峰出现,说明制备的样品为纯Cu2O.

图1 不同NaOH浓度下Cu2O的XRD图
2.1.2 SEM分析
图2为25 ℃下不同NaOH浓度下Cu2O的SEM图.从图2可看出,Cu2O纳米粒子分散相对较好、形貌均一、是表面光滑的纳米立方相晶体,且随着碱浓度的增加,晶体粒径从40 nm(图2(a))增长到600 nm(图2(e)),说明碱浓度对Cu2O纳米粒子的尺寸具有很大的影响,所以可通过调节碱浓度来很好的控制Cu2O纳米粒子的粒径.

(a)0.125 mol/L (b)0.250 mol/L

(c)0.50 mol/L (d)1.0 mol/L

(e)2.0 mol/L图2 不同NaOH浓度下Cu2O的SEM图
2.1.3 光催化性能分析
图3为在25 ℃下,不同NaOH浓度下的Cu2O粒子对MO的降解图和降解动力曲线图.在非均相光催化时,一般认为光催化降解满足Langmuir-Hinshelwood动力学方程,且光催化氧化反应符合一级反应动力学特征,其特征方程为:ln(Ct/C0)=-Kt[24],式中:C0是MO的起始浓度;Ct是经过光照时间t后MO的浓度;K是一级反应速率常数,可以用K值来衡量样品催化性能的强弱.以ln(C0/Ct)对t做图并进行拟合,浓度比的对数与时间呈现线性关系.
从图3(a)可看出,在不同NaOH浓度条件下所制备的样品均具有降解能力.置于黑暗条件时,都显示出了一定的暗吸附能力.当置于模拟可见光条件下120 min时,随着NaOH浓度的逐渐降低(2.0 mol/L~0.125 mol/L),样品的降解率分别是13.43%、43.75%、46.75%、90.52%、94.03%.可以得出在NaOH浓度为0.125 mol/L下样品的光催化性能最好,降解率最高,表现出优异的光催化活性.通过图3(b)的速率曲线图可看出,随着NaOH浓度的逐渐降低其K值也是逐渐增加,其中在浓度为0.125 mol/L时的最高,可达0.029 18 min-1.
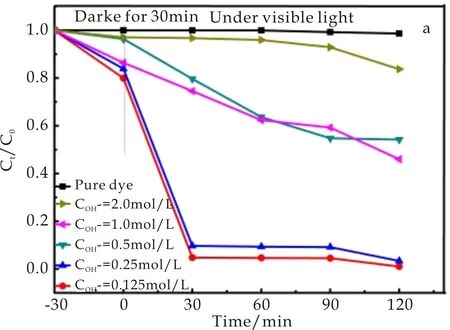
(a)降解曲线图
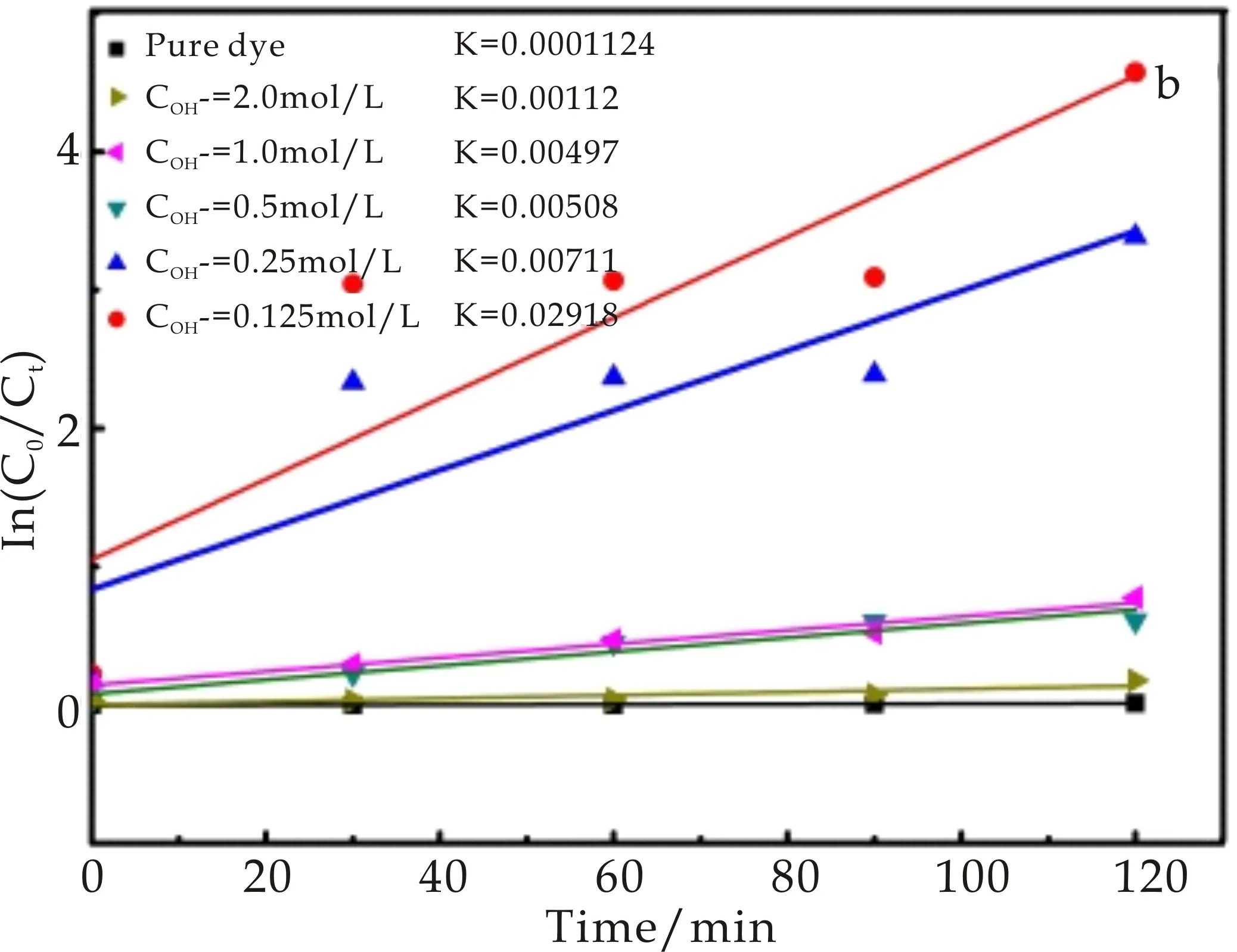
(b)降解动力曲线图图3 不同NaOH浓度下的Cu2O对MO(5 mL)的降解曲线和降解动力曲线
2.1.4 紫外-可见漫反射光谱分析(UV-Vis DRS)
光的吸收强度是评价催化剂好坏的一个标准,它的大小取决于禁带宽度和表面粗糙度[25].图4为不同NaOH浓度下Cu2O的紫外-可见漫反射光谱图.从图4可看出,不同NaOH浓度下制备的产物均在可见光区有一定的吸收,而且随着NaOH浓度的降低,样品对可见光的吸收强度逐渐增加.其中当浓度为0.125 mol/L时,Cu2O对可见光的吸收强度最大;同时随着NaOH浓度的降低,样品的吸收带也发生一定程度的红移,其中0.125 mol/L时红移现象最明显,产生这种现象的原因可能是由于制备的Cu2O的粒径尺寸大小所导致.由于样品对可见光的吸收强度的增加和红移,使得扩大了光响应范围,提高了对太阳光的利用率,所以在光催化实验中表现出优异的光催化活性.
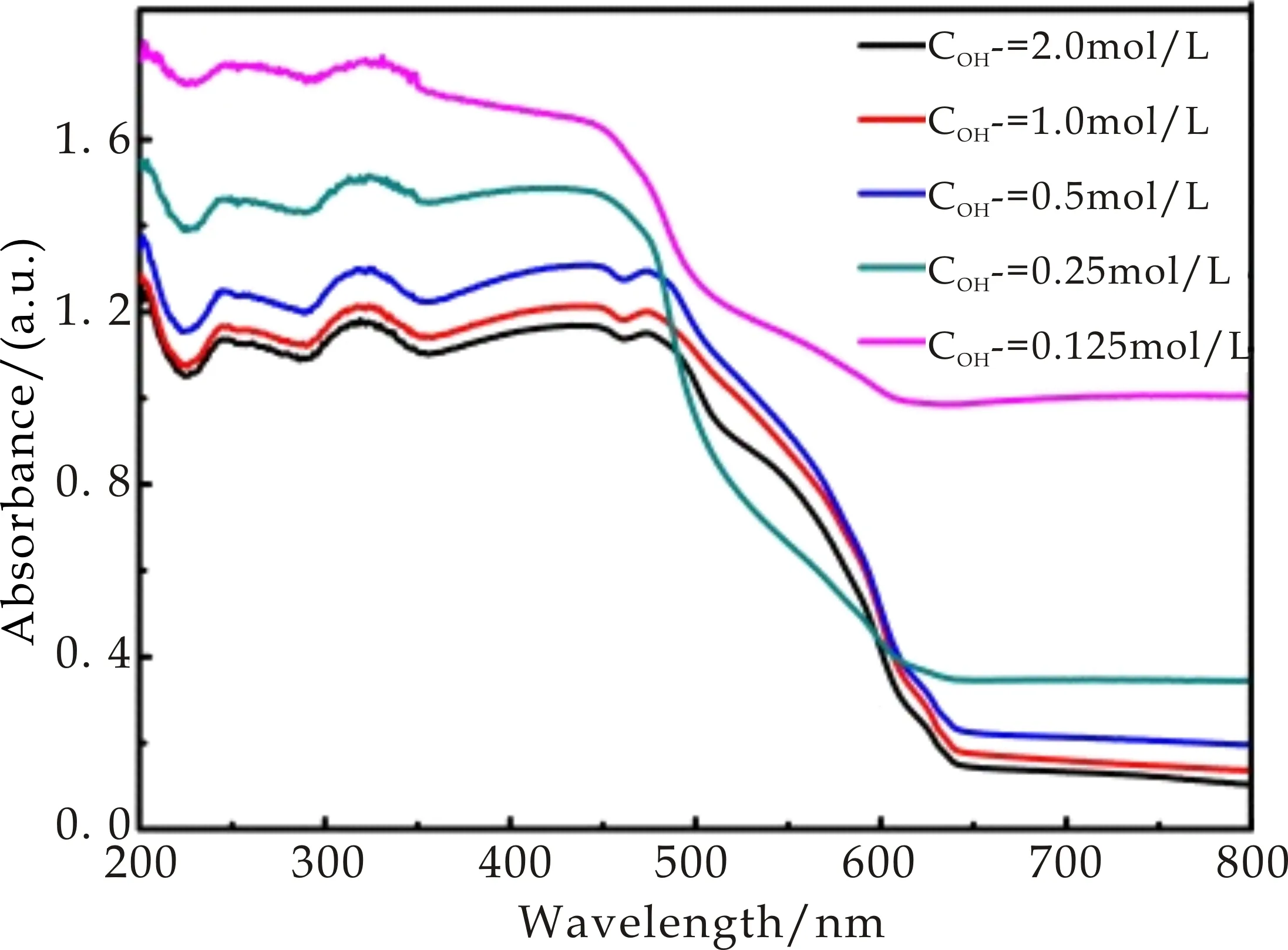
图4 不同NaOH浓度下Cu2O的UV-Vis DRS图
2.2 温度对Cu2O的影响
2.2.1 X射线衍射(XRD)分析
图5为NaOH浓度为0.125 mol/L时,不同温度条件下Cu2O的XRD谱图.从图5可看出,在不同温度下制备的样品均在2θ约为29.6 °、36.4 °、42.3 °和61.3 °处出现强而尖的衍射峰,对应于Cu2O的(110)、(111)、(200)和(220)晶面,这与赤铜矿Cu2O(PDF Card No.05-0677)的衍射峰相一致,而且除此之外没有其它衍射峰出现,说明制备的样品为纯Cu2O.

图5 不同温度下Cu2O的XRD图
2.2.2 SEM和TEM分析
图6为NaOH浓度为0.125 mol/L,不同反应温度(25 ℃~ 55 ℃)下Cu2O的SEM和TEM图.图6(a)、(b)为25 ℃和32 ℃下制备产物的SEM图,从图中可看出Cu2O形态呈立方体,平均粒径分别约为40 nm和35 nm左右;图6(c)、(d)为40 ℃制备的产物的SEM和TEM图,可清晰看出Cu2O形貌也呈立方体状,平均粒径约25 nm,粒径较均匀,分散性较好;图6(e)、(f)显示在47 ℃和55 ℃制备的Cu2O粒径均约为20 nm,但是堆积现象都比较明显.所以可得出随着反应温度的逐渐升高,Cu2O的粒径逐渐降低.对于不同温度下产物粒径的变化可能是由于温度影响溶液中离子的迁移速率,导致Cu2O的成核速率、生长速率和晶核数量发生一定的变化[26],而粒子的粒径是由成核速率与生长速率的比值所决定,温度升高,可能导致成核速率大于生长速率,因此,粒径随着温度的升高而降低.所以,温度对颗粒粒径有一定的影响,导致不同温度下制备的Cu2O的粒径不同.当温度太高时制备的Cu2O的粒径过小,容易发生团聚,从而将会影响其性能.

(a)25 ℃ (b)32 ℃

(c)40 ℃ (d)40 ℃

(e)47 ℃ (f)55 ℃图6 不同温度下Cu2O的SEM图和TEM图
2.2.3 光催化性能分析
图7(a)为NaOH浓度为0.125 mol/L、不同温度下的Cu2O对MO(5 mL)的降解动力曲线图.可以看出,在不同温度条件下所制备的样品均具有降解能力,并且当反应温度为25 ℃、32 ℃、47 ℃和55 ℃时,样品经过黑暗条件下处理30 min时,其吸附率比较低,在可见光下30 min后才展现出一定的降解能力;而当反应温度为40 ℃的样品在黑暗条件下处理30 min时吸附率已经接近98%,对于这种现象的解释可能是由于制备的产物粒径小、分布均匀,所以拥有更高的吸附能力.
从降解动力曲线图7(b)可看出,不加催化剂、25 ℃、32 ℃、47 ℃和55 ℃样品作为催化剂的K值分别为0.000 112 4 min-1、0.028 18 min-1、0.035 01 min-1、0.023 33 min-1和0.017 52 min-1,可看出随着反应温度的增加,催化剂对MO溶液的降解速率常数(K)先增加后降低,表明随着温度的增加制备的催化剂的光催化活性先增加后降低.所以为了研究40 ℃样品的光催化活性和稳定性能,将5 mL的MO溶液的体积增加到50 mL,探究其光催化活性,其结果如图7(c)~(e)所示.
从图7(c)可看出,当可见光照30 min时MO的降解率达到84.2%,随着光照时间的推移,2 h时降解率接近95.6%.从图7(d)可以看出,40 ℃样品对50 mL MO的降解速率常数K值为0.037 08 min-1,对比图7(b)各温度下的样品的K值可得出:40 ℃下样品的光催化活性最佳.对于如此优异的可见光催化性能的原因可能是Cu2O纳米粒子的尺寸越小,其降解MO的速率越快,也说明Cu2O纳米粒子对MO降解速率的高低受样品粒径大小的影响.图7(e)是为了评估40 ℃下Cu2O纳米粒子的稳定性,对其进行MO的重复降解.实验结果表明:在循环4个周期后,光催化活性依然维持在75%左右,说明这种催化剂比较稳定,可以多次重复利用.综上:当NaOH浓度为0.125 mol/L、反应温度为40 ℃时,制备的Cu2O具有优异的光催化活性和利好的稳定性.

(a)对MO(5 mL)的降解图
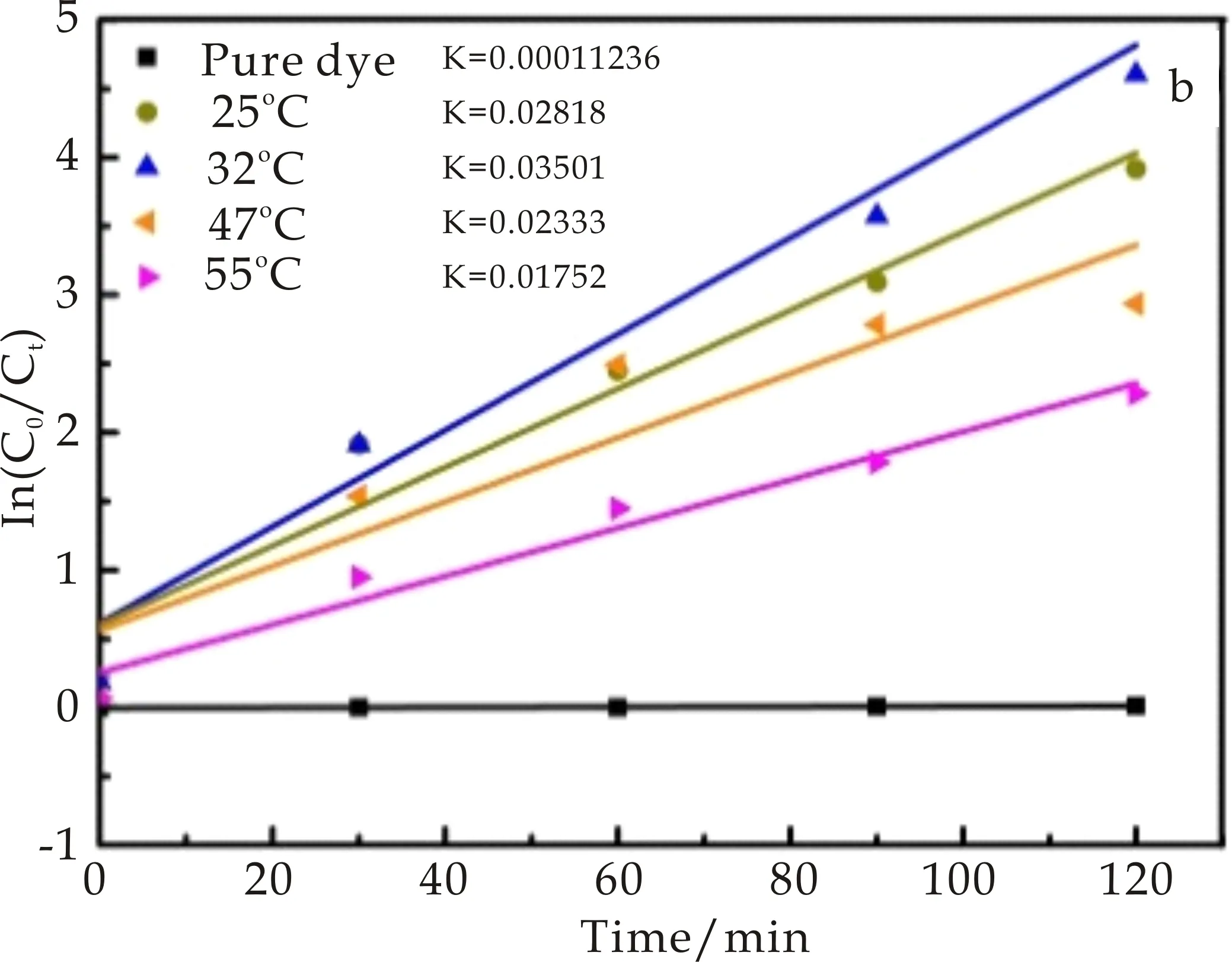
(b)对MO(5 mL)的降解动力曲线图
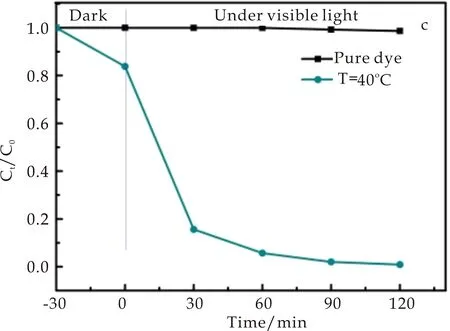
(c)40 ℃下的Cu2O对MO(50 mL)的降解图
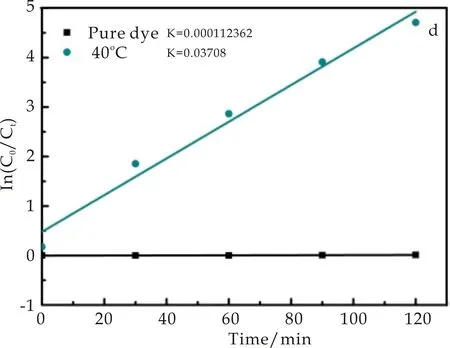
(d)40 ℃下的Cu2O对MO(5 mL)的降解动力曲线图

(e)40 ℃下的Cu2O重复使用图图7 不同温度下的Cu2O对MO的降解图、降解动力曲线图和重复使用图
2.2.4 紫外-可见漫反射光谱分析(UV-Vis DRS)
图8为NaOH浓度为0.125 mol/L、不同反应温度下Cu2O的UV-Vis DRS光谱图.从图8可看出,不同温度下制备的样品在可见光区域均有很好地吸收,并且随着反应温度的升高,样品对可见光的吸收强度先增加后降低,其中40 ℃时样品的强度最高;同时其对可见光的吸收带发生红移,25 ℃和40 ℃下的样品吸收边分别约为918.7 nm和1 013.8 nm,根据公式Eg=1 240/λ,可以估算出其禁带宽度分别为1.35 eV和1.22 eV.显然,40 ℃样品的带隙小,而较小的带隙使催化剂很容易吸收太阳能产生光生电子和空穴,从而光催化时加速了电子传输速率[27].因此,40 ℃样品的催化性能较好.所以在可见光下催化实验中表现出优异的光催化活性的原因.
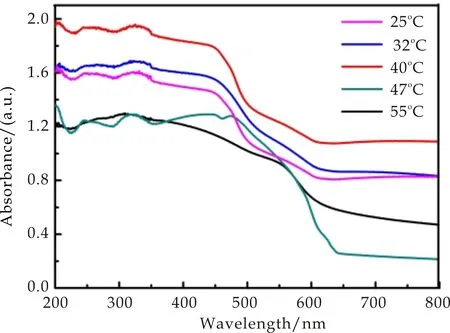
图8 不同反应温度下Cu2O的UV-Vis DRS光谱图
3 结论
采用简单的化学还原法并通过调控NaOH浓度和反应温度制备Cu2O粒子,控制NaOH浓度为0.125 mol/L和反应温度为40 ℃时,制备得Cu2O纳米粒子为25 nm立方体,具有较高的光催化降解性能和稳定性;在可见光照射30 min时对MO(50 mL、20 mg/L)的降解率达84.2%,光照2 h时接近95.6%,并且在循环使用4次后,降解率仍保持在75%左右,具有良好的可见光催化活性及光催化稳定性.
